Abordagem
Durante os períodos de alta prevalência de COVID-19, considere que todos os pacientes com tosse, febre ou outros sintomas sugestivos têm COVID-19 até prova em contrário.Para o tratamento de pacientes com pneumonia por COVID-19 suspeitada ou confirmada, consulte Doença do coronavírus de 2019 (COVID-19).
A pneumonia devida à COVID-19 não é abordada neste tópico.
A antibioticoterapia imediata, correta e adequada é essencial para o tratamento da pneumonia hospitalar.[2][64][65] Os esquemas são baseados na presença ou não de fatores de risco para patógenos resistentes a múltiplos medicamentos. Esses fatores de risco são:[1]
Antibioticoterapia nos 90 dias anteriores
Choque séptico durante a pneumonia associada à ventilação mecânica (PAVM)
Síndrome do desconforto respiratório agudo antes da PAVM
Início de PAVM no dia 5 ou mais de internação hospitalar
Terapia renal substitutiva aguda antes do início da PAVM.
Se um dos fatores de risco acima estiver presente, a terapia combinada com agentes de amplo espectro é indicada.[66]
O uso de qualquer antibiótico no ambiente hospitalar deve ser criterioso, pois pode influenciar o desenvolvimento de cepas resistentes, particularmente na unidade de terapia intensiva (UTI). Surtos de patógenos resistentes a múltiplos medicamentos Gram-negativos decorrem do uso excessivo de betalactâmicos ou fluoroquinolonas.[67] Em geral, se um antimicrobiano tiver uso preferencial, pode ocorrer resistência. Um estudo relatou um surto depois do uso prolongado dos antibióticos carbapenêmicos (20 dias) e colistimetato (13 dias).[68]
Um protocolo pré-especificado de antibióticos em pacientes com um novo diagnóstico de pneumonia hospitalar não é exigido, mas é recomendado, porque garante que os pacientes não serão subtratados, particularmente no começo, quando os médicos têm a oportunidade de diminuir a mortalidade.[2] Um protocolo deve conter uma lista de medicamentos para escolha e o esquema deve ser reduzido subsequentemente, ou a resistência pode aumentar.
Na atual pandemia, tenha um alto nível de suspeita para infecção por COVID-19. Consulte o tópico separado Doença de coronavírus 2019 (COVID-19) para obter recomendações atualizadas sobre o tratamento.
Em novembro de 2018, a European Medicines Agency (EMA) concluiu uma revisão dos efeitos adversos graves, incapacitantes e potencialmente irreversíveis associados aos antibióticos fluoroquinolonas sistêmicos e inalatórios. Entre os efeitos adversos estão tendinite, ruptura de tendão, artralgia, neuropatias e outros efeitos sobre os sistemas musculoesquelético ou nervoso. Em consequência desta revisão, a EMA agora recomenda restringir o uso dos antibióticos fluoroquinolonas somente a casos de infecção bacteriana grave e com risco de vida. Além disso, ela recomenda que as fluoroquinolonas não sejam usadas para infecções leves a moderadas, a menos que outros antibióticos adequados à infecção específica não possam ser usados; e que também não sejam usadas para tratar infeções não graves, não bacterianas ou autolimitadas. Pacientes mais idosos e os que apresentam comprometimento renal ou que sofreram transplante de órgãos sólidos e aqueles tratados com corticosteroides têm maior risco de danos a tendões. Deve-se evitar a coadministração de uma fluoroquinolona e um corticosteroide.[69] A Medicines and Healthcare Products Regulatory Agency do Reino Unido respalda estas recomendações.[70] A Food and Drug Administration (FDA) dos EUA emitiu uma comunicação de segurança semelhante em 2016, restringindo o uso de fluoroquinolonas em casos de sinusite aguda, bronquite aguda e infecções do trato urinário não complicadas.[71] Além dessas restrições, a FDA emitiu avisos sobre o aumento do risco de dissecção de aorta, hipoglicemia significativa e efeitos adversos para a saúde mental em pacientes que tomam fluoroquinolonas.[72][73] Embora as fluoroquinolonas não sejam mais licenciadas para o tratamento da pneumonia nosocomial na Europa, ainda estão aprovadas para essa indicação nos EUA e em outros países, e as diretrizes ainda recomendam seu uso.[1][74] Portanto, o uso de fluoroquinolonas ainda é recomendado nesses casos, mas devem ser usadas com precaução. A FDA recomenda aos profissionais da saúde interromper as fluoroquinolonas sistêmicas imediatamente se o paciente apresentar efeitos adversos graves; o ciclo de tratamento do paciente deve ser concluído com um antibiótico sem fluoroquinolona.[71]
Antibioticoterapia empírica
Esquemas de antibioticoterapia empíricos sempre devem ser adaptados aos padrões locais de resistência; deve-se realizar um antibiograma.[66]
Se um paciente não apresentar fatores de risco para patógenos resistentes a múltiplos medicamentos, é provável que o patógeno causador da pneumonia seja Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus sensível à meticilina (SASM) ou bacilos Gram-negativos entéricos sensíveis ao antibiótico (por exemplo, Escherichia coli, Klebsiella pneumoniae, espécies de Enterobacter, espécies de Proteus ou Serratia marcescens). A terapia envolve monoterapia com cobertura para Pseudomonas aeruginosa: cefepima, ceftazidima, imipeném/cilastatina, meropeném, levofloxacino ou piperacilina/tazobactam.[1][75][76] É de notar a ausência de aminoglicosídeos nesta lista porque eles foram considerados como apresentando mais riscos que benefícios, apesar de cobrirem P aeruginosa causadora de pneumonia hospitalar/PAVM.[77]
Se um paciente tiver fatores de risco para patógenos resistentes a múltiplos medicamentos, é provável que o patógeno causador seja P aeruginosa, K pneumoniae (cepa produtora de betalactamases de espectro estendido [BLEE]), espécies de Acinetobacter, Staphylococcus aureus resistente à meticilina (MRSA) ou Legionella pneumophila. Pneumonia hospitalar/PAVM causadas por qualquer um desses patógenos foram associadas a um aumento da mortalidade.[78] Os fatores de risco para P aeruginosa incluem presença de bacilos Gram-negativos em coloração de Gram de alta qualidade e doença estrutural pulmonar. Se qualquer um desses fatores estiver presente, ou se o paciente estiver intubado e ventilado mecanicamente, ou apresentar choque séptico, a terapia combinada para P aeruginosa deve ser administrada. Em pacientes com probabilidade de apresentar patógenos resistentes a múltiplos medicamentos, o tratamento envolve terapia combinada incluindo uma cefalosporina (por exemplo, cefepima, ceftazidima), um carbapenema (por exemplo, imipeném/cilastatina, meropeném), um betalactâmico/inibidor de betalactamases (por exemplo, piperacilina/tazobactam) ou um monobactâmico (por exemplo, aztreonam), associada a uma fluoroquinolona (por exemplo, ciprofloxacino, levofloxacino) ou um aminoglicosídeo (por exemplo, amicacina, gentamicina, tobramicina); e linezolida ou vancomicina (ou, alternativamente, telavancina).[76]
Se houver suspeita de Pseudomonas como patógeno causador, dois antibióticos deverão ser usados empiricamente com diferentes modos de ação, com regimes que consistem em várias combinações de betalactâmicos antipseudomonas, carbapenêmicos, fluoroquinolonas e aminoglicosídeos. Imipeném/cilastatina ou meropeném (antibióticos carbapenêmicos) podem ser usados, mas ertapeném não, pois não cobre P aeruginosa e é aprovado somente para a pneumonia adquirida na comunidade. O tratamento empírico com um carbapenêmico foi associado com menor mortalidade em curto prazo que o tratamento com não carbapenêmicos, principalmente em pacientes com PAVM; no entanto, também foi associado ao aumento da resistência, o que torna mais difícil escalar o esquema antimicrobiano, caso necessário.[79] Para patógenos Gram-negativos resistentes a múltiplos medicamentos, ceftazidima/avibactam é uma opção de betalactâmicos.[80] Outros antibióticos aprovados com cobertura de P aeruginosa para pacientes com pneumonia hospitalar/PAVM e infecção por patógeno Gram negativo resistente a múltiplos medicamentos incluem cefiderocol (uma nova cefalosporina siderófora), a combinação de antibióticos imipeném/cilastatina/relebactam (um carpabenêmico com um potente inibidor de betalactamase) e ceftolozana/tazobactam (um novo betalactâmico/inibidor de betalactamase).
Os aminoglicosídeos proporcionam eliminação rápida de bactérias Gram-negativas, mas podem causar toxicidade renal ou ototoxicidade. A tobramicina tem penetração pulmonar ligeiramente melhor que a gentamicina e pode ser administrada como agente por via inalatória, embora esse seja um tratamento novo. As fluoroquinolonas foram eficazes e a ciprofloxacina tem um espectro relativamente estreito, mas a resistência ao Pseudomonas aumenta anualmente. As fluoroquinolonas também foram associadas à colite por Clostridium difficile. Os aminoglicosídeos e as fluoroquinolonas são antimicrobianos dependentes da concentração. Para tirar proveito dessa característica, eles são administrados em doses infrequentes e altas, diferentemente dos antimicrobianos dependentes do tempo (por exemplo, betalactâmicos), que são dosados para manter os níveis do medicamento acima da concentração inibitória mínima. Incidentalmente, um estudo comparando a tigeciclina com imipeném/cilastatina constatou que a tigeciclina era não inferior em pacientes com pneumonia hospitalar, mas era inferior em pacientes com pneumonia associada a ventilação mecânica (PAVM).[81] A tigeciclina atualmente está aprovada para pneumonia adquirida na comunidade, não para pneumonia hospitalar. Na caixa desse medicamento agora há um aviso afirmando que ele só deve ser usado quando um agente alternativo não é adequado. Isso se deve ao aumento da mortalidade (0.6%; IC de 95% 0.1, 1.2) associada ao seu uso. Para pacientes com PAVM, a mortalidade com tigeciclina foi de 50.0% versus 7.7% para o grupo de comparação.[82] Em última análise, os esquemas devem ser baseados nos antibiogramas locais.
Vancomicina ou linezolida devem ser adicionadas (ou seja, o paciente tomará 3 antibióticos) se o paciente estiver sob risco de contrair MRSA. Os fatores de risco para MRSA incluem o uso prévio de antimicrobianos nos dias anteriores, internação em uma UTI onde >20% dos isolados de Staphylococcus aureus são positivos para MRSA (ou a porcentagem é desconhecida), e ter um alto risco de mortalidade. Dados sugerem que a linezolida e a vancomicina apresentam eficácia semelhante. Dados de acompanhamento são ambíguos, sugerindo que linezolida e vancomicina são equivalentes ou que a linezolida é superior.[83][84][85][86][87][88]
Se a pneumonia hospitalar for diagnosticada após uso recente de antibióticos ou durante o uso de antibióticos para uma infecção diferente, a terapia empírica deve envolver medicamentos de uma classe diferente.[89]
Antibioticoterapia direcionada ao patógeno
Quando os resultados das culturas estiverem disponíveis, os antibióticos deverão ser reduzidos adequadamente: o tratamento deve ser direcionado com base nas sensibilidades do patógeno específico que cresceu; ou ainda, os antimicrobianos devem ser descontinuados com base nos patógenos que não cresceram na cultura. Por exemplo, a linezolida deve ser continuada se o MRSA crescer na cultura, ou descontinuada se negativo.[90][91]
Exemplos de antibióticos usados para o tratamento de uma infecção Gram-negativa confirmada (por exemplo, Pseudomonas, Acinetobacter, Klebsiella, Serratia) incluem uma cefalosporina (cefepima, ceftazidima, cefiderocol) ou um carbapenêmico (imipeném/cilastatina, meropeném) ou um betalactâmico/inibidor de betalactamase (piperacilina/tazobactam) ou uma fluoroquinolona (ciprofloxacino, levofloxacino) ou um aminoglicosídeo (amicacina, gentamicina, tobramicina) ou uma polimixina (colistimetato), ou um carbapenêmico com um potente inibidor de betalactamase (imipeném/cilastatina/relebactam), ou uma cefalosporina com um inibidor de betalactamase (ceftazidima/avibactam, ceftolozana/tazobactam). A monoterapia com um único antibiótico deve ser suficiente. No entanto, 2 medicamentos podem ser combinados se a infecção estiver localizada em uma área de difícil penetração, como um abscesso pulmonar, um empiema ou uma endocardite concomitante. Esquemas combinados poderiam consistir em uma cefalosporina (cefepima, ceftazidima), um carbapenêmico (imipeném/cilastatina, meropeném) ou um inibidor de betalactamases (piperacilina/tazobactam), associados a uma fluoroquinolona (ciprofloxacino, levofloxacino), um aminoglicosídeo (amicacina, gentamicina, tobramicina) ou uma polimixina (colistimetato). Ceftazidima/avibactam foi aprovado para pneumonia hospitalar e pneumonia associada à ventilação mecânica (PAVM) em decorrência de bactérias em pacientes adultos.[80] Apresenta atividade contra patógenos Gram-negativos resistentes a múltiplos medicamentos, incluindo bactérias produtoras de BLEE e Pseudomonas aeruginosa. Para evitar a resistência global, agentes combinados de cefalosporina/inibidor de betalactamase e carbapenêmicos deve ser reservado a pacientes com infecções comprovadas ou fortemente suspeitas de serem causadas por bactérias suscetíveis ou a pacientes de alto risco com resistência a múltiplos medicamentos.[92]
Tradicionalmente, qualquer infecção pseudomônica era tratada com dois antibióticos. Um estudo de 1989, avaliando pacientes com bacteremia por Pseudomonas e incluindo alguns pacientes com pneumonia, mostrou uma mortalidade inferior entre os que receberam a terapia combinada.[89] Desde então, os estudos mostraram que os resultados são semelhantes entre pacientes com pneumonia hospitalar que recebem terapia simples ou terapia combinada.[93][94][95] Os benefícios da monoterapia incluem menos eventos adversos, menor resistência e um custo mais baixo.
Um exemplo de um patógeno Gram-positivo que é uma causa comum de pneumonia hospitalar é o S aureus. As cepas sensíveis à meticilina são tratadas com penicilina ou cefalosporina. Se o paciente for alérgico às penicilinas, podem ser usados linezolida ou vancomicina. As cepas resistentes à meticilina são tratadas com linezolida ou vancomicina.
Se Enterobacterales produtoras de BLEE forem a causa da pneumonia hospitalar, o tratamento de primeira linha recomendado será um antibiótico carbapenêmico. O tratamento de segunda linha é com uma fluoroquinolona.[96] Na prática, um tratamento de terceira linha é com um inibidor de carbapenêmico/betalactamase ou cefiderocol. Ceftolozane/tazobactam também tem atividade contra algumas BLEEs. Uma causa raramente identificada da pneumonia hospitalar é o L pneumophila. O tratamento pode ser feito com uma fluoroquinolona ou um macrolídeo.
Duração da terapia
Anteriormente, o uso do Clinical Pulmonary Infection Score (CPIS) era recomendado para auxiliar na decisão sobre se o tratamento deve ser ajustado ou descontinuado.[97]
No entanto, dados agrupados de estudos de acurácia mostraram evidências fracas para desencorajar o uso do CPIS para confirmar ou descartar PAVM, ou para determinar a duração da terapêutica antimicrobiana.[1][98]
A recomendação mais recente para a duração da antibioticoterapia é que ela pode ser concluída em 7 dias se o paciente estiver clinicamente e radiologicamente estável, incluindo os valores laboratoriais, e não estiver infectado com Acinetobacter ou P aeruginosa; o CPIS não precisa ser usado.[1][75][99] Não existem dados que justifiquem uma terapia mais longa para MRSA, embora essa prática seja frequente; o tratamento deve ser de 2 semanas, se houver bacteremia, e mais longo se a pneumonia hospitalar/PAVM estiver associada a uma complicação, como um empiema ou endocardite. Pacientes que receberam 7 a 8 dias de antimicrobianos tiveram PAVM menos recorrente devido a patógenos resistentes a múltiplos medicamentos e não houve diferenças na mortalidade, tempo de hospitalização, fracasso do tratamento, e tempo de intubação e ventilação mecânicas.[100][101]
[  ]
[Evidência B] Os Centros de Controle e Prevenção de Doenças (CDC) dos EUA recomendam otimizar a seleção de antibióticos e reavaliar o tratamento com antibióticos quando os resultados dos testes de diagnóstico estiverem disponíveis. O CDC também aconselha a usar a duração efetiva mais curta da terapia, em vez de administrar ciclos prolongados de antibióticos (que historicamente tem sido a abordagem para o tratamento da pneumonia hospitalar).[102] Consequentemente, a maioria dos tratamentos para pneumonia hospitalar pode ter duração mais curta, mas a pneumonia hospitalar decorrente de Pseudomonas ou Acinetobacter ainda deve ser tratada por 2 semanas.[99]
]
[Evidência B] Os Centros de Controle e Prevenção de Doenças (CDC) dos EUA recomendam otimizar a seleção de antibióticos e reavaliar o tratamento com antibióticos quando os resultados dos testes de diagnóstico estiverem disponíveis. O CDC também aconselha a usar a duração efetiva mais curta da terapia, em vez de administrar ciclos prolongados de antibióticos (que historicamente tem sido a abordagem para o tratamento da pneumonia hospitalar).[102] Consequentemente, a maioria dos tratamentos para pneumonia hospitalar pode ter duração mais curta, mas a pneumonia hospitalar decorrente de Pseudomonas ou Acinetobacter ainda deve ser tratada por 2 semanas.[99]
Se nenhuma melhora for observada nesse período, deve-se considerar alterar o esquema de antibioticoterapia para cobrir patógenos resistentes ou incomuns (por exemplo, fúngicos). No entanto, também é importante avaliar a possibilidade de outros eventos pulmonares, como reconsiderar a natureza da efusão como exsudato (por exemplo, empiema) em vez de transudato. Também é importante avaliar outras fontes não pulmonares de infecção. Um procedimento não considerado anteriormente pode ser indicado, como ultrassonografia de membros com um acesso intravenoso para descartar a tromboflebite séptica. Pode ser necessário repetir uma broncoscopia ou toracocentese. Em geral, o fracasso do tratamento pode ser devido a:[103]
Uma complicação
Um diagnóstico errado
Tratamento do patógeno errado.
Estratégias como alterar as configurações do ventilador para suporte de pressão ou usar um modo oscilatório podem ser consideradas pelo médico especialista em respiração.
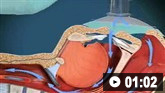
Como dimensionar e inserir a máscara laríngea de via aérea.
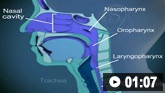
Como selecionar a via aérea nasofaríngea do tamanho correto e inserir o dispositivo de via aérea corretamente.
Como dimensionar e inserir uma via aérea orofaríngea.
Como inserir um tubo traqueal em um adulto usando um laringoscópio.
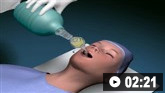
Como usar um aparato reanimador manual autoinflável para fornecer suporte ventilatório a adultos. Vídeo de demonstração da técnica em duas pessoas.
Resposta ao tratamento
A procalcitonina pode ser usada para monitorizar qual a tendência dos valores desde o dia do diagnóstico.[110] Essa informação pode ser usada para determinar quando descontinuar os antimicrobianos.[1]
Como dimensionar e inserir a máscara laríngea de via aérea.
O uso deste conteúdo está sujeito ao nosso aviso legal