Abordagem
O tratamento atual de trombose venosa profunda (TVP) se baseia em uma abordagem diagnóstica algorítmica. A história e o exame físico são relativamente insensíveis e inespecíficos, então devem ser combinados com outros exames diagnósticos no processo de tomada de decisões clínicas. A confirmação do diagnóstico requer a documentação de um coágulo sanguíneo em um vaso profundo na perna, pelve ou veia cava por um estudo de imagem (ultrassonografia duplex ou estudo com contraste vascular, como a venografia por tomografia computadorizada [TC]). No entanto, a suspeita de TVP frequentemente pode ser descartada sem um estudo de imagem, evitando a despesa (e os riscos de radiação e contraste da venografia). Portanto, a primeira etapa ao fazer o diagnóstico de TVP é estabelecer a probabilidade de a TVP estar presente usando um modelo de avaliação de risco, como o baseado no escore de Wells combinado com um nível de dímero D. Com o uso dessa abordagem, mais de um terço dos pacientes com suspeita de TVP pode ter o diagnóstico descartado com segurança sem o uso de imagens.[86]
História
Informações essenciais incluem a presença ou ausência de uma história prévia de TVP ou embolia pulmonar (EP), além de recente exposição a quaisquer dos fatores de risco precipitantes comuns (consultar a seção Fatores de risco).
O paciente pode relatar sintomas de edema na panturrilha (ou, mais raramente, edema em todo o membro inferior), dor localizada ao longo do sistema venoso profundo, edema ou veias superficiais dilatadas nos pés e nas pernas. Os sintomas variam de graves a muito sutis, e os pacientes podem ser assintomáticos.
Sinais e exame físico
O edema dos membros inferiores unilateral pode ser avaliado ao medir a circunferência do membro inferior 10 cm abaixo da tuberosidade tibial. Qualquer diferença entre o membro inferior sintomático e o assintomático aumenta a probabilidade de TVP e uma diferença de >3 cm entre os membros aumenta mais a probabilidade.
Pode haver edema e veias superficiais colaterais dilatadas no lado afetado. Pode haver sensibilidade ao longo do caminho das veias profundas (compressão da panturrilha posterior, compressão da fossa poplítea e compressão ao longo da coxa anterior interna a partir da virilha até o canal adutor).
Duas manobras de exame físico que foram ensinadas historicamente – sensibilidade com dorsiflexão do pé (sinal de Homans) ou dor na panturrilha à palpação (sinal de Pratt) – podem estar presentes; no entanto, eles têm baixa sensibilidade e especificidade e não são um componente dos modelos atuais de avaliação de risco.[87]
Com uma alta carga de trombose, especialmente nas veias ilíacas e femorais, o edema pode obstruir o fluxo venoso profundo e superficial, bem como o influxo arterial, levando à flegmasia cerulea dolens. Aqui, o membro inferior está edemaciado e dolorido, e também aparenta estar isquêmico.
Os sinais de TVP não são específicos e também podem ocorrer em outras condições, como um cisto poplíteo grande ou rompido (cisto de Baker), celulite e trauma ou lesão musculoesqueléticos (sangramento ou hematoma da panturrilha, ruptura do tendão de Aquiles ou ruptura do tendão plantar).[88] Em muitos pacientes, o diagnóstico de celulite ou lesão musculoesquelética é simples, mas a TVP pode coexistir com essas afecções.
Probabilidade pré-teste (critérios de Wells)
Existem vários modelos de avaliação de risco disponíveis para avaliar a probabilidade clínica de TVP; no entanto, o escore de Wells fornece um método para determinar a probabilidade clínica de TVP e é a ferramenta de probabilidade pré-teste mais amplamente aceita usada em algoritmos de diagnóstico de TVP.[89][90] [ Escore de Wells modificado para trombose venosa profunda (TVP) Opens in new window ]
[Figure caption and citation for the preceding image starts]: Escore de WellsMazzolai L, et al. Diagnosis and management of acute deep vein thrombosis. Eur Heart J. 2018 Dec 14;39(47):4208-18 [Citation ends].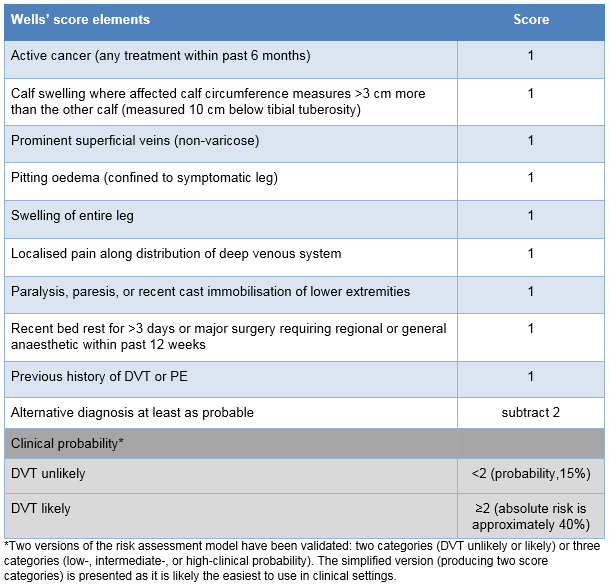
Nível quantitativo de dímero D
O nível de dímero D é indicado em todos os pacientes com escore de Wells <2. Dímero D é um produto de metabolização da fibrina com ligação cruzada; portanto, se houver um coágulo agudo, o nível de dímero D provavelmente estará elevado. Um teste de dímero D quantitativo ou altamente sensível é, portanto, útil para descartar a presença de um TVP aguda. No entanto, um nível elevado de dímero D é inespecífico e frequentemente anormal em pacientes mais velhos, agudamente enfermos, com doenças hepáticas subjacentes, com infecção ou gestantes. Há muitos testes disponíveis para dímero D, mas os melhores são os testes de ensaio de imunoadsorção enzimática altamente sensíveis. Cada um dos testes disponíveis no mercado têm seu próprio valor de corte. O dímero D pode ser relatado em unidades diferentes, portanto, o valor de corte específico para o teste que está sendo usado deve ser anotado.[91]
Um valor normal descarta o diagnóstico de TVP em um paciente com baixa probabilidade clínica de apresentar TVP (ou seja, um escore de Wells <2). Esse alto valor preditivo negativo é útil para reduzir a necessidade de novas imagens sem valor ou da anticoagulação imediata com seus riscos associados. Um teste de dímero D elevado e anormal, quando combinado com uma baixa probabilidade clínica de TVP, deve levar o médico a prosseguir com os exames de imagem.
Independentemente do grupo de pacientes, o dímero D tem um baixo valor preditivo positivo. As abordagens para mitigar a baixa especificidade do dímero D incluíram o ajuste do valor de corte com base na idade do paciente (por exemplo, idade [anos] × 10 microgramas/L [usando ensaios de dímero D com um corte de 500 microgramas/L] em pacientes >50 anos) ou pela probabilidade pré-teste de TVP (se estiver usando um modelo de avaliação de risco com três categorias).[92][93]
Ultrassonografia duplex (DUS) venosa
A DUS venosa é o teste de primeira linha recomendado em todos os pacientes com um escore de Wells igual ou maior que 2, ou em pacientes com um escore de Wells <2 que têm um nível elevado de dímero D. O diagnóstico de coágulo agudo se baseia na incapacidade de retrair por completo as paredes da veia no plano transversal ao pressionar a veia com um transdutor (a presença do trombo impede a compressão).[Figure caption and citation for the preceding image starts]: Plano ultrassonográfico de eixo curto exibindo a veia femoral e a veia femoral profunda adjacentes à artéria femoral antes (à esquerda) e após (à direita) a compressãoDo acervo de Jeffrey W. Olin; usado com permissão [Citation ends].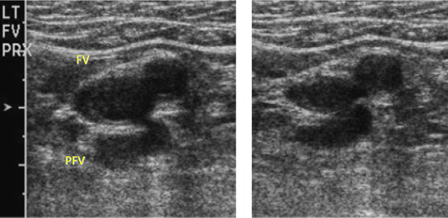
Existem duas técnicas bem validadas para realizar a ultrassonografia venosa do membro inferior. A ultrassonografia de todo o membro inferior avalia as veias da coxa e da panturrilha. Leva mais tempo para ser realizado, é tecnicamente mais exigente e identifica TVP da veia da panturrilha, que pode se resolver sem tratamento (portanto, pode levar a um diagnóstico excessivo e potencialmente a um tratamento excessivo com anticoagulação, sujeitando o paciente a possíveis complicações hemorrágicas). No entanto, é capaz de chegar a uma conclusão diagnóstica em uma única sessão. A DUS proximal avalia apenas as veias acima da panturrilha. Embora mais rápida e mais simples, se negativa, deve ser repetida 5 a 7 dias depois para descartar quaisquer TVPs na veia da panturrilha não detectadas que se propagaram em direção proximal.
A taxa posterior de tromboembolismo venoso após uma avaliação diagnóstica negativa não parece diferir significativamente entre a ultrassonografia de todo o membro inferior e a ultrassonografia proximal serial.[94]
Algoritmo de diagnóstico para TVP
Por enquanto, a melhor forma de excluir TVP é estabelecer que a probabilidade clínica de TVP é baixa combinada com um nível normal de dímero D usando um teste altamente sensível. Uma única ultrassonografia de todo o membro inferior negativa ou duas DUS proximais negativas descartam com segurança o diagnóstico se dímero D estiver elevado ou o escore de Wells for ≥2. O exame de imagem confirma o diagnóstico de TVP.
[Figure caption and citation for the preceding image starts]: Algoritmo para o diagnóstico da trombose venosa profundaCriado pelo BMJ Knowledge Centre [Citation ends].
Outros testes
Outros exames laboratoriais raramente têm algum valor no diagnóstico de TVP aguda. Ocasionalmente, os exames laboratoriais podem indicar uma causa subjacente de uma TVP recém-diagnosticada, como anormalidades que sugerem a presença de uma malignidade (por exemplo, anemia ou leucopenia no hemograma completo). Uma alta contagem plaquetária pode sugerir trombocitose essencial ou doença mieloproliferativa. Contagem plaquetária basal, tempo de tromboplastina parcial ativada, razão normalizada internacional, ureia e creatinina são importantes antes de iniciar a anticoagulação, dependendo do agente anticoagulante escolhido para a terapia. Os testes da função hepática podem detectar anormalidades, impossibilitando o uso de certos anticoagulantes porque alguns não são aprovados em vários graus de disfunção hepática.
Dopplerfluxometria colorida e onda de pulso são às vezes realizadas em conjunto com uma ultrassonografia em modo B. Os achados podem incluir fluxo espontâneo reduzido ou ausente, ausência de variação respiratória, ecos intraluminais ou anormalidades de patência do fluxo colorido. Uma sonda curvilínea pode ser usada para tentar visualizar as veias ilíacas, mas essa modalidade não permite a compressão. A ausência de variações respiratórias na onda de pulso do Doppler levanta a suspeita de uma obstrução venosa proximal. O exame tem baixa sensibilidade (75%) e especificidade média (85%).[95][96] A TC com contraste (venografia por TC) pode ser mais precisa do que a ultrassonografia na detecção de trombose em veias maiores do abdome e pelve, e pode ser utilizada quando a trombose proximal é clinicamente suspeita ou sugerida por padrões de fluxo na ultrassonografia com Doppler.[95]
Gestação
A suspeita clínica de TVP em gestantes é desafiadora devido à sobreposição dos sintomas associados a gestação e trombose. Além disso, há uma prevalência maior de trombose da veia ilíaca em gestantes em comparação com pacientes não gestantes, o que pode fazer com que o diagnóstico preciso seja ainda mais desafiador.[97] O ensaio de dímero D tem uma função limitada na gestação devido a seu aumento natural em cada trimestre.[98] No entanto, um teste de dímero D negativo pode ser útil para descartar um diagnóstico de TVP nesses pacientes.[99] O escore de Wells não foi validado na população gestante e, portanto, não deve ser usado rotineiramente para estratificar o risco de uma paciente gestante com suspeita de TVP. Uma regra de predição clínica, chamada escore LEFt, foi desenvolvida especificamente para a população gestante. Essa regra ainda precisa ser mais rigorosamente validada e não deve ser usada como rotina.[100] O diagnóstico correto dependerá de um alto índice de suspeita e do acompanhamento rigoroso. A DUS venosa continua sendo o teste inicial de escolha para gestantes com suspeita de TVP. Vários estudos que investigam o papel de uma única ultrassonografia de todo o membro inferior ou ultrassonografia de compressão proximal em série para o diagnóstico de TVP foram reunidos em uma metanálise.[101][102][103][104][105] A taxa de falsos-negativos dessa abordagem é baixa, mas o número absoluto de pacientes incluídas nos ensaios é modesto. Por causa da prevalência maior de trombos da veia pélvica isolados nessas pacientes, as diretrizes também recomendam um baixo limite para obter imagens adicionais (por exemplo, ultrassonografia da veia ilíaca ou venografia por ressonância magnética abdominal) nas pacientes com suspeita de trombose venosa abdominal/pélvica (isto é, edema do membro inferior, das nádegas ou dorsalgia).[22]
Testes para doenças subjacentes
Em um paciente com TVP objetivamente documentada, é importante estratificar o paciente como tendo uma TVP com fatores precipitantes (secundária a fatores de risco conhecidos e identificados) ou sem fatores precipitantes (idiopática, portanto nenhum fator de risco conhecido identificado). Os pacientes com TVP sem fatores precipitantes não apresentam história clara de fatores precipitantes (por exemplo, grande trauma no membro inferior, cirurgia recente, câncer ativo, imobilização recente). É mais fácil definir uma TVP com fatores precipitantes, pois vários fatores de risco são conhecidos e amplamente usados para sua definição. Fatores de risco fortes e fracos (fatores precipitantes) para TVP são detalhados na seção Fatores de risco.
O câncer oculto está presente em aproximadamente 3% a 5% dos pacientes com TVP sem fatores precipitantes.[106] No entanto, investigações extensivas (além dos exames laboratoriais de rotina e rastreamento de rotina apropriado para a idade) para câncer em pacientes com primeiro TVP sem fatores precipitantes não são indicadas rotineiramente, pois não demonstraram melhorar o prognóstico ou a mortalidade.[107][108][109] Sinais ou sintomas que sugerem uma possível malignidade devem ser investigados, se presentes.
Normalmente, a trombofilia refere-se a cinco condições hereditárias (fator V de Leiden, gene da protrombina 20210A, deficiências de antitrombina, deficiência de proteína C e deficiência de proteína S) e à síndrome antifosfolipídica (uma doença adquirida). No entanto, muitas variantes genéticas e doenças adquiridas alteram o risco de trombose.[110] As indicações para rastreamento são controversas.[110][111] A trombofilia hereditária não altera de maneira suficiente o risco predito de trombose recorrente para afetar as decisões de tratamento, e uma abordagem conservadora à testagem é razoável.[14] Algumas diretrizes sugerem a testagem apenas nas situações em que o resultado provavelmente alterará uma decisão clínica (por exemplo, nos pacientes com TVP sem fatores precipitantes que estejam considerando interromper os anticoagulantes).[15] No entanto, a presença de uma trombofilia hereditária não aumenta de maneira significativa o risco predito de tromboembolismo venoso recorrente após uma TVP com fatores precipitantes, e as diretrizes desestimulam a testagem neste cenário.[112]
Os anticorpos antifosfolipídeos podem predizer um risco mais alto de trombose futura após um evento de tromboembolismo venoso inicial e podem afetar a escolha da terapia anticoagulante.[44] Se deve haver preferência pelo rastreamento amplo ou pelo rastreamento apenas com base na suspeita clínica é controverso.[113][114] Algumas diretrizes sugerem a testagem apenas nas situações em que o resultado provavelmente alterará uma decisão clínica (por exemplo, em pacientes com TVP sem fatores precipitantes que estiverem considerando interromper os anticoagulantes).[15] Uma diretriz da American Society of Hematology descreve circunstâncias limitadas nas quais os testes para trombofilias hereditárias individuais (ou um conjunto delas) podem ter utilidade, e sugere o impacto da informação sobre as decisões clínicas.[41]
O rastreamento para trombofilia não é indicado em todos os casos de eventos tromboembólicos venosos; no entanto, ele pode ser útil se o local do trombo for incomum, se houver uma grande carga trombótica ou se houver eventos recorrentes. Caso o exame de trombofilia hereditária seja indicado, ele deve ser adiado até, pelo menos, 3 meses de terapia anticoagulante, pois alguns exames de trombofilia são influenciados pela presença de trombose aguda ou de terapia anticoagulante.[110] Para o rastreamento da síndrome antifosfolipídica, os anticorpos anticardiolipina e antibeta 2-glicoproteína I podem ser realizados independentemente da presença de anticoagulantes, mas a maioria dos anticoagulantes interfere nos ensaios de anticoagulante lúpico.[44]
Suspeita de EP
Em pacientes com TVP documentada que serão ou estão sendo tratados de maneira padrão com heparina ou heparina de baixo peso molecular seguida por varfarina ou com um anticoagulante oral direto, como apixabana, rivaroxabana, edoxabana ou dabigatrana por uma duração total de menos de 3 meses, não há indicação de rotina para documentar a presença de EP. No entanto, testes para EP devem ser considerados se houver sinais clínicos ou sintomas que levantem a possibilidade de EP e houver comprometimento cardiopulmonar clinicamente importante, incluindo hipotensão, síncope, sintomas de insuficiência cardíaca direita ou agravamento de hipóxia, pois terapias adicionais (por exemplo, terapias de reperfusão) podem ser indicadas.
Os testes mais comuns para o diagnóstico de EP são a angiotomografia pulmonar de sequência rápida ou cintilografia de ventilação/perfusão pulmonar. Este último é mais frequentemente usado em pacientes com insuficiência renal ou alergia ao contraste iodado.
Consulte nosso tópico Embolia pulmonar para obter informações detalhadas sobre diagnóstico e tratamento.
O uso deste conteúdo está sujeito ao nosso aviso legal