ჰემოდინამიკურად არასტაბილურ პაციენტებს ესაჭიროებათ გადაუდებელი პირველადი რეპერფუზია, ანტიკოაგულაცია და დამხმარე მოვლა.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ცუდი შედეგის შუალედური რისკის მქონე პაციენტებისთვის საჭიროა ანტიკოაგულაცია და მუდმივი მონიტორინგი. რეპერფუზია ჩვეულებრივ გამოიყენება როგორც სამაშველო თერაპია, თუ მოხდება დეკომპენსაცია.
ცუდი შედეგის დაბალი რისკის მქონე პაციენტების მართვა შესაძლებელია ამბულატორიულად, პაციენტის პირადი გარემოებების გათვალისწინებით და რამდენადაც დაკმაყოფილებულია ყველა შემდეგი კრიტერიუმი:[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
კლინიკურად სტაბილური კარგი კარდიოპულმონარული რეზერვით
არ არსებობს უკუჩვენებები, როგორიცაა ბოლოდროინდელი სისხლდენა, თირკმლის ან ღვიძლის მძიმე დაავადება, ან მძიმე თრომბოციტოპენია (ანუ <50,000/მმ³)
მკურნალობაზე ცუდი დამყოლობა
პაციენტი თავს კარგად გრძნობს იმისთვის, რომ მკურნალობდეს სახლში.
პაციენტებმა, რომლებსაც შემთხვევით დაუსვეს ასიმპტომური PE-ს დიაგნოზი, უნდა მიიღონ იგივე საწყისი და გრძელვადიანი ანტიკოაგულაცია, როგორც მსგავსი სიმპტომური PE. დროს.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
გამწვავების კლასიფიკაცია
PE-ის სიმძიმის აღსაწერად გამოყენებულია რამდენიმე კლასიფიკაციის სისტემა და მოკლევადიანი სიკვდილიანობა შეიძლება შეფასდეს კლინიკური პროგნოზირების ხელსაწყოებით, როგორიცაა ფილტვის ემბოლიის სიმძიმის ინდექსი (PESI) ან გამარტივებული PESI ქულები.[154]Tong C, Zhang Z. Evaluation factors of pulmonary embolism severity and prognosis. Clin Appl Thromb Hemost. 2015 Apr;21(3):273-84.
https://www.doi.org/10.1177/1076029613501540
http://www.ncbi.nlm.nih.gov/pubmed/24023267?tool=bestpractice.com
ტერმინი "submassive" გამოიყენება PE-ზე მნიშვნელოვანი ანატომიური მასშტაბით, მაგრამ ნორმოტენზიით და მასიური აღწერს ანატომიურად ვრცელ PE-ს, რომელიც გართულებულია შოკით ან ჰიპოტენზიით.
ევროპის კარდიოლოგთა საზოგადოება PE-ს კატეგორიებად აქცევს:
მაღალი რისკი ჰემოდინამიკური არასტაბილურობის დროს (შოკი ან ჰიპოტენზია)
საშუალო-მაღალი რისკი ჰემოდინამიკური არასტაბილურობის გარეშე,მაგრამ მარჯვენა პარკუჭის (RV) დისფუნქციის ვიზუალიზაციის ნიშნებით,გულის ანომალური ბიომარკერებით სიმძიმის კლინიკური მარკერებითმაგ. PESI მაღალი მაჩვენებლებით)
საშუალო-მაღალი რისკი ჰემოდინამიკური არასტაბილურობის გარეშე,მაგრამ მარჯვენა პარკუჭის (RV) დისფუნქციის ვიზუალიზაციის ნიშნებით,გულის ანომალური ბიომარკერებით სიმძიმის კლინიკური მარკერებით,მაგ. PESI მაღალი მაჩვენებლებით)
დაბალი რისკი, როდესაც არცერთი ეს ფაქტორი არ არსებობს.
შესაძლო ფილტვის ემბოლია შოკთან ან ჰიპოტენზიასთან ერთად
მაღალი რისკის ქვეშ მყოფი პაციენტები (რომლებიც წარმოდგენილი არიან შოკით ან ჰიპოტენზიით [სისტოლური არტერიული წნევა არის <90 მმ.ვწყ.სვ.]) საჭიროებენ აგრესიულ მკურნალობას პირველადი რეპერფუზიით, ანტიკოაგულაციით და დამხმარე თერაპიით.
აუცილებელია დამხმარე თერაპიებისა და ემპირიული ანტიკოაგულაციის (გარდა უკუჩვენებისა) დაუყოვნებლივი ჩატარება.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ამ პოპულაციაში შეიძლება სასურველი იყოს არაფრაქციული ჰეპარინი (UFH); ინტერვენციული თერაპიის კლინიკური კვლევების უმეტესობამ გამოიყენა ჰეპარინი, როგორც რეჟიმის ანტიკოაგულანტული კომპონენტი.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
დამხმარე თერაპია
საჭიროა ადგილობრივი პროტოკოლის გათვალისწინება.
სუნთქვის დახმარება
საჭიროა მაღალი კონცენტრაციის ჟანგბადის დანამატის მიწოდება ჟანგბადით გაჯერების სამიზნე 94-98%-იანი მაჩვენებლით (ან 88-92% იმ პაციენტებში, რომლებიც იმყოფებიან ჰიპერკაპნური სუნთქვის უკმარისობის რისკის ქვეშ).[155]O'Driscoll BR, Howard LS, Earis J, et al; British Thoracic Society Emergency Oxygen Guideline Group; BTS Emergency Oxygen Guideline Development Group. BTS guideline for oxygen use in adults in healthcare and emergency settings. Thorax. 2017 Jun;72(Suppl 1):ii1-90.
https://www.brit-thoracic.org.uk/document-library/clinical-information/oxygen/2017-emergency-oxygen-guideline/bts-guideline-for-oxygen-use-in-adults-in-healthcare-and-emergency-settings
http://www.ncbi.nlm.nih.gov/pubmed/28507176?tool=bestpractice.com
ინტუბაცია და მექანიკური ვენტილაცია შესაძლოა საჭირო გახდეს მძიმე ფორმის ჰიპოქსიის/სუნთქვის უკმარისობის მქონე პაციენტებში. მექანიკურმა ვენტილაციამ შესაძლოა გამოიწვიოს ჰიპოტენზია, შესაბამისად, აუცილებელია არტერიული წნევის მჭიდრო მონიტორინგი.
ინტრავენური სითხეები
თუ სისტოლური BPარის <90 მმ.ვწყ.სვ უნდა მოხდეს ინტრავენურად სითხეების შეყვანა. მარჯვენა პარკუჭოვანი მწვავე უკმარისობა შედეგად დაბალ სისტემურ წუთმოცულობასთან ერთად არის ფილტვის ემბოლიის მქონე პაციენტებში სიკვდილობის მთავარი გამომწვევი მიზეზი.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
კვლევები მიუთითებს, რომ მოცულობის აგრესიული გაფართოება არ არის სარგებელის მომტანი და შესაძლოა გააუარესოს მარჯვენა პარკუჭოვანი ფუნქცია მექნიკური გაფართოების ან რეფლექს მექანიზმის გამოყენება, რომელიც თრგუნავს კუმშვადობას. მიუხედავად ამისა, სითხის უმნიშვნელო საცდელი გადასხმა (500 მლ) შესაძლოა დამხმარე იყოს ფილტვის ემბოლიის, გულის დაბალი ინდექსისა და ნორმალური წნევის მქონე პაციენტებში.[159]Mercat A, Diehl JL, Meyer G, et al. Hemodynamic effects of fluid loading in acute massive pulmonary embolism. Crit Care Med. 1999 Mar;27(3):540-4.
http://www.ncbi.nlm.nih.gov/pubmed/10199533?tool=bestpractice.com
ვაზოაქტიური აგენტები
თუ სისტოლური არტერიული წნევა არის <90 მმ.ვწყ.სვ. ვაზოპრესორების გამოყენება შესაძლებელია ფარმაკოლოგიური, ქირურგიული ან ინტერვენციული რეპერფუზიის მკურნალობის პარალელურად (ან მოცდის პერიოდში).[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
ნორადრენალინმა (ნორეპინეფრინი) შესაძლოა გააუმჯობესოს მარჯვენა პარკუჭის ფუნქცია და მარჯვენა პარკუჭის კორონარული პერფუზია.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
თუმცა, მისი გამოყენება სავარაუდოდ შეზღუდული უნდა იყოს ჰიპოტენზიური პაციენტებისთვის.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
დობუტამინი აძლიერებს გულის კუმშვადობას დარტყმის მოცულობის და წუთმოცულობის გაზრდის მეშვეობით. თუმცა პრეპარატის სისტემურმა ვაზოდილატაციურმა ეფექტმა შესაძლოა გამოიწვიოს ჰიპოტენზია.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
ადრენალინი (ეპინეფრინი) ხასიათდება როგორც ნორადრენალინის (ნორეპინეფრინი) (ვაზოკონსტრიქცია მარჯვენა პარკუჭის მომატებულ პერფუზიასთან ერთად, დადებითი ინოტროპიზმი), ასევე დობუტამინის (პოზიტიური ინოტროპიზმი) სასარგებლო თვისებებით, თუმცა იგი არ ავლენის დობუტამინის ვაზოდილატაციურ ეფექტებს.[160]Layish DT, Tapson VF. Pharmacologic hemodynamic support in massive pulmonary embolism. Chest. 1997 Jan;111(1):218-24.
http://www.ncbi.nlm.nih.gov/pubmed/8996020?tool=bestpractice.com
ანტიკოაგულაციის ინიცირების ფაზა (5-21 დღე)
პაციენტებს, რომლებიც წარმოდგენილნი არიან შესაძლო ფილტვის ემბოლიით, უნდა მიეწოდოთ ანტიკოაგულანტი მწვავე ფაზაში (ფილტვის ემბოლიის დიაგნოზიდან საწყისი 10 დღე), გარდა უკუჩვენებისა.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[161]Willoughby L, Adams DM, Evans RS, et al. Preemptive anticoagulation in patients with a high pretest probability of pulmonary embolism: are guidelines followed? Chest. 2018 May;153(5):1153-9.
https://www.doi.org/10.1016/j.chest.2017.11.007
http://www.ncbi.nlm.nih.gov/pubmed/29154971?tool=bestpractice.com
თუ ფილტვის ემბოლია გამოირიცხა, შესაძლოა ანტიკოაგულაციის შეწყვეტა. თუ ფილტვის PE ემბოლია გამოირიცხა, შესაძლოა ანტიკოაგულაციის შეწყვეტა. დადასტურებული ფილტვის ემბოლიის მქონე პაციენტებმა უნდა გააგრძელონ ანტიკოაგულაციის მიღება სულ მცირე 3 თვის განმავლობაში.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[95]Konstantinides SV, Barco S, Lankeit M, et al. Management of pulmonary embolism: an update. J Am Coll Cardiol. 2016 Mar 1;67(8):976-90.
http://www.onlinejacc.org/content/67/8/976
http://www.ncbi.nlm.nih.gov/pubmed/26916489?tool=bestpractice.com
პარენტელარული ანტიკოაგულაცია
საწყისი ფაზის პარენტერალური ანტიკოაგულაცია უნდა დაიწყოს პაციენტებში მაღალი ან შუალედური კლინიკური (პრე-ტესტი) PE ალბათობით, დიაგნოსტიკური გამოსახულების შედეგების მოლოდინში. თუ ინიშნება პარენტერალური ანტიკოაგულანტი (UFH, დაბალი მოლეკულური წონის ჰეპარინი [LMWH] ან ფონდაპარინუქსი), ის უნდა ემთხვეოდეს K ვიტამინის ანტაგონისტის (VKA) დაწყებას. პარენტერალური ანტიკოაგულაცია UFH-ით მინიმუმ 5 დღის განმავლობაში რეზერვირებულია მაღალი რისკის PE-ს მქონე პაციენტებისთვის, რომლებშიც განიხილება პირველადი რეპერფუზია (ანუ სისტემური თრომბოლიზური თერაპია ან ემბოლექტომია).[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
საშუალო-მაღალი ან საშუალო-დაბალი რისკის მქონე პაციენტებში PE, LMWH ან ფონდაპარინუქსი არის სასურველი პარენტერალური ანტიკოაგულანტები დაწყების ფაზაში ძირითადი სისხლდენის დაბალი სიხშირის და ჰეპარინით გამოწვეული თრომბოციტოპენიის გამო.
პარენტერალური ანტიკოაგულაციის შეწყვეტა შესაძლებელია მას შემდეგ, რაც დამყარდება საერთაშორისო თერაპიული ნორმალიზებული თანაფარდობა (INR) 2.0-დან 3.0-მდე და მინიმუმ 5 დღის გადახურვა VKA-სთან.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[95]Konstantinides SV, Barco S, Lankeit M, et al. Management of pulmonary embolism: an update. J Am Coll Cardiol. 2016 Mar 1;67(8):976-90.
http://www.onlinejacc.org/content/67/8/976
http://www.ncbi.nlm.nih.gov/pubmed/26916489?tool=bestpractice.com
UFH-ს აქვს ხანმოკლე ნახევარგამოყოფის პერიოდი, ადვილად კონტროლდება და ადვილად აბრუნებს პროტამინს.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
პირდაპირი მოქმედების მქონე პერორალური ანტიკოაგულანტი
ორი პირდაპირ მოქმედი პერორალური ანტიკოაგულანტის, რივაროქსაბანის და აპიქსაბანის გამოწერა შეგვიძლია პარენტერული ანტიკოაგულანტით წინასწარი მკურნალობის გარეშე. თუმცა, როგორც დაბიგატრანი, ასევე ედოქსაბანი საჭიროებენ წინასწარ თერაპიას პარენტერული ანტიკოაგულანტით 5-10 დღის განმავლობაში.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ერთ-ერთი მეტა ანალიზის მიხედვით გამოვლინდა, რომ პირდაპირი მოქმედების პერორალურ ანტიკოაგულანტებს გააჩნიათ ჰეპარინი/VKA ვიტამინის ანტაგონისტის რეჟიმის მსგავსი ეფექტიანობა, ამასთანავე მნიშვნელოვანი სისხლდენის შემცირებული რისკი (ფარდობითი რისკი 0.61, 95% კოაგულაციის ინდექსი 0.21-0.68).[95]Konstantinides SV, Barco S, Lankeit M, et al. Management of pulmonary embolism: an update. J Am Coll Cardiol. 2016 Mar 1;67(8):976-90.
http://www.onlinejacc.org/content/67/8/976
http://www.ncbi.nlm.nih.gov/pubmed/26916489?tool=bestpractice.com
[162]van Es N, Coppens M, Schulman S, et al. Direct oral anticoagulants compared with vitamin K antagonists for acute venous thromboembolism: evidence from phase 3 trials. Blood. 2014 Sep 18;124(12):1968-75.
http://www.bloodjournal.org/content/124/12/1968.long
http://www.ncbi.nlm.nih.gov/pubmed/24963045?tool=bestpractice.com
ანალოგიურად, ქსელის ანალიზმა გამოავლინა რამდენიმე სტატისტიკურად მნიშვნელოვანი განსხვავება LMWH/VKA კომბინაციასა და ანტიკოაგულანტების მკურნალობის სხვა სტრატეგიებს შორის (ვენური თრომბოემბოლიისთვის [VTE]); თუმცა, UFH/VKA შეიძლება იყოს ყველაზე ნაკლებად ეფექტური სტრატეგია და აპიქსაბანის დაწყება შეიძლება ასოცირებული იყოს სისხლდენის ყველაზე დაბალ რისკთან.[163]Castellucci LA, Cameron C, Le Gal G, et al. Clinical and safety outcomes associated with treatment of acute venous thromboembolism: a systematic review and meta-analysis. JAMA. 2014 Sep 17;312(11):1122-35.
https://www.doi.org/10.1001/jama.2014.10538
http://www.ncbi.nlm.nih.gov/pubmed/25226478?tool=bestpractice.com
DOAC არ საჭიროებს წამლის დონის ან ჰემოსტატიკური მონიტორინგს, აქვთ მოქმედების სწრაფი დაწყება და ხანმოკლე მოქმედება. ისინი არ ურთიერთქმედებენ საკვებთან, მაგრამ შეუძლიათ ურთიერთქმედება სხვა ფარმაკოთერაპიულ აგენტებთან და მოითხოვონ შრატის კრეატინინის მონიტორინგი. დეგიბატრანის უკუქცევა შესაძლებელია იდარუკიზუმაბით. ანდექსანეტ ალფა დამტკიცებულია აშშ-ის სურსათისა და წამლის სააგენტოს მიერ აპიქსაბანითა და რივაროქსაბანით მიმდინარე ანტიკოაგულაციის უკუქცევის მიზნით პაციენტებში, რომელთაც აღენიშნებათ სიცოცხლისთვის საშიში ან უკონტროლო სისხლდენა. ედოქსაბანის უკუქცევის ეფექტის მქონე აგენტი დღესდღეობით დამტკიცებული არ არის.
შეზღუდულია ან არ არსებობს მონაცემები, რომლებიც მხარს უჭერენ DOAC-ების გამოყენებას თრომბოლიზურ თერაპიასთან ერთად დაწყების ფაზაში. მას შემდეგ, რაც პაციენტი სტაბილიზდება, კლინიცისტებმა უნდა მიიღონ გადაწყვეტილება პაციენტების ამ პოპულაციაში მკურნალობის ფაზის ანტიკოაგულაციის ასარჩევად, როგორც მტკიცებულებების შეზღუდვის, ისე მოვლის პრაგმატიზმის გათვალისწინებით.
პაციენტთა განსაკუთრებული პოპულაცია
VKA რეკომენდებულია თირკმლის მძიმე უკმარისობის მქონე პაციენტებისთვის (კრეატინინის კლირენსი <30 მლ/წთ).[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
აპიქსაბანი ასევე შესაფერისია თირკმლის მძიმე დისფუნქციის ან თირკმლის დაავადების ბოლო სტადიის მქონე პაციენტებში გამოსაყენებლად, თუმცა ამ პაციენტების პოპულაციაში გამოყენების მტკიცებულება შეზღუდულია.[164]Pathak R, Pandit A, Karmacharya P, et al. Meta-analysis on risk of bleeding with apixaban in patients with renal impairment. Am J Cardiol. 2015 Feb 1;115(3):323-7.
https://www.doi.org/10.1016/j.amjcard.2014.10.042
http://www.ncbi.nlm.nih.gov/pubmed/25527282?tool=bestpractice.com
გულმკერდის ექიმთა ამერიკული კოლეჯი (ACCP) რეკომენდაციას უწევს აპიქსაბანს, ედოქსაბანს ან რივაროქსაბანს LMWH-ზე დაწყების ფაზაში აქტიური კიბოს მქონე პაციენტებში (კიბოსთან ასოცირებული თრომბოზი).[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
DOACs განსაკუთრებით ედოქსაბანი და რივაროქსაბანი) დაკავშირებულია კუჭ-ნაწლავის სისხლდენის უფრო მაღალ რისკთან, ვიდრე LMWH. კუჭ-ნაწლავის სანათურის კიბოს მქონე პაციენტებში, ACCP რეკომენდაციას უწევს აპიქსაბანს ან LMWH-ს, როგორც სასურველ აგენტს.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[  ]
How do low‐molecular‐weight heparin (LMWH), vitamin K agonists (VKAs), and direct oral anticoagulants (DOACs) compare for treatment of venous thromboembolism (VTE) in people with cancer?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2813/fullსწორი პასუხის ჩვენება ამერიკის ჰემატოლოგიის საზოგადოება (ASH) რეკომენდაციას უწევს რივაროქსაბანს, აპიქსაბანს ან LMWH-ს საწყისი ფაზის ანტიკოაგულაციისთვის აქტიური კიბოს მქონე პაციენტებში; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]Lyman GH, Carrier M, Ay C, et al. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv. 2021 Feb 23;5(4):927-74.
https://ashpublications.org/bloodadvances/article/5/4/927/475194/American-Society-of-Hematology-2021-guidelines-for
http://www.ncbi.nlm.nih.gov/pubmed/33570602?tool=bestpractice.com
]
How do low‐molecular‐weight heparin (LMWH), vitamin K agonists (VKAs), and direct oral anticoagulants (DOACs) compare for treatment of venous thromboembolism (VTE) in people with cancer?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2813/fullსწორი პასუხის ჩვენება ამერიკის ჰემატოლოგიის საზოგადოება (ASH) რეკომენდაციას უწევს რივაროქსაბანს, აპიქსაბანს ან LMWH-ს საწყისი ფაზის ანტიკოაგულაციისთვის აქტიური კიბოს მქონე პაციენტებში; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]Lyman GH, Carrier M, Ay C, et al. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv. 2021 Feb 23;5(4):927-74.
https://ashpublications.org/bloodadvances/article/5/4/927/475194/American-Society-of-Hematology-2021-guidelines-for
http://www.ncbi.nlm.nih.gov/pubmed/33570602?tool=bestpractice.com
LMWH სასურველია პაციენტებში ღვიძლის მძიმე უკმარისობით და კოაგულოპათია.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
ჯანდაცვის სპეციალისტებმა უნდა მიმართონ ეტიკეტს და/ან ადგილობრივ ფორმულებს, სანამ დანიშნავენ DOAC-ს თირკმლის ან ღვიძლის უკმარისობის მქონე პაციენტისთვის.
ფონდაპარინუქსი ატარებს ჰეპარინით განპირობებული თრომბოციტოპენიის (HIT) გამოწვევის დაბალ რისკს და, სავრაუდოდ, ეფექტურია ჰეპარინით განპირობებული თრომბოციტოპენიის შესაძლო ან დადასტურებული შემთხვევის მქონე პაციენტებისთვის.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[166]Kang M, Alahmadi M, Sawh S, et al. Fondaparinux for the treatment of suspected heparin-induced thrombocytopenia: a propensity score-matched study. Blood. 2015 Feb 5;125(6):924-9.
http://www.bloodjournal.org/content/125/6/924.long
http://www.ncbi.nlm.nih.gov/pubmed/25515959?tool=bestpractice.com
მისი გამოყენების უკუჩვენებაა თირკმელების ფუნქციის მძიმე დარღვევა.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
ორსულობა
დაბალმოლეკულური ჰეპარინი რეკომენდებულია ორსული ქალებისთვის (წონაზე მორგებული დოზა), ან შესაძლო ორსულობის დროს.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[167]Bates SM, Greer IA, Middeldorp S, et al. VTE, thrombophilia, antithrombotic therapy, and pregnancy. Antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest. 2012 Feb;141(2 Suppl):e691S-736S.
https://journal.chestnet.org/article/S0012-3692(12)60136-6/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/22315276?tool=bestpractice.com
ის არ გადადის პლაცენტის ბარიერს. როგორც წესი, საჭირო არ არის რუტინული მონიტორინგი.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[168]Royal College of Obstetricians and Gynaecologists. Reducing the risk of venous thromboembolism during pregnancy and the puerperium. Green-top guideline No. 37a. Apr 2015 [internet publication].
https://www.rcog.org.uk/globalassets/documents/guidelines/gtg-37a.pdf
[169]Bates SM, Rajasekhar A, Middeldorp S, et al. American Society of Hematology 2018 guidelines for management of venous thromboembolism: venous thromboembolism in the context of pregnancy. Blood Adv. 2018 Nov 27;2(22):3317-59.
https://www.doi.org/10.1182/bloodadvances.2018024802
http://www.ncbi.nlm.nih.gov/pubmed/30482767?tool=bestpractice.com
სხვა ანტიკოაგულანტებმა, მათ შორის VKAs, შეიძლება გაიარონ პლაცენტა ნაყოფზე გვერდითი ეფექტების თანმდევი რისკით.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
DOAC უკუნაჩვენებია ორსულობის დროს.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[170]Cohen H, Arachchillage DR, Middeldorp S, et al. Management of direct oral anticoagulants in women of childbearing potential: guidance from the SSC of the ISTH. J Thromb Haemost. 2016 Aug;14(8):1673-6.
https://www.doi.org/10.1111/jth.13366
http://www.ncbi.nlm.nih.gov/pubmed/27346676?tool=bestpractice.com
რეკომენდირებულია კლინიკური მეთვალყურეობა ანტიკოაგულაციის დროს პაციენტებში სუბსეგმენტური PE (ანუ უფრო პროქსიმალური ფილტვის არტერიების ჩართვა), რომელთაც არ აქვთ პროქსიმალური ღრმა ვენების თრომბოზი (DVT) ფეხებში და რომლებსაც აქვთ მორეციდივე VTE-ის დაბალი რისკი. კლინიკური მეთვალყურეობა გულისხმობს პაციენტების ინფორმირებას პროგრესირებადი თრომბოზის კლინიკური ნიშნებისა და სიმპტომების შესახებ, რომლებიც უნდა დააკვირდნენ და მათი არსებობის შემთხვევაში ხელახალი შეფასება.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
პირველადი რეპერფუზია შოკის ან ჰიპოტენზიის დროს
სისტემური თრომბოლიზური თერაპია (სასურველია ალტეპლაზა ან რეტეპლაზა; ტენექტეპლაზა არის ალტერნატივა) რეკომენდებულია ჰემოდინამიკური კომპრომისის მქონე პაციენტებში (შოკი, სისტოლური <90 მმ Hg ან ვაზოპრესორული მოთხოვნა სისტოლური არტერიული წნევის შესანარჩუნებლად >90 მმჰგ), რადგან პაციენტების ამ ჯგუფს აქვს მაღალი სიკვდილიანობა.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[95]Konstantinides SV, Barco S, Lankeit M, et al. Management of pulmonary embolism: an update. J Am Coll Cardiol. 2016 Mar 1;67(8):976-90.
http://www.onlinejacc.org/content/67/8/976
http://www.ncbi.nlm.nih.gov/pubmed/26916489?tool=bestpractice.com
[171]Zuo Z, Yue J, Dong BR, et al. Thrombolytic therapy for pulmonary embolism. Cochrane Database Syst Rev. 2021 Apr 15;4:CD004437.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD004437.pub6/full
http://www.ncbi.nlm.nih.gov/pubmed/33857326?tool=bestpractice.com
[172]Chatterjee S, Chakraborty A, Weinberg I, et al. Thrombolysis for pulmonary embolism and risk of all-cause mortality, major bleeding, and intracranial hemorrhage: a meta-analysis. JAMA. 2014 Jun 18;311(23):2414-21.
https://jamanetwork.com/journals/jama/fullarticle/1881311
http://www.ncbi.nlm.nih.gov/pubmed/24938564?tool=bestpractice.com
[173]Ortel TL, Neumann I, Ageno W, et al. American Society of Hematology 2020 guidelines for management of venous thromboembolism: treatment of deep vein thrombosis and pulmonary embolism. Blood Adv. 2020 Oct 13;4(19):4693-738.
https://www.doi.org/10.1182/bloodadvances.2020001830
http://www.ncbi.nlm.nih.gov/pubmed/33007077?tool=bestpractice.com
[174]Meyer G, Vicaut E, Danays T, et al; PEITHO Investigators. Fibrinolysis for patients with intermediate-risk pulmonary embolism. N Engl J Med. 2014 Apr 10;370(15):1402-11.
https://www.nejm.org/doi/10.1056/NEJMoa1302097
http://www.ncbi.nlm.nih.gov/pubmed/24716681?tool=bestpractice.com
[175]Kline JA, Hernandez-Nino J, Jones AE. Tenecteplase to treat pulmonary embolism in the emergency department. J Thromb Thrombolysis. 2007 Apr;23(2):101-5.
https://www.doi.org/10.1007/s11239-006-9018-3
http://www.ncbi.nlm.nih.gov/pubmed/17221330?tool=bestpractice.com
ACCP რეკომენდაციას უწევს სისტემურ თრომბოლიზურ თერაპიას (თუ უკუნაჩვენებია) პერიფერიული ვენის გამოყენებით პაციენტებისთვის მწვავე PE-ით, რომლებიც დაკავშირებულია ჰიპოტენზიასთან, რომლებსაც არ აქვთ სისხლდენის მაღალი რისკი. ACCP არ იძლევა კონკრეტულ რეკომენდაციებს სასურველ აგენტებზე შედარებითი მონაცემების ნაკლებობის გამო.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
სისტემური თრომბოლიზური თერაპია დაკავშირებულია ნებისმიერი მიზეზით სიკვდილობის უფრო დაბალ მაჩვენებელთან, ვიდრე მხოლოდ ანტიკოაგულაცია მასიური ფილტვის ემბოლიის მქონე პაციენტებში (მწვავე ფილტვის ემბოლია, მდგრადი ჰიპოტენზია- სისტოლური წნევა <90 მმ.ვწყ.სვ. ან სულ მცირე 15 წუთი).[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[171]Zuo Z, Yue J, Dong BR, et al. Thrombolytic therapy for pulmonary embolism. Cochrane Database Syst Rev. 2021 Apr 15;4:CD004437.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD004437.pub6/full
http://www.ncbi.nlm.nih.gov/pubmed/33857326?tool=bestpractice.com
[172]Chatterjee S, Chakraborty A, Weinberg I, et al. Thrombolysis for pulmonary embolism and risk of all-cause mortality, major bleeding, and intracranial hemorrhage: a meta-analysis. JAMA. 2014 Jun 18;311(23):2414-21.
https://jamanetwork.com/journals/jama/fullarticle/1881311
http://www.ncbi.nlm.nih.gov/pubmed/24938564?tool=bestpractice.com
[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
იდეალურ შემთხვევაში, PE უნდა დადასტურდეს CTPA-ით თრომბოლიზური თერაპიის ჩატარებამდე.[95]Konstantinides SV, Barco S, Lankeit M, et al. Management of pulmonary embolism: an update. J Am Coll Cardiol. 2016 Mar 1;67(8):976-90.
http://www.onlinejacc.org/content/67/8/976
http://www.ncbi.nlm.nih.gov/pubmed/26916489?tool=bestpractice.com
თუ პაციენტს ემუქრება გარდაუვალი გულის გაჩერება, მკურნალობა შეიძლება დაიწყოს მხოლოდ კლინიკური ნიშნით.[96]British Thoracic Society Standards of Care Committee Pulmonary Embolism Guideline Development Group. British Thoracic Society guidelines for the management of suspected acute pulmonary embolism. Thorax. 2003 Jun;58(6):470-83.
http://thorax.bmj.com/content/58/6/470.long
http://www.ncbi.nlm.nih.gov/pubmed/12775856?tool=bestpractice.com
სისტემური თრომბოლიზური თერაპია იწვევს კოლტის სწრაფ დაშლას და აუმჯობესებს მარჯვენა პარკუჭის ფუნქციას, ფილტვში სისხლის დინებას და ფილტვის პერფუზიას.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
თრომბოლიზი ჰეპარინთან ერთად დაკავშირებულია ნაკლებ 30-დღიან სიკვდილობასთან, ვიდრე მხოლოდ ჰეპარინი (2.3% [24/1033] vs 3.9% [40/1024], შესაბამისად; დაჯამებული შანსების თანაფარდობა [OR] 0.59, 95% CI 0.36 - 0.96, P = 0.03). აღნიშნული მონაცემები ეფუძნება მწვავე ფილტვის ემბოლიის მქონე პაციენტების შემთხვევათა მეტაანალიზს.[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
თუმცა, თრომბოლიზი დაკავშირებულია დიდი და მცირე სისხლდენის, ჰემორაგიული ინსულტის ჩათვლით, მნიშვნელოვნად გაზრდილ რისკთან.[171]Zuo Z, Yue J, Dong BR, et al. Thrombolytic therapy for pulmonary embolism. Cochrane Database Syst Rev. 2021 Apr 15;4:CD004437.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD004437.pub6/full
http://www.ncbi.nlm.nih.gov/pubmed/33857326?tool=bestpractice.com
[172]Chatterjee S, Chakraborty A, Weinberg I, et al. Thrombolysis for pulmonary embolism and risk of all-cause mortality, major bleeding, and intracranial hemorrhage: a meta-analysis. JAMA. 2014 Jun 18;311(23):2414-21.
https://jamanetwork.com/journals/jama/fullarticle/1881311
http://www.ncbi.nlm.nih.gov/pubmed/24938564?tool=bestpractice.com
[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
პაციენტებში, რომლებიც თრომბოლიზურ თერაპიას და ჰეპარინს ერთად იღებდნენ, მეტი იყო სისხლდენის ეპიზოდის სიხშირე, ვიდრე მხოლოდ ანტიკოაგულანტის ფონზე (9.9% [96/974] vs 3.6% [35/961], შესაბამისად; შანსების თანაფარდობა 2.91, 95% CI 1.95 - 4.36).[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
პაციენტებში, რომლებიც თრომბოლიზურ თერაპიას და ჰეპარინს ერთად იღებდნენ, მეტი იყო სისხლდენის ეპიზოდის სიხშირე, ვიდრე მხოლოდ ანტიკოაგულანტის ფონზე (9.9% [96/974] vs 3.6% [35/961], შესაბამისად; შანსების თანაფარდობა 2.91, 95% CI 1.95 - 4.36).[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
თრომბოლიზის აბსოლუტური უკუჩვენებებია: ჰემორაგიული ინსულტი ან უცნობი წარმოშობის ინსულტი ნებისმიერ დროს; იშემიური ინსულტი ბოლო 6 თვის განმავლობაში; ცენტრალური ნერვული სისტემის დაზიანება ან სიმსივნე; უახლოეს წარსულში ტრავმა/ოპერაცია/თავის ტრავმა (ბოლო 3 კვირის განმავლობაში); გასტროინტესტინური სისხლდენა ბოლო თვის განმავლობაში; სისხლდენის დადასტურებული რისკი.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[177]Van de Werf F, Ardissino D, Betriu A, et al; task force on the management of acute myocardial infarction of the European Society of Cardiology. Management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J. 2003 Jan;24(1):28-66.
https://academic.oup.com/eurheartj/article/24/1/28/562262
http://www.ncbi.nlm.nih.gov/pubmed/12559937?tool=bestpractice.com
თრომბოლიზის შედარებითი უკუჩვენებებია: გარდამავალი იშემიური შეტევა ბოლო 6 თვის განმავლობაში; პერორალური ანტიკოაგულაციური თერაპია; ორსულობა ან ორსულობის შემდგომი 1 კვირის პერიოდი; ტრავმული რეანიმაცია (ფილტვის ემბოლიის ეპიზოდთან კავშირში); რეფრაქტორული ჰიპერტენზია (სისტოლური წნევა >180 მმ.ვწყ.სვ); ღვიძლის შორსწასული დაავადება; ინფექციური ენდოკარდიტი; კუჭის აქტიური წყლული.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[177]Van de Werf F, Ardissino D, Betriu A, et al; task force on the management of acute myocardial infarction of the European Society of Cardiology. Management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J. 2003 Jan;24(1):28-66.
https://academic.oup.com/eurheartj/article/24/1/28/562262
http://www.ncbi.nlm.nih.gov/pubmed/12559937?tool=bestpractice.com
თრომბოლიზური თერაპია ჩვეულებრივ არ არის რეკომენდებული ჰემოდინამიურად სტაბილური პაციენტებისთვის მწვავე PE.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
რანდომიზებულ ორმაგ ბრმა კვლევაში, პირველადი რეპერფუზიის თრომბოლიზური თერაპია პლუს ჰეპარინი ნორმატიული პაციენტებში საშუალო რისკის მქონე PE (მწვავე მარჯვენა პარკუჭის დისფუნქცია და მიოკარდიუმის დაზიანება აშკარა ჰემოდინამიკური კომპრომისის გარეშე) თავიდან აიცილა ჰემოდინამიკური დეკომპენსაცია მხოლოდ ჰეპარინთან შედარებით, მაგრამ გაზარდა რისკი. ძირითადი სისხლდენა და ინსულტი.[174]Meyer G, Vicaut E, Danays T, et al; PEITHO Investigators. Fibrinolysis for patients with intermediate-risk pulmonary embolism. N Engl J Med. 2014 Apr 10;370(15):1402-11.
https://www.nejm.org/doi/10.1056/NEJMoa1302097
http://www.ncbi.nlm.nih.gov/pubmed/24716681?tool=bestpractice.com
ქირურგიული ემბოლექტომია ან კათეტერული თერაპია
სისტემური თრომბოლიზური თერაპია ზრდის სისხლდენის რისკს, მათ შორის ინტრაკრანიული სისხლდენისაც.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[176]Marti C, John G, Konstantinides S, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015 Mar 7;36(10):605-14.
https://academic.oup.com/eurheartj/article/36/10/605/514452
http://www.ncbi.nlm.nih.gov/pubmed/24917641?tool=bestpractice.com
ქირურგიული ფილტვის ემბოლექტომია და კათეტერით მიმართული თერაპია (რომელიც, როგორც წესი, მოიცავს თრომბის მექანიკური და ფარმაკოთერაპიული ფრაგმენტაციის კომბინაციას) სავარაუდოდ უფრო დაბალი თანმხლები სისხლდენის რისკი აქვთ, ვიდრე სისტემურ თერაპიას.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[178]Dolovich LR, Ginsberg JS, Douketis JD, et al. A meta-analysis comparing low-molecular-weight heparins with unfractionated heparin in the treatment of venous thromboembolism: examining some unanswered questions regarding location of treatment, product type, and dosing frequency. Arch Intern Med. 2000 Jan 24;160(2):181-8.
https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/485206
http://www.ncbi.nlm.nih.gov/pubmed/10647756?tool=bestpractice.com
[179]Konstantinides SV, Barco S. Systemic thrombolytic therapy for acute pulmonary embolism: who is a candidate? Semin Respir Crit Care Med. 2017 Feb;38(1):56-65.
http://www.ncbi.nlm.nih.gov/pubmed/28208199?tool=bestpractice.com
[180]Goldberg JB, Giri J, Kobayashi T, et al. Surgical management and mechanical circulatory support in high-risk pulmonary embolisms: historical context, current status, and future directions: a scientific statement from the American Heart Association. Circulation. 2023 Feb 28;147(9):e628-e47.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001117
http://www.ncbi.nlm.nih.gov/pubmed/36688837?tool=bestpractice.com
ქირურგიული ემბოლექტომია რეკომენდებულია იმ შემთხვევაში, თუ სისტემური თრომბოლიზი წარუმატებელი იყო ან გვაქვს აბსოლუტური უკუჩვენება.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[180]Goldberg JB, Giri J, Kobayashi T, et al. Surgical management and mechanical circulatory support in high-risk pulmonary embolisms: historical context, current status, and future directions: a scientific statement from the American Heart Association. Circulation. 2023 Feb 28;147(9):e628-e47.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001117
http://www.ncbi.nlm.nih.gov/pubmed/36688837?tool=bestpractice.com
ემბოლექტომიის შემდეგ სიკვდილობის მაჩვენებელი მერყეობს 4%-დან 27%-მდე.[181]Fukuda I, Daitoku K. Surgical Embolectomy for Acute Pulmonary Thromboembolism. Ann Vasc Dis. 2017 Jun 25;10(2):107-114.
https://www.doi.org/10.3400/avd.ra.17-00038
http://www.ncbi.nlm.nih.gov/pubmed/29034035?tool=bestpractice.com
მწვავე მასიური ფილტვის თრომბოემბოლიის მქონე პაციენტების ერთ კოჰორტაში, რომელთაც ჩაუტარდათ ქირურგიული ემბოლექტომია, 10-წლიანი გადარჩენადობა იყო 84%.[182]Fukuda I, Taniguchi S, Fukui K, et al. Improved outcome of surgical pulmonary embolectomy by aggressive intervention for critically ill patients. Ann Thorac Surg. 2011 Mar;91(3):728-32.
https://www.doi.org/10.1016/j.athoracsur.2010.10.086
http://www.ncbi.nlm.nih.gov/pubmed/21352987?tool=bestpractice.com
კათეტერზე მიმართული თერაპია, რომელიც, როგორც წესი, მოიცავს თრომბის მექანიკურ და ფარმაკოთერაპიულ ფრაგმენტაციას, შეიძლება ჩაითვალოს პაციენტებში მწვავე PE-ით, რომლებიც დაკავშირებულია ჰიპოტენზიასთან, რომლებსაც ასევე აქვთ სისხლდენის მაღალი რისკი, წარუმატებელი სისტემური თრომბოლიზი ან შოკი, რომელიც შესაძლოა გამოიწვიოს სიკვდილამდე სისტემურამდე. თრომბოლიზი შეიძლება ამოქმედდეს (მაგ., რამდენიმე საათში), თუ ხელმისაწვდომია შესაბამისი ექსპერტიზა და რესურსები.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
კათეტერული თერაპია იყენებს თრომბოლიზური მედიკამენტის დაბალ დოზას (სრული სისტემური თრომბოლიზის დოზის დაახლოებით ერთ მესამედს), ამიტომ ითვლება, რომ ამცირებს სისხლდენის რისკს შორეული ადგილებიდან (მაგ. ინტრაკრანიული ან გასტროინტესტინური).[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
კათეტერული თერაპიის არარანდომიზებული კვლევის მეტა ანალიზმა გამოავლინა კლინიკური წარმატების მაჩვენებელი 87%, რომელიც დაკავშირებულია ძირითად და მცირე გართულებების 2% და 8%-იან რისკებთან, შესაბამისად.[183]Kuo WT, Gould MK, Louie JD, at al. Catheter-directed therapy for the treatment of massive pulmonary embolism: systematic review and meta-analysis of modern techniques. J Vasc Interv Radiol. 2009 Nov;20(11):1431-40.
http://www.ncbi.nlm.nih.gov/pubmed/19875060?tool=bestpractice.com
მტკიცებულება შეზღუდულია მცირე კვლევებით, კვლევის დიზაინით (ანუ არარანდომიზირებული) და შუალედური ეფექტურობის საბოლოო წერტილების გამოყენებით[184]Jimenez D, Martin-Saborido C, Muriel A, et al. Efficacy and safety outcomes of recanalisation procedures in patients with acute symptomatic pulmonary embolism: systematic review and network meta-analysis. Thorax. 2018 May;73(5):464-71.
https://www.doi.org/10.1136/thoraxjnl-2017-210040
http://www.ncbi.nlm.nih.gov/pubmed/29133351?tool=bestpractice.com
ქვედა ღრუ ვენის ფილტრის მოთავსება
ქვედა ღრუ ვენის (IVC) ფილტრი შეიძლება განთავსდეს პაციენტებში:[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[179]Konstantinides SV, Barco S. Systemic thrombolytic therapy for acute pulmonary embolism: who is a candidate? Semin Respir Crit Care Med. 2017 Feb;38(1):56-65.
http://www.ncbi.nlm.nih.gov/pubmed/28208199?tool=bestpractice.com
მწვავე PE და ანტიკოაგულანტული თერაპიის აბსოლუტური უკუჩვენებით, როგორიცაა აქტიური დიდი სისხლდენა
დადასტურებული მორეციდივე PE-ით ადექვატური ანტიკოაგულაციის მიუხედავად.
ACCP გაიდლაინები რეკომენდაციას უწევს IVC ფილტრის გამოყენებას მხოლოდ მწვავე PE (მაგ., დიაგნოზი წინა 1 თვეში) და ანტიკოაგულანტული თერაპიის აბსოლუტური უკუჩვენებით (მაგ. აქტიური დიდი სისხლდენა, მძიმე თრომბოციტოპენია, სისხლდენის მაღალი რისკი, ცენტრალური ნერვული სისტემის დაზიანება). ACCP რეკომენდაციას უწევს IVC ფილტრების გამოყენებას ანტიკოაგულაციის გარდა მწვავე PE-ს მქონე პაციენტებში.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
სხვა გაიდლაინებში განიხილება IVC ფილტრის გამოყენების შედარებითი ჩვენება, რომელიც მოიცავს მასიური PE ნარჩენი ღრმა ვენური თრომბის მქონე პაციენტში შემდგომი PE, თავისუფლად მცურავი ილიოფემორალური ან IVC თრომბი და მძიმე კარდიოფილტვის დაავადება და ღრმა ვენური თრომბოზი (DVT) (მაგ. პულმონალური ფილტვის ჰიპერტენზიით).[185]American College of Radiology; Society of Interventional Radiology. ACR-SIR-SPR practice parameter for the performance of inferior vena cava (IVC) filter placement for the prevention of pulmonary embolism. 2021 [internet publication].
https://www.acr.org/-/media/ACR/Files/Practice-Parameters/ivc-fliterplacement.pdf
ზოგიერთ კლინიკაში ქვედა ღრუ ვენის ფილტრი იდგმება ფილტვის ქირურგიული ემბოლექტომიის დროს, ინტრაოპერატიულად ან დაუყოვნებლივ ოპერაციის შემდეგ.[186]Leacche M, Unic D, Goldhaber SZ, et al. Modern surgical treatment of massive pulmonary embolism: Results in 47 consecutive patients after rapid diagnosis and aggressive surgical approach. J Thorac Cardiovasc Surg. 2005 May;129(5):1018-23.
http://www.ncbi.nlm.nih.gov/pubmed/15867775?tool=bestpractice.com
[187]Aklog L, Williams CS, Byrne JG, et al. Acute pulmonary embolectomy: a contemporary approach. Circulation. 2002 Mar 26;105(12):1416-9.
http://circ.ahajournals.org/content/105/12/1416.long
http://www.ncbi.nlm.nih.gov/pubmed/11914247?tool=bestpractice.com
[188]Greelish JP, Leacche M, Solenkova NS, et al. Improved midterm outcomes for type A (central) pulmonary emboli treated surgically. J Thorac Cardiovasc Surg. 2011 Dec;142(6):1423-9.
https://www.jtcvs.org/article/S0022-5223(11)00280-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/21481423?tool=bestpractice.com
ქვედა ღრუ ვენის ფილტრის ჩადგმა მოწოდებულია რაც შეიძლება ადრე იმ შემთხვევაში, თუ ეს არის მკურნალობის ერთადერთი შესაძლო მეთოდი. არსებობს მცირე მტკიცებულება, რომელიც მიუთითებს მოთავსების იდეალურ დროზე. თუმცა, სიკვდილის ყველაზე მაღალი რისკი არის პრეზენტაციის პირველი 2 საათის განმავლობაში, რაც შეიძლება მიუთითებდეს, რომ ეს არის გონივრული ვადა ფილტრის განთავსებისთვის.[189]Tow DE, Wagner HN. Urokinase pulmonary embolism trial: Phase I results. JAMA. 1970 Dec 21;214(12):2163-72.
https://jamanetwork.com/journals/jama/article-abstract/358702
ობსერვაციული კვლევები ვარაუდობს, რომ ვენური ფილტრის ჩასმამ შეიძლება შეამციროს PE-თან დაკავშირებული სიკვდილიანობის მაჩვენებლები მწვავე ფაზაში, მაგრამ ფილტრთან დაკავშირებული VTE-ის რისკის მატებასთან ერთად.[190]Stein PD, Matta F, Keyes DC, et al. Impact of vena cava filters on in-hospital case fatality rate from pulmonary embolism. Am J Med. 2012 May;125(5):478-84.
https://www.amjmed.com/article/S0002-9343(11)00481-5/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/22310013?tool=bestpractice.com
[191]Muriel A, Jiménez D, Aujesky D, et al. Survival effects of inferior vena cava filter in patients with acute symptomatic venous thromboembolism and a significant bleeding risk. J Am Coll Cardiol. 2014 Apr 29;63(16):1675-83.
http://www.ncbi.nlm.nih.gov/pubmed/24576432?tool=bestpractice.com
ხშირია ქვედა ღრუ ვენის პერმანენტულ ფილტრებთან დაკავშირებული გართულებები, თუმცა ისინი იშვიათადაა ფატალური.[191]Muriel A, Jiménez D, Aujesky D, et al. Survival effects of inferior vena cava filter in patients with acute symptomatic venous thromboembolism and a significant bleeding risk. J Am Coll Cardiol. 2014 Apr 29;63(16):1675-83.
http://www.ncbi.nlm.nih.gov/pubmed/24576432?tool=bestpractice.com
საერთო ჯამში, ადრეული გართულებები (რომელიც მოიცავს შეყვანის ადგილს) ხდება პაციენტთა დაახლოებით 10%-ში. გვიანი გართულებები უფრო ხშირია და მოიცავს განმეორებით ღრმა ვენის თრომბოზს (პაციენტთა დაახლოებით 20%) დ პოსტ-თრომბულ სინდრომს (პაციენტთა 40%-მდე).[192]Rajasekhar A, Streiff MB. Vena cava filters for management of venous thromboembolism: a clinical review. Blood Rev. 2013 Sep;27(5):225-41.
http://www.ncbi.nlm.nih.gov/pubmed/23932118?tool=bestpractice.com
[193]PREPIC Study Group. Eight-year follow-up of patients with permanent vena cava filters in the prevention of pulmonary embolism: the PREPIC (Prévention du Risque d'Embolie Pulmonaire par Interruption Cave) randomized study. Circulation. 2005 Jul 19;112(3):416-22.
http://circ.ahajournals.org/content/112/3/416.long
http://www.ncbi.nlm.nih.gov/pubmed/16009794?tool=bestpractice.com
ქვედა ღრუ ვენას დახშობა აზიანებს დაახლოებით პაციენტთა 22%-ს მე-5 წელზე და 33%-ს მე-9 წელზე, ანტიკოაგულაციის გამოყენების ხანგრძლივობის მიუხედავად.[193]PREPIC Study Group. Eight-year follow-up of patients with permanent vena cava filters in the prevention of pulmonary embolism: the PREPIC (Prévention du Risque d'Embolie Pulmonaire par Interruption Cave) randomized study. Circulation. 2005 Jul 19;112(3):416-22.
http://circ.ahajournals.org/content/112/3/416.long
http://www.ncbi.nlm.nih.gov/pubmed/16009794?tool=bestpractice.com
ფილტრის შემდეგ ანტიკოაგულაცია განიხილება ყოველი შემთხვევითვის ინდივიდუალურად, შედარებითი და აბსოლუტური უკუჩვენებებიდან გამომდინარე.[194]Decousus H, Leizorovicz A, Parent F, et al; Prévention du Risque d'Embolie Pulmonaire par Interruption Cave Study Group. A clinical trial of vena caval filters in the prevention of pulmonary embolism in patients with proximal deep-vein thrombosis. N Engl J Med. 1998 Feb 12;338(7):409-15.
https://www.nejm.org/doi/10.1056/NEJM199802123380701
http://www.ncbi.nlm.nih.gov/pubmed/9459643?tool=bestpractice.com
ანტიკოაგულაცია უნდა დაიწყოს თუ უკუჩვენება აღმოიფხვრება ან თუ რისკის/სარგებლის ანალიზი მიუთითებს, რომ ეს არის გონივრული კურსი.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
თუ გამოიყენება დროებითი ფილტრი, იგი უნდა ამოვიღოთ ანტიკოაგულანტების გამოყენების დაშვებისთანავე.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
დადასტურებული PE-ს მქონე პაციენტების პროგნოზული სტრატიფიკაცია შოკის ან ჰიპოტენზიის გარეშე: ფილტვის ემბოლიის სიმძიმის ინდექსი
დადასტურებული ფილტვის ემბოლიის მქონე (შოკის ან ჰიპოტენზიის გარეშე) პაციენტებში საჭიროა რისკის სტრატიფიკაცია, მაგ. ფილტვის ემბოლიის სიმძიმის ინდექსით (PESI), ან ფილტვის ემბოლიის გამარტივებული ინდექსით (sPESI).[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[95]Konstantinides SV, Barco S, Lankeit M, et al. Management of pulmonary embolism: an update. J Am Coll Cardiol. 2016 Mar 1;67(8):976-90.
http://www.onlinejacc.org/content/67/8/976
http://www.ncbi.nlm.nih.gov/pubmed/26916489?tool=bestpractice.com
PESI ახდენს პაციენტების კლასიფიცირებას რისკის 5 კატეგორიიდან 1-ში, რაც დაკავშირებულია 30-დღიანი სიკვდილობის რისკის მატებასთან. PESI-ის რისკის კატეგორიები გამომდინარეობს 11 კლინიკური კრიტერიუმის შეჯამებიდან; sPESI -ს მხოლოდ 6 კრიტერიუმი აქვს და რისკის ორი კატეგორია (დაბალი [0 ქულა] ან მაღალი [≥1 ქულა] 30-დღიანი სიკვდილობის პროგნოზის მიზნით).
კვლევებით ნაჩვენებია, რომ PESI და sPESI მსგავსი სიზუსტით ახდენს მოკლევადიანი სიკვდილობის პროგნოზირებას, თუმცა შემოკლებული ვერსია უფრო ადვილი გამოსაყენებელია.[195]Vinson DR, Ballard DW, Mark DG, et al; MAPLE Investigators of the KP CREST Network. Risk stratifying emergency department patients with acute pulmonary embolism: does the simplified Pulmonary Embolism Severity Index perform as well as the original? Thromb Res. 2016 Dec;148:1-8.
http://www.ncbi.nlm.nih.gov/pubmed/27764729?tool=bestpractice.com
[196]Zhou XY, Ben SQ, Chen HL, et al. The prognostic value of pulmonary embolism severity index in acute pulmonary embolism: a meta-analysis. Respir Res. 2012 Dec 4;13:111.
https://respiratory-research.biomedcentral.com/articles/10.1186/1465-9921-13-111
http://www.ncbi.nlm.nih.gov/pubmed/23210843?tool=bestpractice.com
მეტაანალიზით შეფასდა PESI/sPESI -ს პროგნოზული ღირებულება ნებისმიერი მიზეზით სიკვდილობის ანალიზის კუთხით. დაჯამებული მგრძნობელობა იყო 91%, ხოლო დაჯამებული სპეციფიკურობა 41%.[196]Zhou XY, Ben SQ, Chen HL, et al. The prognostic value of pulmonary embolism severity index in acute pulmonary embolism: a meta-analysis. Respir Res. 2012 Dec 4;13:111.
https://respiratory-research.biomedcentral.com/articles/10.1186/1465-9921-13-111
http://www.ncbi.nlm.nih.gov/pubmed/23210843?tool=bestpractice.com
PESI გამოყენებულია პაციენტების შესარჩევად, რომლებიც შეესაბამებიან ამბულატორიული მართვის კრიტერიუმებს.[197]Roy PM, Moumneh T, Penaloza A, et al. Outpatient management of pulmonary embolism. Thromb Res. 2017 Jul;155:92-100.
https://www.doi.org/10.1016/j.thromres.2017.05.001
http://www.ncbi.nlm.nih.gov/pubmed/28525830?tool=bestpractice.com
[198]Bledsoe JR, Woller SC, Stevens SM, et al. Management of Low-Risk Pulmonary Embolism Patients Without Hospitalization: The Low-Risk Pulmonary Embolism Prospective Management Study. Chest. 2018 Aug;154(2):249-256.
https://www.doi.org/10.1016/j.chest.2018.01.035
http://www.ncbi.nlm.nih.gov/pubmed/29410163?tool=bestpractice.com
სოციალური ფონისა და მკურნალობაზე დამყოლობის მიხედვით, ევროპის კარდიოლოგთა საზოგადოება რეკომენდაციას გასცემს დაბალი რისკის (PESI-ს პირველი ან მეორე კლასი, ან sPESI-ის 0 ქულა) პაციენტების ადრეული გაწერისა და ამბულატორიული მართვის თაობზე.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: PESI კრიტერიუმები და რისკის სტრატიფიკაციაშექმნილია BMJ ცოდნის ცენტრის მიერ [Citation ends].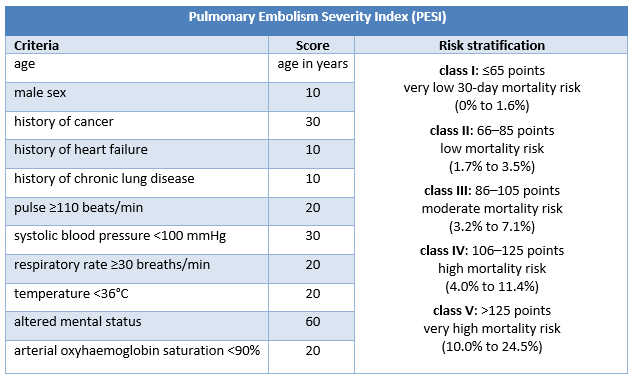 [Figure caption and citation for the preceding image starts]: sPESI კრიტერიუმები და რისკის სტრატიფიკაციაშექმნილია BMJ ცოდნის ცენტრის მიერ [Citation ends].
[Figure caption and citation for the preceding image starts]: sPESI კრიტერიუმები და რისკის სტრატიფიკაციაშექმნილია BMJ ცოდნის ცენტრის მიერ [Citation ends].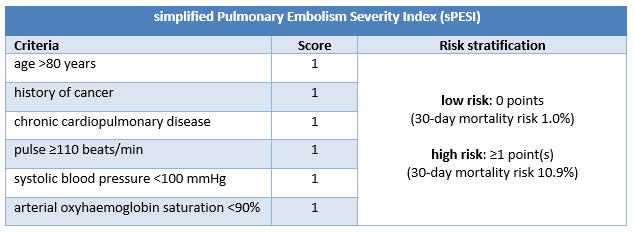
"გადამრჩენელი" თრომბოლიზი
მარჯვენა პარკუჭის ფუნქციის შეფასება ექოკარდიოგრაფიით და ტროპონინის ტესტირებით შესაძლოა გათვალისწინებული იქნას PESI-ით რისკის სტრატიფიკაციის ≥III კლასში ან sPESI ≥1 კატეგორიაში.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
დადასტურებული PE-ს მქონე პაციენტებში შოკის ან ჰიპოტენზიის გარეშე: მარჯვენა პარკუჭის დისფუნქცია პროგნოზირებს არასასურველ შედეგს და იძლევა შემდგომი რისკის სტრატიფიკაციის საშუალებას; ტროპონინის ამაღლებული დონე ასოცირდება მოკლევადიანი სიკვდილიანობის, PE-თან დაკავშირებული სიკვდილიანობის და სერიოზული გვერდითი მოვლენების გაზრდილ რისკთან.[130]Vanni S, Polidori G, Vergara R, et al. Prognostic value of ECG among patients with acute pulmonary embolism and normal blood pressure. Am J Med. 2009 Mar;122(3):257-64.
http://www.ncbi.nlm.nih.gov/pubmed/19272487?tool=bestpractice.com
[131]Jaff MR, McMurtry MS, Archer SL, et al. Management of massive and submassive pulmonary embolism, iliofemoral deep vein thrombosis, and chronic thromboembolic pulmonary hypertension: a scientific statement from the American Heart Association. Circulation. 2011 Apr 26;123(16):1788-830.
http://circ.ahajournals.org/content/123/16/1788.long
http://www.ncbi.nlm.nih.gov/pubmed/21422387?tool=bestpractice.com
[132]Weekes AJ, Thacker G, Troha D, et al. Diagnostic accuracy of right ventricular dysfunction markers in normotensive emergency department patients with acute pulmonary embolism. Ann Emerg Med. 2016 Sep;68(3):277-91.
http://www.ncbi.nlm.nih.gov/pubmed/26973178?tool=bestpractice.com
[199]Bajaj A, Saleeb M, Rathor P, et al. Prognostic value of troponins in acute nonmassive pulmonary embolism: A meta-analysis. Heart Lung. 2015 Jul-Aug;44(4):327-34.
https://www.doi.org/10.1016/j.hrtlng.2015.03.007
http://www.ncbi.nlm.nih.gov/pubmed/25976228?tool=bestpractice.com
[200]Becattini C, Vedovati MC, Agnelli G. Prognostic value of troponins in acute pulmonary embolism: a meta-analysis. Circulation. 2007 Jul 24;116(4):427-33.
https://www.doi.org/10.1161/CIRCULATIONAHA.106.680421
http://www.ncbi.nlm.nih.gov/pubmed/17606843?tool=bestpractice.com
საშუალო მაღალი რისკის მქონე პაციენტები
PESI ≥III, ან sPESI ≥1 კატეგორიები, მარჯვენა პარკუჭის დისფუნქციითა და დადებითი ტროპონინის I ან T ტესტით, მიეკუთვნება საშუალო-მაღალი რისკის ჯგუფს.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
"გადამრჩენელი" თრომბოლიზი შეიძლება მითითებული იყოს საშუალო-მაღალი რისკის ჯგუფის პაციენტებში, რომელთაც კარდიოპულმონური უკმარისობის სხვა ნიშნებიც აქვთ (მაგ. გულისცემის გახშირება, სუნთქვის გახშირება, ვენური წნევის მატება) და დაწყებულია ანტიკოაგულაციური თერაპია და:[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[179]Konstantinides SV, Barco S. Systemic thrombolytic therapy for acute pulmonary embolism: who is a candidate? Semin Respir Crit Care Med. 2017 Feb;38(1):56-65.
http://www.ncbi.nlm.nih.gov/pubmed/28208199?tool=bestpractice.com
უარესდება (როგორც ჩანს სისტოლური არტერიული წნევის დაქვეითება, გულისცემის მატება, გაზის გაცვლის გაუარესება, არაადეკვატური პერფუზიის ნიშნები, RV ფუნქციის გაუარესება ან გულის ბიომარკერების გაზრდა), მაგრამ ჯერ არ განუვითარდათ ჰიპოტენზია.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ვლინდება ჰემოდინამიკური დეკომპენსაციის ნიშნები (მაგ. სისტოლური წნევა <90 მმ.ვწყ.სვ. სულ მცირე 15 წუთით, ან სისტოლური წნევა მცირდება მინიმუმ 40 მმ.ვწყ.სვ.-ით ბოლო 15 წუთის განმავლობაში, ან გამოვლინდა ორგანოების ჰიპოპერფუზიის ნიშნები).
სისხლდენის რისკის გააზრება იმოქმედებს თრომბოლიზური თერაპიის შერჩევაზე.
საშუალო მაღალი რისკის მქონე პაციენტები
ნორმატიული პაციენტები PESI რისკის სტრატიფიკაციით ≥III, ან sPESI ≥1, ნორმალური ექოკარდიოგრაფიით და/ან გულის ტროპონინის ტესტით ითვლება შუალედურ დაბალ რისკებად.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
საშუალო-დაბალი რისკის პაციენტები საჭიროებენ მონიტორინგს თუ ტროპონინი დადებითია (თუნდაც არ იყოს მარჯვენა პარკუჭის დისფუნქცია); ანტიკოაგულანტებით თერაპია უნდა გაგრძელდეს საშუალო-დაბალი რისკის მქონე ყველა პაციენტში.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
სხვა პროგნოზული ინდექსები
RIETE (Registro Informatizado de la Enfermedad TromboEmbolica venosa) და HESTIA კრიტერიუმები შეიძლება დაგვეხმაროს პაციენტების სელექციაში (ვენური თრომბოემბოლიზმით, ცუდი კლინიკური გამოსავლის დაბალი რისკი), რომელთა მართვაც შესაძლებელია ამბულატორიულად.[201]Trujillo-Santos J, Lozano F, Lorente MA, et al. A prognostic score to identify low-risk outpatients with acute deep vein thrombosis in the lower limbs. Am J Med. 2015 Jan;128(1):90.e9-15.
https://www.doi.org/10.1016/j.amjmed.2014.08.023
http://www.ncbi.nlm.nih.gov/pubmed/25242230?tool=bestpractice.com
[202]Zondag W, Vingerhoets LM, Durian MF, et al. Hestia criteria can safely select patients with pulmonary embolism for outpatient treatment irrespective of right ventricular function. J Thromb Haemost. 2013 Apr;11(4):686-92.
https://www.doi.org/10.1111/jth.12146
http://www.ncbi.nlm.nih.gov/pubmed/23336721?tool=bestpractice.com
[203]Weeda ER, Kohn CG, Peacock WF, et al. External Validation of the Hestia Criteria for Identifying Acute Pulmonary Embolism Patients at Low Risk of Early Mortality. Clin Appl Thromb Hemost. 2017 Oct;23(7):769-774.
https://www.doi.org/10.1177/1076029616651147
http://www.ncbi.nlm.nih.gov/pubmed/27225840?tool=bestpractice.com
სამკურნალო ფაზის ანტიკოაგულანტული თერაპია
ACCP გაიდლაინები გვირჩევენ, რომ პაციენტებს, რომლებსაც არ აქვთ უკუჩვენება, მიეცეს ანტიკოაგულაციის 3-თვიანი მკურნალობის კურსი. აპიქსაბანი, დაბიგატრანი, ედოქსაბანი ან რივაროქსაბანი რეკომენდებულია K ვიტამინის ანტაგონისტთან შედარებით (VKA).[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
მკურნალობის ეტაპის დასრულების შემდეგ, ყველა პაციენტი უნდა შეფასდეს გაფართოებული ფაზის თერაპიისთვის.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
სამკურნალო ფაზის ანტიკოაგულანტული თერაპია
ანტიკოაგულანტული თერაპიის გაგრძელების მიზანი გაფართოებულ ფაზაში (ანუ, პირველი 3 თვის შემდეგ და დაგეგმილი შეწყვეტის თარიღის გარეშე) არის VTE-ის მეორადი პრევენცია.
ACCP რეკომენდაციით პროლონგირებული ანტიკოაგულაციური თერაპიის დაწყება საჭიროა შემდგომ პაციენტებში.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
PE-ს მქონე პირები, რომლებსაც დიაგნოზირებული აქვთ გარდამავალი პროვოკაციის არარსებობის შემთხვევაში (არაპროვოცირებული PE ან PE პროვოცირებული მუდმივი რისკის ფაქტორით). ამ პაციენტებს უნდა დაენიშნოთ DОАК.
მათ, ვისაც PE დიაგნოზი დაუსვეს გარდამავალი რისკ-ფაქტორის არარსებობისას (არაპროვოცირებული PE ან PE პროვოცირებული მუდმივი რისკის ფაქტორით), რომლებიც ვერ იღებენ DOAC-ს. ამ პაციენტებს უნდა მიეცესVKA.
გახანგრძლივებული ფაზის ანტიკოაგულაცია არ არის რეკომენდებული PE-ს მქონე პაციენტებში, რომლებიც დიაგნოზირებულია ძირითადი ან უმნიშვნელო გარდამავალი რისკფაქტორის კონტექსტში.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
გადაწყვეტილება გახანგრძლივებული თერაპიის დაწყების ან გაგრძელების შესახებ უნდა ეფუძნებოდეს პაციენტის წინასწარგანწყობას და მორეციდივე VTE-ს ან სისხლდენის სავარაუდო რისკს.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
მორეციდივე VTE-ის რისკის ზუსტი პროგნოზირება საწყისი მოვლენის შემდეგ რთულია. დროებითი პროვოცირების ფაქტორების არსებობა ან არარსებობა არის რეციდივის ყველაზე ძლიერი პროგნოზირება. პაციენტები სერიოზული გარდამავალი პროვოკაციით(მაგ.ოპერაცია} VTE-ის განვითარებამდე 3 თვით ადრე აქვთ რეციდივის დაბალი რისკი. მცირე გარდამავალი რისკ-ფაქტორები (მაგ., სამედიცინო ჰოსპიტალიზაცია, ესტროგენის გამოყენება, შორ მანძილზე მოგზაურობა) დიაგნოზიდან 2 თვის განმავლობაში პროგნოზირებს რეციდივის შუალედურ რისკს. პაციენტები, რომლებსაც არ აქვთ VTE-ის (მაგ., არაპროვოცირებული VTE) ან მუდმივი პროვოკაციების (მაგ. კიბო) იდენტიფიცირებადი რისკ-ფაქტორი, არიან რეციდივის მაღალი რისკის ქვეშ.[20]Kearon C, Ageno W, Cannegieter SC, et al. Categorization of patients as having provoked or unprovoked venous thromboembolism: guidance from the SSC of ISTH. J Thromb Haemost. 2016 Jul;14(7):1480-3.
https://www.doi.org/10.1111/jth.13336
http://www.ncbi.nlm.nih.gov/pubmed/27428935?tool=bestpractice.com
პაციენტები მორეციდივე არაპროვოცირებული PE და პროქსიმალური DVT-ით მიჩნეულია შემდგომი რეციდივის განსაკუთრებით მაღალი რისკის ქვეშ.[173]Ortel TL, Neumann I, Ageno W, et al. American Society of Hematology 2020 guidelines for management of venous thromboembolism: treatment of deep vein thrombosis and pulmonary embolism. Blood Adv. 2020 Oct 13;4(19):4693-738.
https://www.doi.org/10.1182/bloodadvances.2020001830
http://www.ncbi.nlm.nih.gov/pubmed/33007077?tool=bestpractice.com
სისხლდენის რისკის შეფასებისას გასათვალისწინებელია შემდეგი ფაქტორები: ასაკი > 65 წელზე მეტი (განსაკუთრებით >75 წელი), წინა სისხლდენა, კიბო, თირკმლის უკმარისობა, ღვიძლის უკმარისობა, თრომბოციტოპენია, წინა ინსულტი, შაქრიანი დიაბეტი, ანემია, ანტითრომბოციტული თერაპია, ცუდი ანტიკოაგულანტების კონტროლი. , კომორბიდობა შემცირებული ფუნქციური შესაძლებლობებით, ბოლოდროინდელი ოპერაცია, ხშირი დაცემა, ალკოჰოლის ბოროტად გამოყენება, არასტეროიდული ანთების საწინააღმდეგო საშუალებების გამოყენება.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
პაციენტებს, რომელსაც არცერთი ეს რისფაქტორი არა აქვს განიხილება დაბალი რისკის მქონედ; ერთი რისკ ფაქტორი შეესაბამება საშუალო რისკს; და ორი ან მეტი რისკ ფაქტორი შეესაბამება მაღალ რისკს.
რისკის პროგნოზირების რამდენიმე მოდელი ცდილობდა გამოევლინა პაციენტები არაპროვოცირებული და/ან მცირე გარდამავალი პროვოკაციით, რომლებსაც აქვთ განმეორებითი VTE-ის დაბალი რისკი. მათგან, HER-DOO2 მოდელი შეფასებული იყო უამრავ პერსპექტიულ კლინიკურ ვალიდაციის კვლევაში და გამოიყენებოდა პაციენტების სუბპოპულაციის იდენტიფიცირებისთვის, რომლებსაც აქვთ რეციდივის დაბალი რისკი ანტიკოაგულაციური თერაპიის შეწყვეტის შემდეგ (მკურნალობის ფაზის დასრულების შემდეგ).[204]Rodger MA, Le Gal G, Anderson DR, et al. Validating the HERDOO2 rule to guide treatment duration for women with unprovoked venous thrombosis: multinational prospective cohort management study. BMJ. 2017 Mar 17;356:j1065.
https://www.doi.org/10.1136/bmj.j1065
http://www.ncbi.nlm.nih.gov/pubmed/28314711?tool=bestpractice.com
აგენტის არჩევანი
პაციენტებში, რომლებიც იღებენ უწყვეტ ანტიკოაგულაციურ თერაპიას, როგორც წესი არ არის თავდაპირველი ანტიკოაგულანტის შეცვლის საჭიროება. ACCP გაიდლაინები რეკომენდაციას უწევს აპიქსაბანის ან რივაროქსაბანის შემცირებული დოზის გამოყენებას პაციენტებისთვის, რომლებიც იღებენ აპიქსაბანს ან რივაროქსაბანს; კონკრეტული პრეპარატისა და დოზის არჩევისას გათვალისწინებული უნდა იყოს პაციენტის სხეულის მასის ინდექსი, თირკმლის ფუნქცია და დოზირების რეჟიმის დაცვა.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
როგორც აპიქსაბანის, ასევე რივაროქსაბანის დაბალი დოზები ერთნაირად ეფექტურია გახანგრძლივებული ფაზის ანტიკოაგულანტული თერაპიისთვის და დაკავშირებულია არასერიოზული სისხლდენის ზომიერ შემცირებასთან შედარებით სამკურნალო დოზებთან შედარებით.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[205]Agnelli G, Buller HR, Cohen A, et al. Apixaban for extended treatment of venous thromboembolism. N Engl J Med. 2013 Feb 21;368(8):699-708.
https://www.doi.org/10.1056/NEJMoa1207541
http://www.ncbi.nlm.nih.gov/pubmed/23216615?tool=bestpractice.com
[206]Weitz JI, Lensing AW, Prins MH, et al; EINSTEIN CHOICE Investigators. Rivaroxaban or aspirin for extended treatment of venous thromboembolism. N Engl J Med. 2017 Mar 30;376(13):1211-22.
https://www.nejm.org/doi/10.1056/NEJMoa1700518
http://www.ncbi.nlm.nih.gov/pubmed/28316279?tool=bestpractice.com
≥6 თვიანი კვლევების თანახმად, ფილტვის ემბოლიის მართვის კუთხით, განსხვავება არ არის პირდაპირი მოქმედების პერორალურ ანტიკოაგულანტებსა და ჩვეულებრივ ანტიკოაგულაციას შორის.[207]Li M, Li J, Wang X, et al. Oral direct thrombin inhibitors or oral factor Xa inhibitors versus conventional anticoagulants for the treatment of pulmonary embolism. Cochrane Database Syst Rev. 2023 Apr 14;4(4):CD010957.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010957.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/37057837?tool=bestpractice.com
[208]Becattini C, Agnelli G. Risk stratification and management of acute pulmonary embolism. Hematology Am Soc Hematol Educ Program. 2016 Dec 2;2016(1):404-12.
http://asheducationbook.hematologylibrary.org/content/2016/1/404.long
http://www.ncbi.nlm.nih.gov/pubmed/27913508?tool=bestpractice.com
[  ]
How do oral direct thrombin inhibitors (DTIs) and oral factor Xa inhibitors compare with conventional anticoagulation for the treatment of pulmonary embolism?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4357/fullსწორი პასუხის ჩვენება[მტკიცებულების დონე B]120fe7b2-87cd-4301-a316-38128bb67120ccaBროგორ ედრება ერთმანეთს პირდაპირი თრომბინის ინჰიბიტორები და პერორალური ფაქტორ Xa ინჰიბიტორები სტანდარტულ ანტიკოაგულანტებს ფილტვის ემბოზლიზმის მკურნალობის თვალსაზრისით?
]
How do oral direct thrombin inhibitors (DTIs) and oral factor Xa inhibitors compare with conventional anticoagulation for the treatment of pulmonary embolism?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4357/fullსწორი პასუხის ჩვენება[მტკიცებულების დონე B]120fe7b2-87cd-4301-a316-38128bb67120ccaBროგორ ედრება ერთმანეთს პირდაპირი თრომბინის ინჰიბიტორები და პერორალური ფაქტორ Xa ინჰიბიტორები სტანდარტულ ანტიკოაგულანტებს ფილტვის ემბოზლიზმის მკურნალობის თვალსაზრისით?
გახანგრძლივებული ფაზის ანტიკოაგულაციის უწყვეტი გამოყენება ხელახლა უნდა შეფასდეს წელიწადში ერთხელ მაინც, ისევე როგორც ნებისმიერ დროს პაციენტის ჯანმრთელობის მდგომარეობის მნიშვნელოვანი ცვლილება.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
გახანგრძლივებული თერაპიის გაგრძელების მტკიცებულება 4 წელზე მეტი ხნის განმავლობაში შეუსწავლელია. ACCP გაიდლაინები გვირჩევენ საერთო გადაწყვეტილების საერთო მიღებას, პაციენტის ღირებულებებისა და პრეფერენციების გათვალისწინებით.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
პაციენტები პერიოდულად უნდა გადაიხედონ სისხლდენის რისკის, თერაპიული დაავადებების ტვირთის და ღირებულებებისა და უპირატესობების ნებისმიერი ცვლილების შესახებ.
თუ გადაწყვეტილება მიიღება გახანგრძლივებული ფაზის ანტიკოაგულაციის შეწყვეტის შესახებ, ACCP გაიდლაინები გვირჩევენ ასპირინის მიღებას (თუ უკუნაჩვენებია) განმეორებითი VTE-ის თავიდან ასაცილებლად.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ასპირინის გამოყენების სარგებელი დაბალანსებული უნდა იყოს სისხლდენის რისკთან და მიღების გვერდით ეფექტებთან. თუმცა, ასპირინი არ უნდა ჩავთვალოთ გონივრულ ალტერნატივად პაციენტებში, რომლებსაც სურთ გახანგრძლივებული ანტიკოაგულაციის გაგრძელება, რადგან ასპირინი ბევრად ნაკლებად ეფექტურია. ასპირინის მიღების ჩვენებები, ყველა შემთხვევაში თავიდან უნდა შეფასდეს, მაშინ როდესაც პაციენტი წყვეტს ანტიკოაგულანტებით თერაპიას, რადგან შესაძლოა ის მოხსნილი იყო ანტიკოაგულანტების დანიშვნისას.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
კიბოს აქტიური ფორმა
აქტიური კიბოს მქონე პაციენტებისთვის, ACCP გაიდლაინები რეკომენდაციას უწევს აპიქსაბანს, ედოქსაბანს ან რივაროქსაბანს LMWH-ზე გახანგრძლივებული ფაზის ანტიკოაგულაციისთვის.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
DOACs განსაკუთრებით ედოქსაბანი და რივაროქსაბანი) დაკავშირებულია კუჭ-ნაწლავის სისხლდენის უფრო მაღალ რისკთან, ვიდრე LMWH. კუჭ-ნაწლავის სანათურის კიბოს მქონე პაციენტებში, ACCP რეკომენდაციას უწევს აპიქსაბანს ან LMWH-ს, როგორც სასურველ აგენტს.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[  ]
How do low‐molecular‐weight heparin (LMWH), vitamin K agonists (VKAs), and direct oral anticoagulants (DOACs) compare for treatment of venous thromboembolism (VTE) in people with cancer?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2813/fullსწორი პასუხის ჩვენება ASH გირჩევთ გამოიყენოთ DOAC ან LMWH გაფართოებული ფაზისთვის; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]Lyman GH, Carrier M, Ay C, et al. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv. 2021 Feb 23;5(4):927-74.
https://ashpublications.org/bloodadvances/article/5/4/927/475194/American-Society-of-Hematology-2021-guidelines-for
http://www.ncbi.nlm.nih.gov/pubmed/33570602?tool=bestpractice.com
]
How do low‐molecular‐weight heparin (LMWH), vitamin K agonists (VKAs), and direct oral anticoagulants (DOACs) compare for treatment of venous thromboembolism (VTE) in people with cancer?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2813/fullსწორი პასუხის ჩვენება ASH გირჩევთ გამოიყენოთ DOAC ან LMWH გაფართოებული ფაზისთვის; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]Lyman GH, Carrier M, Ay C, et al. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv. 2021 Feb 23;5(4):927-74.
https://ashpublications.org/bloodadvances/article/5/4/927/475194/American-Society-of-Hematology-2021-guidelines-for
http://www.ncbi.nlm.nih.gov/pubmed/33570602?tool=bestpractice.com
ამ პაციენტებში რეკომენდებულია გაფართოებული ფაზის ანტიკოაგულანტული თერაპია (ანუ დაგეგმილი შეწყვეტის თარიღი არ არის), სანამ კიბო აქტიური რჩება.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[165]Lyman GH, Carrier M, Ay C, et al. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv. 2021 Feb 23;5(4):927-74.
https://ashpublications.org/bloodadvances/article/5/4/927/475194/American-Society-of-Hematology-2021-guidelines-for
http://www.ncbi.nlm.nih.gov/pubmed/33570602?tool=bestpractice.com
ორსულობა
ანტიკოაგულანტული თერაპია უნდა ჩატარდეს მშობიარობის შემდგომ მინიმუმ 6 კვირის განმავლობაში ქალებში პოსტნატალური VTE-ის მაღალი რისკის ქვეშ და მკურნალობის მინიმალური საერთო ხანგრძლივობისთვის 3 თვე საწყისი PE დიაგნოზიდან.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[168]Royal College of Obstetricians and Gynaecologists. Reducing the risk of venous thromboembolism during pregnancy and the puerperium. Green-top guideline No. 37a. Apr 2015 [internet publication].
https://www.rcog.org.uk/globalassets/documents/guidelines/gtg-37a.pdf
LMWH გამოიყენება მშობიარობის წინა პერიოდში, რადგან სხვა ანტიკოაგულანტებმა, მათ შორის VKAs, შეიძლება გადალახონ პლაცენტა ნაყოფზე გვერდითი ეფექტების თანმდევი რისკით.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
გაგრძელება LMWH ან VKA არის ვარიანტი მეძუძური დედებისთვის. DOAC არ არის რეკომენდებული მეძუძური დედებისთვის, რადგან ისინი გამოიყოფა დედის რძეში და მეძუძური ბავშვის უსაფრთხოება დადგენილი არ არის.[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
თირკმლის მძიმე ფუნქციური დარღვევა
ACCP რეკომენდაციას უწევს K ვიტამინის ანტაგონისტს პაციენტებში, რომელთაც თირკმლის მძიმე უკმარისობა აქვთ (კრეატინინის კლირენსი <30 მლ/წთ).[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
აპიქსაბანი ასევე შესაფერისია თირკმლის მძიმე დისფუნქციის ან თირკმლის დაავადების ბოლო სტადიის მქონე პაციენტებში გამოსაყენებლად, თუმცა ამ პაციენტების პოპულაციაში გამოყენების მტკიცებულება შეზღუდულია.[164]Pathak R, Pandit A, Karmacharya P, et al. Meta-analysis on risk of bleeding with apixaban in patients with renal impairment. Am J Cardiol. 2015 Feb 1;115(3):323-7.
https://www.doi.org/10.1016/j.amjcard.2014.10.042
http://www.ncbi.nlm.nih.gov/pubmed/25527282?tool=bestpractice.com
ღვიძლის უკმარისობა და კოაგულოპათია
ACCP გაიდლაინებით დაბალმოლეკულური ჰეპარინი რეკომენდებულია პაციენტთა ამ ჯგუფში.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
სამედიცინო პროფესიონალებმა უნდა იხილონ ეტიკეტი და/ან ადგილობრივი ფორმულარი, სანამ გამოწერენ პირდაპირი მოქმედების ანტიკოაგულანტს ღვიძლის უკმარისობის მქონე პაციენტში.
ანტიფოსფოლიპიდური სინდრომი
ანტიფოსფოლიპიდური სინდრომის მქონე პაციენტებში, ACCP და თრომბოზისა და ჰემოსტაზის საერთაშორისო საზოგადოების გაიდლაინები რეკომენდაციას უწევენ VKA-ს, როგორც სასურველ აგენტს.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[209]Zuily S, Cohen H, Isenberg D, et al. Use of direct oral anticoagulants in patients with thrombotic antiphospholipid syndrome: guidance from the Scientific and Standardization Committee of the International Society on Thrombosis and Haemostasis. J Thromb Haemost. 2020 Sep;18(9):2126-37.
https://www.doi.org/10.1111/jth.14935
http://www.ncbi.nlm.nih.gov/pubmed/32881337?tool=bestpractice.com
რანდომიზებული კონტროლირებადი კვლევების მტკიცებულებები ვარაუდობს, რომ DOACs შეიძლება არ იყოს ისეთი ეფექტური, როგორც VKAs ანტიფოსფოლიპიდური სინდრომის მქონე პაციენტებში თრომბოზის სამკურნალოდ. ამიტომ, ACCP გაიდლაინები გვირჩევენ ამ პაციენტებში DOAC-ების თავიდან აცილებას.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ანტიკოაგულანტები მორეციდივე ვენური თრომბოემბოლიის დროს
მორეციდივე თრომბოემბოლია იშვიათია პაციენტებში, რომლებიც თერაპიული დოზებით იღებენ ანტიკოაგულანტებს, გარდა კიბოს შემთხვევისა (დაბალმოლეკულური ჰეპარინის შემთხვევაში რეციდივის რისკი თერაპიის დროს არის 7-9%).[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
[210]Posch F, Königsbrügge O, Zielinski C, et al. Treatment of venous thromboembolism in patients with cancer: a network meta-analysis comparing efficacy and safety of anticoagulants. Thromb Res. 2015 Sep;136(3):582-9.
https://www.doi.org/10.1016/j.thromres.2015.07.011
http://www.ncbi.nlm.nih.gov/pubmed/26210891?tool=bestpractice.com
ფილტვის ემბოლიის დადასტურების მცდელობის პარალელურად, გასათვალისწინებელია ანტიკოაგულანტებით მკურნალობაზე დამყოლობა ან თანმდევი ავთვისებიანი მდგომარეობა.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
ACCP გაიდლაინებით რეკომენდებულია დროებით დაბალმოლეკულურ ჰეპარინზე გადასვლა (სულ მცირე ერთი თვით) იმ პაციენტებში, რომლებიც ნამდვილად მკურნალობენ სხვა ანტიკოაგულანტით (ან თერაპიული ფარგლების დაცვით K ვიტამინის ანტაგონისტების შემთხვევაში).[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
დაბალმოლეკულური ჰეპარინის მომატებული დოზა (ერთი მეოთხედიდან ერთ მესამედამდე) შეესაბამება მორეციდივე ფილტვის ემბოლიის მქონე პაციენტებს, რომლებიც დაბალმოლეკულურ ჰეპარინს იღებდნენ.[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
მორეციდივე VTE ანტიკოაგულანტული თერაპიის შეწყვეტის შემდეგ
პაციენტებისთვის, რომლებიც აღარ იღებენ ანტიკოაგულანტულ თერაპიას და განიცდიან მეორე PE-ს იდენტიფიცირებადი რისკ-ფაქტორის გარეშე (ანუ, არაპროვოცირებული), გაიდლაინები გვირჩევენ ანტიკოაგულანტებით მკურნალობის შემდეგ ხანგრძლივობას:[4]Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603.
https://www.doi.org/10.1093/eurheartj/ehz405
http://www.ncbi.nlm.nih.gov/pubmed/31504429?tool=bestpractice.com
[21]Stevens SM, Woller SC, Baumann Kreuziger L, et al. Antithrombotic therapy for VTE disease: second update of the CHEST guideline and expert panel report. 2021 Dec;160(6):e545-608.
https://journal.chestnet.org/article/S0012-3692(21)01506-3/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34352278?tool=bestpractice.com
სისხლდენის დაბალი-საშუალო რისკი: გახანგრძლივებული თერაპია ანტიკოაგულანტით, პერიოდულად რისკი-სარგებლის შეფასება
სისხლდენის მაღალი რისკი: შეწყვიტეთ ანტიკოაგულაცია 3 თვის შემდეგ.
 ]
ამერიკის ჰემატოლოგიის საზოგადოება (ASH) რეკომენდაციას უწევს რივაროქსაბანს, აპიქსაბანს ან LMWH-ს საწყისი ფაზის ანტიკოაგულაციისთვის აქტიური კიბოს მქონე პაციენტებში; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]
]
ამერიკის ჰემატოლოგიის საზოგადოება (ASH) რეკომენდაციას უწევს რივაროქსაბანს, აპიქსაბანს ან LMWH-ს საწყისი ფაზის ანტიკოაგულაციისთვის აქტიური კიბოს მქონე პაციენტებში; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165] [Figure caption and citation for the preceding image starts]: sPESI კრიტერიუმები და რისკის სტრატიფიკაციაშექმნილია BMJ ცოდნის ცენტრის მიერ [Citation ends].
[Figure caption and citation for the preceding image starts]: sPESI კრიტერიუმები და რისკის სტრატიფიკაციაშექმნილია BMJ ცოდნის ცენტრის მიერ [Citation ends].
 ]
[მტკიცებულების დონე B]
]
[მტკიცებულების დონე B] ]
ASH გირჩევთ გამოიყენოთ DOAC ან LMWH გაფართოებული ფაზისთვის; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]
]
ASH გირჩევთ გამოიყენოთ DOAC ან LMWH გაფართოებული ფაზისთვის; ASH აღიარებს, რომ ეს რეკომენდაცია პირობითია დაფუძნებული ძალიან დაბალი სიზუსტის მტკიცებულებებზე.[165]