Abordagem
A abordagem diagnóstica dependerá da situação do paciente.
Gestantes
A infecção aguda durante a gestação é quase sempre assintomática em mulheres, podendo, porém, ter consequências devastadoras se transmitida ao feto. O rastreamento pré-natal para Toxoplasma não é um procedimento de rotina nos EUA. No entanto, alguns países (como a França e a Áustria) recomendam o teste rotineiro durante a gestação.
Linfadenopatia cervical/occipital nova ou evidências de microcefalia, calcificações intracranianas, hidrocefalia ou restrição do crescimento intrauterino do feto detectados por ultrassonografia em gestantes aumentam a suspeita de infecção aguda ou recente.
Nesses casos, a imunoglobulina (Ig) G e a IgM anti-Toxoplasma devem ser verificadas na mãe. Um resultado negativo da IgM anti-Toxoplasma descarta infecção aguda. Em casos raros, talvez seja necessário repetir o teste de IgM se o resultado for inicialmente negativo e houver forte suspeita clínica de infecção. Em áreas de alta prevalência, é necessário verificar as sorologias mais que uma vez durante a gestação.
Se os resultados da IgM e da IgG forem negativos, a mãe provavelmente não terá tido exposição ao Toxoplasma gondii. Se o resultado da IgG for positivo e da IgM negativo, a mãe apresenta história remota de infecção, havendo pequeno risco de infecção no feto. Se o resultado da IgM anti-Toxoplasma for positivo, é impossível descartar a infecção aguda, sendo necessário realizar testes mais conclusivos em um laboratório de referência para Toxoplasma. O resultado positivo da IgM não é prova de infecção aguda: a IgM pode persistir por até 1 ano após a infecção aguda, havendo altos índices de falsos-positivos com alguns métodos de testagem. O índice de avidez de IgG específico para Toxoplasma é útil em gestantes que apresentam IgG e IgM detectáveis, pois pode diferenciar entre infecção recente e crônica. Epidemiologicamente, as infecções novas são as únicas com risco significativo para o feto; no entanto, o mecanismo de prevenção da infecção por IgG no feto é desconhecido.
Os laboratórios de referência têm capacidade para realizar uma bateria de testes, incluindo teste de corante para IgG, ensaio de imunoadsorção enzimática (ELISA)-IgM, teste de aglutinação diferencial, ELISA-IgA e ensaio da imunoabsorção-aglutinação (ISAGA)/ELISA-IgE como testes confirmatórios.[11] Se for determinado que a mãe apresenta infecção aguda, será necessário realizar a reação em cadeia da polimerase para Toxoplasma no líquido amniótico para avaliar a transmissão ao feto.[31] Ela deve ser realizada ≥4 semanas após a infecção materna primária aguda e ≥18 semanas de gestação para reduzir o risco de resultados falsos-negativos.[11] Também se pode realizar ultrassonografia do feto para avaliar dilatação ventricular, calcificações intracranianas, ascite e hepatomegalia.[11]
Neonatos de mães com suspeita de infecção durante a gestação
A doença congênita é com frequência subclínica no neonato, podendo mimetizar outras doenças neonatais, o que torna o diagnóstico mais complicado que o da infecção adquirida em adultos. Além disso, o diagnóstico sorológico é mais difícil porque a IgG materna atravessa a placenta, atingindo o feto.
O exame físico e da história, incluindo avaliação neurológica pediátrica e exame oftalmológico da retina, deve ser realizado em todos os neonatos com risco de doença congênita, na tentativa de detectar sinais clínicos da doença.
A avaliação sorológica deve ser realizada por laboratório de referência experiente, incluindo com frequência: imunoglobulina quantitativa, teste de corante para IgG, ensaio da imunoabsorção-aglutinação de IgM (ISAGA) e ELISA-IgA.[11] A presença de anticorpos IgG, IgM e/ou IgA específicos contra Toxoplasma em neonatos corrobora o diagnóstico de infecção intrauterina.[11] Recomenda-se a consulta com um especialista em doenças infecciosas para obter orientação quanto à interpretação dos resultados sorológicos e determinar o ciclo do tratamento nos neonatos.
Os ensaios de reação em cadeia da polimerase para Toxoplasma (sangue periférico, líquido cefalorraquidiano e urina) devem ser realizados o mais rápido possível após o nascimento e, se detectados, confirmam o diagnóstico.[11] Além disso, realize hemograma completo com contagem diferencial, testes da função hepática incluindo gama-glutamiltransferase e bilirrubinas, avaliação do líquido cefalorraquidiano (LCR) com celularidade, proteína, glicose, IgG quantitativa e IgG/IgM específicos para toxoplasmose e exame de imagem do cérebro.[11]
O ensaio de liberação de gamainterferona, que mede a produção de gamainterferona no sangue total estimulada por antígeno do T gondii pode ser usado para se descartar a infecção congênita em neonatos, evitando-se, dessa forma, a necessidade de acompanhamento sorológico. A sensibilidade e a especificidade do teste em lactentes com suspeita de doença congênita foram relatados em 94% e 98%, respectivamente.[32] No entanto, o teste não está disponível comercialmente nem é realizado de forma rotineira nos laboratórios de referência. Na sua ausência, a toxoplasmose congênita pode ser definitivamente diagnosticada pela persistência de anticorpos IgG anti-Toxoplasma além do primeiro ano de vida, refletindo a resposta imune do bebê.[11]
Pacientes que são imunocomprometidos
A suspeita de toxoplasmose deve ser alta para os pacientes imunocomprometidos, seja em decorrência de vírus da imunodeficiência humana/síndrome de imunodeficiência adquirida (HIV/AIDS), medicamentos imunossupressores ou outras causas, que apresentam febre e alteração do estado mental, convulsão ou outro deficit neurológico focal com lesões realçadas na tomografia computadorizada ou ressonância magnética do cérebro. Caso um paciente imunossuprimido apresente febre, mal-estar, hepatite, pneumonite, miocardite ou coriorretinite, a toxoplasmose deverá ser incluída no diagnóstico diferencial. As lesões no sistema nervoso central geralmente são múltiplas, sendo observadas com maior frequência nos pacientes infectados com HIV. Os receptores de transplante podem apresentar doença cardíaca, pulmonar ou disseminada.
O primeiro teste a ser feito na avaliação da toxoplasmose é a sorologia para IgG anti-Toxoplasma. No entanto, as sorologias podem ser difíceis de interpretar naqueles que são imunocomprometidos devido aos níveis geralmente baixos de imunoglobulinas. A reação em cadeia da polimerase para Toxoplasma pode ser feita em uma amostra de sangue ou de outros fluidos corporais ou tecidos, dependendo da localização dos sintomas. Além disso, a biópsia de um órgão afetado (por exemplo, biópsia cardíaca em um paciente com miocardite) pode revelar o diagnóstico.
O ensaio de immunospot ligado a enzimas pode ser útil na estratificação do risco de recorrência da encefalite toxoplásmica em pacientes infectados com HIV e T gondii com IgG+.[33] No entanto, este ensaio não é usado nos laboratórios de referência porque ainda não foram determinados os valores de corte visando a diferenciação de pacientes com respostas imunes específicas de T gondii adequadas ou insuficientes.[Figure caption and citation for the preceding image starts]: Tomografia computadorizada: cérebro da toxoplasmose no sistema nervoso centralDo acervo de Louis M. Weiss, MD, MPH; uso autorizado [Citation ends].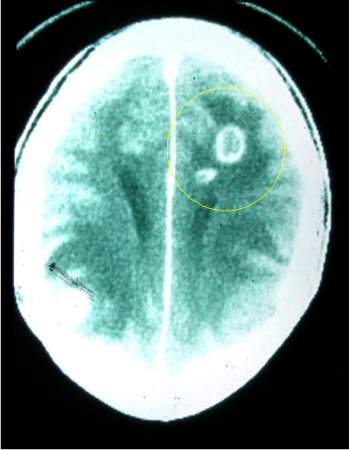 [Figure caption and citation for the preceding image starts]: Patologia cerebral: embora esta seja uma patologia do tecido de camundongo, ela é muito semelhante em aparência à do tecido humanoDo acervo de Louis M. Weiss, MD, MPH; uso autorizado [Citation ends].
[Figure caption and citation for the preceding image starts]: Patologia cerebral: embora esta seja uma patologia do tecido de camundongo, ela é muito semelhante em aparência à do tecido humanoDo acervo de Louis M. Weiss, MD, MPH; uso autorizado [Citation ends].
Coriorretinite
A maioria dos casos de coriorretinite toxoplásmica decorre de infecção congênita que não se torna clinicamente aparente até a reativação no olho. No entanto, foram relatados surtos de coriorretinite aguda correlacionada com contaminação pela água.[34] Embora a presença de lesões no fundo de olho deva motivar a suspeita de toxoplasmose, a comprovação de que o Toxoplasma é a causa dessa doença é frequentemente inexistente. Os títulos de anticorpos séricos são geralmente baixos na presença de lesões oculares ativas causadas por doença congênita. Além disso, a aparência das lesões inflamatórias não é exclusiva da toxoplasmose. Lesões semelhantes podem ser encontradas com outras doenças granulomatosas, como tuberculose, doença da arranhadura do gato ou toxocaríase. Em pessoas imunocomprometidas, o citomegalovírus, o vírus do herpes simples ou a sífilis também devem ser considerados.
Após o exame oftalmológico completo revelar evidências de lesão retiniana com inflamação relacionada, deve-se verificar a sorologia em busca de evidências de infecção anterior. Em geral, se as lesões retinianas forem características e as sorologias positivas, o diagnóstico provável será de coriorretinite toxoplásmica. Se as lesões retinianas forem atípicas e as sorologias forem positivas, o diagnóstico será menos conclusivo. A reação em cadeia da polimerase para Toxoplasma pode ser realizada em fluido aquoso ou vítreo do olho para auxiliar no diagnóstico e está disponível comercialmente.[35]
Caso se trate de paciente neonato ou lactente com doença congênita, as lesões típicas serão bilaterais. Caso se trate de paciente pediátrico ou adolescente com reativação da doença congênita, as lesões ativas poderão surgir na periferia das cicatrizes retinianas anteriores, sendo geralmente unilaterais. Em ambos os casos, haverá presença de IgG anti-Toxoplasma, ainda que provavelmente com baixos títulos, não estando a IgM geralmente presente.
A American Academy of Pediatrics recomenda a avaliação seriada, preferencialmente por um especialista em retina, para os lactentes com toxoplasmose congênita confirmada até o final do terceiro ano de vida, mesmo que o exame inicial seja negativo. Eles também recomendam o acompanhamento oftalmológico estrito dos lactentes com alta suspeita de toxoplasmose congênita até que a infecção seja descartada na sorologia.[11]
Caso se trate de paciente adulto com doença oftalmológica aguda, as lesões retinianas ativas geralmente serão unilaterais, e os resultados de IgM e/ou IgG serão positivos. Evidências sugerem diferenças de gênero nas apresentações da toxoplasmose ocular. Homens apresentam, com mais frequência, doença primária ativa, em comparação com mulheres (24.4% vc 12.9%), enquanto as mulheres apresentam, com mais frequência, doença recorrente ativa (36.0% vs. 28.5% em homens). Além disso, a lesões retinianas, inclusive a mácula, são mais comuns em mulheres (56.1% vs. 39.8% para homens), indicando um potencial aumento do risco de comprometimento da visão central. Apesar dessas diferenças nos quadros clínicos, os desfechos gerais, como acuidade visual e complicações oculares, foram similares.[36]
Se os resultados de IgG e IgM antitoxoplasma forem negativos no soro não diluído, provavelmente a coriorretinite não será decorrente de toxoplasmose. A demonstração de anticorpos antitoxoplasma ou de DNA de Toxoplasma pela reação em cadeia da polimerase no humor aquoso da câmara anterior do olho afetado pode estabelecer o diagnóstico nos casos duvidosos, porém, os riscos desse procedimento quase nunca superam o risco baixo dos ciclos curtos de tratamento, sendo que os médicos com frequência prescrevem um ciclo de tratamento.[37]
O uso deste conteúdo está sujeito ao nosso aviso legal