O manejo do diabetes do tipo 2 envolve uma série de intervenções comportamentais e farmacológicas para prevenir ou protelar complicações e otimizar a qualidade de vida.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
O manejo precisa ser individualizado, levando em consideração as necessidades e circunstâncias específicas do paciente, sendo as metas glicêmicas discutidas e acordadas com ele. Dieta e estilo de vida são fundamentais para esse manejo. A educação estruturada deve ser oferecida ao paciente (e/ou aos seus familiares ou cuidadores) no momento do diagnóstico e próximo a ele, com reforço e revisão anuais.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
A educação contínua sobre automanejo por uma enfermeira educadora em diabetes ou nutricionista promove o autocuidado com o diabetes e dá suporte a mudanças benéficas no estilo de vida.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[103]Sherifali D, Bai JW, Kenny M, et al. Diabetes self-management programmes in older adults: a systematic review and meta-analysis. Diabet Med. 2015 Nov;32(11):1404-14.
https://onlinelibrary.wiley.com/doi/full/10.1111/dme.12780
http://www.ncbi.nlm.nih.gov/pubmed/25865179?tool=bestpractice.com
[104]Pillay J, Armstrong MJ, Butalia S, et al. Behavioral programs for type 2 diabetes mellitus: a systematic review and network meta-analysis. Ann Intern Med. 2015 Dec 1;163(11):848-60.
http://annals.org/aim/article/2446188/behavioral-programs-type-2-diabetes-mellitus-systematic-review-network-meta
http://www.ncbi.nlm.nih.gov/pubmed/26414227?tool=bestpractice.com
[105]Chatterjee S, Davies MJ, Heller S, et al. Diabetes structured self-management education programmes: a narrative review and current innovations. Lancet Diabetes Endocrinol. 2018 Feb;6(2):130-42.
http://www.ncbi.nlm.nih.gov/pubmed/28970034?tool=bestpractice.com
Isso requer conhecimento geral sobre nutrição e estilo de vida saudável, nutrição individualizada e planos de exercícios com base em uma avaliação inicial e metas de tratamento.
Intervenções que melhoram o automanejo podem reduzir o desconforto do diabetes significativamente.[106]Fisher L, Hessler D, Glasgow RE, et al. REDEEM: a pragmatic trial to reduce diabetes distress. Diabetes Care. 2013 Sep;36(9):2551-8.
http://care.diabetesjournals.org/content/36/9/2551.long
http://www.ncbi.nlm.nih.gov/pubmed/23735726?tool=bestpractice.com
A assistência aos adultos com diabetes do tipo 2 deve incluir o controle imediato de todos os fatores de risco cardiovascular importantes para atingir metas individualizadas. Além do controle da glicose, isso inclui o abandono do hábito de fumar, controle da pressão arterial, controle lipídico, consideração do uso de antiagregantes plaquetários para os pacientes com alto risco de doença cardiovascular (DCV) e medidas para reduzir a evolução da doença renal relacionada ao diabetes.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[107]Cheng J, Zhang W, Zhang X, et al. Effect of angiotensin-converting enzyme inhibitors and angiotensin II receptor blockers on all-cause mortality, cardiovascular deaths, and cardiovascular events in patients with diabetes mellitus: a meta-analysis. JAMA Intern Med. 2014 May;174(5):773-85.
http://www.ncbi.nlm.nih.gov/pubmed/24687000?tool=bestpractice.com
O uso de agentes anti-hiperglicêmicos é fundamental para o tratamento do diabetes do tipo 2. A seleção de medicamentos é baseada em fatores como circunstâncias clínicas e preferências do paciente; a eficácia do medicamento em termos de resposta metabólica e, principalmente, de proteção cardiovascular e renal; bem como seus requisitos de segurança, tolerabilidade e monitoramento.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Além disso, considerações especiais devem ser feitas para aqueles com diabetes do tipo 2 e doença renal crônica, como o uso de inibidores da ECA ou antagonistas do receptor de angiotensina II e inibidores da proteína cotransportadora de sódio e glicose 2 (SGLT2) quando a proteinúria está presente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Cuidados individualizados
Adote uma abordagem individualizada para o tratamento, adaptada às necessidades e circunstâncias específicas do seu paciente. Em relação ao paciente, leve em consideração:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Preferências pessoais
Comorbidades
Riscos da polimedicação
Capacidade de se beneficiar de intervenções em longo prazo
Deficiências (por exemplo, comprometimento visual).
Isso é particularmente importante em um contexto de multimorbidade.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Discuta e chegue a um acordo sobre uma meta individual de HbA1c com o paciente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Para determinar a meta mais adequada de HbA1c para seu paciente, consulte os protocolos locais e um especialista, caso necessário. Considere relaxar o nível alvo de HbA1c caso a caso, se for apropriado para o seu paciente individual, com atenção especial para aqueles que são idosos ou frágeis (veja abaixo).[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Encoraje o paciente a atingir o seu objetivo e mantê-lo, a menos que quaisquer efeitos adversos resultantes (incluindo hipoglicemia) ou o esforço necessário para atingir os seus objetivos prejudiquem a sua qualidade de vida.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Use cada revisão para reavaliar as necessidades e circunstâncias do paciente e considerar se é necessário suspender algum medicamento que não seja efetivo.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Procure fazer uma avaliação rotineira da fragilidade sempre que examinar um idoso com diabetes.[83]Strain WD, Hope SV, Green A, et al. Type 2 diabetes mellitus in older people: a brief statement of key principles of modern day management including the assessment of frailty – a national collaborative stakeholder initiative. Diabet Med. 2018 Jul;35(7):838-45.
https://onlinelibrary.wiley.com/doi/10.1111/dme.13644
http://www.ncbi.nlm.nih.gov/pubmed/29633351?tool=bestpractice.com
[84]Sinclair A, Gallagher A. Managing frailty and associated comorbidities in older adults with diabetes: position statement on behalf of the Association of British Clinical Diabetologists (ABCD). 2019 [internet publication].
https://abcd.care/sites/abcd.care/files/site_uploads/Resources/Position-Papers/ABCD-Position-Paper-Frailty.pdf
[85]Strain WD, Down S, Brown P, et al. Diabetes and frailty: an expert consensus statement on the management of older adults with type 2 diabetes. Diabetes Ther. 2021 May;12(5):1227-47.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8099963
http://www.ncbi.nlm.nih.gov/pubmed/33830409?tool=bestpractice.com
Use uma ferramenta validada (por exemplo, o Índice de Fragilidade eletrônico [eFI], o escore de fragilidade Rockwood ou Timed Up and Go) para confirmar uma suspeita clínica de fragilidade.[84]Sinclair A, Gallagher A. Managing frailty and associated comorbidities in older adults with diabetes: position statement on behalf of the Association of British Clinical Diabetologists (ABCD). 2019 [internet publication].
https://abcd.care/sites/abcd.care/files/site_uploads/Resources/Position-Papers/ABCD-Position-Paper-Frailty.pdf
[85]Strain WD, Down S, Brown P, et al. Diabetes and frailty: an expert consensus statement on the management of older adults with type 2 diabetes. Diabetes Ther. 2021 May;12(5):1227-47.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8099963
http://www.ncbi.nlm.nih.gov/pubmed/33830409?tool=bestpractice.com
Os pacientes frágeis precisam de uma abordagem personalizada para o tratamento; a redução da terapia é tão importante quanto a intensificação. Especificamente, tenha em mente que:[83]Strain WD, Hope SV, Green A, et al. Type 2 diabetes mellitus in older people: a brief statement of key principles of modern day management including the assessment of frailty – a national collaborative stakeholder initiative. Diabet Med. 2018 Jul;35(7):838-45.
https://onlinelibrary.wiley.com/doi/10.1111/dme.13644
http://www.ncbi.nlm.nih.gov/pubmed/29633351?tool=bestpractice.com
As metas glicêmicas recomendadas para um bom controle em pessoas jovens em boa forma são muito rígidas para os pacientes idosos frágeis.[83]Strain WD, Hope SV, Green A, et al. Type 2 diabetes mellitus in older people: a brief statement of key principles of modern day management including the assessment of frailty – a national collaborative stakeholder initiative. Diabet Med. 2018 Jul;35(7):838-45.
https://onlinelibrary.wiley.com/doi/10.1111/dme.13644
http://www.ncbi.nlm.nih.gov/pubmed/29633351?tool=bestpractice.com
[84]Sinclair A, Gallagher A. Managing frailty and associated comorbidities in older adults with diabetes: position statement on behalf of the Association of British Clinical Diabetologists (ABCD). 2019 [internet publication].
https://abcd.care/sites/abcd.care/files/site_uploads/Resources/Position-Papers/ABCD-Position-Paper-Frailty.pdf
Verifique seus protocolos locais e considere consultar um especialista.
Os esquemas de medicamentos mais adequados para um paciente frágil, incluindo a escolha do medicamento e a dose ideal, precisarão de consideração cuidadosa.[83]Strain WD, Hope SV, Green A, et al. Type 2 diabetes mellitus in older people: a brief statement of key principles of modern day management including the assessment of frailty – a national collaborative stakeholder initiative. Diabet Med. 2018 Jul;35(7):838-45.
https://onlinelibrary.wiley.com/doi/10.1111/dme.13644
http://www.ncbi.nlm.nih.gov/pubmed/29633351?tool=bestpractice.com
"Comece devagar e avance devagar" ao dosar e ajustar medicamentos em idosos frágeis.[83]Strain WD, Hope SV, Green A, et al. Type 2 diabetes mellitus in older people: a brief statement of key principles of modern day management including the assessment of frailty – a national collaborative stakeholder initiative. Diabet Med. 2018 Jul;35(7):838-45.
https://onlinelibrary.wiley.com/doi/10.1111/dme.13644
http://www.ncbi.nlm.nih.gov/pubmed/29633351?tool=bestpractice.com
Equilibre o benefício pretendido do tratamento com o risco de efeitos adversos do tratamento.[108]Hambling CE, Khunti K, Cos X, et al. Factors influencing safe glucose-lowering in older adults with type 2 diabetes: a PeRsOn-centred ApproaCh To IndiVidualisEd (PROACTIVE) glycemic goals for older people: a position statement of Primary Care Diabetes Europe. Prim Care Diabetes. 2019 Aug;13(4):330-52.
https://www.primary-care-diabetes.com/article/S1751-9918(18)30300-0/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/30792156?tool=bestpractice.com
Na prática, a menos que receba orientação em contrário de uma necessidade clínica específica ou esquema de dosagem, aguarde de 3 a 6 meses para avaliar o impacto de qualquer intervenção que busque melhorar o controle glicêmico, seja farmacológica ou não farmacológica. Tenha em mente que esse prazo varia de acordo com cada paciente e com os níveis iniciais de glicose no sangue; considere cuidadosamente o risco que a HbA1c do paciente pode representar e avance para intervenções mais intensas mais rapidamente, se necessário.
Dieta, atividade física e sono
O aconselhamento nutricional deve ser adaptado às necessidades do paciente e deve ser fornecido por um profissional da saúde com experiência e competência específicas em nutrição.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
As diretrizes da European Association for the Study of Diabetes (EASD) para o manejo alimentar do diabetes observam que uma variedade de alimentos e padrões alimentares são adequados para o manejo do diabetes.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
O National Institute for Health and Care Excellence (NICE) do Reino Unido e a EASD recomendam incentivar o paciente a seguir os mesmos conselhos de alimentação saudável que a população em geral.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Em particular, incentive o paciente a:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Incluir fontes de carboidratos minimamente processados, ricas em fibras e com baixo índice glicêmico em sua dieta, como frutas, vegetais, nozes, sementes, grãos integrais e leguminosas
Consumir laticínios com baixo teor de gordura e peixes oleosos
Limitar o consumo de alimentos que contêm ácidos graxos saturados e trans
Minimizar o consumo de carnes vermelhas e processadas, sódio, bebidas açucaradas e grãos refinados.
Ofereça recomendações individualizadas sobre consumo de carboidratos e bebidas alcoólicas e padrões de refeições.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Reduzir o risco de hipoglicemia deve ser um objetivo particular para o indivíduo que faz uso de insulina ou de secretagogo de insulina.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Incentive a ingestão de açúcares livres ou adicionados abaixo de 10% da ingestão total de energia.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Adoçantes não nutritivos podem ser usados para substituir açúcares em alimentos e bebidas.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Embora a substituição limitada de alimentos contendo sacarose por outros carboidratos no plano alimentar seja permitida, aconselhe o paciente a ter cuidado para evitar um consumo excessivo de energia.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
A ingestão de fibra alimentar deve ser de pelo menos 35 g/dia, sendo considerados alimentos enriquecidos com fibras e suplementos de fibras quando não for possível obter uma ingestão suficiente apenas com a dieta.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Desencoraje o paciente de comer alimentos comercializados especificamente para pessoas com diabetes.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Há um debate constante sobre o potencial papel das dietas com baixo teor de carboidratos em indivíduos com diabetes do tipo 2. Evidências sugerem que essas dietas podem ser seguras e eficazes em curto prazo para controlar o peso e melhorar o controle glicêmico e o risco cardiovascular.[109]Diabetes UK. Position statement: low carb diets for people with diabetes. May 2021 [internet publication].
https://www.diabetes.org.uk/professionals/position-statements-reports/food-nutrition-lifestyle/low-carb-diets-for-people-with-diabetes
Uma metanálise não encontrou nenhuma diferença nos efeitos de redução da glicose, peso ou níveis de colesterol de lipoproteína de baixa densidade (LDL) entre dietas com baixo e alto teor de carboidratos a 1 ano ou mais.[110]Snorgaard O, Poulsen GM, Andersen HK, et al. Systematic review and meta-analysis of dietary carbohydrate restriction in patients with type 2 diabetes. BMJ Open Diabetes Res Care. 2017 Feb 23;5(1):e000354.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5337734
http://www.ncbi.nlm.nih.gov/pubmed/28316796?tool=bestpractice.com
Outra metanálise concluiu que havia evidências de qualidade moderada a baixa de que alguns pacientes podem alcançar a remissão do diabetes do tipo 2 ao seguirem uma dieta com baixo teor de carboidratos por 6 meses.[111]Goldenberg JZ, Day A, Brinkworth GD, et al. Efficacy and safety of low and very low carbohydrate diets for type 2 diabetes remission: systematic review and meta-analysis of published and unpublished randomized trial data. BMJ. 2021 Jan 13;372:m4743.
https://www.bmj.com/content/372/bmj.m4743.long
http://www.ncbi.nlm.nih.gov/pubmed/33441384?tool=bestpractice.com
A EASD não recomenda dietas cetogênicas com muito baixo teor de carboidratos.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
A American Diabetes Association (ADA) recomenda considerar a redução da ingestão de carboidratos em geral para os adultos para melhorar o controle glicêmico.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Uma variedade de padrões alimentares, que abrangem alguns dos princípios fundamentais descritos acima, são recomendados pela EASD, incluindo as dietas mediterrânica, nórdica e vegetariana/vegana.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Os padrões alimentares mediterrâneo ou baseado em vegetais com alto teor de gordura insaturada também são recomendados pela European Society of Cardiology (ESC) para reduzir o risco cardiovascular, sendo o primeiro também recomendados pela ADA.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Há evidências crescentes de que as dietas mediterrânea e vegetariana/vegana melhoram a glicemia e outros fatores de risco cardiometabólicos nas pessoas com diabetes do tipo 2, com a dieta nórdica melhorando o IMC e outros fatores de risco cardiometabólicos.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
[112]Papamichou D, Panagiotakos DB, Itsiopoulos C. Dietary patterns and management of type 2 diabetes: a systematic review of randomised clinical trials. Nutr Metab Cardiovasc Dis. 2019 Jun;29(6):531-43.
https://www.primary-care-diabetes.com/article/S1751-9918(18)30300-0/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/30952576?tool=bestpractice.com
[113]Pollakova D, Andreadi A, Pacifici F, et al. The impact of vegan diet in the prevention and treatment of type 2 diabetes: a systematic review. Nutrients. 2021 Jun 21;13(6):2123.
https://www.mdpi.com/2072-6643/13/6/2123
http://www.ncbi.nlm.nih.gov/pubmed/34205679?tool=bestpractice.com
[114]Tosatti JAG, Alves MT, Gomes KB. The role of the mediterranean dietary pattern on metabolic control of patients with diabetes mellitus: a narrative review. Adv Exp Med Biol. 2021;1307:115-28.
http://www.ncbi.nlm.nih.gov/pubmed/32253710?tool=bestpractice.com
No entanto, é necessário cuidado para evitar a exclusão de nutrientes importantes em longo prazo.
Não há evidências suficientes para recomendar o uso rotineiro de suplementos fitoterápicos e micronutrientes (por exemplo, canela, curcumina, vitamina D, aloe vera) para melhorar o controle glicêmico em pacientes com diabetes.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Integre as orientações alimentares a um plano personalizado de controle do diabetes que inclua outros aspectos de alteração do estilo de vida, incluindo aumentar a atividade física e perder peso.[28]World Gastroenterology Organisation and International Federation for the Surgery of Obesity and Metabolic Diseases. IFSO-WGO guidelines on obesity. 2023 [internet publication].
https://www.worldgastroenterology.org/guidelines/obesity/obesity-english
[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[115]National Institute for Health and Care Excellence. Preventing excess weight gain. March 2015 [internet publication].
https://www.nice.org.uk/guidance/ng7
[116]National Institute for Health and Care Excellence. Weight management: lifestyle services for overweight or obese adults. May 2014 [internet publication].
https://www.nice.org.uk/guidance/ph53
[117]National Institute for Health and Care Excellence. Obesity: identification, assessment and management. July 2023 [internet publication].
https://www.nice.org.uk/guidance/cg189
[118]National Institute for Health and Care Excellence. Physical activity: brief advice for adults in primary care. May 2013 [internet publication].
https://www.nice.org.uk/guidance/ph44
Em termos de atividade física, incentive o paciente a:
Reduzir o comportamento sedentário e a ser fisicamente mais ativo.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[115]National Institute for Health and Care Excellence. Preventing excess weight gain. March 2015 [internet publication].
https://www.nice.org.uk/guidance/ng7
Incorporar atividades em sua vida diária (por exemplo, caminhada rápida, jardinagem, andar de bicicleta).[115]National Institute for Health and Care Excellence. Preventing excess weight gain. March 2015 [internet publication].
https://www.nice.org.uk/guidance/ng7
[117]National Institute for Health and Care Excellence. Obesity: identification, assessment and management. July 2023 [internet publication].
https://www.nice.org.uk/guidance/cg189
Dessa forma, o paciente pode aumentar gradualmente a quantidade e a intensidade das atividades praticadas.[115]National Institute for Health and Care Excellence. Preventing excess weight gain. March 2015 [internet publication].
https://www.nice.org.uk/guidance/ng7
Faça 45-60 minutos de atividade de intensidade moderada por dia, principalmente se não reduzir a ingestão de energia, para prevenir a obesidade. Aconselhe as pessoas que vivem com obesidade e perderam peso que podem precisar fazer 60-90 minutos de atividade por dia para evitar recuperar o peso.[117]National Institute for Health and Care Excellence. Obesity: identification, assessment and management. July 2023 [internet publication].
https://www.nice.org.uk/guidance/cg189
Uma revisão sistemática e metanálise de estudos observacionais concluiu que a atividade física, mesmo abaixo das quantidades recomendadas, estava associada à redução da incidência de complicações relacionadas ao diabetes.[119]Rietz M, Lehr A, Mino E, et al. Physical activity and risk of major diabetes-related complications in individuals with diabetes: a systematic review and meta-analysis of observational studies. Diabetes Care. 2022 Dec 1;45(12):3101-11.
https://link.springer.com/chapter/10.1007/5584_2020_513
http://www.ncbi.nlm.nih.gov/pubmed/36455117?tool=bestpractice.com
Tanto a ADA quanto a ESC recomendam orientar os pacientes sobre os níveis semanais mínimos ideais de exercício aeróbio: 150 minutos por semana em intensidade moderada, ou 75 minutos por semana em intensidade vigorosa (se não houver contraindicações).[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Elas também recomendam que, além do exercício aeróbio, o exercício de resistência deve ser realizado pelo menos duas vezes por semana (desde que não seja contraindicado) para se obterem benefícios adicionais.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Ambas recomendam que todas as pessoas com diabetes sejam incentivadas a aumentar seu nível de atividade física (por exemplo, caminhada, jardinagem, tarefas domésticas, ioga, dança, natação) acima do nível basal, mesmo que não atinjam os níveis ideais de exercício recomendados.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A ESC também faz as seguintes recomendações sobre atividade física em indivíduos com diabetes do tipo 2:[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
As intervenções de exercícios devem ser adaptadas a qualquer comorbidade e/ou complicação do diabetes (por exemplo, fragilidade, neuropatia, retinopatia).
Considere intervenções baseadas na teoria comportamental (por exemplo, estabelecer metas) para incentivar a prática de exercícios.
O uso de intervenções estruturadas com exercícios para os pacientes com DCV estabelecida para beneficiar o controle metabólico, a capacidade de exercício e a qualidade de vida, e redução dos eventos cardiovasculares. Um teste ergométrico deve ser considerado nesses pacientes antes de se iniciar um programa de exercícios estruturado.
Se o paciente estiver com sobrepeso:
O NICE recomenda uma meta inicial de perda de peso corporal de 5% a 10%.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Evidências sugerem que uma perda de peso de >5% em adultos com sobrepeso ou obesidade melhora o controle glicêmico, os níveis lipídicos e a pressão arterial.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Os programas de perda de peso com alimentação saudável e atividade física que resultam em um deficit energético podem levar à remissão do diabetes do tipo 2.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
[49]Evert AB, Dennison M, Gardner CD, et al. Nutrition therapy for adults with diabetes or prediabetes: a consensus report. Diabetes Care. 2019 May;42(5):731-54.
https://care.diabetesjournals.org/content/42/5/731.long
http://www.ncbi.nlm.nih.gov/pubmed/31000505?tool=bestpractice.com
[120]Lean ME, Leslie WS, Barnes AC, et al. Primary care-led weight management for remission of type 2 diabetes (DiRECT): an open-label, cluster-randomised trial. Lancet. 2018 Feb 10;391(10120):541-51.
http://www.ncbi.nlm.nih.gov/pubmed/29221645?tool=bestpractice.com
[121]Gregg EW, Chen H, Wagenknecht LE, et al; Look AHEAD Research Group. Association of an intensive lifestyle intervention with remission of type 2 diabetes. JAMA. 2012 Dec 19;308(23):2489-96.
https://jamanetwork.com/journals/jama/fullarticle/1486829
http://www.ncbi.nlm.nih.gov/pubmed/23288372?tool=bestpractice.com
A EASD recomenda um programa de substituição total da dieta de baixa energia (por exemplo, 3500 kJ/dia [840 kcal/dia] por 12 a 20 semanas), fornecido por profissionais da saúde treinados, com medicamentos hipoglicemiantes e anti-hipertensivos cuidadosamente ajustados, para proporcionar perda de peso suficiente para induzir a remissão do diabetes do tipo 2 (10% a 15 % de peso corporal ou superior).[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
O Ensaio Clínico de Remissão de Diabetes (DiRECT) de controle de perda de peso com apoio para pessoas diagnosticadas com diabetes do tipo 2 nos últimos 6 anos e um índice de massa corporal (IMC) de 27 kg/m² a 45 kg/m², constatou que quase metade dos participantes alcançou remissão para um estado não diabético e sem uso de medicamentos antidiabéticos a 12 meses.[120]Lean ME, Leslie WS, Barnes AC, et al. Primary care-led weight management for remission of type 2 diabetes (DiRECT): an open-label, cluster-randomised trial. Lancet. 2018 Feb 10;391(10120):541-51.
http://www.ncbi.nlm.nih.gov/pubmed/29221645?tool=bestpractice.com
Após 2 anos, mais de um terço dos participantes do ensaio apresentou remissão sustentada.[122]Lean ME, Leslie WS, Barnes AC, et al. Durability of a primary care-led weight-management intervention for remission of type 2 diabetes: 2-year results of the DiRECT open-label, cluster-randomised trial. Lancet Diabetes Endocrinol. 2019 May;7(5):344-55.
http://www.ncbi.nlm.nih.gov/pubmed/30852132?tool=bestpractice.com
Apoie o paciente com tratamentos baseados em evidências para alcançar e manter a perda de peso. Com o auxílio de profissionais da saúde treinados, podem ser utilizados diversos tipos de dietas para perda de peso e composições de macronutrientes, desde que atendam a outras recomendações alimentares.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Isso inclui produtos de fórmula nutricionalmente completos e de baixo valor energético, no entanto, nem dietas cetogênicas com alto teor de carboidratos, nem dietas cetogênicas com muito baixo teor de carboidratos são recomendadas pela EASD.[45]Diabetes and Nutrition Study Group (DNSG) of the European Association for the Study of Diabetes (EASD). Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023 Jun;66(6):965-85.
https://link.springer.com/article/10.1007/s00125-023-05894-8
http://www.ncbi.nlm.nih.gov/pubmed/37069434?tool=bestpractice.com
Após o sucesso de um esquema piloto, o National Health Service da Inglaterra está expandindo seu programa de 3 meses de sopas e shakes substitutos totais da dieta para pessoas diagnosticadas com diabetes do tipo 2 nos últimos 6 meses.[123]NHS England. NHS to expand soups and shakes for people with type 2 diabetes. April 2023 [internet publication].
https://www.england.nhs.uk/2023/04/nhs-to-expand-soups-and-shakes-for-people-with-type-2-diabetes
Considere fazer exames para verificar a saúde do sono, incluindo sintomas de distúrbios do sono, interrupção do sono devido a sintomas de diabetes ou necessidades de manejo, e preocupação com o sono.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Considere consultar um especialista em sono.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
A obesidade e o diabetes são fatores de risco para apneia do sono, e um sono inadequado pode afetar o controle glicêmico.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Estudos demonstraram que a adesão a um estilo de vida saudável (por exemplo, dieta favorável, atividade física, não fumar, ingestão moderada de álcool e peso normal) está associada a um risco relativo reduzido de mortalidade em pessoas com diabetes do tipo 2.[48]Schlesinger S, Neuenschwander M, Ballon A, et al. Adherence to healthy lifestyles and incidence of diabetes and mortality among individuals with diabetes: a systematic review and meta-analysis of prospective studies. J Epidemiol Community Health. 2020 May;74(5):481-487.
http://www.ncbi.nlm.nih.gov/pubmed/32075860?tool=bestpractice.com
Manejo do risco cardiovascular
Pressão arterial (PA)
Consulte seus protocolos locais. As diretrizes diferem em relação às metas recomendadas de PA para as pessoas com diabetes do tipo 2.
Nas pesquisas EUROASPIRE mais recentes (EAIV 2012/13 e EAV 2016/17), 80% dos homens e 87% das mulheres com diagnóstico de diabetes também tinham história de hipertensão.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
O controle ideal da PA reduz o risco de complicações microvasculares e macrovasculares.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
O NICE recomenda manter a PA com mudanças de estilo de vida ou tratamento medicamentoso para atingir metas de:[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Abaixo de 135/85 mmHg para adultos com menos de 80 anos, com base no monitoramento ambulatorial ou domiciliar da PA (ou <140/90 mmHg com base na PA clínica)
Abaixo de 145/85 mmHg para pacientes com 80 anos ou mais, com base no monitoramento ambulatorial ou domiciliar da PA (ou <150/90 mmHg com base na PA clínica)
Abaixo de 130/80 mmHg (PA clínica) para pacientes com doença renal crônica (DRC) e relação albumina/creatinina (RCA) de 70 mg/mmol ou mais; abaixo de 140/90 mmHg (PA clínica) para aqueles com DRC e RCA <70 mg/mmol.
Embora o NICE recomende o uso do julgamento clínico para os pacientes com fragilidade ou múltiplas morbidades, seu comitê de diretrizes concluiu que não havia evidências que sugerissem que as metas de PA deveriam ser diferentes nas pessoas com diabetes do tipo 2; portanto, essas recomendações para metas de PA se aplicam a pessoas com e sem diabetes do tipo 2.[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
O NICE também recomenda usar as mesmas metas de PA para pessoas com e sem doenças cardiovasculares.[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
O NICE ressalta a importância de se fazer a medição da PA em posição ortostática e deitada/sentada nos indivíduos com diabetes do tipo 2, com base na opinião de especialistas no sentido de que esse grupo de pacientes tem maior risco que o normal de hipotensão postural:[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Se houver uma queda na leitura sistólica após ficar em posição ortostática por pelo menos um minuto (a partir da posição deitada ou sentada) de 20 mmHg ou mais (ou 10 mmHg ou mais na leitura diastólica), as causas prováveis (incluindo os medicamentos atuais) devem ser consideradas e manejadas adequadamente (por exemplo, medidas para prevenção de queda), e as futuras leituras de PA devem ser realizadas na posição ortostática.
Uma avaliação mais aprofundada por um especialista deve ser considerada se os sintomas persistirem apesar dessas medidas, ou se as medições da PA (realizadas na posição deitada ou ortostática) não confirmarem hipotensão postural apesar de os sintomas serem sugestivos.
Se o paciente apresentar uma queda postural significativa na PA ou sintomas de hipotensão postural (por exemplo, quedas, tontura postural), o NICE recomenda tratar a hipertensão até se atingir uma meta com base em medições na posição ortostática.
As diretrizes de 2023 da ESC sobre o tratamento da DCV no diabetes recomendam uma abordagem individualizada para tratar a hipertensão nos indivíduos com diabetes:[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Nos indivíduos até 65 anos de idade: PA sistólica (PAS) alvo de 130 mmHg e <130 mmHg, se tolerada (mas não inferior a 120 mmHg)
E idosos (>65 anos de idade): PAS alvo de 130 a 139 mmHg
Uma meta de PAS <130 mmHg pode ser considerada para reduzir ainda mais o risco de AVC nos pacientes com risco particularmente alto de evento cerebrovascular.
Independentemente da meta específica de PA, tanto as mudanças de estilo de vida como os medicamentos anti-hipertensivos podem ser necessários para se atingir o controle da PA. Ficou demonstrado que a redução no consumo de sódio (para <100 mmol/dia) e o alto consumo de frutas, vegetais e laticínios com baixo teor de gordura melhoram o controle da PA.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Essa modificação do estilo de vida é apoiada pela ESC para os indivíduos com diabetes do tipo 2 e hipertensão, além de restrição das bebidas alcoólicas, aumento da prática de exercícios e perda do peso, quando adequado.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
No Reino Unido, o NICE recomenda uma abordagem gradual ao tratamento farmacológico da hipertensão em pessoas sem DRC, ou com DRC e uma RAC de ≤30 mg/mmol (categorias A1 e A2 de RAC), como se segue.[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
[86]National Institute for Health and Care Excellence. Chronic kidney disease: assessment and management. November 2021 [internet publication].
https://www.nice.org.uk/guidance/ng203
Para recomendações sobre a escolha do agente hipertensivo em pessoas com DRC e uma RAC >30 mg/mmol (categoria A3 ou superior de RAC), veja abaixo Considerações farmacoterapêuticas específicas para pacientes com DRC.
Etapa 1[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Para o tratamento inicial, administre:
Etapa 2[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Caso a hipertensão continue descontrolada com as terapias de primeira linha:
Etapa 3[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Antes de considerar a próxima etapa do tratamento, discuta a adesão com o paciente e reveja os medicamentos para garantir que estejam sendo tomados às doses ideais toleradas.
Se a PA do paciente continuar descontrolada apesar das terapias de etapa 2, ofereça uma combinação de terapia tripla com:
Etapa 4[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Se a PA não for controlada apesar das doses ideais toleradas dos medicamentos da terapia tripla na etapa 3, considere que o paciente apresenta uma hipertensão resistente. Antes de considerar tratamento adicional, confirme as medições clínicas da PA elevadas usando registros ambulatoriais ou domiciliares da PA, avalie a hipotensão postural e discuta a adesão. Para as pessoas com hipertensão resistente confirmada, considere adicionar um quarto medicamento anti-hipertensivo ou encaminhe esses pacientes a um especialista em hipertensão. Considere também possíveis causas secundárias de hipertensão (por exemplo, adenoma de Conn, feocromocitoma, hipertensão renovascular): nas pessoas com sinais e sintomas que sugiram uma causa secundária, considere a necessidade de investigações especializadas e/ou encaminhamento. Os pacientes com PA com quatro medicamentos anti-hipertensivos ainda não controlada devem ser encaminhados a um especialista.
Para pessoas com doenças cardiovasculares, siga as recomendações para indicações específicas da doença nas diretrizes NICE para sua condição.[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Se a PA permanecer descontrolada, ofereça tratamento medicamentoso anti-hipertensivo de acordo com a terapia gradual descrita acima.[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
A diretriz da ESC adota uma abordagem amplamente semelhante à do NICE, mas destaca mensagens importantes:[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Há fortes evidências para apoiar o uso de um inibidor da ECA ou antagonista do receptor de angiotensina II, particularmente nos pacientes que têm microalbuminúria, proteinúria ou hipertrofia ventricular esquerda. Esses medicamentos têm propriedades renoprotetoras que vão além de seus efeitos anti-hipertensivos isolados.
A terapia dupla é recomendada como tratamento de primeira linha porque a maioria dos pacientes não alcançará o controle da PA com um único medicamento anti-hipertensivo. Eles podem ser administrados como uma formulação combinada patenteada (se disponível) para melhorar a adesão e obter um controle mais rápido da PA. A combinação de um IECA ou antagonista do receptor de angiotensina II, com um bloqueador dos canais de cálcio ou um diurético semelhante à tiazida, é recomendada.
Os betabloqueadores devem ser considerados em qualquer etapa do tratamento da hipertensão se houver uma indicação específica (por exemplo, doença arterial coronariana, fibrilação atrial, insuficiência cardíaca).
Há uma ênfase crescente em incorporar o uso do monitoramento domiciliar da PA no diagnóstico e no tratamento da hipertensão em adultos, incluindo aqueles com diabetes.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[124]Margolis KL, Asche SE, Bergdall AR, et al. Effect of home blood pressure telemonitoring and pharmacist management on blood pressure control: a cluster randomized clinical trial. JAMA. 2013 Jul 3;310(1):46-56.
https://jamanetwork.com/journals/jama/fullarticle/1707720
http://www.ncbi.nlm.nih.gov/pubmed/23821088?tool=bestpractice.com
Lipídios
Consulte seus protocolos locais. As diretrizes recomendam diferentes abordagens para a terapia de modificação lipídica.
O NICE recomenda:
O uso de uma ferramenta de avaliação de risco validada, como o QRISK3, para avaliar o risco de DCV nos próximos 10 anos em pessoas com diabetes do tipo 2 com idade entre 25 e 84 anos (aqueles com 85 anos ou mais devem ser considerados com risco aumentado de DCV devido à idade somente, especialmente se fumarem e/ou tiverem PA elevada).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
QRISK®3 calculator
Opens in new window
Na sua diretriz sobre diabetes do tipo 2 (última atualização em 2022), o NICE recomenda o uso do QRISK2 para avaliar o risco de doença cardiovascular em adultos com diabetes do tipo 2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
No entanto, a diretriz de 2023 do NICE sobre DCV recomenda o uso do QRISK3.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
O NICE reconhece que pode ser necessário usar o QRISK2 até que os sistemas clínicos eletrônicos sejam atualizados com o QRISK3.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Dependendo da disponibilidade local, o QRISK2 ou o QRISK3 são uma ferramenta razoável para avaliar o risco de DCV em adultos com diabetes do tipo 2.
O NICE especifica as populações para as quais o QRISK3 deve ser usado (pois o QRISK2 pode subestimar o risco de DCV nesses pacientes), inclusive indivíduos com transtorno mental grave, lúpus eritematoso sistêmico, enxaqueca ou disfunção erétil, e pessoas que fazem uso de corticosteroides ou antipsicóticos atípicos.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
O NICE também observa que as ferramentas de risco de DCV (incluindo o QRISK3) podem subestimar o risco em alguns grupos (por exemplo, aqueles tratados para HIV, aqueles que abandonaram o tabagismo recentemente, etc.) e enfatiza que o julgamento clínico é necessário para interpretar os escores de risco.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
O NICE não recomenda o uso de uma ferramenta de avaliação de risco para as pessoas com alto risco de DCV, incluindo aquelas com uma taxa de filtração glomerular estimada (TFGe) <60 mL/min/1.73 m² e/ou albuminúria, ou um distúrbio hereditário do metabolismo lipídico (por exemplo, hipercolesterolemia familiar).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Oferecer terapia com estatina de alta intensidade (ou seja, atorvastatina na extremidade inferior da faixa de dose de alta intensidade) para a prevenção primária de DCV para pessoas com (e sem) diabetes do tipo 2 que têm ≥10% de risco em 10 anos (estimado usando QRISK3) de desenvolver DCV.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
O NICE observa que não se deve descartar o tratamento com atorvastatina para a prevenção primária apenas porque o escore de risco em 10 anos do paciente é inferior a 10% se ele tiver uma preferência informada por tomar uma estatina ou se houver preocupação de que o risco possa estar subestimado.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
O NICE também recomenda considerar esse tratamento para asb pessoas com 85 anos ou mais, com consciência dos fatores que podem tornar o tratamento inadequado (por exemplo, expectativa de vida, fragilidade, comorbidades ou outros medicamentos em uso).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Oferecer terapia com estatina de alta intensidade (ou seja, atorvastatina na extremidade superior da faixa de doses de alta intensidade) para prevenção secundária para as pessoas com (e sem) diabetes com DCV estabelecida, independentemente do seu nível de colesterol e desde que tenham função renal normal.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Uma dose mais baixa deve ser oferecida para a prevenção secundária se a pessoa apresentar alto risco de efeitos adversos das estatinas ou estiver tomando outros medicamentos que puderem interagir com a estatina, ou se ela tiver preferência por uma dose mais baixa.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
As pessoas com DRC que necessitarem de prevenção secundária para DCV devem receber atorvastatina na extremidade inferior da faixa de doses de alta intensidade (ou seja, a mesma da prevenção primária).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
A decisão de iniciar (ou intensificar) a terapia hipolipemiante deve ser tomada com o paciente após uma discussão informada sobre os riscos e benefícios do tratamento, considerando os fatores individuais do paciente (por exemplo, preferências, comorbidades, outros medicamentos).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
As estatinas são contraindicadas na gestação. As estatinas devem ser interrompidas 3 meses antes da paciente tentar engravidar e não devem ser reiniciadas até que a amamentação termine.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Antes de iniciar a terapia de modificação lipídica, uma avaliação clínica deve ser realizada, incluindo revisão do status de tabagismo e diabetes, consumo de álcool, PA e IMC (ou outra medida de obesidade).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Devem ser realizados exames de sangue basais, incluindo função renal, nível de transaminases hepáticas e perfil lipídico completo (ou seja, colesterol total e colesterol de lipoproteína de alta densidade [HDL] e níveis de triglicerídeos, a partir dos quais o colesterol não HDL e o colesterol de lipoproteína de baixa densidade [LDL] são calculados; uma amostra em jejum não é necessária).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Exames de sangue para verificar o nível do hormônio estimulante da tireoide (TSH) devem ser solicitados se houver sintomas de disfunção tireoidiana, e os níveis de creatinina quinase devem ser realizados se a pessoa tiver sintomas musculares generalizados persistentes e inexplicáveis (dor, sensibilidade ou fraqueza).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Os achados clínicos, o perfil lipídico completo e a história familiar devem ser usados para avaliar a probabilidade de um distúrbio lipídico familiar (em vez de basear a decisão nos valores lipídicos somente).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Os distúrbios lipídicos familiares estão fora do escopo deste tópico: para mais informações sobre quando suspeitar e como diagnosticar hipercolesterolemia familiar, consulte Hipercolesterolemia.
Providencie avaliação especializada das pessoas com concentração de colesterol total de mais de 9.0 mmol/L ou concentração de colesterol não HDL de mais de 7.5 mmol/L, mesmo na ausência de uma história familiar de primeiro grau de doença coronariana prematura.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
As comorbidades e causas secundárias de dislipidemia devem ser tratadas (e, se apropriado, mudanças de estilo de vida devem ser discutidas) ao mesmo tempo em que o início da terapia com estatina para a prevenção secundária (ou antes de se iniciar uma estatina para prevenção primária).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Dados consistentes demonstraram a eficácia das estatinas para prevenir eventos cardiovasculares e reduzir a mortalidade cardiovascular em pacientes com diabetes, sem evidências de diferenças entre os sexos; seu uso está associado com um número limitado de eventos adversos.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Em termos de monitoramento, o NICE recomenda o seguinte:[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
De 2 a 3 meses após iniciar ou alterar um tratamento hipolipemiante, realize um perfil lipídico completo e um nível de transaminases hepáticas (as transaminases hepáticas devem ser verificada novamente em 12 meses; não serão necessários mais testes das transaminases hepáticas, a menos que haja indicação clínica).
Naqueles que usam estatina para prevenção primária, busque uma redução maior que 40% no colesterol não HDL, e naqueles que usam estatina para prevenção secundária, busque um colesterol LDL de 2.0 mmol/L ou menos (ou colesterol não HDL de 2.6 mmol/L ou menos). Se a meta lipídica apropriada não for atingida:
Discuta a adesão e o momento da dose
Otimize a adesão à dieta e às medidas de modificação do estilo de vida
Considere aumentar a intensidade/dose da estatina, se apropriado. Se a pessoa tiver DRC e a TFGe for 30 mL/min/1.73 m² ou mais, a dose de atorvastatina deve ser aumentada (se a TFGe for <30 mL/min/1.73 m², qualquer aumento de dose deve ser acordado com um especialista renal).
Se forem relatados efeitos adversos com a terapia com estatina de alta intensidade, considere as seguintes opções com o paciente:
Interromper a administração de estatina e reintroduzir assim que os sintomas desaparecerem, para verificar se estão relacionados à estatina; ou
Mudar para uma estatina alternativa de alta intensidade; ou
Reduzir a dose; ou
Mudar para uma estatina de menor intensidade.
Revise a medicação anualmente. Use essas revisões para discutir a adesão aos medicamentos e à modificação do estilo de vida e para abordar os fatores de risco de DCV. Aqueles em prevenção secundária devem receber um perfil lipídico completo anual para informar a discussão (e isso também deve ser considerado para aqueles em prevenção primária).
Não interrompa as estatinas por um aumento no nível glicêmico ou da HbA1c.
As diretrizes da ESC recomendam o rastreamento dos pacientes com diabetes para danos graves a órgãos-alvo e a avaliação de sintomas e história médica sugestivos de doença cardiovascular aterosclerótica (DCVA) para entender seu risco cardiovascular.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Quando não há DCVA sintomática nem danos graves a órgãos-alvo, elas recomendam o uso da ferramenta SCORE2-Diabetes para estimar o risco de DCV em 10 anos.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A ESC categoriza os pacientes com diabetes do tipo 2 de acordo com essas avaliações nos seguintes grupos de risco cardiovascular (usados para orientar o tratamento):[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Risco muito alto
Alto risco
Risco moderado
Com base nessas categorias, a ESC recomenda para os pacientes com diabetes do tipo 2:[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Em baixo risco cardiovascular: não é possível fazer recomendações claras sobre metas devido à ausência de evidências
Com risco cardiovascular moderado: uma meta de colesterol LDL de <2.6 mmol/L (<100 mg/dL)
Com alto risco cardiovascular: uma meta de colesterol LDL de <1.8 mmol/L (<70 mg/dL) e redução do colesterol LDL de pelo menos 50%; um objetivo secundário de uma meta de colesterol não HDL de <2.6 mmol/L (<100 mg/dL)
Com risco cardiovascular muito alto: uma meta de colesterol LDL de <1.4 mmol/L (<55 mg/dL) e redução do colesterol LDL de pelo menos 50%; um objetivo secundário de uma meta de colesterol não HDL de <2.2 mmol/L (<85 mg/dL).
A ESC recomenda estatinas como tratamento hipolipemiante de primeira linha nos pacientes com diabetes e níveis elevados de colesterol LDL.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
O perfil de risco cardiovascular (muito alto, alto, moderado) do paciente individual e os níveis alvo de colesterol LDL (ou colesterol não HDL) correspondentes devem ser usados para determinar a administração de estatinas.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A ESC recomenda a redução intensiva do colesterol LDL com estatinas para as pessoas com DRC.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Esquemas específicos para outras terapias hipolipemiantes estão fora do escopo deste tópico: consulte Hipercolesterolemia para obter mais informações. A seguir estão algumas orientações gerais.
As diretrizes do NICE e da ESC recomendam que, se a meta lipídica apropriada em uma pessoa com DCVA estabelecida não for atingida com a terapia com estatina máxima tolerada, a intensificação da terapia hipolipemiante (ou seja, terapias hipolipemiantes adicionais) deve ser considerada individualmente, em colaboração com o paciente.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Para alguns pacientes com diabetes e DCV estabelecida que apresentam níveis persistentemente elevados de colesterol LDL apesar da terapia com estatina máxima tolerada, a adição de ezetimiba ou de um anticorpo monoclonal inibidor da pró-proteína convertase subtilisina/kexin tipo 9 (PCSK9) pode conferir benefício clínico.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[126]Giugliano RP, Cannon CP, Blazing MA, et al; IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial) Investigators. Benefit of adding ezetimibe to statin therapy on cardiovascular outcomes and safety in patients with versus without diabetes mellitus: results From IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial). Circulation. 2018 Apr 10;137(15):1571-82.
http://www.ncbi.nlm.nih.gov/pubmed/29263150?tool=bestpractice.com
[127]Sabatine MS, Giugliano RP, Keech AC, et al; FOURIER Steering Committee and Investigators. Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med. 2017 May 4;376(18):1713-22.
https://www.nejm.org/doi/10.1056/NEJMoa1615664
http://www.ncbi.nlm.nih.gov/pubmed/28304224?tool=bestpractice.com
[128]Squizzato A, Suter MB, Nerone M, et al. PCSK9 inhibitors for treating dyslipidemia in patients at different cardiovascular risk: a systematic review and a meta-analysis. Intern Emerg Med. 2017 Oct;12(7):1043-53.
http://www.ncbi.nlm.nih.gov/pubmed/28695455?tool=bestpractice.com
[129]Lee YJ, Cho JY, You SC, et al. Moderate-intensity statin with ezetimibe vs. high-intensity statin in patients with diabetes and atherosclerotic cardiovascular disease in the RACING trial. Eur Heart J. 2023 Mar 14;44(11):972-83.
https://academic.oup.com/eurheartj/article/44/11/972/6931821?login=false
http://www.ncbi.nlm.nih.gov/pubmed/36529993?tool=bestpractice.com
The BMJ: PCSK9 inhibitors and ezetimibe for the reduction of cardiovascular events: a clinical practice guideline with risk-stratified recommendations
Opens in new window
Além disso, o NICE recomenda considerar a adição de ezetimiba (à terapia com estatina máxima tolerada) nos pacientes com DCV estabelecida para reduzir adicionalmente o risco de DCV, mesmo que a meta lipídica para prevenção secundária seja atingida com uma estatina somente.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
A ESC recomenda uma terapia combinada de estatina associada a ezetimiba para os pacientes que não atingem sua meta de colesterol LDL apenas com a terapia com estatina (não há especificação da categoria de risco cardiovascular para esta recomendação) ou como uma opção para redução intensiva do colesterol LDL nos pacientes com diabetes e DRC.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Outras terapias hipolipemiantes também devem ser consideradas individualmente se a terapia com estatinas for contraindicada ou não for tolerada em nenhuma intensidade/dose, e podem ser necessárias além da terapia com estatina se o paciente tiver indicações adicionais para tratamento hipolipemiante (por exemplo, hipertrigliceridemia, um distúrbio lipídico familiar).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Abandono do hábito de fumar
Se o paciente fuma, dê conselhos sobre como abandonar o hábito de fumar e informações sobre como acessar os serviços para o abandono do hábito de fumar.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[130]National Institute for Health and Care Excellence. Tobacco: preventing uptake, promoting quitting and treating dependence. January 2023 [internet publication].
https://www.nice.org.uk/guidance/ng209
A ESC recomenda que terapias farmacológicas (por exemplo, terapia de reposição de nicotina, vareniclina, bupropiona) sejam consideradas, bem como aconselhamento, para melhorar a taxa de sucesso da cessação.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Terapia antiagregante plaquetária
As pessoas com diabetes do tipo 2 e DCV precisarão de terapia antiagregante plaquetária para prevenção secundária. Geralmente, ela será na forma de aspirina em baixas doses ou clopidogrel.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A terapia antiagregante plaquetária reduz o risco de AVC, infarto do miocárdio ou morte vascular.[131]Antithrombotic Trialists' Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ. 2002 Jan 12;324(7329):71-86.
http://www.bmj.com/content/324/7329/71.full
http://www.ncbi.nlm.nih.gov/pubmed/11786451?tool=bestpractice.com
O papel dos antiagregantes plaquetários na prevenção primária da DCV não está claro, e as diretrizes diferem em suas recomendações. Consulte seus protocolos locais.
O NICE recomenda contra a terapia antiagregante plaquetária de rotina (aspirina ou clopidogrel) como prevenção primária para os adultos com diabetes do tipo 2 sem DCV.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Isso ocorre porque o aumento do risco de sangramento importante é considerado maior que quaisquer benefícios potenciais da prevenção primária.[132]Visseren FLJ, Mach F, Smulders YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021 Sep 7;42(34):3227-337.
https://academic.oup.com/eurheartj/article/42/34/3227/6358713
http://www.ncbi.nlm.nih.gov/pubmed/34458905?tool=bestpractice.com
O estudo ASCEND comparou aspirina em baixas doses com placebo entre 15,480 adultos com diabetes, mas sem DCV evidente. Ele revelou que os benefícios do uso de aspirina na prevenção de eventos vasculares graves foram amplamente contrabalançados pelo aumento do risco de eventos de sangramento importantes em um acompanhamento médio de 7.4 anos.[133]ASCEND Study Collaborative Group; Bowman L, Mafham M, Wallendszus K, et al. Effects of aspirin for primary prevention in persons with diabetes mellitus. N Engl J Med. 2018 Oct 18;379(16):1529-39.
https://www.nejm.org/doi/10.1056/NEJMoa1804988
http://www.ncbi.nlm.nih.gov/pubmed/30146931?tool=bestpractice.com
No entanto, a ESC recomenda que a aspirina em baixas doses possa ser considerada para a prevenção de um primeiro evento vascular grave em adultos com diabetes do tipo 2 sem história de DCVA sintomática ou revascularização, desde que não haja contraindicações claras.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Eles reconhecem que a terapia deve ser individualizada, pois aqueles com maior risco cardiovascular podem se beneficiar mais da terapia antiagregante plaquetária.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Ela recomenda o uso de aspirina em baixas doses nos pacientes com DRC e DCVA.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A ESC também recomenda que o uso concomitante de um inibidor da bomba de prótons apropriado seja considerado (com base no risco individual de sangramento do paciente) para os pacientes que tomam um único medicamento antiagregante plaquetário (por exemplo, aspirina em baixas doses) para reduzir o risco de hemorragia digestiva destacado pelo estudo ASCEND (no qual três quartos dos pacientes não estavam tomando um inibidor da bomba de prótons).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Eles fazem a mesma recomendação para aqueles que tomam um único anticoagulante.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Além disso, eles recomendam que um inibidor da bomba de prótons apropriado seja usado quando uma combinação de medicamentos antitrombóticos estiver sendo tomada.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Considerações específicas de farmacoterapia para pacientes com DRC
Caso o paciente com diabetes do tipo 2 tenha doença renal crônica (DRC) ou a desenvolva a qualquer momento após o diagnóstico, o NICE recomenda o seguinte:
Administre um antagonista do receptor de angiotensina II ou um inibidor da ECA (ajuste na dose mais alta aprovada que o indivíduo puder tolerar) se a relação entre albumina e creatinina (RAC) estiver 3 mg/mmol ou mais (ou seja, proteinúria clinicamente importante).[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[86]National Institute for Health and Care Excellence. Chronic kidney disease: assessment and management. November 2021 [internet publication].
https://www.nice.org.uk/guidance/ng203
Administre um inibidor de SGLT2 (além do antagonista do receptor de angiotensina II ou inibidor da ECA) se o paciente já estiver recebendo um antagonista do receptor de angiotensina II ou inibidor da ECA (ajuste na dose mais alta aprovada que o indivíduo puder tolerar) e:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[Evidência A]61a0123d-3704-47cf-8cd7-ef9b0668234eguidelineAQual é a efetividade clínica dos inibidores da proteína cotransportadora de sódio e glicose 2 (SGTL2) como farmacoterapia complementar para adultos com doença renal crônica (DRC) e diabetes do tipo 2?[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Considere um inibidor de SGLT2 (além do antagonista do receptor de angiotensina II ou do inibidor da ECA) se o paciente já estiver recebendo um antagonista do receptor de angiotensina II ou um inibidor da ECA (ajuste na dose mais alta aprovada que o indivíduo puder tolerar) e:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[Evidência A]61a0123d-3704-47cf-8cd7-ef9b0668234eguidelineAQual é a efetividade clínica dos inibidores da proteína cotransportadora de sódio e glicose 2 (SGTL2) como farmacoterapia complementar para adultos com doença renal crônica (DRC) e diabetes do tipo 2?[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente tiver DRC em estágio 3 ou 4 (ou seja, com TFGe <60 mL/min/1.73 m²) associada ao diabetes do tipo 2 com albuminúria, considere a utilização de finerenona (um antagonista não esteroide do receptor mineralocorticoide) se:[134]National Institute for Health and Care Excellence. Finerenone for treating chronic kidney disease in type 2 diabetes. March 2023 [internet publication].
https://www.nice.org.uk/guidance/ta877
É usado como um complemento ao padrão de cuidados otimizado (que deve incluir, a menos que sejam inadequadas, as doses licenciadas mais altas toleradas de inibidores da ECA ou antagonistas do receptor de angiotensina II e inibidores de SGLT2) e
O paciente tem TFGe ≥25 mL/min/1.73 m².
Se o paciente tiver DRC e necessitar de um agente anti-hipertensivo:
Siga as recomendações descritas em Manejo de risco cardiovascular, que também se aplicam a pessoas sem DRC, se o paciente apresentar RAC ≤30 mg/mmol (categorias A1 e A2 de RAC).[86]National Institute for Health and Care Excellence. Chronic kidney disease: assessment and management. November 2021 [internet publication].
https://www.nice.org.uk/guidance/ng203
Administre um antagonista do receptor de angiotensina II ou um inibidor da ECA (titulado para a dose licenciada mais alta que a pessoa pode tolerar) se o paciente tiver uma RAC >30 mg/mmol (categoria A3 ou superior de RAC).[86]National Institute for Health and Care Excellence. Chronic kidney disease: assessment and management. November 2021 [internet publication].
https://www.nice.org.uk/guidance/ng203
Sempre que possível, trate a hipertensão em pessoas com DRC com medicamentos administrados apenas uma vez ao dia.[82]National Institute for Health and Care Excellence. Hypertension in adults: diagnosis and management. Nov 2023 [internet publication].
https://www.nice.org.uk/guidance/ng136
Esses medicamentos devem ser acrescentados ao padrão de cuidados otimizado (consulte a seção de Farmacoterapia anti-hiperglicêmica).
Os inibidores de SGLT2 não são adequados para todos e só devem ser usados dentro dos limites de sua autorização de comercialização; alguns inibidores de SGLT2 não estão licenciados para essa indicação em algumas regiões, incluindo no Reino Unido.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Essas recomendações do NICE baseiam-se em evidências de ensaios clínicos randomizados e controlados que mostraram que:
Os inibidores de SGLT2 reduzem o risco de evolução da DRC, a mortalidade e os eventos cardiovasculares em adultos com diabetes do tipo 2 e DRC.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[Evidência A]61a0123d-3704-47cf-8cd7-ef9b0668234eguidelineAQual é a efetividade clínica dos inibidores da proteína cotransportadora de sódio e glicose 2 (SGTL2) como farmacoterapia complementar para adultos com doença renal crônica (DRC) e diabetes do tipo 2?[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Os antagonistas do receptor de angiotensina II reduzem o risco de doença renal terminal e insuficiência cardíaca.[86]National Institute for Health and Care Excellence. Chronic kidney disease: assessment and management. November 2021 [internet publication].
https://www.nice.org.uk/guidance/ng203
Não há uma diferença clara entre os inibidores da ECA e os antagonistas do receptor de angiotensina II em vários desfechos, incluindo doença renal terminal, mortalidade por todas as causas, mortalidade cardiovascular e hospitalização.[86]National Institute for Health and Care Excellence. Chronic kidney disease: assessment and management. November 2021 [internet publication].
https://www.nice.org.uk/guidance/ng203
As recomendações de farmacoterapia para pacientes com diabetes do tipo 2 e DRC fornecidas pela diretriz de prática clínica Kidney Disease: Improving Global Outcomes (KDIGO) de 2022 estão amplamente alinhadas com as diretrizes NICE descritas acima.[135]Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 Clinical Practice Guideline for diabetes management in chronic kidney disease. Kidney Int. 2022 Nov;102(5s):S1-127.
https://www.kidney-international.org/article/S0085-2538(22)00507-5/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/36272764?tool=bestpractice.com
Eles também sugerem que um antagonista do receptor mineralocorticoide não esteroide com benefício renal ou cardiovascular comprovado seja considerado para pacientes com diabetes do tipo 2, TFGe ≥25 mL/min/1.73 m², concentração sérica normal de potássio e proteinúria clinicamente importante, apesar da dose máxima tolerada de um antagonista do receptor de angiotensina II ou de um inibidor da ECA.[135]Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 Clinical Practice Guideline for diabetes management in chronic kidney disease. Kidney Int. 2022 Nov;102(5s):S1-127.
https://www.kidney-international.org/article/S0085-2538(22)00507-5/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/36272764?tool=bestpractice.com
A United Kingdom Kidney Association (UKKA) em 2023 recomenda o uso de um inibidor de SGLT2 nas pessoas com diabetes do tipo 2 e DRC (independentemente da doença renal primária, mas excluindo aquelas com doença renal policística ou receptores de transplante renal) que tiverem:[136]Herrington WG, Frankel AH. UK Kidney Association clinical practice guideline: sodium-glucose co-transporter-2 (SGLT-2) inhibition in adults with kidney disease. Apr 2023 [internet publication].
https://guidelines.ukkidney.org
Uma TFGe de 20-45 mL/min/1.73 m², ou
Uma TFGe de >45 mL/min/1.73 m² e uma relação albumina/creatinina urinária (RCAu) de ≥25 mg/mmol (uma relação proteína/creatinina urinária de 35 mg/mmol pode ser considerada equivalente), ou
Insuficiência cardíaca sintomática, independentemente da fração de ejeção, ou
Doença coronariana estabelecida.
A UKKA também sugere que, nas pessoas com diabetes do tipo 2 e DRC (excluindo receptores de transplante renal), um inibidor de SGLT2 deve ser:[136]Herrington WG, Frankel AH. UK Kidney Association clinical practice guideline: sodium-glucose co-transporter-2 (SGLT-2) inhibition in adults with kidney disease. Apr 2023 [internet publication].
https://guidelines.ukkidney.org
Iniciado se a TFGe for >45-60 mL/min/1.73 m² e a RCAu for <25 mg/mmol para modificar o risco cardiovascular e retardar a taxa de declínio da função renal (reconhecendo que os efeitos sobre o controle glicêmico serão limitados).
Considerado se a TFGe for <20 mL/min/1.73 m² para retardar a progressão da doença renal, com base em evidências de que esse benefício ainda é observado na TFGe baixa.
A UKKA recomenda que os inibidores de SGLT2 sejam mantidos até que a terapia renal substitutiva seja necessária.[136]Herrington WG, Frankel AH. UK Kidney Association clinical practice guideline: sodium-glucose co-transporter-2 (SGLT-2) inhibition in adults with kidney disease. Apr 2023 [internet publication].
https://guidelines.ukkidney.org
As diretrizes da ESC de 2023 sobre o manejo da DCV no diabetes recomendam tratar os pacientes com diabetes do tipo 2 e DRC com um inibidor de SGLT2 e/ou finerenona, pois estes reduzem o risco cardiovascular e o risco de insuficiência renal, além do padrão de assistência (por exemplo, inibidor da ECA ou antagonista do receptor de angiotensina II).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Especificamente, além do uso de um inibidor da ECA ou antagonista do receptor de angiotensina II, elas recomendam o uso de:[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A ESC também faz recomendações em uma atualização de 2023 de suas diretrizes para insuficiência cardíaca para inibidores de SGLT2 e finerenona nos pacientes com diabetes do tipo 2 e DRC para reduzir o risco de hospitalização por insuficiência cardíaca (inibidores de SGLT2 e finerenona) ou morte cardiovascular (inibidores de SGLT2).[137]McDonagh TA, Metra M, Adamo M, et al. 2023 focused update of the 2021 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023 Oct 1;44(37):3627-39.
https://academic.oup.com/eurheartj/article/44/37/3627/7246292?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622666?tool=bestpractice.com
Valores-alvo glicêmicos e automonitoramento
As metas de HbA1c devem ser individualizadas em todos os estágios do tratamento; o paciente deve ser envolvido em quaisquer decisões sobre sua meta glicêmica individual.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[138]Laiteerapong N, Cooper JM, Skandari MR, et al. Individualized glycemic control for US adults with type 2 diabetes: a cost-effectiveness analysis. Ann Intern Med. 2018 Feb 6;168(3):170-8.
http://www.ncbi.nlm.nih.gov/pubmed/29230472?tool=bestpractice.com
[139]Ismail-Beigi F, Moghissi E, Tiktin M, et al. Individualizing glycemic targets in type 2 diabetes mellitus: implications of recent clinical trials. Ann Intern Med. 2011 Apr 19;154(8):554-9.
http://www.ncbi.nlm.nih.gov/pubmed/21502652?tool=bestpractice.com
As metas individualizadas de HbA1c melhoram a qualidade de vida em comparação com o controle uniforme e rigoroso.[139]Ismail-Beigi F, Moghissi E, Tiktin M, et al. Individualizing glycemic targets in type 2 diabetes mellitus: implications of recent clinical trials. Ann Intern Med. 2011 Apr 19;154(8):554-9.
http://www.ncbi.nlm.nih.gov/pubmed/21502652?tool=bestpractice.com
No Reino Unido, o NICE recomenda:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente maneja seu diabetes do tipo 2 com estilo de vida e dieta, ou com estilo de vida e dieta combinados com um único medicamento que não esteja associado a hipoglicemia, ajude-o a buscar um nível de HbA1c de 48 mmol/mol (6.5%)
Se o paciente estiver tomando um medicamento associado a hipoglicemia, ajude-o a buscar como meta um nível de HbA1c de 53 mmol/mol (7.0%).
A ESC recomenda um controle glicêmico rigoroso (HbA1c <7.0%; se apropriado/possível) para reduzir complicações microvasculares, e ela aconselha considerar o mesmo para reduzir a doença arterial coronariana no longo prazo (de preferência usando agentes com benefício cardiovascular comprovado).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Considere um nível ligeiramente superior de HbA1c caso a caso para:[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Pacientes idosos ou frágeis
Pacientes que provavelmente não alcançarão benefícios de redução de risco a longo prazo (por exemplo, aqueles com uma expectativa de vida reduzida)
Pacientes para os quais o controle rigoroso da glicose sanguínea apresentar um alto risco de consequências de hipoglicemia, incluindo pessoas com risco de queda; pessoas com comprometimento da consciência sobre hipoglicemia; aqueles que dirigem ou operam máquinas como parte do seu trabalho
Pacientes para os quais o manejo intensivo não é apropriado (por exemplo, pessoas com comorbidades significativas).
Lembre-se de que os esquemas de medicamentos mais apropriados para um paciente frágil, incluindo a escolha do medicamento e a dose ideal, precisarão de consideração cuidadosa e provavelmente serão diferentes daqueles recomendados para pacientes mais jovens e em boa forma.[83]Strain WD, Hope SV, Green A, et al. Type 2 diabetes mellitus in older people: a brief statement of key principles of modern day management including the assessment of frailty – a national collaborative stakeholder initiative. Diabet Med. 2018 Jul;35(7):838-45.
https://onlinelibrary.wiley.com/doi/10.1111/dme.13644
http://www.ncbi.nlm.nih.gov/pubmed/29633351?tool=bestpractice.com
A ADA recomenda o uso de medicamentos com baixo risco de hipoglicemia para os idosos, e a desintensificação e/ou simplificação dos planos de tratamento (dentro de metas glicêmicas individualizadas) nessa população quando os danos ou encargos do tratamento puderem superar os benefícios.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Se o paciente dirigir, verifique se ele está ciente das diretrizes locais relevantes sobre o nível de glicose plasmática. No Reino Unido, a Driver and Vehicle Licensing Agency aconselha ter como meta um nível de, pelo menos, 5 mmol/L (90 mg/dL) antes de dirigir.[140]Driver and Vehicle Licensing Agency. Information for drivers with diabetes. June 2021 [internet publication].
https://www.gov.uk/government/publications/information-for-drivers-with-diabetes
O automonitoramento dos níveis de glicose pode ajudar no automanejo e no ajuste da medicação, principalmente nas pessoas que tomam insulina. Ele pode fornecer informações sobre o impacto do estilo de vida e do manejo medicamentoso sobre a glicemia e os sintomas, principalmente quando combinado com educação e suporte; os planos de monitoramento da glicose devem ser individualizados.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Tradicionalmente, o automonitoramento envolve a medição dos níveis de glicose a partir de amostras de sangue capilar (automonitoramento da glicose sanguínea, SMBG) que usa testes de glicose sanguínea por punção digital.
O NICE e a European Association for the Study of Diabetes/American Diabetes Association (EASD/ADA) recomendam o SMBG como uma opção para pessoas com diabetes do tipo 2 que usam insulina.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
O NICE também recomenda a oferta de rotina de SMBG para adultos com diabetes do tipo 2 se:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Houver evidências de episódios hipoglicêmicos ou
O paciente tomar medicamentos por via oral que possam aumentar o risco de hipoglicemia ao dirigir ou operar máquinas ou
A pessoa estiver grávida ou esteja planejando engravidar.
O NICE recomenda considerar SMBG de curta duração em adultos com diabetes do tipo 2 (e revisar o tratamento, se necessário):[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Ao iniciar o tratamento com corticosteroides orais ou intravenosos, ou
Para confirmar a suspeita de hipoglicemia.
A mais recente tecnologia de monitoramento contínuo da glicose (MCG) também está sendo utilizada. O MCG envolve um pequeno dispositivo descartável com um sensor subcutâneo constantemente conectado à pele, que mede os níveis de glicose no fluido intersticial e envia as leituras para um dispositivo com tela ou dispositivo inteligente.[141]Lewis DM, Oser TK, Wheeler BJ. Continuous glucose monitoring. BMJ. 2023 Mar 3;380:e072420.
http://www.ncbi.nlm.nih.gov/pubmed/36868576?tool=bestpractice.com
Os dispositivos de MCG podem fornecer dados em tempo real ou dados de escaneamentos intermitentes. O MCG pode fornecer mais informações que o SMBG, mas pode não estar prontamente disponível em todas as regiões para pessoas com diabetes do tipo 2.
O NICE recomenda oferecer MCG a adultos com diabetes do tipo 2 se eles:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
A EASD/ADA também afirma que o MCG fornece mais informações e tem vantagens claras sobre o SMBG e pode ser útil para pessoas com diabetes do tipo 2, particularmente aquelas tratadas com insulina.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
O uso do SMCG é recomendado pela ADA para as pessoas com diabetes que têm alto risco de hipoglicemia.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
O NICE observa que o MCG deve ser fornecido por uma equipe com experiência em seu uso, e deve ser fornecido suporte e educação adequados ao paciente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
As medições de glicose sanguínea capilar ainda precisarão ser realizadas para se verificar a acurácia do dispositivo de MCG, e deverão estar disponíveis como backup caso o dispositivo de MCG falhe.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Farmacoterapia anti-hiperglicêmica: princípios gerais
Se o paciente não conseguir atingir sua meta individualizada para a HbA1c com intervenções no estilo de vida, a farmacoterapia é recomendada para reduzir o risco de complicações microvasculares (nefropatia, retinopatia, neuropatia) e macrovasculares (doença arterial coronariana, cerebrovascular e vascular periférica).[142]UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). Lancet. 1998 Sep 12;352(9131):854-65.
http://www.ncbi.nlm.nih.gov/pubmed/9742977?tool=bestpractice.com
[143]Holman RR, Paul SK, Bethel MA, et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med. 2008 Oct 9;359(15):1577-89.
https://www.nejm.org/doi/full/10.1056/NEJMoa0806470
http://www.ncbi.nlm.nih.gov/pubmed/18784090?tool=bestpractice.com
Em geral, as estratégias globais de farmacoterapia mudaram para se concentrar na melhora dos desfechos das doenças cardiovascular e renal, em vez de serem orientadas apenas pelo controle glicêmico. Isto se baseia em evidências de ensaios clínicos randomizados de alta qualidade que demonstram os benefícios de alguns agentes sobre a doença cardiovascular (DCV) aterosclerótica, a insuficiência cardíaca e a doença renal crônica (DRC), em grande parte independentes do seu potencial para redução da glicose.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Em particular, os inibidores de SGLT2 parecem ter benefícios nos pacientes com diabetes do tipo 2 que apresentam múltiplos fatores de risco para DCV, e tanto os inibidores de SGLT2 quanto os agonistas do receptor do peptídeo semelhante ao glucagon 1 (GLP-1) parecem benéficos naqueles com DCV e/ou doença renal estabelecidas.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[144]Patel A, MacMahon S, et al; ADVANCE Collaborative Group. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med. 2008 Jun 6;358(24):2560-72.
https://www.nejm.org/doi/full/10.1056/NEJMoa0802987
http://www.ncbi.nlm.nih.gov/pubmed/18539916?tool=bestpractice.com
[145]Gerstein HC, Miller ME, Byington RP, et al; Action to Control Cardiovascular Risk in Diabetes Study Group. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med. 2008 Jun 12;358(24):2545-59.
https://www.nejm.org/doi/full/10.1056/NEJMoa0802743
http://www.ncbi.nlm.nih.gov/pubmed/18539917?tool=bestpractice.com
[146]Li S, Vandvik PO, Lytvyn L, et al. SGLT-2 inhibitors or GLP-1 receptor agonists for adults with type 2 diabetes: a clinical practice guideline. BMJ. 2021 May 11;373:n1091.
https://www.bmj.com/content/373/bmj.n1091.long
http://www.ncbi.nlm.nih.gov/pubmed/33975892?tool=bestpractice.com
Além disso, a metformina tem prováveis benefícios cardiovasculares.[147]Griffin SJ, Leaver JK, Irving GJ. Impact of metformin on cardiovascular disease: a meta-analysis of randomised trials among people with type 2 diabetes. Diabetologia. 2017 Sep;60(9):1620-9.
https://link.springer.com/article/10.1007%2Fs00125-017-4337-9
http://www.ncbi.nlm.nih.gov/pubmed/28770324?tool=bestpractice.com
Em linha com as tendências globais, o NICE recomenda agora uma abordagem para o tratamento do diabetes do tipo 2 que se afaste de uma que se concentre apenas em atingir metas individualizadas de HbA1c, para uma que incorpore terapias que não só reduzam os níveis glicêmicos, mas que tenham benefícios cardiovasculares e renais comprovados.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
As recomendações neste tópico se baseiam principalmente na abordagem do NICE.
Deve-se observar que nos estudos mais antigos, como o ACCORD, o ADVANCE e o Veterans Affairs Diabetes Trial (VADT), o uso de vários medicamentos para alcançar níveis quase normais de HbA1c não foi benéfico ou aumentou a mortalidade entre pacientes com diabetes do tipo 2 e DCV ou alto risco de DCV.[144]Patel A, MacMahon S, et al; ADVANCE Collaborative Group. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med. 2008 Jun 6;358(24):2560-72.
https://www.nejm.org/doi/full/10.1056/NEJMoa0802987
http://www.ncbi.nlm.nih.gov/pubmed/18539916?tool=bestpractice.com
[145]Gerstein HC, Miller ME, Byington RP, et al; Action to Control Cardiovascular Risk in Diabetes Study Group. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med. 2008 Jun 12;358(24):2545-59.
https://www.nejm.org/doi/full/10.1056/NEJMoa0802743
http://www.ncbi.nlm.nih.gov/pubmed/18539917?tool=bestpractice.com
[148]Gerstein HC, Miller ME, Genuth S, et al; ACCORD Study Group. Long-term effects of intensive glucose lowering on cardiovascular outcomes. N Engl J Med. 2011 Mar 3;364(9):818-28.
http://www.ncbi.nlm.nih.gov/pubmed/21366473?tool=bestpractice.com
[149]Reaven PD, Emanuele NV, Wiitala WL, et al; VADT Investigators. Intensive glucose control in patients with type 2 diabetes - 15-year follow-up. N Engl J Med. 2019 Jun 6;380(23):2215-24.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6706253
http://www.ncbi.nlm.nih.gov/pubmed/31167051?tool=bestpractice.com
[150]Duckworth W, Abraira C, Moritz T, et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med. 2009 Jan 8;360(2):129-39.
https://www.nejm.org/doi/full/10.1056/NEJMoa0808431
http://www.ncbi.nlm.nih.gov/pubmed/19092145?tool=bestpractice.com
Entretanto, os inibidores de SGLT2 não estavam disponíveis e os agonistas do receptor de GLP-1 raramente foram usados nesses estudos.
A escolha dos agentes deve ser individualizada, tendo em conta as preferências, necessidades e circunstâncias clínicas do paciente (por exemplo, peso, comorbidades, riscos de complicações), a eficácia do agente em termos de resposta metabólica e proteção cardiovascular e renal, efeitos adversos e outros fatores.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Na hora de escolher, revisar e trocar medicamentos, sempre:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se a terapia combinada for indicada, introduza os medicamentos de maneira gradual, verificando a tolerabilidade e eficácia de cada medicamento.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se um adulto com diabetes do tipo 2 estiver sintomaticamente hiperglicêmico em qualquer fase do tratamento, considere a terapia de resgate com insulina ou sulfonilureia e reveja o tratamento quando o controle da glicose sanguínea for alcançado.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Farmacoterapia anti-hiperglicêmica: tratamento inicial
O NICE produziu um fluxograma que resume as suas recomendações para a escolha de medicamentos de primeira linha em adultos com diabetes do tipo 2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
NICE: Type 2 diabetes in adults: choosing medicines
Opens in new window
[Figure caption and citation for the preceding image starts]: Diabetes do tipo 2 em adultos: escolha dos medicamentos - como escolher medicamentos de primeira linhaNICE NG28 (2022) Diabetes do tipo 2 em adultos: escolha de medicamentos; usado com permissão [Citation ends].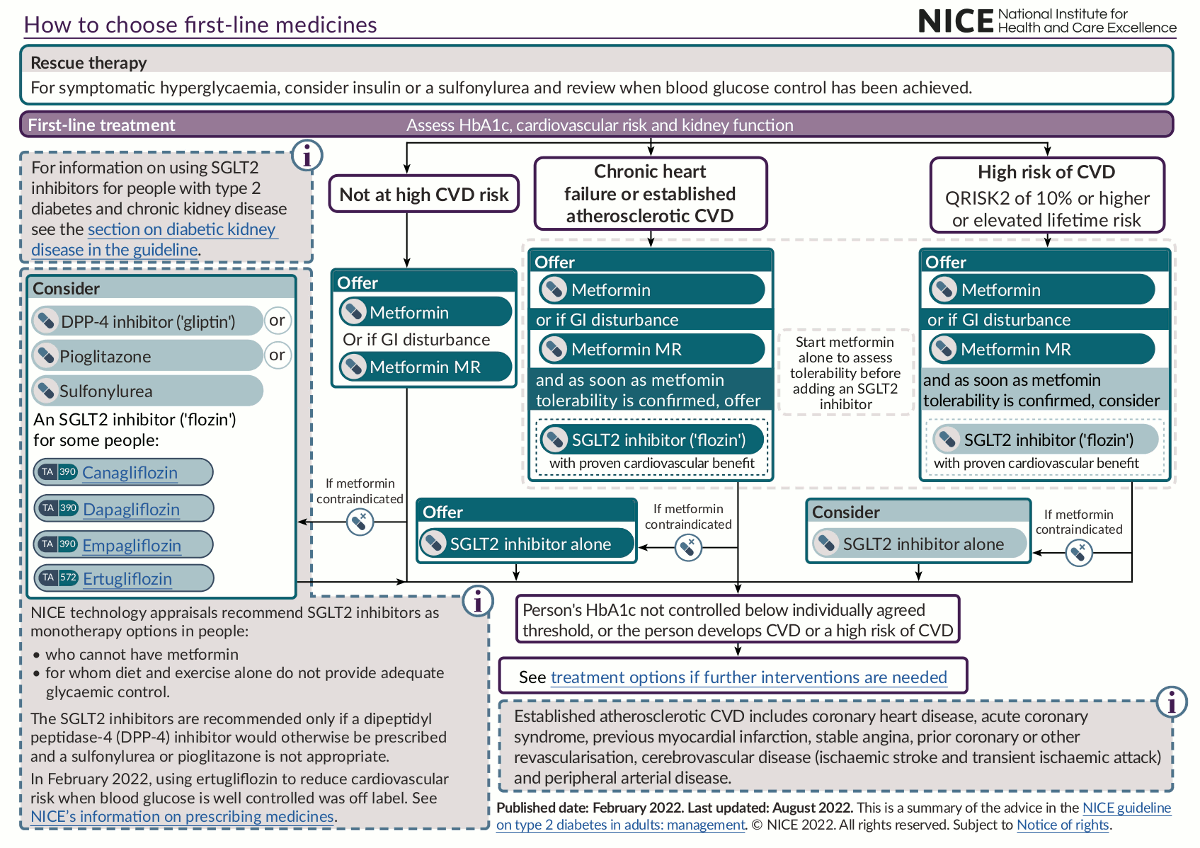
Avalie a HbA1c, o risco cardiovascular e a função renal do paciente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Determine se o paciente tem insuficiência cardíaca crônica ou doença cardiovascular aterosclerótica estabelecida (DCV; inclui doença coronariana, síndrome coronariana aguda, infarto do miocárdio prévio, angina estável, revascularização coronariana ou outra revascularização prévia, doença cerebrovascular [AVC isquêmico e ataque isquêmico transitório] e doença arterial periférica), ou tem alto risco de desenvolver doença cardiovascular. Use esta avaliação do risco cardiovascular para adaptar o tratamento medicamentoso.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Na sua diretriz sobre diabetes do tipo 2 (última atualização em 2022), o NICE recomenda o uso do QRISK2 para avaliar o risco de doença cardiovascular em adultos com diabetes do tipo 2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
No entanto, a diretriz de 2023 do NICE sobre DCV recomenda o uso do QRISK3. O NICE reconhece que pode ser necessário usar o QRISK2 até que os sistemas clínicos eletrônicos sejam atualizados com o QRISK3.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Referimo-nos ao QRISK3 abaixo, mas, dependendo da disponibilidade local, tanto o QRISK2 como o QRISK3 são uma ferramenta razoável para avaliar o risco de DCV em adultos com diabetes do tipo 2.
Observe que o NICE especifica certas populações (por exemplo, pessoas com transtornos mentais graves) para as quais o QRISK3 deve ser usado, pois o QRISK2 pode subestimar o risco de DCV nesses pacientes.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Além disso, o NICE observa que qualquer ferramenta de risco de DCV (incluindo o QRISK3) pode subestimar o risco em alguns grupos (por exemplo, aqueles tratados para HIV) e enfatiza o uso do julgamento clínico para interpretar os escores de risco.[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
O NICE não recomenda o uso de ferramentas de risco de DCV para as pessoas com alto risco de DCV (por exemplo, aquelas com TFGe <60 mL/min/1.73 m² e/ou albuminúria).[125]National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Dec 2023 [internet publication].
https://www.nice.org.uk/guidance/ng238/chapter/Recommendations
Metformina
Prescreva metformina como o tratamento medicamentoso de primeira linha para todos os adultos com diabetes do tipo 2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
A dose de metformina de liberação imediata deve ser aumentada gradualmente ao longo de várias semanas para minimizar o risco de efeitos adversos gastrointestinais.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se ocorrer algum distúrbio gastrointestinal com a metformina de liberação imediata, uma formulação de liberação modificada pode ser usada.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
No entanto, a metformina de liberação modificada está associada a uma redução da HbA1c estatisticamente mais desfavorável, mas provavelmente clinicamente semelhante, e a uma melhora mínima da intolerância gastrointestinal em comparação com a metformina de liberação imediata.[151]Abrilla AA, Pajes ANNI, Jimeno CA. Metformin extended-release versus metformin immediate-release for adults with type 2 diabetes mellitus: a systematic review and meta-analysis of randomized controlled trials. Diabetes Res Clin Pract. 2021 Aug;178:108824.
https://www.diabetesresearchclinicalpractice.com/article/S0168-8227(21)00183-2/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33887354?tool=bestpractice.com
Se a metformina for contraindicada ou não tolerada, a terapia medicamentosa alternativa deve se basear no perfil de risco cardiovascular do paciente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente não tiver DCV/não apresentar alto risco de DCV, considere usar um dos seguintes medicamentos em vez de metformina:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Um inibidor da dipeptidil peptidase-4 (DPP-4) ou
Pioglitazona ou
Uma sulfonilureia ou
Um inibidor de SGLT2 (um inibidor de SGLT2 é recomendado em algumas pessoas: aquelas nas quais a metformina é contraindicada ou não tolerada, quando a dieta e o exercício por si só não proporcionam um controle glicêmico adequado, somente se um inibidor de DPP-4 fosse ser prescrito e uma sulfonilureia ou a pioglitazona não forem apropriadas).[152]National Institute for Health and Care Excellence. Canagliflozin, dapagliflozin and empagliflozin as monotherapies for treating type 2 diabetes. May 2016 [internet publication].
https://www.nice.org.uk/guidance/ta390
[153]National Institute for Health and Care Excellence. Ertugliflozin as monotherapy or with metformin for treating type 2 diabetes. March 2019 [internet publication].
https://www.nice.org.uk/guidance/ta572
Se o paciente tiver alto risco de desenvolver doença cardiovascular (idade ≥40 anos com QRISK3 ≥10%, ou idade <40 anos com ≥1 fator de risco cardiovascular), considere um inibidor de SGLT2 com benefício cardiovascular comprovado (por exemplo, canagliflozina, dapagliflozina, empagliflozina) em vez da metformina.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente tiver insuficiência cardíaca crônica ou DCV aterosclerótica estabelecida, prescreva um inibidor de SGLT2 com benefício cardiovascular comprovado em vez de metformina.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Antes de iniciar o tratamento com um inibidor de SGLT2, sempre:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Verifique se o paciente apresenta um risco aumentado de cetoacidose diabética (CAD), por exemplo:
Se teve um episódio anterior de CAD
Se está agudamente doente com uma doença intercorrente
O paciente está seguindo uma dieta cetogênica ou com teor de carboidratos muito baixo.
Informe o paciente sobre o risco de CAD e aborde os fatores de risco modificáveis para CAD; por exemplo, aqueles que seguem uma dieta com teor muito baixo de carboidratos ou dieta cetogênica podem precisar adiar o tratamento até que tenham mudado sua dieta.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Medicamentos com benefícios cardiovasculares e renais
A menos que a metformina seja contraindicada/não tolerada, assim que a tolerabilidade à metformina for confirmada (após aumento gradual da dose de metformina de liberação imediata ao longo de várias semanas):[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente apresentar alto risco de desenvolver DCV, considere um inibidor de SGLT2 com benefício cardiovascular comprovado, além da metformina.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente tiver insuficiência cardíaca crônica ou DCV aterosclerótica estabelecida, adicione um inibidor de SGLT2 com benefício cardiovascular comprovado ao seu esquema de tratamento, ou seja, junto com a metformina.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Estas recomendações se aplicam a todas as fases do tratamento. Portanto, se um paciente que originalmente não tinha DCV desenvolver DCV, adicione um inibidor de SGLT2 com benefício cardiovascular comprovado ao seu esquema de tratamento existente ou administre um inibidor de SGLT2 no lugar de um medicamento existente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Da mesma forma, se for recém-descoberto que um paciente apresenta alto risco de DCV, considere adicionar um inibidor de SGLT2 aos seus tratamentos vigentes ou mudar um de seus medicamentos em uso para um inibidor de SGLT2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Embora o NICE não recomende os agonistas do receptor de GLP-1 como tratamento de primeira linha para diabetes do tipo 2, uma atualização de 2022 de um relatório de consenso conjunto da American Diabetes Association (ADA) e da European Association for the Study of Diabetes (EASD) recomenda que a monoterapia com um agonista do receptor de GLP-1 (por exemplo, dulaglutida, exenatida, liraglutida, lixisenatida, semaglutida) ou um inibidor de SGLT2 pode ser considerada como uma alternativa à metformina, com base em evidências sobre os benefícios cardiovasculares e renais dessas classes de medicamentos, independentemente de seus efeitos redutores da glicose.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[146]Li S, Vandvik PO, Lytvyn L, et al. SGLT-2 inhibitors or GLP-1 receptor agonists for adults with type 2 diabetes: a clinical practice guideline. BMJ. 2021 May 11;373:n1091.
https://www.bmj.com/content/373/bmj.n1091.long
http://www.ncbi.nlm.nih.gov/pubmed/33975892?tool=bestpractice.com
Especificamente, a ADA/EASD recomenda:[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Um agonista do receptor de GLP-1 ou um inibidor de SGLT2 com benefício comprovado deve ser usado nas pessoas com DCV estabelecida, e deve ser considerado nas pessoas sem DCV estabelecida mas com múltiplos fatores de risco cardiovascular., Nas pessoas com insuficiência cardíaca, deve ser utilizado um inibidor de SGLT2.
Nas pessoas com DRC e TFGe ≥20 mL/min/1.73 m² e uma RAC urinária >3.0 mg/mmol (>30 mg/g), deve ser iniciado um inibidor de SGLT2 com benefício comprovado. As indicações e os limites da TFGe podem variar de acordo com a região. Se tal tratamento não for tolerado ou for contraindicado, um agonista do receptor de GLP-1 com benefício comprovado sobre os desfechos cardiovasculares pode ser considerado e deve ser mantido até que a terapia de substituição renal seja indicada.
Nas pessoas com insuficiência cardíaca, DRC, DCV estabelecida ou múltiplos fatores de risco para DCV, a decisão de usar agonistas do receptor de GLP-1 ou inibidores de SGLT2 com benefício comprovado deve ser independente do uso da metformina e da HbA1c basal.
A ESC faz recomendações muito semelhantes às da ADA/EASD. A ESC recomenda o uso de um inibidor de SGLT2 (com benefício comprovado) noa pacientes com diabetes do tipo 2 e DRC quando a TFGe for ≥20 mL/min/1.73 m² para reduzir os riscos de DCV e insuficiência renal.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Além disso, elas recomendam (independentemente da HbA1c basal/alvo e de qualquer medicamento concomitante para redução da glicose):[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Agonistas do receptor de GLP-1 e inibidores de SGLT2, com benefícios cardiovasculares comprovados, para os pacientes com diabetes do tipo 2 e DCVA para reduzir os eventos cardiovasculares. Elas ainda aconselham que esses mesmos agentes podem ser considerados, assim como a metformina, para aqueles sem DCVA ou danos graves a órgãos-alvo, mas com risco de DCV em 10 anos ≥10%, para reduzir o risco cardiovascular. Elas aconselham que o tratamento com metformina não deve ser um pré-requisito para o uso desses outros agentes para benefício cardiovascular.
Inibidores de SGLT2 (com benefício comprovado) nos pacientes com diabetes do tipo 2 e insuficiência cardíaca (independentemente da fração de ejeção), para reduzir os riscos de hospitalização por insuficiência cardíaca ou morte cardiovascular.[137]McDonagh TA, Metra M, Adamo M, et al. 2023 focused update of the 2021 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023 Oct 1;44(37):3627-39.
https://academic.oup.com/eurheartj/article/44/37/3627/7246292?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622666?tool=bestpractice.com
Inibidores de SGLT2 (com benefício comprovado) nos pacientes com diabetes do tipo 2 com múltiplos fatores de risco para DCVA ou DCVA estabelecida, para reduzir o risco de hospitalização por insuficiência cardíaca.
Além disso, a ESC recomenda que, se for necessário um manejo glicêmico adicional para os pacientes com DCVA após o uso de medicamentos antidiabéticos com benefícios cardiovasculares comprovados (por exemplo, inibidores de SGLT2, agonistas do receptor de GLP-1), os agentes com segurança cardiovascular comprovada devem ser priorizados em relação aos agentes sem evidências de benefício ou segurança cardiovascular.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A ESC também recomenda que, se for necessário um manejo glicêmico adicional para os pacientes com (ou em risco de) insuficiência cardíaca após o tratamento com um inibidor de SGLT2 (com benefício comprovado), os medicamentos antidiabéticos com efeitos neutros sobre a insuficiência cardíaca em ensaios de desfechos cardiovasculares devem ser considerados.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A KDIGO observa que, se for necessário controle glicêmico adicional nos pacientes com diabetes do tipo 2 e DRC após o tratamento de primeira linha com metformina e inibidores de SGLT2, os agonistas do receptor de GLP-1 são geralmente preferenciais.[135]Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 Clinical Practice Guideline for diabetes management in chronic kidney disease. Kidney Int. 2022 Nov;102(5s):S1-127.
https://www.kidney-international.org/article/S0085-2538(22)00507-5/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/36272764?tool=bestpractice.com
Da mesma forma, a ESC recomenda o uso de um agonista do receptor de GLP-1 para controle adicional da glicose (se necessário) nos pacientes com DRC e TFGe >15 mL/min/1.73 m² (dado que esses agentes apresentam baixo risco de hipoglicemia e têm efeitos benéficos sobre o peso, o risco cardiovascular e a albuminúria).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
A atualização da UKKA de 2023 sugere iniciar um inibidor de SGLT2 para os pacientes com diabetes do tipo 2 e DRC (excluindo receptores de transplante renal) com uma TFGe de >45-60 mL/min/1.73 m² (e relação albumina/creatinina urinária <25 mg/mmol) para modificar o risco cardiovascular e diminuir a taxa de declínio da função renal (com base em metanálises de grandes ensaios clínicos randomizados, mostrando que os benefícios cardiovasculares e renais estão presentes em uma faixa de TFGe´s).[136]Herrington WG, Frankel AH. UK Kidney Association clinical practice guideline: sodium-glucose co-transporter-2 (SGLT-2) inhibition in adults with kidney disease. Apr 2023 [internet publication].
https://guidelines.ukkidney.org
Eles observam que os efeitos sobre o controle glicêmico podem ser limitados, pois os efeitos de redução da glicose dos inibidores de SGLT2 são reduzidos com o declínio da TFGe.[136]Herrington WG, Frankel AH. UK Kidney Association clinical practice guideline: sodium-glucose co-transporter-2 (SGLT-2) inhibition in adults with kidney disease. Apr 2023 [internet publication].
https://guidelines.ukkidney.org
Farmacoterapia anti-hiperglicêmica: escalonamento da terapia
O NICE produziu um fluxograma que resume as suas recomendações para a escolha dos medicamentos para o tratamento adicional em adultos com diabetes do tipo 2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
NICE: Type 2 diabetes in adults: choosing medicines
Opens in new window
[Figure caption and citation for the preceding image starts]: Diabetes do tipo 2 em adultos: escolha de medicamentos - como escolher medicamentos para tratamento adicionalNICE NG28 (2022) Diabetes do tipo 2 em adultos: escolha de medicamentos; usado com permissão [Citation ends].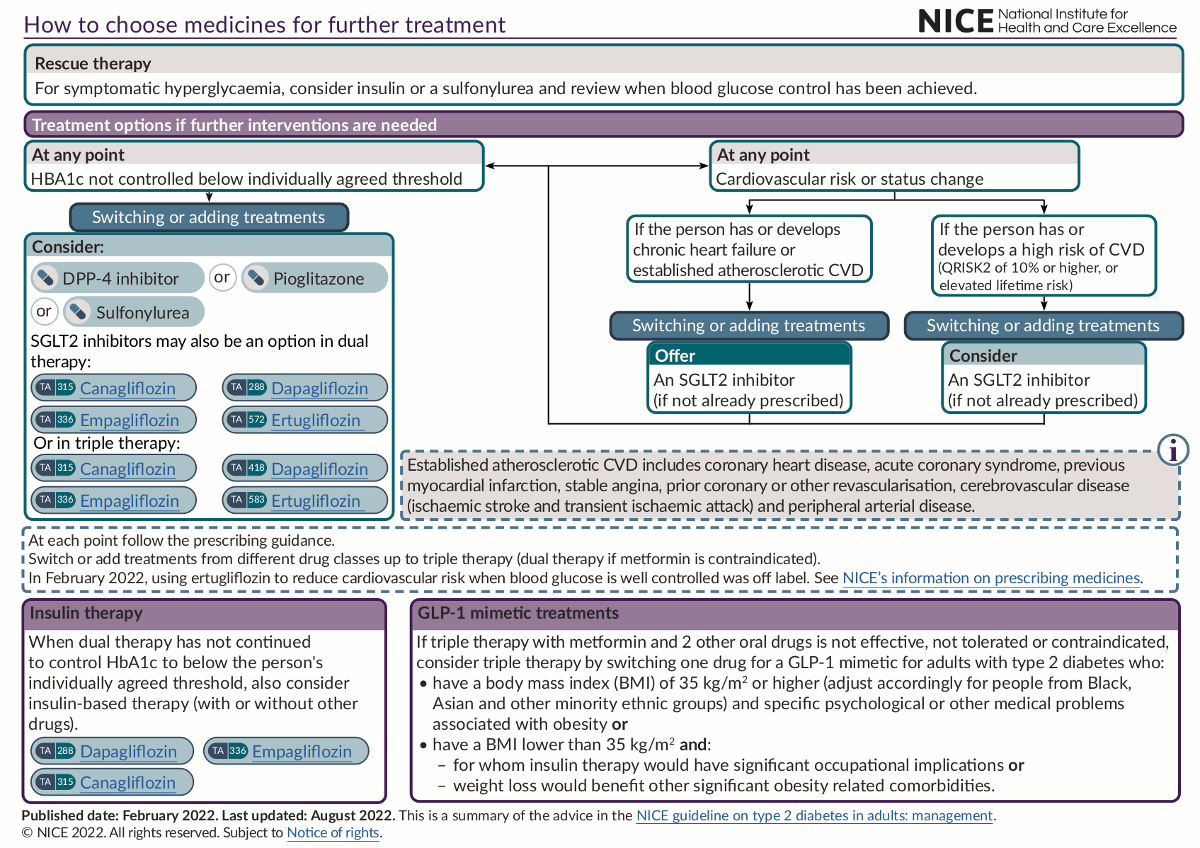
Se a HbA1c do paciente não estiver controlada abaixo do limite acordado individualmente, pode ser apropriado trocar ou adicionar tratamentos. Os medicamentos devem ser introduzidos de forma gradual, verificando a tolerabilidade e a eficácia de cada medicamento.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se a terapia inicial não tiver continuado a controlar a HbA1c abaixo do limite acordado individualmente pela pessoa para intervenção adicional, considere trocar, ou adicionar:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Um inibidor de DPP-4[153]National Institute for Health and Care Excellence. Ertugliflozin as monotherapy or with metformin for treating type 2 diabetes. March 2019 [internet publication].
https://www.nice.org.uk/guidance/ta572
[154]National Institute for Health and Care Excellence. Canagliflozin in combination therapy for treating type 2 diabetes. June 2014 [internet publication].
https://www.nice.org.uk/guidance/ta315
[155]National Institute for Health and Care Excellence. Empagliflozin in combination therapy for treating type 2 diabetes. March 2015 [internet publication].
https://www.nice.org.uk/guidance/ta336
[156]National Institute for Health and Care Excellence. Dapagliflozin in combination therapy for treating type 2 diabetes. Nov 2016 [internet publication].
https://www.nice.org.uk/guidance/ta288
Pioglitazona
Uma sulfonilureia ou
Um inibidor de SGLT2.[154]National Institute for Health and Care Excellence. Canagliflozin in combination therapy for treating type 2 diabetes. June 2014 [internet publication].
https://www.nice.org.uk/guidance/ta315
[155]National Institute for Health and Care Excellence. Empagliflozin in combination therapy for treating type 2 diabetes. March 2015 [internet publication].
https://www.nice.org.uk/guidance/ta336
[156]National Institute for Health and Care Excellence. Dapagliflozin in combination therapy for treating type 2 diabetes. Nov 2016 [internet publication].
https://www.nice.org.uk/guidance/ta288
[157]National Institute for Health and Care Excellence. Ertugliflozin with metformin and a dipeptidyl peptidase-4 inhibitor for treating type 2 diabetes. Jun 2019 [internet publication].
https://www.nice.org.uk/guidance/TA583
Se a terapia dupla com metformina e outro medicamento oral não tiver continuado a controlar a HbA1c para abaixo do limite acordado individualmente pelo paciente para intervenção adicional, considere:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se a metformina for contraindicada ou não tolerada e a terapia dupla com 2 medicamentos orais não tiver continuado a controlar a HbA1c para abaixo do limiar de intervenção acordado individualmente com o paciente, considere o tratamento à base de insulina (ver Farmacoterapia anti-hiperglicêmica: tratamentos à base de insulina).[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se a terapia tripla com metformina e outros 2 agentes orais não for efetiva, não for tolerada ou for contraindicada, considere a terapia tripla trocando um medicamento por um agonista do receptor de GLP-1 ou tirzepatida (um polipeptídeo insulinotrópico dependente de glicose (GIP)/agonista do receptor de GLP-1) nos:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[159]National Institute for Health and Care Excellence. Tirzepatide for treating type 2 diabetes. Oct 2023 [internet publication].
https://www.nice.org.uk/guidance/ta924/chapter/1-Recommendations
Pacientes com IMC ≥35 kg/m² (ajuste de acordo para negros, asiáticos e pessoas de outros grupos étnicos minoritários) e problemas psicológicos específicos ou outros problemas clínicos associados à obesidade, ou
Aqueles com IMC <35 kg/m² e para os quais a terapia com insulina teria implicações ocupacionais significativas, ou a perda de peso beneficiaria outras comorbidades significativas relacionadas à obesidade.
Vale ressaltar que a ADA recomenda que um agonista do receptor de GLP-1 ou um agonista duplo de GIP/GLP-1 seja preferível à insulina quando for necessário um aumento do manejo glicêmico para adultos com diabetes do tipo 2.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Alertas
Considere cuidadosamente as combinações de medicamentos, garantindo que sejam seguras e apropriadas para o seu paciente. Se possível, evite combinar insulina com pioglitazona. A Medicines and Healthcare Products Regulatory Agency (MHRA) do Reino Unido alerta que os pacientes devem ser observados quanto a sinais e sintomas de insuficiência cardíaca, ganho de peso e edema se a pioglitazona for usada em combinação com a insulina. Isso se deve ao aumento da incidência de insuficiência cardíaca quando a pioglitazona é usada em combinação com a insulina, especialmente em pacientes com fatores predisponentes.[160]Medicines and Healthcare products Regulatory Agency. Insulin combined with pioglitazone: risk of cardiac failure. December 2014 [internet publication].
https://www.gov.uk/drug-safety-update/insulin-combined-with-pioglitazone-risk-of-cardiac-failure
Somente ofereça um agonista do receptor de GLP-1 em combinação com a insulina sob aconselhamento de um especialista e suporte contínuo de uma equipe multidisciplinar liderada por um especialista.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
A MHRA alerta sobre casos de cetoacidose diabética nos pacientes com diabetes do tipo 2 que recebem uma combinação de agonista do receptor de GLP-1 e insulina, cujas doses de insulina concomitante tiverem sido rapidamente reduzidas ou descontinuadas.[161]Medicines and Healthcare products Regulatory Agency. GLP-1 receptor agonists: reports of diabetic ketoacidosis when concomitant insulin was rapidly reduced or discontinued. June 2019 [internet publication].
https://www.gov.uk/drug-safety-update/glp-1-receptor-agonists-reports-of-diabetic-ketoacidosis-when-concomitant-insulin-was-rapidly-reduced-or-discontinued
A MHRA alerta que o mesmo risco não pode ser descartado para o agonista duplo do receptor de GIP/GLP-1, tirzepatida, e deve-se ter cautela se ele for usado em combinação com insulina.
Tenha em mente que as recomendações para medicamentos com benefícios cardiovasculares e renais se aplicam a todas as fases do tratamento. Portanto, se um paciente que originalmente não tinha DCV desenvolver DCV, adicione um inibidor de SGLT2 com benefício cardiovascular comprovado ao seu esquema de tratamento existente ou administre um inibidor de SGLT2 no lugar de um medicamento existente.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Da mesma forma, se for recém-descoberto que um paciente apresenta alto risco de DCV, considere adicionar um inibidor de SGLT2 aos seus tratamentos vigentes ou mudar um de seus medicamentos em uso para um inibidor de SGLT2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Propriedades clínicas de agentes anti-hiperglicêmicos específicos
Selecione os agentes caso a caso, após uma conversa cuidadosa com o paciente sobre os prós e os contras de cada opção. Os agentes que oferecem proteção cardiovascular e renal e reduzem a mortalidade por todas as causas, ou a cardiovascular, podem ser preferenciais.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Metformina
A metformina é um “sensibilizador” da insulina, administrado por via oral.[162]Cosentino F, Grant PJ, Aboyans V, et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J. 2020 Jan 7;41(2):255-323.
https://www.doi.org/10.1093/eurheartj/ehz486
http://www.ncbi.nlm.nih.gov/pubmed/31497854?tool=bestpractice.com
Ela é altamente efetiva na redução dos níveis de glicose sanguínea, incorre em risco mínimo de hipoglicemia quando usada como monoterapia, é neutra em termos de peso (com potencial para uma perda de peso modesta), tem um bom perfil de segurança e há experiência de longo prazo com seu uso.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[163]Tsapas A, Karagiannis T, Kakotrichi P, et al. Comparative efficacy of glucose-lowering medications on body weight and blood pressure in patients with type 2 diabetes: a systematic review and network meta-analysis. Diabetes Obes Metab. 2021 Sep;23(9):2116-24.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14451
http://www.ncbi.nlm.nih.gov/pubmed/34047443?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
Essas propriedades, juntamente com seu custo favorável, significam que ela é geralmente o agente de primeira escolha recomendado nos pacientes com diabetes do tipo 2 (no entanto, deve-se observar que algumas diretrizes, como as da ESC em 2023, defendem o uso de outros agentes de primeira linha quando o paciente tiver fatores de risco ou comorbidades adicionais específicos, como DCVA ou DRC).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
É provável que a metformina tenha efeitos benéficos sobre os eventos cardiovasculares adversos graves (por exemplo, infarto do miocárdio, AVC, morte cardiovascular) e a mortalidade por todas as causas, e seu uso em longo prazo provavelmente melhora o prognóstico cardiovascular (embora a ESC informe que os benefícios cardiovasculares da metformina são inconclusivos).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[142]UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). Lancet. 1998 Sep 12;352(9131):854-65.
http://www.ncbi.nlm.nih.gov/pubmed/9742977?tool=bestpractice.com
[143]Holman RR, Paul SK, Bethel MA, et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med. 2008 Oct 9;359(15):1577-89.
https://www.nejm.org/doi/full/10.1056/NEJMoa0806470
http://www.ncbi.nlm.nih.gov/pubmed/18784090?tool=bestpractice.com
[147]Griffin SJ, Leaver JK, Irving GJ. Impact of metformin on cardiovascular disease: a meta-analysis of randomised trials among people with type 2 diabetes. Diabetologia. 2017 Sep;60(9):1620-9.
https://link.springer.com/article/10.1007%2Fs00125-017-4337-9
http://www.ncbi.nlm.nih.gov/pubmed/28770324?tool=bestpractice.com
[165]Monami M, Candido R, Pintaudi B, et al. Effect of metformin on all-cause mortality and major adverse cardiovascular events: an updated meta-analysis of randomized controlled trials. Nutr Metab Cardiovasc Dis. 2021 Mar 10;31(3):699-704.
https://www.nmcd-journal.com/article/S0939-4753(20)30508-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33549430?tool=bestpractice.com
A metformina parece ter um efeito neutro sobre a insuficiência cardíaca e a doença renal diabética.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
A metformina pode ser usada com segurança (com uma possível redução de dose) nos pacientes com taxas de filtração glomerular estimadas (TFGe) reduzidas com monitoramento cuidadoso, mas é contraindicada se a TFGe for <30 mL/min/1.73 m².[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[135]Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 Clinical Practice Guideline for diabetes management in chronic kidney disease. Kidney Int. 2022 Nov;102(5s):S1-127.
https://www.kidney-international.org/article/S0085-2538(22)00507-5/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/36272764?tool=bestpractice.com
[166]de Boer IH, Khunti K, Sadusky T, et al. Diabetes management in chronic kidney disease: a consensus report by the American Diabetes Association (ADA) and kidney disease: improving global outcomes (KDIGO). Diabetes Care. 2022 Dec 1;45(12):3075-90.
https://diabetesjournals.org/care/article/45/12/3075/147614/Diabetes-Management-in-Chronic-Kidney-Disease-A
http://www.ncbi.nlm.nih.gov/pubmed/36189689?tool=bestpractice.com
Os efeitos adversos gastrointestinais são comuns com a metformina.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Níveis diminuídos/deficientes de vitamina B12 também são um efeito colateral comum reconhecido do tratamento, especialmente naqueles que recebem uma dose mais alta ou uma duração de tratamento mais longa, e naqueles com fatores de risco existentes.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[167]Medicines and Healthcare products Regulatory Agency. Metformin and reduced vitamin B12 levels: new advice for monitoring patients at risk. June 2022 [internet publication].
https://www.gov.uk/drug-safety-update/metformin-and-reduced-vitamin-b12-levels-new-advice-for-monitoring-patients-at-risk
Inibidores da SGLT2
Os inibidores de SGLT2 são inibidores da recaptação renal da glicose.[162]Cosentino F, Grant PJ, Aboyans V, et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J. 2020 Jan 7;41(2):255-323.
https://www.doi.org/10.1093/eurheartj/ehz486
http://www.ncbi.nlm.nih.gov/pubmed/31497854?tool=bestpractice.com
Eles são medicamentos orais e os exemplos incluem a canagliflozina, a dapagliflozina, a empagliflozina e a ertugliflozina.
Eles têm um efeito de redução da glicose de intermediário a alto, com menor eficácia glicêmica a TFGe mais baixas.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
Eles não aumentam o risco de hipoglicemia e estão associados a uma perda moderada do peso (2-3 kg) na prática clínica.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[163]Tsapas A, Karagiannis T, Kakotrichi P, et al. Comparative efficacy of glucose-lowering medications on body weight and blood pressure in patients with type 2 diabetes: a systematic review and network meta-analysis. Diabetes Obes Metab. 2021 Sep;23(9):2116-24.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14451
http://www.ncbi.nlm.nih.gov/pubmed/34047443?tool=bestpractice.com
Eles causam glicosúria renal e têm um efeito diurético, o qual reduz a pressão arterial.[168]Scheen AJ. Pharmacodynamics, efficacy and safety of sodium-glucose co-transporter type 2 (SGLT2) inhibitors for the treatment of type 2 diabetes mellitus. Drugs. 2015 Jan;75(1):33-59.
http://www.ncbi.nlm.nih.gov/pubmed/25488697?tool=bestpractice.com
Há também evidências consideráveis que apoiam os benefícios dos inibidores específicos de SGLT2 na redução de eventos cardíacos adversos graves, infartos do miocárdio, hospitalizações por insuficiência cardíaca, mortes cardiovasculares, mortalidade por todas as causas e melhora dos desfechos renais, nos pacientes com diabetes do tipo 2 com doença estabelecida/alto risco de DCV.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[169]Palmer SC, Tendal B, Mustafa RA, et al. Sodium-glucose cotransporter protein-2 (SGLT-2) inhibitors and glucagon-like peptide-1 (GLP-1) receptor agonists for type 2 diabetes: systematic review and network meta-analysis of randomised controlled trials. BMJ. 2021 Jan 13;372:m4573.
https://www.bmj.com/content/372/bmj.m4573.long
http://www.ncbi.nlm.nih.gov/pubmed/33441402?tool=bestpractice.com
Os benefícios são em grande parte independentes do seu efeito de redução da glicose.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Especificamente, demonstrou-se que a canagliflozina e a empagliflozina têm efeitos benéficos sobre os principais eventos adversos cardíacos e a mortalidade cardiovascular; a canagliflozina, a dapagliflozina, a empagliflozina e a ertugliflozina demonstraram efeitos benéficos sobre a insuficiência cardíaca; e a canagliflozina, a dapagliflozina e a empagliflozina demonstraram efeitos benéficos renais, inclusive sobre a progressão da doença renal diabética e a prevenção de desfechos renais importantes (diálise, transplante ou morte por doença renal).[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[170]Zelniker TA, Wiviott SD, Raz I, et al. Comparison of the effects of glucagon-like peptide receptor agonists and sodium-glucose cotransporter 2 inhibitors for prevention of major adverse cardiovascular and renal outcomes in type 2 diabetes mellitus. Circulation. 2019 Apr 23;139(17):2022-31.
http://www.ncbi.nlm.nih.gov/pubmed/30786725?tool=bestpractice.com
[171]Neal B, Perkovic V, Mahaffey KW, et al; CANVAS Program Collaborative Group. Canagliflozin and cardiovascular and renal events in type 2 diabetes. N Engl J Med. 2017 Aug 17;377(7):644-57.
http://www.nejm.org/doi/full/10.1056/NEJMoa1611925#t=article
http://www.ncbi.nlm.nih.gov/pubmed/28605608?tool=bestpractice.com
[172]Cherney DZ, Zinman B, Inzucchi SE, et al. Effects of empagliflozin on the urinary albumin-to-creatinine ratio in patients with type 2 diabetes and established cardiovascular disease: an exploratory analysis from the EMPA-REG OUTCOME randomised, placebo-controlled trial. Lancet Diabetes Endocrinol. 2017 Aug;5(8):610-21.
http://www.ncbi.nlm.nih.gov/pubmed/28666775?tool=bestpractice.com
[173]Mahaffey KW, Jardine MJ, Bompoint S, et al. Canagliflozin and cardiovascular and renal outcomes in type 2 diabetes mellitus and chronic kidney disease in primary and secondary cardiovascular prevention groups. Circulation. 2019 Aug 27;140(9):739-50.
https://www.ahajournals.org/doi/full/10.1161/CIRCULATIONAHA.119.042007
http://www.ncbi.nlm.nih.gov/pubmed/31291786?tool=bestpractice.com
[174]Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet. 2019 Jan 5;393(10166):31-39.
http://www.ncbi.nlm.nih.gov/pubmed/30424892?tool=bestpractice.com
[175]Perkovic V, Jardine MJ, Neal B, et al. Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med. 2019 Jun 13;380(24):2295-306.
https://www.nejm.org/doi/10.1056/NEJMoa1811744
http://www.ncbi.nlm.nih.gov/pubmed/30990260?tool=bestpractice.com
[176]Zinman B, Wanner C, Lachin JM, et al; EMPA-REG OUTCOME Investigators. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med. 2015 Nov 26;373(22):2117-28.
https://www.nejm.org/doi/10.1056/NEJMoa1504720?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%3dwww.ncbi.nlm.nih.gov
http://www.ncbi.nlm.nih.gov/pubmed/26378978?tool=bestpractice.com
[177]Mahaffey KW, Neal B, Perkovic V, et al; CANVAS Program Collaborative Group. Canagliflozin for primary and secondary prevention of cardiovascular events: results from the CANVAS program (Canagliflozin Cardiovascular Assessment Study). Circulation. 2018 Jan 23;137(4):323-34.
https://www.ahajournals.org/doi/full/10.1161/circulationaha.117.032038
http://www.ncbi.nlm.nih.gov/pubmed/29133604?tool=bestpractice.com
[178]Rådholm K, Figtree G, Perkovic V, et al. Canagliflozin and heart failure in type 2 diabetes mellitus. Circulation. 2018 Jul 31;138(5):458-68.
https://www.ahajournals.org/doi/full/10.1161/CIRCULATIONAHA.118.034222
http://www.ncbi.nlm.nih.gov/pubmed/29526832?tool=bestpractice.com
[179]Wiviott SD, Raz I, Bonaca MP, et al; DECLARE–TIMI 58 Investigators. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med. 2019 Jan 24;380(4):347-57.
https://www.nejm.org/doi/full/10.1056/NEJMoa1812389
http://www.ncbi.nlm.nih.gov/pubmed/30415602?tool=bestpractice.com
[180]Neuen BL, Young T, Heerspink HJL, et al. SGLT2 inhibitors for the prevention of kidney failure in patients with type 2 diabetes: a systematic review and meta-analysis. Lancet Diabetes Endocrinol. 2019 Nov;7(11):845-54.
http://www.ncbi.nlm.nih.gov/pubmed/31495651?tool=bestpractice.com
A análise dos dados sugere que os inibidores de SGLT2 têm efeitos benéficos nos desfechos relacionados com a insuficiência cardíaca em pessoas com insuficiência cardíaca, independentemente da fração de ejeção ou do status de diabético.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[181]Kato ET, Silverman MG, Mosenzon O, et al. Effect of dapagliflozin on heart failure and mortality in type 2 diabetes mellitus. Circulation. 2019 May 28;139(22):2528-36.
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.119.040130
http://www.ncbi.nlm.nih.gov/pubmed/30882238?tool=bestpractice.com
[182]Figtree GA, Rådholm K, Barrett TD, et al. Effects of canagliflozin on heart failure outcomes associated with preserved and reduced ejection fraction in type 2 diabetes mellitus. Circulation. 2019 May 28;139(22):2591-3.
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.119.040057
http://www.ncbi.nlm.nih.gov/pubmed/30882240?tool=bestpractice.com
[183]McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med. 2019 Nov 21;381(21):1995-2008.
https://www.nejm.org/doi/10.1056/NEJMoa1911303
http://www.ncbi.nlm.nih.gov/pubmed/31535829?tool=bestpractice.com
[184]National Institute for Health and Care Excellence. Dapagliflozin for treating chronic heart failure with reduced ejection fraction. February 2021 [internet publication].
https://www.nice.org.uk/guidance/TA679
[185]Vaduganathan M, Docherty KF, Claggett BL, et al. SGLT-2 inhibitors in patients with heart failure: a comprehensive meta-analysis of five randomised controlled trials. Lancet. 2022 Sep 3;400(10354):757-67.
https://pubmed.ncbi.nlm.nih.gov/36041474
http://www.ncbi.nlm.nih.gov/pubmed/36041474?tool=bestpractice.com
[186]Packer M, Anker SD, Butler J, et al. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med. 2020 Oct 8;383(15):1413-24.
https://www.nejm.org/doi/10.1056/NEJMoa2022190?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32865377?tool=bestpractice.com
[187]Chen C, Peng H, Li M, et al. Patients with type 2 diabetes mellitus and heart failure benefit more from sodium-glucose cotransporter 2 inhibitor: a systematic review and meta-analysis. Front Endocrinol (Lausanne). 2021 Oct 25:12:664533.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8572881
http://www.ncbi.nlm.nih.gov/pubmed/34759887?tool=bestpractice.com
Além disso, uma metanálise de dados de ensaios clínicos randomizados e controlados mostrou que os inibidores de SGLT2 reduzem o risco de hipercalemia grave nas pessoas com diabetes do tipo 2 com risco cardiovascular elevado ou com doença renal crônica, sem aumentarem o risco de hipocalemia.[188]Neuen BL, Oshima M, Agarwal R, et al. Sodium-glucose cotransporter 2 inhibitors and risk of hyperkalemia in people with type 2 diabetes: a meta-analysis of individual participant data from randomized, controlled trials. Circulation. 2022 May 10;145(19):1460-70.
https://www.ahajournals.org/doi/full/10.1161/CIRCULATIONAHA.121.057736?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/35394821?tool=bestpractice.com
Até o momento, existe maior incerteza em torno dos benefícios cardiovasculares associados à ertugliflozina do que aos outros inibidores de SGLT2.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
[189]Cinti F, Moffa S, Impronta F, et al. Spotlight on ertugliflozin and its potential in the treatment of type 2 diabetes: evidence to date. Drug Des Devel Ther. 2017 Oct 3;11:2905-19.
https://www.dovepress.com/spotlight-on-ertugliflozin-and-its-potential-in-the-treatment-of-type--peer-reviewed-fulltext-article-DDDT
http://www.ncbi.nlm.nih.gov/pubmed/29042751?tool=bestpractice.com
Em sua diretriz sobre diabetes do tipo 2, o NICE informou que a ertugliflozina não demonstrou redução consistente de insuficiência cardíaca em comparação com o placebo na metanálise de rede, nem apresentou melhor significância estatística que o placebo para o desfecho de eventos adversos cardiovasculares importantes (MACE) de 3 pontos (incluindo morte cardiovascular, infarto do miocárdio não fatal e AVC não fatal).[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Além disso, um ensaio clínico randomizado e duplo-cego de fase 3 avaliou os efeitos da ertugliflozina versus placebo sobre os desfechos cardiovasculares e renais em pessoas com diabetes do tipo 2 e doença cardiovascular aterosclerótica estabelecida; os resultados mostraram não inferioridade ao placebo no desfecho primário de eventos adversos cardiovasculares importantes, mas nenhuma superioridade nos principais desfechos cardiovasculares e renais secundários.[190]ClinicalTrials.gov. Cardiovascular outcomes following ertugliflozin treatment in type 2 diabetes mellitus participants with vascular disease: the VERTIS CV study (MK-8835-004). April 2019 [internet publication].
https://clinicaltrials.gov/ct2/show/NCT01986881
[191]Cannon CP, Pratley R, Dagogo-Jack S, et al. Cardiovascular outcomes with ertugliflozin in type 2 diabetes. N Engl J Med. 2020 Oct 8;383(15):1425-35.
https://www.nejm.org/doi/10.1056/NEJMoa2004967?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32966714?tool=bestpractice.com
Os inibidores de SGLT2 estão associados a um aumento do risco de infecções genitais micóticas (geralmente leves e tratáveis), e a um aumento do risco de cetoacidose diabética (embora a incidência seja baixa).[73]Medicines and Healthcare products Regulatory Agency. SGLT2 inhibitors: updated advice on the risk of diabetic ketoacidosis. April 2016 [internet publication].
https://www.gov.uk/drug-safety-update/sglt2-inhibitors-updated-advice-on-the-risk-of-diabetic-ketoacidosis
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[192]Ueda P, Svanström H, Melbye M, et al. Sodium glucose cotransporter 2 inhibitors and risk of serious adverse events: nationwide register based cohort study. BMJ. 2018 Nov 14;363:k4365.
https://www.bmj.com/content/363/bmj.k4365.long
http://www.ncbi.nlm.nih.gov/pubmed/30429124?tool=bestpractice.com
[193]Erondu N, Desai M, Ways K, et al. Diabetic ketoacidosis and related events in the canagliflozin type 2 diabetes clinical program. Diabetes Care. 2015 Sep;38(9):1680-6.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4542268
http://www.ncbi.nlm.nih.gov/pubmed/26203064?tool=bestpractice.com
[194]Peters AL, Buschur EO, Buse JB, et al. Euglycemic diabetic ketoacidosis: a potential complication of treatment with sodium-glucose cotransporter 2 inhibition. Diabetes Care. 2015 Sep;38(9):1687-93.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4542270
http://www.ncbi.nlm.nih.gov/pubmed/26078479?tool=bestpractice.com
[195]Fleming N, Hamblin PS, Story D, et al. Evolving evidence of diabetic ketoacidosis in patients taking sodium-glucose cotransporter 2 inhibitors. J Clin Endocrinol Metab. 2020 Aug 1;105(8):dgaa200.
https://academic.oup.com/jcem/article/105/8/2475/5821255?login=false
http://www.ncbi.nlm.nih.gov/pubmed/32302001?tool=bestpractice.com
A Food and Drug Administration (FDA) dos EUA emitiu um alerta sobre o risco de lesão renal aguda com a canagliflozina e a dapagliflozina.[196]US Food and Drug Administration (FDA). FDA drug safety communication: FDA strengthens kidney warnings for diabetes medicines canagliflozin (Invokana, Invokamet) and dapagliflozin (Farxiga, Xigduo XR). June 2016 [internet publication].
https://www.fda.gov/drugs/drug-safety-and-availability/fda-drug-safety-communication-fda-strengthens-kidney-warnings-diabetes-medicines-canagliflozin
A MHRA e a European Medicines Agency (EMA) alertam para um aumento do risco de amputação de membros inferiores (principalmente pododáctilos) em pacientes com diabetes do tipo 2 que tomam canagliflozina, e a MHRA enfatiza a importância dos cuidados preventivos com os pés para todos os pacientes com diabetes.[197]European Medicines Agency. SGLT2 inhibitors: information on potential risk of toe amputation to be included in prescribing information. February 2017 [internet publication].
https://www.ema.europa.eu/en/documents/referral/sglt2-inhibitors-previously-canagliflozin-article-20-procedure-sglt2-inhibitors-information_en-0.pdf
[198]Medicines and Healthcare products Regulatory Agency. SGLT2 inhibitors: updated advice on increased risk of lower-limb amputation (mainly toes). March 2017 [internet publication].
https://www.gov.uk/drug-safety-update/sglt2-inhibitors-updated-advice-on-increased-risk-of-lower-limb-amputation-mainly-toes
Portanto, os pacientes com úlceras nos pés ou com alto risco de amputação devem receber educação abrangente sobre cuidados com os pés durante o tratamento com inibidores de SGLT2. As diretrizes da EASD/ADA sobre o tratamento da hiperglicemia no diabetes do tipo 2 observam que, embora os estudos iniciais tenham destacado potenciais preocupações de segurança relacionadas com os inibidores de SGLT2, incluindo lesão renal aguda e amputação, estudos de longo prazo que avaliaram e monitoraram prospectivamente estes eventos não observaram um desequilíbrio significativo nos riscos.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[199]Dorsey-Treviño EG, González-González JG, Alvarez-Villalobos N, et al. Sodium-glucose cotransporter 2 (SGLT-2) inhibitors and microvascular outcomes in patients with type 2 diabetes: systematic review and meta-analysis. J Endocrinol Invest. 2020 Mar;43(3):289-304.
http://www.ncbi.nlm.nih.gov/pubmed/31489568?tool=bestpractice.com
A MHRA e a FDA também alertam sobre casos de fasciite necrosante do períneo (também conhecida como gangrena de Fournier) observados na vigilância pós-comercialização dos inibidores de SGLT2.[200]US Food and Drug Administration. FDA drug safety communication: FDA warns about rare occurrences of a serious infection of the genital area with SGLT2 inhibitors for diabetes. August 2018 [internet publication].
https://www.fda.gov/drugs/drug-safety-and-availability/fda-warns-about-rare-occurrences-serious-infection-genital-area-sglt2-inhibitors-diabetes
[201]Medicines and Healthcare products Regulatory Agency. SGLT2 inhibitors: reports of Fournier’s gangrene (necrotising fasciitis of the genitalia or perineum). February 2019 [internet publication].
https://www.gov.uk/drug-safety-update/sglt2-inhibitors-reports-of-fournier-s-gangrene-necrotising-fasciitis-of-the-genitalia-or-perineum
Agonistas do receptor de GLP-1
Os agonistas do receptor de GLP-1 são medicamentos à base de incretinas.[162]Cosentino F, Grant PJ, Aboyans V, et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J. 2020 Jan 7;41(2):255-323.
https://www.doi.org/10.1093/eurheartj/ehz486
http://www.ncbi.nlm.nih.gov/pubmed/31497854?tool=bestpractice.com
As incretinas são um grupo de hormônios metabólicos que diminuem os níveis de glicose no sangue, estimulando a liberação de insulina e inibindo a liberação de glucagon; as duas incretinas mais importantes são os peptídeos intestinais GLP-1 e o GIP. Os agonistas do receptor de GLP-1 promovem a secreção de insulina e a supressão do glucagon dependentes de glicose, desaceleram o esvaziamento gástrico, limitam os incrementos glicêmicos pós-refeição e reduzem o apetite e a ingestão de energia.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Os exemplos incluem a dulaglutida, a exenatida, a liraglutida, a lixisenatida e a semaglutida. Geralmente elas são administradas por via subcutânea, embora exista uma formulação oral disponível da semaglutida.
Eles têm um efeito redutor da glicose alto/muito alto e não causam hipoglicemia.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
Evidências apoiam benefícios dos agonistas específicos sobre o receptor de GLP-1 na redução de eventos adversos cardíacos importantes e na progressão da doença renal diabética nos pacientes de alto risco com diabetes do tipo 2; esses benefícios ocorrem em grande parte independentemente dos seus efeitos sobre a redução da glicose.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[169]Palmer SC, Tendal B, Mustafa RA, et al. Sodium-glucose cotransporter protein-2 (SGLT-2) inhibitors and glucagon-like peptide-1 (GLP-1) receptor agonists for type 2 diabetes: systematic review and network meta-analysis of randomised controlled trials. BMJ. 2021 Jan 13;372:m4573.
https://www.bmj.com/content/372/bmj.m4573.long
http://www.ncbi.nlm.nih.gov/pubmed/33441402?tool=bestpractice.com
[202]Giugliano D, Scappaticcio L, Longo M, et al. GLP-1 receptor agonists and cardiorenal outcomes in type 2 diabetes: an updated meta-analysis of eight CVOTs. Cardiovasc Diabetol. 2021 Sep 15;20(1):189.
https://cardiab.biomedcentral.com/articles/10.1186/s12933-021-01366-8
http://www.ncbi.nlm.nih.gov/pubmed/34526024?tool=bestpractice.com
Por exemplo, a dulaglutida e a semaglutida demonstraram reduzir os principais eventos cardiovasculares, mas não as mortalidades por todas as causas ou cardiovascular.[203]Gerstein HC, Colhoun HM, Dagenais GR, et al; REWIND Investigators. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet. 2019 Jul 13;394(10193):121-30.
http://www.ncbi.nlm.nih.gov/pubmed/31189511?tool=bestpractice.com
[204]Marso SP, Bain SC, Consoli A, et al; SUSTAIN-6 Investigators. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med. 2016 Nov 10;375(19):1834-44.
http://www.nejm.org/doi/full/10.1056/NEJMoa1607141#t=article
http://www.ncbi.nlm.nih.gov/pubmed/27633186?tool=bestpractice.com
[205]Kaul S. Mitigating cardiovascular risk in type 2 diabetes with antidiabetes drugs: a review of principal cardiovascular outcome results of EMPA-REG OUTCOME, LEADER, and SUSTAIN-6 trials. Diabetes Care. 2017 Jul;40(7):821-31.
https://care.diabetesjournals.org/content/40/7/821.long
http://www.ncbi.nlm.nih.gov/pubmed/28637887?tool=bestpractice.com
A liraglutida reduziu significativamente a mortalidade cardiovascular e a mortalidade por todas as causas em pessoas com diabetes e doença cardiovascular ou alto risco de DCV em um ensaio randomizado.[206]Marso SP, Daniels GH, Brown-Frandsen K, et al; LEADER Steering Committee on behalf of the LEADER Trial Investigators. Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med. 2016 Jul 28;375(4):311-22.
http://www.nejm.org/doi/full/10.1056/NEJMoa1603827#t=article
http://www.ncbi.nlm.nih.gov/pubmed/27295427?tool=bestpractice.com
No entanto, ensaios demonstraram que a exenatida e a lixisenatida não reduzem eventos cardiovasculares importantes.[207]Hu Y. Advances in reducing cardiovascular risk in the management of patients with type 2 diabetes mellitus. Chronic Dis Transl Med. 2019 Mar 15;5(1):25-36.
https://www.sciencedirect.com/science/article/pii/S2095882X18300653
http://www.ncbi.nlm.nih.gov/pubmed/30993261?tool=bestpractice.com
Demonstrou-se que a dulaglutida, liraglutida e a semaglutida (subcutânea) produzem desfechos renais benéficos, impulsionados pelos desfechos sobre a albuminúria.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[208]Yuan D, Sharma H, Krishnan A, et al. Effect of glucagon-like peptide 1 receptor agonists on albuminuria in adult patients with type 2 diabetes mellitus: a systematic review and meta-analysis. Diabetes Obes Metab. 2022 Sep;24(9):1869-81.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14776
http://www.ncbi.nlm.nih.gov/pubmed/35589615?tool=bestpractice.com
Uma metanálise de ensaios clínicos randomizados controlados por placebo que estudaram agonistas do receptor de GLP-1 em pacientes com diabetes do tipo 2 mostrou que o tratamento não reduziu as hospitalizações por insuficiência cardíaca e a mortalidade nos pacientes com insuficiência cardíaca, mas que ele pode prevenir novos episódios de insuficiência cardíaca e a mortalidade em pacientes sem insuficiência cardíaca.[209]Ferreira JP, Saraiva F, Sharma A, et al. Glucagon-like peptide 1 receptor agonists in patients with type 2 diabetes with and without chronic heart failure: a meta-analysis of randomized placebo-controlled outcome trials. Diabetes Obes Metab. 2023 Jun;25(6):1495-502.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14997
http://www.ncbi.nlm.nih.gov/pubmed/36722252?tool=bestpractice.com
A redução nos eventos ateroscleróticos observados com os agonistas do receptor de GLP-1 não foi influenciada pela presença ou não de insuficiência cardíaca.[209]Ferreira JP, Saraiva F, Sharma A, et al. Glucagon-like peptide 1 receptor agonists in patients with type 2 diabetes with and without chronic heart failure: a meta-analysis of randomized placebo-controlled outcome trials. Diabetes Obes Metab. 2023 Jun;25(6):1495-502.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14997
http://www.ncbi.nlm.nih.gov/pubmed/36722252?tool=bestpractice.com
Os agonistas do receptor de GLP-1 produzem uma perda de peso de intermediária a muito alta.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[163]Tsapas A, Karagiannis T, Kakotrichi P, et al. Comparative efficacy of glucose-lowering medications on body weight and blood pressure in patients with type 2 diabetes: a systematic review and network meta-analysis. Diabetes Obes Metab. 2021 Sep;23(9):2116-24.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14451
http://www.ncbi.nlm.nih.gov/pubmed/34047443?tool=bestpractice.com
Eles são adequados para os pacientes obesos sem gastroparesia que desejarem perder peso, estiverem dispostos a tomar injeções e puderem tolerar o efeito adverso comum de náusea inicial.[210]Htike ZZ, Zaccardi F, Papamargaritis D, et al. Efficacy and safety of glucagon-like peptide-1 receptor agonists in type 2 diabetes: a systematic review and mixed-treatment comparison analysis. Diabetes Obes Metab. 2017 Apr;19(4):524-36.
http://www.ncbi.nlm.nih.gov/pubmed/27981757?tool=bestpractice.com
Em uma revisão, o uso de um agonista do receptor de GLP-1 ocasionou perda de 1.4 kg em comparação com o placebo, e uma perda de 4.8 kg em comparação com a insulina.[211]Amori RE, Lau J, Pittas AG. Efficacy and safety of incretin therapy in type 2 diabetes: systematic review and meta-analysis. JAMA. 2007 Jul 11;298(2):194-206.
http://www.ncbi.nlm.nih.gov/pubmed/17622601?tool=bestpractice.com
Uma revisão sistemática e metanálise da liraglutida indica que ela produziu uma redução de peso significativa com um perfil de segurança razoável para pacientes com sobrepeso ou obesidade, independentemente do status diabético, em comparação com placebo.[212]Konwar M, Bose D, Jaiswal SK, et al. Efficacy and safety of liraglutide 3.0 mg in patients with overweight and obese with or without diabetes: a systematic review and meta-analysis. Int J Clin Pract. 2022 Jul 19:2022:1201977.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9325632
http://www.ncbi.nlm.nih.gov/pubmed/35936066?tool=bestpractice.com
A ADA recomenda que, para os adultos com diabetes e sobrepeso ou obesidade, um agonista do receptor de GLP-1 com maior eficácia na perda de peso (isto é, semaglutida) seja uma opção de escolha quando a farmacoterapia for indicada como adjuvante às mudanças de estilo de vida para controle do peso.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Ela informa que essa abordagem tem benefícios adicionais independentes do peso (por exemplo, glicêmicos e cardiometabólicos).[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Os agonistas do receptor de GLP-1 são efetivos na melhora da esteatose, e alguns ensaios clínicos randomizados e controlados demonstraram benefícios potenciais com a liraglutida e a semaglutida em pacientes com esteatose hepática associada a disfunção metabólica (EHDM; anteriormente conhecida como esteatose hepática não alcoólica [EHNA]), incluindo notadamente o retardo da progressão da fibrose hepática.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
A ADA recomenda considerar o uso de um agonista do receptor de GLP-1 (com benefício demonstrado na EHDM, anteriormente conhecida como EHNA) para os adultos com diabetes do tipo 2 (particularmente aqueles com sobrepeso ou obesidade) e doença hepática gordurosa associada a disfunção metabólica (DHGDM, anteriormente conhecida como doença hepática gordurosa não alcoólica [DHGNA]), como adjuvante às intervenções de estilo de vida para a perda do peso.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
A ADA também recomenda que os agonistas do receptor de GLP-1 sejam uma opção de escolha para o tratamento da hiperglicemia em pessoas com diabetes do tipo 2 com EHDM (anteriormente EHNA) confirmada por biópsia ou de alto risco com fibrose hepática clinicamente significativa em testes não invasivos.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Os efeitos adversos mais comuns dos inibidores de GLP-1 são gastrointestinais, como náuseas, vômitos e diarreia, mas tendem a diminuir com o tempo. Além disso, a MHRA alerta sobre casos de cetoacidose diabética em pacientes com diabetes do tipo 2 que recebem uma combinação de agonista do receptor de GLP-1 e insulina, cujas doses de insulina concomitante tiverem sido reduzidas rapidamente ou descontinuadas.[161]Medicines and Healthcare products Regulatory Agency. GLP-1 receptor agonists: reports of diabetic ketoacidosis when concomitant insulin was rapidly reduced or discontinued. June 2019 [internet publication].
https://www.gov.uk/drug-safety-update/glp-1-receptor-agonists-reports-of-diabetic-ketoacidosis-when-concomitant-insulin-was-rapidly-reduced-or-discontinued
A pancreatite foi relatada em ensaios clínicos com agonistas do receptor de GLP-1, mas a causalidade não foi estabelecida.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Há evidências conflitantes sobre se os agonistas do receptor de GLP-1 aumentam o risco de distúrbios da tireoide.
Uma metanálise de ensaios clínicos randomizados e controlados de 2022 concluiu que os agonistas do receptor de GLP-1 não aumentaram ou diminuíram o risco de câncer de tireoide, hipertireoidismo, hipotireoidismo, tireoidite, massa tireoidiana e bócio, embora tenha observado que devido à baixa incidência dessas doenças, esses achados precisavam ser examinados mais detalhadamente.[213]Hu W, Song R, Cheng R, et al. Use of GLP-1 Receptor agonists and occurrence of thyroid disorders: a meta-analysis of randomized controlled trials. Front Endocrinol (Lausanne). 2022 Jul 11:13:927859.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9309474
http://www.ncbi.nlm.nih.gov/pubmed/35898463?tool=bestpractice.com
No entanto, uma análise tipo caso-controle aninhada de 2562 indivíduos com câncer de tireoide relatou que o uso de agonistas do receptor de GLP-1 esteve associado a um aumento do risco de todos os cânceres de tireoide e câncer medular de tireoide, em particular após 1-3 anos de tratamento.[214]Bezin J, Gouverneur A, Pénichon M, et al. GLP-1 receptor agonists and the risk of thyroid cancer. Diabetes Care. 2023 Feb 1;46(2):384-90.
https://diabetesjournals.org/care/article-abstract/46/2/384/147888/GLP-1-Receptor-Agonists-and-the-Risk-of-Thyroid?redirectedFrom=fulltext
http://www.ncbi.nlm.nih.gov/pubmed/36356111?tool=bestpractice.com
Uma revisão sistemática e metanálise de rede combinando 84 ensaios que investigaram o efeito de agonistas do receptor de GLP-1 e inibidores de DPP-4 (terapias à base de incretina) concluíram que eles não estavam associados a um risco aumentado de cânceres do sistema digestório em pacientes com diabetes do tipo 2.[215]Chai S, Yu S, Yang Z, et al. Effect of incretin-based therapies on cancers of digestive system among 101 595 patients with type 2 diabetes mellitus: a systematic review and network meta-analysis combining 84 trials with a median duration of 30 weeks. BMJ Open Diabetes Res Care. 2019 Sep 20;7(1):e000728.
https://drc.bmj.com/content/7/1/e000728.long
http://www.ncbi.nlm.nih.gov/pubmed/31641525?tool=bestpractice.com
A EMA está revendo os dados sobre o risco de pensamentos suicidas e pensamentos de automutilação com os agonistas do receptor de GLP-1 após relatos de tais ocorrências em pessoas em uso de liraglutida e semaglutida.
Agonista duplo dos receptores de GIP/GLP-1
A tirzepatida é o primeiro e único agonista duplo dos receptores de GIP/GLP-1 disponível. Ela aumenta a sensibilidade e a secreção de insulina, suprime a secreção de glucagon e retarda o esvaziamento gástrico. Em 2023, o NICE recomendou o uso da tirzepatida (como adjuvante à dieta e aos exercícios) em adultos cujo diabetes do tipo 2 não estiver adequadamente controlado, somente se a terapia antidiabética tripla for inefetiva, contraindicada ou não tolerada, e se eles atenderem a um dos seguintes critérios:[159]National Institute for Health and Care Excellence. Tirzepatide for treating type 2 diabetes. Oct 2023 [internet publication].
https://www.nice.org.uk/guidance/ta924/chapter/1-Recommendations
IMC ≥35 kg/m² (ajuste de acordo para pessoas negras, asiáticas e outros grupos étnicos minoritários) e problemas psicológicos ou outros problemas médicos específicos associados à obesidade; ou
IMC <35 kg/m² e implicações ocupacionais significativas da insulinoterapia ou benefícios potenciais da perda de peso sobre outras complicações significativas relacionadas à obesidade.
O NICE posiciona a tirzepatida como uma alternativa ao uso de um agonista do receptor de GLP-1 (ou seja, a tirzepatida é uma opção a ser considerada no mesmo nível da via de tratamento do diabetes do tipo 2 no Reino Unido que os agonistas do receptor de GLP-1).[159]National Institute for Health and Care Excellence. Tirzepatide for treating type 2 diabetes. Oct 2023 [internet publication].
https://www.nice.org.uk/guidance/ta924/chapter/1-Recommendations
O NICE observa que a tirzepatida é usada antes na via de tratamento internacionalmente, mas em sua revisão ela foi considerada apenas como uma opção alternativa ao início de um agonista do receptor de GLP-1.[159]National Institute for Health and Care Excellence. Tirzepatide for treating type 2 diabetes. Oct 2023 [internet publication].
https://www.nice.org.uk/guidance/ta924/chapter/1-Recommendations
A tirzepatida está aprovada na Europa para o tratamento de adultos com diabetes mellitus do tipo 2 insuficientemente controlado como um adjuvante à dieta e ao exercício (como monoterapia quando a metformina é considerada inadequada devido a intolerância ou contraindicações; ou em adição a outros medicamentos para o tratamento do diabetes). As orientações americanas sobre diabetes do tipo 2 em adultos da ADA incluem recomendações para um agonista duplo dos receptores de GIP/GLP-1 (ou seja, a tirzepatida) como opção de escolha quando a farmacoterapia é indicada para controle do peso em pessoas com sobrepeso ou obesidade (a ADA enfatiza que essa abordagem adicionou benefícios glicêmicos e cardiometabólicos independentes do peso).[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Demonstrou-se que a tirzepatida tem um efeito maior nos níveis de glicose e no controle do peso que os agonistas seletivos do receptor de GLP-1 isoladamente, sem aumento do risco de hipoglicemia.[216]Rosenstock J, Wysham C, Frías JP, et al. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): a double-blind, randomised, phase 3 trial. Lancet. 2021 Jul 10;398(10295):143-55.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(21)01324-6/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34186022?tool=bestpractice.com
[217]Frías JP, Davies MJ, Rosenstock J, et al. Tirzepatide versus semaglutide once weekly in patients with type 2 diabetes. N Engl J Med. 2021 Aug 5;385(6):503-15.
https://www.nejm.org/doi/10.1056/NEJMoa2107519?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/34170647?tool=bestpractice.com
[218]Frias JP, Nauck MA, Van J, et al. Efficacy and safety of LY3298176, a novel dual GIP and GLP-1 receptor agonist, in patients with type 2 diabetes: a randomised, placebo-controlled and active comparator-controlled phase 2 trial. Lancet. 2018 Nov 17;392(10160):2180-93.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(18)32260-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/30293770?tool=bestpractice.com
[219]Inagaki N, Takeuchi M, Oura T, et al. Efficacy and safety of tirzepatide monotherapy compared with dulaglutide in Japanese patients with type 2 diabetes (SURPASS J-mono): a double-blind, multicentre, randomised, phase 3 trial. Lancet Diabetes Endocrinol. 2022 Sep;10(9):623-33.
https://www.thelancet.com/journals/landia/article/PIIS2213-8587(22)00188-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/35914543?tool=bestpractice.com
Os ensaios clínicos demonstraram que, em pacientes com diabetes do tipo 2, a tirzepatida foi superior à insulina degludec ajustada (com maiores reduções na HbA1c e no peso corporal e um menor risco de hipoglicemia), e em pacientes com diabetes do tipo 2 e um risco cardiovascular elevado, a tirzepatida foi superior à insulina glargina (com redução maior e clinicamente significativa da HbA1c e uma menor incidência de hipoglicemia).[220]Ludvik B, Giorgino F, Jódar E, et al. Once-weekly tirzepatide versus once-daily insulin degludec as add-on to metformin with or without SGLT2 inhibitors in patients with type 2 diabetes (SURPASS-3): a randomised, open-label, parallel-group, phase 3 trial. Lancet. 2021 Aug 14;398(10300):583-98.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(21)01443-4/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34370970?tool=bestpractice.com
[221]Del Prato S, Kahn SE, Pavo I, et al. Tirzepatide versus insulin glargine in type 2 diabetes and increased cardiovascular risk (SURPASS-4): a randomised, open-label, parallel-group, multicentre, phase 3 trial. Lancet. 2021 Nov 13;398(10313):1811-24.
http://www.ncbi.nlm.nih.gov/pubmed/34672967?tool=bestpractice.com
O NICE observa que doses mais altas de tirzepatida estão associadas a um maior grau de perda de peso, enquanto os efeitos na HbA1c parecem ser menos dose-dependentes, presentes mesmo a doses baixas.[159]National Institute for Health and Care Excellence. Tirzepatide for treating type 2 diabetes. Oct 2023 [internet publication].
https://www.nice.org.uk/guidance/ta924/chapter/1-Recommendations
As análises (incluindo uma metanálise pré-especificada) dos resultados iniciais sobre a segurança cardiovascular em curto prazo da tirzepatida dos ensaios clínicos SURPASS conduzidas nos pacientes com diabetes do tipo 2 sugerem que não há risco cardiovascular excessivo ou aumento no risco de eventos cardiovasculares importantes com a tirzepatida quando comparada aos controles (incluindo a semaglutida e a dulaglutida, agonistas do receptor de GLP-1 com benefícios cardiovasculares conhecidos).[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[221]Del Prato S, Kahn SE, Pavo I, et al. Tirzepatide versus insulin glargine in type 2 diabetes and increased cardiovascular risk (SURPASS-4): a randomised, open-label, parallel-group, multicentre, phase 3 trial. Lancet. 2021 Nov 13;398(10313):1811-24.
http://www.ncbi.nlm.nih.gov/pubmed/34672967?tool=bestpractice.com
[222]Sattar N, McGuire DK, Pavo I, et al. Tirzepatide cardiovascular event risk assessment: a pre-specified meta-analysis. Nat Med. 2022 Mar;28(3):591-8.
https://www.nature.com/articles/s41591-022-01707-4
http://www.ncbi.nlm.nih.gov/pubmed/35210595?tool=bestpractice.com
Além disso, a análise post-hoc do ensaio clínico SURMOUNT-1 (conduzido para avaliar a eficácia e a segurança da tirzepatida em pacientes com obesidade ou sobrepeso), que excluiu particularmente os pacientes com diabetes do tipo 2, concluiu que foram observados benefícios significativos na redução do risco cardiovascular com a tirzepatida em comparação com o placebo.[223]Hankosky ER, Wang H, Neff LM, et al. Tirzepatide reduces the predicted risk of atherosclerotic cardiovascular disease and improves cardiometabolic risk factors in adults with obesity or overweight: SURMOUNT-1 post hoc analysis. Diabetes Obes Metab. 2024 Jan;26(1):319-28.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.15318
http://www.ncbi.nlm.nih.gov/pubmed/37932236?tool=bestpractice.com
Entretanto, são necessárias pesquisas adicionais sobre os efeitos cardiovasculares de longo prazo da tirzepatida. Os ensaios em andamento SURPASS-CVOT (em pacientes com diabetes do tipo 2) e SURMOUNT-MMO (em pacientes com obesidade sem diabetes) buscarão fornecer dados mais robustos sobre a segurança cardiovascular da tirzepatida e seus efeitos sobre os desfechos cardiovasculares e a morbidade e mortalidade.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[224]Nicholls SJ, Bhatt DL, Buse JB, et al. Comparison of tirzepatide and dulaglutide on major adverse cardiovascular events in participants with type 2 diabetes and atherosclerotic cardiovascular disease: SURPASS-CVOT design and baseline characteristics. Am Heart J. 2024 Jan;267:1-11.
https://www.sciencedirect.com/science/article/pii/S0002870323002806?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/37758044?tool=bestpractice.com
[225]ClinicalTrials.gov. A study of tirzepatide (LY3298176) on the reduction on morbidity and mortality in adults with obesity (SURMOUNT-MMO). ClinicalTrials.gov Identifier: NCT05556512. Oct 2024 [internet publication].
https://clinicaltrials.gov/study/NCT05556512
Uma análise post-hoc do SURPASS-4, que comparou a tirzepatida com a insulina glargina em pacientes com diabetes do tipo 2 e risco cardiovascular aumentado ou DCV estabelecida, sugeriu que a tirzepatida pode estar associada a benefícios renais.[226]Heerspink HJL, Sattar N, Pavo I, et al. Effects of tirzepatide versus insulin glargine on kidney outcomes in type 2 diabetes in the SURPASS-4 trial: post-hoc analysis of an open-label, randomised, phase 3 trial. Lancet Diabetes Endocrinol. 2022 Nov;10(11):774-85.
http://www.ncbi.nlm.nih.gov/pubmed/36152639?tool=bestpractice.com
A tirzepatida foi razoavelmente bem tolerada nos ensaios, com os efeitos adversos mais comuns sendo semelhantes aos observados com os agonistas do receptor de GLP-1 (náuseas, vômitos e dispepsia). O aumento lento da dose de tirzepatida pode minimizar o risco desses efeitos adversos.[159]National Institute for Health and Care Excellence. Tirzepatide for treating type 2 diabetes. Oct 2023 [internet publication].
https://www.nice.org.uk/guidance/ta924/chapter/1-Recommendations
Os mesmos avisos e precauções observados acima para os agonistas do receptor de GLP-1 se aplicam à tirzepatida.
Inibidores da DPP-4
Os inibidores de DPP-4 são medicamentos orais à base de incretinas.[162]Cosentino F, Grant PJ, Aboyans V, et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J. 2020 Jan 7;41(2):255-323.
https://www.doi.org/10.1093/eurheartj/ehz486
http://www.ncbi.nlm.nih.gov/pubmed/31497854?tool=bestpractice.com
As incretinas GLP-1 e GIP são rapidamente inativadas pela enzima DPP-4. Os inibidores de DPP-4 (também conhecidos como gliptinas) incluem a alogliptina, a linagliptina, a saxagliptina, a sitagliptina e a vildagliptina. Eles têm um efeito modesto de redução da glicose, são neutros em termos de peso e são geralmente bem tolerados, com um risco mínimo de hipoglicemia.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[163]Tsapas A, Karagiannis T, Kakotrichi P, et al. Comparative efficacy of glucose-lowering medications on body weight and blood pressure in patients with type 2 diabetes: a systematic review and network meta-analysis. Diabetes Obes Metab. 2021 Sep;23(9):2116-24.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14451
http://www.ncbi.nlm.nih.gov/pubmed/34047443?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
No geral, os inibidores de DPP-4 não estão associados a nenhum aumento ou redução de eventos adversos cardíacos importantes, mortalidade por todas as causas ou insuficiência cardíaca; no entanto, a saxagliptina pode estar associada a um aumento do risco de hospitalização por insuficiência cardíaca (e, portanto, não é recomendada pela ESC para uso em pacientes com risco ou história de insuficiência cardíaca).[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[227]Mannucci E, Nreu B, Montereggi C, et al. Cardiovascular events and all-cause mortality in patients with type 2 diabetes treated with dipeptidyl peptidase-4 inhibitors: an extensive meta-analysis of randomized controlled trials. Nutr Metab Cardiovasc Dis. 2021 Sep 22;31(10):2745-55.
https://www.nmcd-journal.com/article/S0939-4753(21)00279-9/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34364771?tool=bestpractice.com
A vildagliptina, o único inibidor de DPP-4 mencionado acima não estudado em um ensaio dedicado com desfechos cardiovasculares, foi associada a um aumento dos volumes do ventrículo esquerdo (de significância clínica desconhecida) em um pequeno estudo, mas nenhum efeito significativo sobre a fração de ejeção do ventrículo esquerdo (FEVE) foi demonstrado.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
[228]McMurray JJV, Ponikowski P, Bolli GB, et al. Effects of vildagliptin on ventricular function in patients with type 2 diabetes mellitus and heart failure: a randomized placebo-controlled trial. JACC Heart Fail. 2018 Jan;6(1):8-17.
https://www.sciencedirect.com/science/article/pii/S2213177917305358?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/29032139?tool=bestpractice.com
Para pacientes com diabetes do tipo 2 com ou em risco de insuficiência cardíaca, as diretrizes da ESC recomendam que a linagliptina e a sitagliptina têm um efeito neutro sobre o risco de hospitalização por insuficiência cardíaca e devem ser consideradas como opções para redução da glicose nesses pacientes.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Os inibidores de DPP-4 não retardam a progressão da doença renal diabética; no entanto, foi observada uma redução no risco de progressão da albuminúria com a linagliptina em um ensaio clínico controlado com placebo.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Os inibidores de DPP-4 podem ser usados nos casos de insuficiência renal, embora possa ser necessário o ajuste da dose.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
A dor articular é um evento adverso potencialmente raro.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
A pancreatite foi relatada em ensaios clínicos, mas a causalidade não foi estabelecida; os medicamentos devem ser descontinuados se houver suspeita de pancreatite. Análises recentes sugeriram que os inibidores de DPP-4 estão associados a um aumento do risco de lesão hepática aguda (em comparação com os inibidores de SGLT2) nos pacientes com diabetes do tipo 2.[229]Pradhan R, Yin H, Yu OHY, et al. Incretin-based drugs and the risk of acute liver injury among patients with type 2 diabetes. Diabetes Care. 2022 Oct 1;45(10):2289-98.
https://diabetesjournals.org/care/article/45/10/2289/147257/Incretin-Based-Drugs-and-the-Risk-of-Acute-Liver
http://www.ncbi.nlm.nih.gov/pubmed/35866685?tool=bestpractice.com
Além disso, o sistema de relatos de eventos adversos da FDA observou que havia sinais consistentes de eventos relacionados à vesícula biliar ou biliares associados aos inibidores de DPP-4 com dados do mundo real, e que os médicos deveriam estar cientes disso na prática clínica.[230]He L, Wang J, Li Z, et al. Dipeptidyl peptidase 4 inhibitors and gallbladder or biliary diseases: data from the U.S. Food and Drug Administration adverse event reporting system. Diabetes Care. 2023 Feb 1;46(2):e72-3.
https://diabetesjournals.org/care/article/46/2/e72/148158/Dipeptidyl-Peptidase-4-Inhibitors-and-Gallbladder
http://www.ncbi.nlm.nih.gov/pubmed/36534433?tool=bestpractice.com
Sulfonilureias
As sulfonilureias são medicamentos orais que estimulam a liberação de insulina pelas células beta pancreáticas. Os exemplos incluem a gliclazida e a glimepirida.
As sulfonilureias têm um elevado efeito redutor da glicose e são objeto de longa experiência clínica.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
Elas podem reduzir as complicações microvasculares, mas não proporcionam redução do risco cardiovascular nem retardam a progressão da doença renal diabética, e podem causar ganho de peso e hipoglicemia.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[163]Tsapas A, Karagiannis T, Kakotrichi P, et al. Comparative efficacy of glucose-lowering medications on body weight and blood pressure in patients with type 2 diabetes: a systematic review and network meta-analysis. Diabetes Obes Metab. 2021 Sep;23(9):2116-24.
https://dom-pubs.pericles-prod.literatumonline.com/doi/10.1111/dom.14451
http://www.ncbi.nlm.nih.gov/pubmed/34047443?tool=bestpractice.com
Desfechos adversos cardiovasculares foram relatados em alguns estudos, embora revisões sistemáticas não tenham encontrado um aumento na mortalidade por todas as causas em comparação com outros tratamentos ativos.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[231]Khunti K, Chatterjee S, Gerstein HC, et al. Do sulphonylureas still have a place in clinical practice? Lancet Diabetes Endocrinol. 2018 Oct;6(10):821-32.
https://www.thelancet.com/journals/landia/article/PIIS2213-8587(18)30025-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/29501322?tool=bestpractice.com
Além disso, um ensaio clínico randomizado e controlado em adultos com diabetes do tipo 2 mostrou segurança cardiovascular comparável da sulfonilureia glimepirida em comparação com o inibidor de DPP-4 linagliptina ao longo de 6.3 anos, e um estudo escocês de segurança comparativa no mundo real concluiu que é improvável que as sulfonilureias de segunda linha aumentem o risco cardiovascular ou a mortalidade por todas as causas.[232]Rosenstock J, Kahn SE, Johansen OE, et al. Effect of linagliptin vs glimepiride on major adverse cardiovascular outcomes in patients with type 2 diabetes: the CAROLINA randomized clinical trial. JAMA. 2019 Sep 24;322(12):1155-66.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6763993
http://www.ncbi.nlm.nih.gov/pubmed/31536101?tool=bestpractice.com
[233]Wang H, Cordiner RLM, Huang Y, et al. Cardiovascular safety in type 2 diabetes with sulfonylureas as second-line drugs: a nationwide population-based comparative safety study. Diabetes Care. 2023 May 1;46(5):967-77.
https://diabetesjournals.org/care/article/46/5/967/148656/Cardiovascular-Safety-in-Type-2-Diabetes-With
http://www.ncbi.nlm.nih.gov/pubmed/36944118?tool=bestpractice.com
Elas devem ser utilizadas com precaução nas pessoas com risco de hipoglicemia.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Pioglitazona
A pioglitazona é um medicamento oral que é um “sensibilizador” da insulina.[162]Cosentino F, Grant PJ, Aboyans V, et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J. 2020 Jan 7;41(2):255-323.
https://www.doi.org/10.1093/eurheartj/ehz486
http://www.ncbi.nlm.nih.gov/pubmed/31497854?tool=bestpractice.com
Ela faz parte de um grupo de medicamentos chamados tiazolidinedionas. Ela tem um alto efeito redutor da glicose e não causa hipoglicemia.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
Ela demonstrou possíveis benefícios cardiovasculares, bem como benefícios potenciais sobre a DHGDM (também conhecida como DHGNA) e a EHDM (também conhecida como EHNA).[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
A ADA recomenda a pioglitazona como agente de escolha para o tratamento da hiperglicemia em pessoas com diabetes do tipo 2 com EHDM confirmada por biópsia ou de alto risco com fibrose hepática clinicamente significativa em testes não invasivos.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
No entanto, ela tem sido associada a retenção de líquidos, insuficiência cardíaca congestiva, ganho de peso e fraturas ósseas.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
[164]Tsapas A, Avgerinos I, Karagiannis T, et al. Comparative effectiveness of glucose-lowering drugs for type 2 diabetes: a systematic review and network meta-analysis. Ann Intern Med. 2020 Aug 18;173(4):278-86.
https://www.acpjournals.org/doi/10.7326/M20-0864?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
http://www.ncbi.nlm.nih.gov/pubmed/32598218?tool=bestpractice.com
A ESC não recomenda o uso de pioglitazona noa pacientes com risco ou história de insuficiência cardíaca devido à sua associação com um aumento do risco de insuficiência cardíaca incidente em pacientes com diabetes.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
O uso da pioglitazona está associado a um pequeno aumento do risco de câncer de bexiga.[234]US Food and Drug Administration. FDA drug safety communication: updated FDA review concludes that use of type 2 diabetes medicine pioglitazone may be linked to an increased risk of bladder cancer. December 2016 [internet publication].
https://www.fda.gov/drugs/drug-safety-and-availability/fda-drug-safety-communication-updated-fda-review-concludes-use-type-2-diabetes-medicine-pioglitazone
Outra tiazolidinediona, a rosiglitazona, foi retirada do mercado devido a preocupações de segurança persistentes.[235]European Medicines Agency. Questions and answers on the suspension of rosiglitazone-containing medicines (Avandia, Avandamet and Avaglim). September 2010 [internet publication].
https://www.ema.europa.eu/en/documents/medicine-qa/questions-answers-suspension-rosiglitazone-containing-medicines-avandia-avandamet-avaglim_en.pdf
Farmacoterapia anti-hiperglicêmica: tratamentos baseados em insulina
Ao iniciar a insulinoterapia, o paciente deve manter a metformina, desde que não haja contraindicações ou intolerâncias.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Revise a continuação da necessidade de outras terapias para redução da glicose sanguínea (por exemplo, considere o risco aditivo de hipoglicemia e se há benefícios adicionais em continuar com outros medicamentos, como cardiometabólicos ou relacionados aos rins).[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Escolha o tipo de insulina mais adequado para o paciente e desenvolva um esquema individualizado, baseado nas seguintes opções:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Administre insulina isofana basal (protamina neutra de Hagedorn, NPH) injetada uma ou duas vezes ao dia, de acordo com a necessidade
Considerar iniciar a insulina NPH e a insulina de ação curta (particularmente se a HbA1c da pessoa for 75 mmol/mol [9.0%] ou superior), administradas:
Considerar o uso de insulina detemir ou insulina glargina como alternativa à insulina NPH se:
O paciente precisar da assistência de um cuidador ou profissional da saúde para injetar a insulina, e o uso de insulina detemir ou insulina glargina reduziria a frequência das injeções de duas para uma vez ao dia ou
O estilo de vida do paciente é restringido por episódios hipoglicêmicos sintomáticos recorrentes ou
Caso contrário, o paciente precisaria de injeções de insulina NPH duas vezes ao dia em combinação com medicamentos redutores orais da glicemia
Considerar preparações pré-misturadas (bifásicas) que incluam análogos de insulina de ação curta, em vez de preparações pré-misturadas (bifásicas) que incluam preparações de insulina humana de ação curta, se:.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
O paciente prefere injetar insulina imediatamente antes das refeições ou
A hipoglicemia é um problema ou
Os níveis glicêmicos aumentam acentuadamente após as refeições.
Considere mudar para insulina detemir ou insulina glargina no lugar de insulina NPH se o paciente:[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Não atingir sua meta de HbA1c devido a hipoglicemia significativa ou
Tiver hipoglicemia significativa com insulina NPH, independentemente do nível de HbA1c alcançado ou
Não for capaz de usar o dispositivo necessário para injetar insulina NPH, mas conseguir administrar sua própria insulina com segurança e precisão se trocada para um dos análogos de insulina de ação prolongada ou
Precisar da ajuda de um cuidador ou profissional de saúde para administrar injeções de insulina e para quem a mudança para um dos análogos de insulina de ação prolongada reduziria o número de injeções diárias.
Se o paciente estiver em regime de insulina basal (insulina NPH, insulina detemir ou insulina glargina), monitore a necessidade de insulina de ação curta antes das refeições (ou uma preparação de insulina pré-misturada [bifásica]).[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
Se o paciente estiver tomando insulina pré-misturada (bifásica), monitore a necessidade de uma nova injeção de insulina de ação curta antes das refeições ou de uma mudança para um esquema de bolus basal com insulina NPH, insulina detemir ou insulina glargina, se o controle da glicemia permanecer inadequado.[36]National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. Jun 2022 [internet publication].
https://www.nice.org.uk/guidance/ng28
A maioria das pessoas com diabetes do tipo 2 usará dispositivos de aplicação de insulina (canetas de insulina).
Estes podem ser ajustados para administrar doses definidas de insulina, estão amplamente disponíveis e oferecem conveniência e precisão na dosagem da insulina.
Com menos frequência, as bombas de insulina e os sistemas de bomba do tipo patch são usados caso a caso em pessoas que precisam de múltiplas doses diárias de insulina.
As bombas de insulina são normalmente reservadas para as pessoas com diabetes do tipo 1. Se uma bomba de insulina for apropriada para o paciente, seu uso exigirá um envolvimento significativo do paciente para obter benefícios clínicos além da terapia baseada em injeção de múltiplas doses diárias.
A insulina exógena é uma forma muito eficaz de reduzir a glicose sérica e a HbA1c, mas seu uso deve ser orientado na maioria dos pacientes por testes regulares de glicose sanguínea automonitorados (teste de glicose sanguínea por punção digital) ou por monitoramento contínuo da glicose.
A hipoglicemia (glicose ≤3.9 mmol/L [≤70 mg/dL]) é a possível complicação mais grave da insulinoterapia. As pessoas que dirigem devem ter um cuidado especial para evitar a hipoglicemia, e devem ser informadas dos perigos. Consulte a seção Complicações deste tópico.
Outro efeito colateral significativo é o ganho de peso.
Efeitos colaterais menos comuns podem incluir fome, náuseas, diaforese, irritação no local da injeção ou anafilaxia.
Doses complementares de insulina
Quando a insulina em esquema basal-bolus é usada por pacientes motivados e bem informados, a dose de insulina de ação rápida administrada antes de cada refeição pode ser baseada no teor de carboidrato previsto para a próxima refeição e, às vezes, ajustada para atividade física prevista.
Uma dose complementar (ou de ajuste) pode ser adicionada à insulina em bolus com base no nível glicêmico pré-prandial. Na prática, uma abordagem conservadora para calcular uma dose complementar é presumir que 1 unidade de insulina reduzirá a glicemia do paciente em 2 a 4 mmol/L (36-72 mg/dL). A dose complementar também pode ser calculada usando-se a dose diária total de insulina do paciente, se a ingestão alimentar estiver estável. A dose complementar pode ser adicionada à prescrição de insulina prandial do paciente (baseada no tamanho geral da refeição ou na contagem de carboidratos) e administrada como a dose total em bolus.
Alternativas para um esquema de insulina basal-bolus
Embora o NICE recomende a consideração de um esquema de insulina em bolus basal para os pacientes que forem incapazes de manter as metas glicêmicas com insulina basal somente, a ADA/EASD também observa uma opção alternativa de adicionar um agonista do receptor de GLP-1 à insulina basal para intensificar o tratamento.[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Além disso, as diretrizes para diabetes de 2024 da ADA incluem que, se a insulina for usada em um adulto com diabetes do tipo 2, é recomendado usá-la em combinação com um agonista do receptor de GLP-1 ou um agonista duplo dos receptores de GIP/GLP-1 para maior eficácia glicêmica (e benefícios adicionais sobre o peso e o risco de hipoglicemia), com a dose de insulina ajustada conforme necessário quando um desses agentes é adicionado ou aumentado.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
Dados de ensaios apoiam a combinação de insulina basal e um agonista do receptor de GLP-1 para reduzir a HbA1c e limitar o ganho de peso e a hipoglicemia quando comparados com um esquema de insulina intensificado.[236]Wysham CH, Lin J, Kuritzky L. Safety and efficacy of a glucagon-like peptide-1 receptor agonist added to basal insulin therapy versus basal insulin with or without a rapid-acting insulin in patients with type 2 diabetes: results of a meta-analysis. Postgrad Med. 2017 May;129(4):436-45.
http://www.ncbi.nlm.nih.gov/pubmed/28294702?tool=bestpractice.com
[237]Maiorino MI, Chiodini P, Bellastella G, et al. Insulin and glucagon-like peptide 1 receptor agonist combination therapy in type 2 diabetes: a systematic review and meta-analysis of randomized controlled trials. Diabetes Care. 2017 Apr;40(4):614-24.
https://care.diabetesjournals.org/content/40/4/614.long
http://www.ncbi.nlm.nih.gov/pubmed/28325801?tool=bestpractice.com
[238]Aroda VR, Arulandu JR, Cannon AJ. Insulin/glucagon-like peptide-1 receptor agonist combination therapy for the treatment of type 2 diabetes: are two agents better than one? Clin Diabetes. 2018 Apr;36(2):138-47.
https://diabetesjournals.org/clinical/article/36/2/138/32834/Insulin-Glucagon-Like-Peptide-1-Receptor-Agonist
http://www.ncbi.nlm.nih.gov/pubmed/29686453?tool=bestpractice.com
Isto poderia ser particularmente útil para os pacientes com obesidade que necessitam de altas doses de insulina devido a resistência insulínica, tornando o efeito colateral do ganho de peso resultante do uso da insulina especialmente problemático.
Evidências mostram que um inibidor de SGLT2 pode ser adicionado à insulina basal para reduzir a glicose sanguínea sem qualquer ganho de peso ou hipoglicemia.[239]Tang H, Cui W, Li D, et al. Sodium-glucose co-transporter 2 inhibitors in addition to insulin therapy for management of type 2 diabetes mellitus: a meta-analysis of randomized controlled trials. Diabetes Obes Metab. 2017 Jan;19(1):142-7.
http://www.ncbi.nlm.nih.gov/pubmed/27598833?tool=bestpractice.com
[240]Rosenstock J, Jelaska A, Zeller C, et al. Impact of empagliflozin added on to basal insulin in type 2 diabetes inadequately controlled on basal insulin: a 78-week randomized, double-blind, placebo-controlled trial. Diabetes Obes Metab. 2015 Oct;17(10):936-48.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5034797
http://www.ncbi.nlm.nih.gov/pubmed/26040302?tool=bestpractice.com
[241]Rosenstock J, Jelaska A, Frappin G, et al. Improved glucose control with weight loss, lower insulin doses, and no increased hypoglycemia with empagliflozin added to titrated multiple daily injections of insulin in obese inadequately controlled type 2 diabetes. Diabetes Care. 2014 Jul;37(7):1815-23.
https://care.diabetesjournals.org/content/37/7/1815.long
http://www.ncbi.nlm.nih.gov/pubmed/24929430?tool=bestpractice.com
Esses esquemas só devem ser iniciados por um especialista em diabetes.
Regras para quando o paciente se sentir mal
Certifique-se de que o paciente esteja ciente de que qualquer doença intercorrente pode fazer com que os níveis de glicose aumentem.[242]Down S. How to advise on sick day rules. Diabetes Primary Care. 2020 Apr;22(3):47-8.
https://diabetesonthenet.com/wp-content/uploads/pdf/dotn024ae8fb1b78500b7bc752b98e9b6d92.pdf
Dê ao paciente orientações orais e por escrito claras e individualizadas ("regras para quando se sentir mal") sobre como adaptar o manejo durante doenças intercorrentes. Alguns medicamentos precisam ser suspensos durante doenças intercorrentes; é importante garantir que o paciente esteja ciente de que precisará reiniciar qualquer medicamento suspenso quando estiver se sentindo melhor e puder comer e beber.
DiabetesontheNet: sick day rules
Opens in new window
O mnemônico SADMANS pode ser útil como um lembrete dos medicamentos a serem pausados temporariamente durante os dias de doença, onde a doença leva à desidratação:[243]Diabetes Canada. Clinical practice guidelines for the prevention and management of diabetes in Canada: appendix 8 - sick-day medication list. 2018 [internet publication].
https://guidelines.diabetes.ca/cpg
S - sulfonilureias
A - inibidores da ECA
D - diuréticos, inibidores diretos da renina
M - metformina
A - antagonistas de receptores de angiotensina II
N - anti-inflamatórios não esteroidais
S - inibidores de SGLT2
Se um adulto com diabetes do tipo 2 não estiver bem, considere a necessidade de providenciar uma internação hospitalar ou procure o conselho de um especialista. Use seu julgamento clínico e leve em consideração a idade, a fragilidade, as comorbidades e o risco de complicações do paciente e a presença de hiperglicemia, hipoglicemia e/ou cetose.
Lembre-se de que existe um risco considerável de hipoglicemia em alguns pacientes. Esta é uma preocupação particular nos pacientes idosos e/ou frágeis, naqueles com apetite reduzido (e subsequente redução da ingestão oral) devido à doença aguda e naqueles que tomam medicamentos que os colocam em risco específico de hipoglicemia (por exemplo, sulfonilureias e insulina). Esses pacientes precisarão de monitoramento rigoroso da glicose sanguínea e podem necessitar de ajustes na medicação.
Cirurgia bariátrica para o tratamento de pacientes com obesidade
As diretrizes da Organização Mundial de Gastroenterologia e da Federação Internacional para a Cirurgia da Obesidade e Doenças Metabólicas sobre obesidade observam que a cirurgia bariátrica é o tratamento de longo prazo mais eficaz para a obesidade e muitas das condições de saúde associadas.[28]World Gastroenterology Organisation and International Federation for the Surgery of Obesity and Metabolic Diseases. IFSO-WGO guidelines on obesity. 2023 [internet publication].
https://www.worldgastroenterology.org/guidelines/obesity/obesity-english
A gastrectomia vertical e o bypass gástrico em Y de Roux são atualmente os procedimentos bariátricos mais realizados em todo o mundo.[28]World Gastroenterology Organisation and International Federation for the Surgery of Obesity and Metabolic Diseases. IFSO-WGO guidelines on obesity. 2023 [internet publication].
https://www.worldgastroenterology.org/guidelines/obesity/obesity-english
Uma avaliação clínica, psicológica e nutricional abrangente envolvendo uma equipe multidisciplinar deve ser concluída antes da cirurgia bariátrica ser considerada, para determinar a adequação do paciente e identificar quaisquer questões que precisem ser abordadas; acompanhamento ao longo da vida, bem como o abandono do hábito de fumar, cessação do uso de álcool e de substâncias também são necessários.[28]World Gastroenterology Organisation and International Federation for the Surgery of Obesity and Metabolic Diseases. IFSO-WGO guidelines on obesity. 2023 [internet publication].
https://www.worldgastroenterology.org/guidelines/obesity/obesity-english
As diretrizes do NICE recomendam:[117]National Institute for Health and Care Excellence. Obesity: identification, assessment and management. July 2023 [internet publication].
https://www.nice.org.uk/guidance/cg189
Oferecer uma avaliação rápida para cirurgia bariátrica a qualquer pessoa com IMC igual ou superior a 35 kg/m² que tenha diabetes do tipo 2 de início recente (diagnóstico nos últimos 10 anos), desde que também esteja recebendo, ou em vias de receber, avaliação por uma equipe especializada em controle do peso.
Considerar uma avaliação rápida para cirurgia bariátrica para qualquer pessoa com IMC de 30 a 34.9 kg/m² que tenha diabetes do tipo 2 de início recente, desde que também esteja recebendo, ou receba, avaliação por uma equipe especializada em controle do peso.
Considerar uma avaliação rápida para cirurgia bariátrica para qualquer pessoa de origem familiar do sul da Ásia, China e outros países asiáticos, do Oriente Médio, negros africanos ou afro-caribenhos, que tenha diabetes do tipo 2 de início recente usando um limiar de IMC mais baixo (reduzido em 2.5 kg/ m²) do que outras populações.
A diretriz de consenso de 2022 da ADA/EASD recomenda que a cirurgia bariátrica seja considerada como uma opção para adultos com diabetes do tipo 2 que forem candidatos cirúrgicos apropriados e que tiverem:[102]Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-86.
https://diabetesjournals.org/care/article/45/11/2753/147671/Management-of-Hyperglycemia-in-Type-2-Diabetes
http://www.ncbi.nlm.nih.gov/pubmed/36148880?tool=bestpractice.com
Um IMC ≥40.0 kg/m² se de ascendência não asiática
Um IMC ≥37.5 kg/m² se de ascendência asiática
Um IMC de 35.0 a 39.9 kg/m² (32.5 a 37.4 kg/m² se for de ascendência asiática) e que não conseguirem obter perda de peso duradoura e melhora das comorbilidades (incluindo a hiperglicemia) com métodos não cirúrgicos.
Além disso, a ESC recomenda que a cirurgia bariátrica seja considerada para os pacientes com risco alto ou muito alto de DCV com IMC ≥35 kg/m² quando esforços repetitivos e estruturados de mudanças no estilo de vida combinados com medicamentos para redução do peso não resultarem em uma perda de peso sustentada.[80]Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-140.
https://academic.oup.com/eurheartj/article/44/39/4043/7238227?login=false
http://www.ncbi.nlm.nih.gov/pubmed/37622663?tool=bestpractice.com
Ensaios clínicos randomizados demonstraram um benefício da cirurgia bariátrica (também conhecida como cirurgia metabólica) em comparação com a terapia medicamentosa isolada em relação a remissão do diabetes, controle glicêmico, necessidade de medicamentos para redução da glicose, qualidade de vida e redução dos marcadores de fator de risco cardiovascular em curto prazo (por exemplo, 1-3 anos) em pessoas com diabetes do tipo 2, bem como para possível prevenção do diabetes do tipo 2.[28]World Gastroenterology Organisation and International Federation for the Surgery of Obesity and Metabolic Diseases. IFSO-WGO guidelines on obesity. 2023 [internet publication].
https://www.worldgastroenterology.org/guidelines/obesity/obesity-english
[244]Carlsson LM, Peltonen M, Ahlin S, et al. Bariatric surgery and prevention of type 2 diabetes in Swedish obese subjects. N Engl J Med. 2012 Aug 23;367(8):695-704.
https://www.nejm.org/doi/10.1056/NEJMoa1112082?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%3dwww.ncbi.nlm.nih.gov
http://www.ncbi.nlm.nih.gov/pubmed/22913680?tool=bestpractice.com
[245]Schauer PR, Kashyap SR, Wolski K, et al. Bariatric surgery versus intensive medical therapy in obese patients with diabetes. N Engl J Med. 2012 Apr 26;366(17):1567-76.
https://www.nejm.org/doi/10.1056/NEJMoa1200225?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%3dwww.ncbi.nlm.nih.gov
http://www.ncbi.nlm.nih.gov/pubmed/22449319?tool=bestpractice.com
[246]Schauer PR, Bhatt DL, Kirwan JP, et al; STAMPEDE Investigators. Bariatric surgery versus intensive medical therapy for diabetes - 5-year outcomes. N Engl J Med. 2017 Feb 16;376(7):641-51.
https://www.nejm.org/doi/10.1056/NEJMoa1600869
http://www.ncbi.nlm.nih.gov/pubmed/28199805?tool=bestpractice.com
[247]Kashyap SR, Bhatt DL, Wolski K, et al. Metabolic effects of bariatric surgery in patients with moderate obesity and type 2 diabetes: analysis of a randomized control trial comparing surgery with intensive medical treatment. Diabetes Care. 2013 Aug;36(8):2175-82.
http://care.diabetesjournals.org/content/36/8/2175.long
http://www.ncbi.nlm.nih.gov/pubmed/23439632?tool=bestpractice.com
[248]Ikramuddin S, Korner J, Lee WJ, et al. Roux-en-Y gastric bypass vs intensive medical management for the control of type 2 diabetes, hypertension, and hyperlipidemia: the Diabetes Surgery Study randomized clinical trial. JAMA. 2013 Jun 5;309(21):2240-9.
http://jamanetwork.com/journals/jama/fullarticle/1693889
http://www.ncbi.nlm.nih.gov/pubmed/23736733?tool=bestpractice.com
[249]Halperin F, Ding SA, Simonson DC, et al. Roux-en-Y gastric bypass surgery or lifestyle with intensive medical management in patients with type 2 diabetes: feasibility and 1-year results of a randomized clinical trial. JAMA Surg. 2014 Jul;149(7):716-26.
http://jamanetwork.com/journals/jamasurgery/fullarticle/1876617
http://www.ncbi.nlm.nih.gov/pubmed/24899464?tool=bestpractice.com
Estudos de coorte sugerem que tanto o bypass em Y de Roux como a gastrectomia vertical levam à remissão do diabetes por 5 anos, em média, em mais da metade dos pacientes, e reduzem consideravelmente a mortalidade, AVC, infarto do miocárdio e complicações microvasculares em indivíduos com diabetes do tipo 2.[250]Yska JP, van Roon EN, de Boer A, et al. Remission of type 2 diabetes mellitus in patients after different types of bariatric surgery: a population-based cohort study in the United Kingdom. JAMA Surg. 2015 Dec;150(12):1126-33.
https://jamanetwork.com/journals/jamasurgery/fullarticle/2446843
http://www.ncbi.nlm.nih.gov/pubmed/26422580?tool=bestpractice.com
[251]Fisher DP, Johnson E, Haneuse S, et al. Association between bariatric surgery and macrovascular disease outcomes in patients with type 2 diabetes and severe obesity. JAMA. 2018 Oct 16;320(15):1570-82.
https://jamanetwork.com/journals/jama/fullarticle/2707461
http://www.ncbi.nlm.nih.gov/pubmed/30326126?tool=bestpractice.com
[252]O'Brien R, Johnson E, Haneuse S, et al. Microvascular outcomes in patients with diabetes after bariatric surgery versus usual care: a matched cohort study. Ann Intern Med. 2018 Sep 4;169(5):300-10.
http://www.ncbi.nlm.nih.gov/pubmed/30083761?tool=bestpractice.com
Uma revisão sistemática e metanálise de ensaios clínicos randomizados e controlados concluiu que o bypass em Y de Roux resultou em uma taxa mais alta de remissão do diabetes do tipo 2 em comparação com a gastrectomia vertical após 1 ano, mas que as taxas de remissão não diferiram nos estudos com um acompanhamento de 2 e 5 anos.[253]Borgeraas H, Hofsø D, Hertel JK, et al. Comparison of the effect of Roux-en-Y gastric bypass and sleeve gastrectomy on remission of type 2 diabetes: a systematic review and meta-analysis of randomized controlled trials. Obes Rev. 2020 Jun;21(6):e13011.
https://onlinelibrary.wiley.com/doi/10.1111/obr.13011
http://www.ncbi.nlm.nih.gov/pubmed/32162437?tool=bestpractice.com
Comparado à gastrectomia vertical, o bypass em Y de Roux leva à maior perda de peso e outros benefícios, mas é uma operação mais desafiadora do ponto de vista técnico, com taxas mais altas de nova operação e reinternação.
Os benefícios e os riscos da cirurgia bariátrica também variam substancialmente entre os subgrupos de pacientes com diabetes do tipo 2. Em estudos observacionais, os benefícios médios parecem ser maiores nas pessoas com início mais recente de diabetes do tipo 2 e naquelas que não estão em insulinoterapia.[254]O'Keefe KL, Kemmeter PR, Kemmeter KD. Bariatric surgery outcomes in patients aged 65 years and older at an American Society for Metabolic and Bariatric Surgery Center of Excellence. Obes Surg. 2010 Sep;20(9):1199-205.
http://www.ncbi.nlm.nih.gov/pubmed/20532834?tool=bestpractice.com
[255]Park JY. Prediction of type 2 diabetes remission after bariatric or metabolic surgery. J Obes Metab Syndr. 2018 Dec 30;27(4):213-22.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6513303
http://www.ncbi.nlm.nih.gov/pubmed/31089566?tool=bestpractice.com
Benefícios foram documentados para pessoas mais jovens (idade 40-50 anos), bem como para aqueles com mais de 65 anos de idade.[254]O'Keefe KL, Kemmeter PR, Kemmeter KD. Bariatric surgery outcomes in patients aged 65 years and older at an American Society for Metabolic and Bariatric Surgery Center of Excellence. Obes Surg. 2010 Sep;20(9):1199-205.
http://www.ncbi.nlm.nih.gov/pubmed/20532834?tool=bestpractice.com
[255]Park JY. Prediction of type 2 diabetes remission after bariatric or metabolic surgery. J Obes Metab Syndr. 2018 Dec 30;27(4):213-22.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6513303
http://www.ncbi.nlm.nih.gov/pubmed/31089566?tool=bestpractice.com
Os procedimentos de cirurgia bariátrica, em particular o bypass gástrico em Y de Roux, têm sido associados a complicações subsequentes relacionadas ao álcool.[28]World Gastroenterology Organisation and International Federation for the Surgery of Obesity and Metabolic Diseases. IFSO-WGO guidelines on obesity. 2023 [internet publication].
https://www.worldgastroenterology.org/guidelines/obesity/obesity-english
[256]Mahmud N, Panchal S, Abu-Gazala S, et al. Association between bariatric surgery and alcohol use-related hospitalization and all-cause mortality in a veterans affairs cohort. JAMA Surg. 2023 Feb 1;158(2):162-71.
https://pubmed.ncbi.nlm.nih.gov/36515960
http://www.ncbi.nlm.nih.gov/pubmed/36515960?tool=bestpractice.com
É importante ter isto em conta ao selecionar os pacientes para estes procedimentos e considerar aconselhamento com relação ao álcool.[256]Mahmud N, Panchal S, Abu-Gazala S, et al. Association between bariatric surgery and alcohol use-related hospitalization and all-cause mortality in a veterans affairs cohort. JAMA Surg. 2023 Feb 1;158(2):162-71.
https://pubmed.ncbi.nlm.nih.gov/36515960
http://www.ncbi.nlm.nih.gov/pubmed/36515960?tool=bestpractice.com
Planejamento da gravidez
As mulheres com diabetes do tipo 2 devem usar um método eficaz de contracepção até o momento em que planejem engravidar.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
As mulheres devem ser avaliadas antes da gestação quanto a retinopatia, nefropatia, neuropatia e possível doença cardiovascular, que podem agravar ou complicar-se durante a gestação.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Explique às mulheres com diabetes que estiverem planejando engravidar que:[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Se elas tiverem um bom controle da glicose sanguínea antes da concepção e durante a gravidez, isso reduzirá os riscos de aborto espontâneo, malformação congênita, natimorto e morte neonatal
Os riscos podem ser reduzidos, mas não eliminados.
Entre em acordo em relação a metas individualizadas para o automonitoramento da glicose sanguínea com as mulheres que tiverem diabetes e estiverem planejando uma gestação, levando em consideração o risco de hipoglicemia.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
O NICE recomenda que a HbA1c seja <48 mmol/mol (6.5%) antes da concepção, se esse nível puder ser alcançado sem hipoglicemia problemática.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Qualquer redução em direção a essa meta provavelmente reduzirá o risco de malformações congênitas. O NICE recomenda a medição mensal dos níveis de HbA1c para mulheres com diabetes que planejam engravidar.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Aconselhe fortemente as mulheres com diabetes cujo nível de HbA1c estiver acima de 86 mmol/mol (10%) a não engravidarem até que o nível de HbA1c esteja mais baixo, devido aos riscos associados.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Revise os medicamentos da paciente. Interrompa qualquer medicamento contraindicado na gravidez se a paciente estiver planejando engravidar, ou assim que a gravidez for confirmada; use agentes alternativos adequados para gestantes.
As mulheres com diabetes podem ser aconselhadas a usar metformina (com ou sem insulina) no período pré-concepção (e durante a gravidez), quando os prováveis benefícios de um melhor controle da glicose sanguínea superarem o potencial de danos. Interrompa todos os outros agentes redutores orais da glicemia antes (e durante) a gravidez, incluindo os inibidores de SGLT2.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
[136]Herrington WG, Frankel AH. UK Kidney Association clinical practice guideline: sodium-glucose co-transporter-2 (SGLT-2) inhibition in adults with kidney disease. Apr 2023 [internet publication].
https://guidelines.ukkidney.org
Interrompa o uso de inibidores da ECA e os antagonistas do receptor de angiotensina II antes da concepção ou assim que a gravidez for confirmada.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Interrompa o uso de estatinas antes da gravidez ou assim que a gravidez for confirmada.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Aconselhe as mulheres que planejarem engravidar a tomarem ácido fólico (5 mg/dia), que deve ser mantido até as 12 semanas de gestação.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Mulheres com diabetes apresentam aumento de risco de gerar bebês com defeitos do tubo neural em comparação com a população geral.[257]Tinker SC, Gilboa SM, Moore CA, et al. Specific birth defects in pregnancies of women with diabetes: National Birth Defects Prevention Study, 1997-2011. Am J Obstet Gynecol. 2020 Feb;222(2):176.e1-11.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7186569
http://www.ncbi.nlm.nih.gov/pubmed/31454511?tool=bestpractice.com
Durante a gestação
Durante a gestação, as mulheres devem ser cuidadas por uma equipe multidisciplinar que inclua um nutricionista, um técnico de enfermagem, um endocrinologista e um obstetra.
Ofereça às gestantes com diabetes preexistente uma avaliação da retina por exame de imagem digital com midríase usando tropicamida após a primeira consulta clínica pré-natal (a menos que elas tenham feito uma avaliação da retina nos 3 meses anteriores) e, novamente, a 28 semanas. Se houver presença de alguma retinopatia diabética no momento em que a consulta é marcada, realize uma avaliação adicional da retina entre 16 e 20 semanas.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
As diretrizes do NICE recomendam os seguintes valores-alvo glicêmicos em gestantes com diabetes do tipo 2 preexistente (desde que estes sejam alcançáveis sem causar hipoglicemia problemática):[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
[Evidência C]4efe3e6f-336e-471b-b4bd-bb6de160be6aguidelineCQuais são os efeitos do controle mais rígido da glicose sanguínea comparado a um controle menos rígido em gestantes com diabetes gestacional?[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Em jejum: <5.3 mmol/L (<95.4 mg/dL), e
1 hora após as refeições: <7.8 mmol/L (<140.4 mg/dL), ou
2 horas após as refeições: 6.4 mmol/L (<115.2 mg/dL).
Aconselhe as gestantes com diabetes que façam uso de insulina a manter o nível de glicose plasmática capilar acima de 4 mmol/L (72 mg/dL).[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Meça os níveis de HbA1c em todas as gestantes com diabetes preexistente na primeira consulta pré-natal para determinar o nível de risco da gestação. Considere medir os níveis de HbA1c no segundo e terceiro trimestres da gestação de mulheres com diabetes preexistente para avaliar o nível de risco da gestação.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Revise os medicamentos da paciente. Suspenda quaisquer agentes contraindicados na gestação assim que a gravidez for confirmada e utilize alternativas que sejam adequadas para gestantes, conforme descrito na seção “Planejamento da gestação” acima.
As mulheres que estiverem amamentando podem retomar ou manter a metformina imediatamente após o nascimento, mas devem evitar outras terapias orais para redução da glicose sanguínea durante a amamentação.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
As mulheres diabéticas em aleitamento materno devem continuar evitando qualquer medicamento para complicações do diabetes que tiver sido interrompido por questões de segurança quando começaram a planejar a gravidez.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
O NICE recomenda a insulina NPH como a primeira escolha para a insulina de ação prolongada durante a gravidez.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Considere continuar o tratamento com análogos de insulina de ação prolongada (insulina detemir ou insulina glargina) para mulheres com diabetes que estabeleceram um bom controle da glicose sanguínea enquanto usavam esses análogos antes da gravidez.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
A evidência disponível sobre análogos de insulina de ação rápida (insulina aspart e insulina lispro) não mostra um efeito adverso na gravidez ou na saúde do bebê.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
Na prática, a maioria das gestantes com diabetes do tipo 2 precisará de insulina.
Gestantes devem testar, todos os dias, os níveis de glicose sanguínea em jejum, antes da refeição, 1 hora após a refeição e ao deitar-se.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
O padrão deve ser examinado a cada poucas semanas no início da gestação para que o conteúdo nutricional e o tempo, os padrões de exercício e as doses de insulina possam ser modificados para atingir o controle ideal. O monitoramento por SMCG durante a gestação pode ser considerado individualmente (além do automonitoramento) para aquelas que tomam insulina e estão passando por hipoglicemia grave problemática ou que têm níveis instáveis de glicose no sangue que causam preocupação, apesar dos esforços para otimizar o controle.[34]American Diabetes Association. Standards of care in diabetes - 2024. Diabetes Care. 2024 Jan;47(suppl 1):S1-321.
https://diabetesjournals.org/care/issue/47/Supplement_1
[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
As necessidades de insulina geralmente aumentam no início da gestação, diminuindo a partir de aproximadamente 8 a 16 semanas antes de aumentarem durante o tempo de gestação restante.
Aconselhe gestantes com diabetes do tipo 2 a tomar aspirina em baixas doses desde as 12 semanas de gestação até o nascimento do bebê.[99]National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. Dec 2020 [internet publication].
https://www.nice.org.uk/guidance/ng3
[258]National Institute for Health and Care Excellence. Hypertension in pregnancy: diagnosis and management. April 2023 [internet publication].
https://www.nice.org.uk/guidance/ng133

