Aneurisma aórtico abdominal
- Descripción general
- Teoría
- Diagnóstico
- Manejo
- Seguimiento
- Recursos
Algoritmo de tratamiento
Tenga en cuenta que las formulaciones/vías y dosis pueden diferir entre los nombres y marcas de los fármacos, las fórmulas de los fármacos o las localizaciones. Las recomendaciones de tratamiento son específicas para cada grupo de pacientes: ver aviso legal
rotura de AAA
medidas estándar de reanimación
Deben iniciarse inmediatamente las medidas de reanimación estándar. Entre ellas se incluyen: el manejo de las vías respiratorias (oxigenoterapia o intubación endotraqueal y ventilación asistida si el paciente está inconsciente); asegurar el acceso intravenoso (catéter venoso central); catéter arterial y catéter urinario; asegurar la disponibilidad de hemoderivados (concentrado de eritrocitos, plaquetas y plasma fresco congelado) y transfusión para reanimación, anemia grave y coagulopatía; y notificar a los equipos de anestesia, unidad de cuidados intensivos (UCI) y quirófano.
la rehidratación agresiva puede causar coagulopatía por dilución y por hipotermia y puede provocar la destrucción de coágulos secundaria debido al aumento del flujo sanguíneo, el aumento de la presión de perfusión y la reducción de la viscosidad de la sangre que produce la exacerbación del sangrado.[121]Roberts K, Revell M, Youssef H, et al. Hypotensive resuscitation in patients with ruptured abdominal aortic aneurysm. Eur J Vasc Endovasc Surg. 2006 Apr;31(4):339-44. http://www.ncbi.nlm.nih.gov/pubmed/16388972?tool=bestpractice.com [122]Ohki T, Veith FJ. Endovascular grafts and other image-guided catheter-based adjuncts to improve the treatment of ruptured aortoiliac aneurysms. Ann Surg. 2000 Oct;232(4):466-79. http://www.ncbi.nlm.nih.gov/pubmed/10998645?tool=bestpractice.com En el preoperatorio se recomienda una presión arterial sistólica (PAS) de 50-70 mmHg y la retención de líquidos.[121]Roberts K, Revell M, Youssef H, et al. Hypotensive resuscitation in patients with ruptured abdominal aortic aneurysm. Eur J Vasc Endovasc Surg. 2006 Apr;31(4):339-44. http://www.ncbi.nlm.nih.gov/pubmed/16388972?tool=bestpractice.com [122]Ohki T, Veith FJ. Endovascular grafts and other image-guided catheter-based adjuncts to improve the treatment of ruptured aortoiliac aneurysms. Ann Surg. 2000 Oct;232(4):466-79. http://www.ncbi.nlm.nih.gov/pubmed/10998645?tool=bestpractice.com Las guías de práctica clínica del American College of Cardiology/American Heart Association (ACC/AHA) recomiendan la hipotensión permisiva para reducir el sangrado.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com Sin embargo, los objetivos recomendados varían y no existe consenso entre los grupos de guías de práctica clínica mundiales.
Cómo insertar un tubo traqueal en una persona adulta, utilizando un laringoscopio.
Cómo utilizar el aparato bolsa-válvula-mascarilla para proporcionar asistencia ventilatoria en adultos. Vídeo de demostración de la técnica para dos personas.
reparación quirúrgica urgente
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
El American College of Cardiology/American Heart Association (ACC/AHA) recomienda realizar una tomografía computarizada (TC) a los pacientes que presenten un AAA roto y se encuentren hemodinámicamente estables para evaluar si el AAA es susceptible de reparación endovascular.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com Esta recomendación está respaldada por los resultados del ensayo controlado aleatorizado multicéntrico IMPROVE, que sugieren que, para la mayoría de los pacientes, la TC confirmatoria no añadió retrasos significativos al tratamiento y facilitó una planificación preoperatoria adecuada.[110]Powell JT, Hinchcliffe RJ, Thompson MM, et al; IMPROVE Trial Investigators. Observations from the IMPROVE trial concerning the clinical care of patients with ruptured abdominal aortic aneurysm. Br J Surg. 2014 Feb;101(3):216-24. https://bjssjournals.onlinelibrary.wiley.com/doi/full/10.1002/bjs.9410 http://www.ncbi.nlm.nih.gov/pubmed/24469620?tool=bestpractice.com
Si la anatomía es adecuada, el ACC/AHA recomienda la reparación endovascular frente a la reparación abierta para reducir el riesgo de morbilidad y mortalidad.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com En pacientes con rotura de AAA confirmada, la mortalidad a 3 años fue menor entre aquellos asignados al azar a reparación endovascular de aneurisma (EVAR) que a una estrategia de reparación abierta (48% frente a 56%; cociente de riesgo [HR] 0.57, IC 95%: 0.36 a 0.90).[111]IMPROVE Trial Investigators. Comparative clinical effectiveness and cost effectiveness of endovascular strategy v open repair for ruptured abdominal aortic aneurysm: three year results of the IMPROVE randomised trial. BMJ. 2017 Nov 14;359:j4859. https://www.bmj.com/content/359/bmj.j4859.long http://www.ncbi.nlm.nih.gov/pubmed/29138135?tool=bestpractice.com La diferencia entre grupos de tratamiento no fue evidente después de 7 años de seguimiento (HR 0.92, IC 95%: 0.75 a 1.13). Las tasas de reintervención no fueron significativamente diferentes entre los grupos aleatorizados a los 3 años (HR 1.02, IC 95%: 0.79 a 1.32).[111]IMPROVE Trial Investigators. Comparative clinical effectiveness and cost effectiveness of endovascular strategy v open repair for ruptured abdominal aortic aneurysm: three year results of the IMPROVE randomised trial. BMJ. 2017 Nov 14;359:j4859. https://www.bmj.com/content/359/bmj.j4859.long http://www.ncbi.nlm.nih.gov/pubmed/29138135?tool=bestpractice.com Hay algunas pruebas que sugieren que una estrategia endovascular para la reparación de la ruptura de AAA puede reducir la mortalidad con mayor efectividad en mujeres que en hombres.[111]IMPROVE Trial Investigators. Comparative clinical effectiveness and cost effectiveness of endovascular strategy v open repair for ruptured abdominal aortic aneurysm: three year results of the IMPROVE randomised trial. BMJ. 2017 Nov 14;359:j4859. https://www.bmj.com/content/359/bmj.j4859.long http://www.ncbi.nlm.nih.gov/pubmed/29138135?tool=bestpractice.com [112]Sweeting MJ, Balm R, Desgranges P, et al; Ruptured Aneurysm Trialists. Individual-patient meta-analysis of three randomized trials comparing endovascular versus open repair for ruptured abdominal aortic aneurysm. Br J Surg. 2015 Sep;102(10):1229-39. https://bjssjournals.onlinelibrary.wiley.com/doi/full/10.1002/bjs.9852 http://www.ncbi.nlm.nih.gov/pubmed/26104471?tool=bestpractice.com
Hay algunas evidencias que sugieren que el modo de anestesia para la reparación quirúrgica del AAA afecta a los resultados.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [113]Armstrong RA, Squire YG, Rogers CA, et al. Type of anesthesia for endovascular abdominal aortic aneurysm repair. J Cardiothorac Vasc Anesth. 2019 Feb;33(2):462-71. http://www.ncbi.nlm.nih.gov/pubmed/30342821?tool=bestpractice.com En 2024, la Sociedad Europea de Cirugía Vascular (ESVS) emitió una recomendación débil que favorecía la anestesia local sobre la anestesia general en entornos electivos, basándose en la posible reducción del tiempo del procedimiento, los ingresos en la UCI y la estancia hospitalaria postoperatoria.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [114]Liu Y, Wang T, Zhao J, et al. Influence of anesthetic techniques on perioperative outcomes after endovascular aneurysm repair. Ann Vasc Surg. 2021 May;73:375-84. http://www.ncbi.nlm.nih.gov/pubmed/33383135?tool=bestpractice.com [115]Zottola ZR, Kruger JL, Kong DS, et al. Locoregional anesthesia is associated with reduced hospital stay and need for intensive care unit care of elective endovascular aneurysm repair patients in the Vascular Quality Initiative. J Vasc Surg. 2023 Apr;77(4):1061-9. https://www.jvascsurg.org/article/S0741-5214(22)02534-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/36400363?tool=bestpractice.com [116]Kothandan H, Haw Chieh GL, Khan SA, et al. Anesthetic considerations for endovascular abdominal aortic aneurysm repair. Ann Card Anaesth. 2016 Jan-Mar;19(1):132-41. https://pmc.ncbi.nlm.nih.gov/articles/PMC4900395 http://www.ncbi.nlm.nih.gov/pubmed/26750684?tool=bestpractice.com El ensayo controlado aleatorizado multicéntrico IMPROVE detectó una reducción significativa de la mortalidad a los 30 días en los pacientes sometidos a EVAR con anestesia local sola en comparación con anestesia general (OR ajustada 0.27; 0.1 a 0.7).[110]Powell JT, Hinchcliffe RJ, Thompson MM, et al; IMPROVE Trial Investigators. Observations from the IMPROVE trial concerning the clinical care of patients with ruptured abdominal aortic aneurysm. Br J Surg. 2014 Feb;101(3):216-24. https://bjssjournals.onlinelibrary.wiley.com/doi/full/10.1002/bjs.9410 http://www.ncbi.nlm.nih.gov/pubmed/24469620?tool=bestpractice.com Un metanálisis independiente en el que se comparó el modo de anestesia para la reparación endovascular de la rotura del AAA replicó estos hallazgos o mejoró los resultados con la EVAR bajo anestesia local.[117]Harky A, Ahmad MU, Santoro G, et al. Local versus general anesthesia in nonemergency endovascular abdominal aortic aneurysm repair: a systematic review and meta-analysis. J Cardiothorac Vasc Anesth. 2020 Apr;34(4):1051-9. http://www.ncbi.nlm.nih.gov/pubmed/31473112?tool=bestpractice.com Sin embargo, otra revisión sistemática no mostró ningún beneficio en cuanto a mortalidad con la anestesia local, pero sí demostró estancias hospitalarias más cortas.[118]Deng J, Liu J, Rong D, et al. A meta-analysis of locoregional anesthesia versus general anesthesia in endovascular repair of ruptured abdominal aortic aneurysm. J Vasc Surg. 2021 Feb;73(2):700-10. https://www.doi.org/10.1016/j.jvs.2020.08.112 http://www.ncbi.nlm.nih.gov/pubmed/32882348?tool=bestpractice.com Los datos del Registro Vascular Nacional del Reino Unido (9783 pacientes que recibieron un EVAR infrarrenal estándar electivo; anestesia general, n = 7069; anestesia regional, n = 2347; anestesia local, n = 367) mostraron una tasa de mortalidad más baja a los 30 días después de la anestesia regional en comparación con la general.[119]Dovell G, Rogers CA, Armstrong R, et al. The effect of mode of anaesthesia on outcomes after elective endovascular repair of abdominal aortic aneurysm. Eur J Vasc Endovasc Surg. 2020 May;59(5):729-38. https://www.ejves.com/article/S1078-5884(20)30118-0/fulltext http://www.ncbi.nlm.nih.gov/pubmed/32291124?tool=bestpractice.com El estudio multicéntrico internacional Endurant Stent Graft Natural Selection Global Post-Market Registry (ENGAGE) examinó los resultados de 1231 pacientes sometidos a EVAR bajo anestesia general (62% de los pacientes), regional (27%) y local (11%).[120]Broos PP, Stokmans RA, Cuypers PW, et al. Effects of anesthesia type on perioperative outcome after endovascular aneurysm repair. J Endovasc Ther. 2015 Oct;22(5):770-7. http://www.ncbi.nlm.nih.gov/pubmed/26276553?tool=bestpractice.com El tipo de anestesia no influyó en la mortalidad o morbilidad perioperatoria, pero el uso de anestesia local o regional durante la EVAR pareció ser beneficioso en la disminución del tiempo del procedimiento, la necesidad de ingreso en la UCI y la duración de la estancia hospitalaria postoperatoria.[120]Broos PP, Stokmans RA, Cuypers PW, et al. Effects of anesthesia type on perioperative outcome after endovascular aneurysm repair. J Endovasc Ther. 2015 Oct;22(5):770-7. http://www.ncbi.nlm.nih.gov/pubmed/26276553?tool=bestpractice.com
antibioticoterapia perioperatoria
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
Se indica la antibioticoterapia para los pacientes que se someten a una reparación urgente por rotura de AAA para cubrir microorganismos gramnegativos y grampositivos y prevenir infecciones del injerto.
La cobertura con antibióticos de amplio espectro se adapta a la presentación clínica y a los cultivos de cada paciente conforme a los protocolos locales.
tratamiento de causa infecciosa/inflamatoria
Tratamiento adicional recomendado para ALGUNOS pacientes del grupo seleccionado
Una vez que el paciente está estable y se ha priorizado la reparación quirúrgica urgente de la rotura, debe abordarse la etiología infecciosa o inflamatoria.
Si se sospecha que el paciente tiene un aneurisma infeccioso, el diagnóstico precoz y el tratamiento rápido son esenciales para mejorar los resultados.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com A menudo es necesario un desbridamiento extenso durante la reparación quirúrgica urgente en estos pacientes. Existe un alto riesgo de complicaciones infecciosas secundarias y puede que sea necesaria una nueva intervención quirúrgica para nuevas lesiones infecciosas.Deben realizarse cultivos intraoperatorios para orientar con precisión el tratamiento antibiótico posterior; sin embargo, a menudo se administran antibióticos empíricos, ya que los cultivos de sangre periférica y de muestras quirúrgicas son negativos en una gran proporción de pacientes.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com Puede estar indicada una antibioticoterapia prolongada (de 4 a 6 semanas de duración a toda la vida) en función del patógeno específico, el tipo de reparación quirúrgica y el estado inmunológico del paciente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
La aortitis inflamatoria (causada, por ejemplo, por la arteritis de Takayasu o la arteritis de células gigantes) se trata con dosis altas de corticosteroides y cirugía.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [205]Ben Jmaà H, Karray R, Jmal H, et al. Surgical and endoluminal management of the inflammatory aortitis: a Tunisian center experience [in French]. J Med Vasc. 2017 Jul;42(4):213-20. http://www.ncbi.nlm.nih.gov/pubmed/28705339?tool=bestpractice.com
aneurisma de aorta abdominal sintomático pero sin rotura
reparación quirúrgica urgente
En pacientes con aneurisma aórtico sintomático, la reparación urgente está indicada independientemente del diámetro.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [78]National Institute for Health and Care Excellence. Abdominal aortic aneurysm: diagnosis and management. Mar 2020 [internet publication]. https://www.nice.org.uk/guidance/ng156 [127]Mazzolai L, Teixido-Tura G, Lanzi S, et al; ESC Committee for Practice Guidelines. 2024 ESC guidelines for the management of peripheral arterial and aortic diseases. Eur Heart J. 2024 Sep 29;45(36):3538-700. https://academic.oup.com/eurheartj/article/45/36/3538/7738955 El desarrollo de dolor nuevo o el empeoramiento del dolor existente puede indicar la expansión del aneurisma o una rotura inminente. Por lo tanto, es mejor tratar el aneurisma sintomático no roto con urgencia.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com En algunas circunstancias, la intervención puede retrasarse varias horas para optimizar las condiciones y garantizar el éxito de la reparación; se debe controlar a estos pacientes estrictamente en la UCI.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com
La reparación endovascular (EVAR) se utiliza cada vez más en el manejo de pacientes con AAA sintomático.[128]De Martino RR, Nolan BW, Goodney PP, Chang CK, et al; Vascular Study Group of Northern New England. Outcomes of symptomatic abdominal aortic aneurysm repair. J Vasc Surg. 2010 Jul;52(1):5-12.e1. https://www.jvascsurg.org/article/S0741-5214(10)00259-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/20471771?tool=bestpractice.com [129]Chandra V, Trang K, Virgin-Downey W, et al. Management and outcomes of symptomatic abdominal aortic aneurysms during the past 20 years. J Vasc Surg. 2017 Dec;66(6):1679-85. http://www.ncbi.nlm.nih.gov/pubmed/28619644?tool=bestpractice.com En los estudios observacionales, las tasas de mortalidad por todas las causas a corto plazo no difirieron entre la reparación endovascular y la reparación abierta del AAA sintomático.[128]De Martino RR, Nolan BW, Goodney PP, Chang CK, et al; Vascular Study Group of Northern New England. Outcomes of symptomatic abdominal aortic aneurysm repair. J Vasc Surg. 2010 Jul;52(1):5-12.e1. https://www.jvascsurg.org/article/S0741-5214(10)00259-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/20471771?tool=bestpractice.com [129]Chandra V, Trang K, Virgin-Downey W, et al. Management and outcomes of symptomatic abdominal aortic aneurysms during the past 20 years. J Vasc Surg. 2017 Dec;66(6):1679-85. http://www.ncbi.nlm.nih.gov/pubmed/28619644?tool=bestpractice.com [130]Ten Bosch JA, Willigendael EM, Kruidenier LM, et al. Early and mid-term results of a prospective observational study comparing emergency endovascular aneurysm repair with open surgery in both ruptured and unruptured acute abdominal aortic aneurysms. Vascular. 2012 Apr;20(2):72-80. http://www.ncbi.nlm.nih.gov/pubmed/22454547?tool=bestpractice.com
reducción del riesgo cardiovascular preoperatorio
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
El tratamiento preoperatorio de los factores de riesgo cardiovascular modificables mejora la supervivencia a largo plazo después de la reparación del AAA.[196]Khashram M, Williman JA, Hider PN, et al. Management of modifiable vascular risk factors improves late survival following abdominal aortic aneurysm repair: a systematic review and meta-analysis. Ann Vasc Surg. 2017 Feb;39:301-11. http://www.ncbi.nlm.nih.gov/pubmed/27666804?tool=bestpractice.com
El entrenamiento preoperatorio con ejercicios redujo las complicaciones cardíacas posquirúrgicas en un pequeño ensayo aleatorizado controlado (EAC) de pacientes sometidos a reparación abierta o endovascular del AAA, aunque una revisión de la Cochrane y una revisión sistemática independiente de la prehabilitación (entrenamiento con ejercicios) antes de la cirugía del AAA no mostraron ningún beneficio en los resultados.[197]Barakat HM, Shahin Y, Khan JA, et al. Preoperative supervised exercise improves outcomes after elective abdominal aortic aneurysm repair: a randomized controlled trial. Ann Surg. 2016 Jul;264(1):47-53. http://www.ncbi.nlm.nih.gov/pubmed/26756766?tool=bestpractice.com [198]Fenton C, Tan AR, Abaraogu UO, et al. Prehabilitation exercise therapy before elective abdominal aortic aneurysm repair. Cochrane Database Syst Rev. 2021 Jul 8;7(7):CD013662. https://www.doi.org/10.1002/14651858.CD013662.pub2 http://www.ncbi.nlm.nih.gov/pubmed/34236703?tool=bestpractice.com [199]Bonner RJ, Wallace T, Jones AD, et al. The content of pre-habilitative interventions for patients undergoing repair of abdominal aortic aneurysms and their effect on post-operative outcomes: a systematic review. Eur J Vasc Endovasc Surg. 2021 May;61(5):756-65. https://www.doi.org/10.1016/j.ejvs.2021.01.043 http://www.ncbi.nlm.nih.gov/pubmed/33678532?tool=bestpractice.com Aunque el entrenamiento preoperatorio con ejercicios puede ser beneficioso para los pacientes sometidos a reparación de AAA, es necesario realizar más investigaciones con EAC antes de recomendarlo de forma más generalizada.[200]Wee IJY, Choong AMTL. A systematic review of the impact of preoperative exercise for patients with abdominal aortic aneurysm. J Vasc Surg. 2020 Jun;71(6):2123-31.e1. https://www.doi.org/10.1016/j.jvs.2018.09.039 http://www.ncbi.nlm.nih.gov/pubmed/30606665?tool=bestpractice.com
El uso perioperatorio de estatinas ralentiza el crecimiento del aneurisma, reduce el riesgo de rotura y disminuye la mortalidad por reparación o rotura del AAA.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com El tratamiento de estatinas debe iniciarse al menos 1 mes antes de la cirugía para reducir la morbilidad y la mortalidad cardiovascular, y continuarse indefinidamente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [141]Risum Ø, Sandven I, Sundhagen JO, et al. Editor's choice - effect of statins on total mortality in abdominal aortic aneurysm repair: a systematic review and meta-analysis. Eur J Vasc Endovasc Surg. 2021 Jan;61(1):114-20. https://www.doi.org/10.1016/j.ejvs.2020.08.007 http://www.ncbi.nlm.nih.gov/pubmed/32928667?tool=bestpractice.com
Los pacientes con AAA presentan un mayor riesgo de sufrir eventos cardiovasculares adversos graves. La evidencia es limitada, pero en ausencia de contraindicaciones, los pacientes con AAA deben recibir un tratamiento antiplaquetario único (ácido acetilsalicílico o clopidogrel).[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [142]Aboyans V, Bauersachs R, Mazzolai L, et al. Antithrombotic therapies in aortic and peripheral arterial diseases in 2021: a consensus document from the ESC working group on aorta and peripheral vascular diseases, the ESC working group on thrombosis, and the ESC working group on cardiovascular pharmacotherapy. Eur Heart J. 2021 Oct 14;42(39):4013-24. https://www.doi.org/10.1093/eurheartj/ehab390 http://www.ncbi.nlm.nih.gov/pubmed/34279602?tool=bestpractice.com Esto debe continuar durante el periodo perioperatorio.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
La hipertensión debe controlarse para reducir la morbilidad y la mortalidad cardiovascular.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
No se recomienda el inicio de betabloqueantes antes de la reparación del AAA.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com Sin embargo, se puede continuar con un betabloqueante si un paciente ya lo está tomando en una dosis adecuada.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com Ensayos de gran tamaño muestral en los que el beta-bloqueo se inició unos días antes de la cirugía no han indicado ningún beneficio, o incluso daño, del beta-bloqueo perioperatorio.[201]Brady AR, Gibbs JS, Greenhalgh RM, et al; POBBLE Trial Investigators. Perioperative beta-blockade (Pobble) for patients undergoing infrarenal vascular surgery: results of a randomized double-blind controlled trial. J Vasc Surg. 2005 Apr;41(4):602-9. https://www.jvascsurg.org/article/S0741-5214(05)00189-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/15874923?tool=bestpractice.com [202]Devereaux PJ, Yang H, Yusuf S, et al; POISE Study Group. Effects of extended-release metoprolol succinate in patients undergoing non-cardiac surgery (POISE trial): a randomised controlled trial. Lancet. 2008 May 31;371(9627):1839-47. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(08)60601-7/fulltext http://www.ncbi.nlm.nih.gov/pubmed/18479744?tool=bestpractice.com [203]Yang H, Raymer K, Butler R, et al. The effects of perioperative beta-blockade: results of the Metoprolol after Vascular Surgery (MaVS) study, a randomized controlled trial. Am Heart J. 2006 Nov;152(5):983-90. http://www.ncbi.nlm.nih.gov/pubmed/17070177?tool=bestpractice.com
antibioticoterapia perioperatoria
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
Se administra antibioticoterapia perioperatoria. La cobertura con antibióticos de amplio espectro es necesaria y se realiza conforme a los protocolos locales.
tratamiento de causa infecciosa/inflamatoria
Tratamiento adicional recomendado para ALGUNOS pacientes del grupo seleccionado
Una vez que el paciente está estable y se ha priorizado la reparación quirúrgica urgente del AAA sintomático, debe abordarse la etiología infecciosa o inflamatoria.
Si se sospecha que el paciente tiene un aneurisma infeccioso, el diagnóstico precoz y el tratamiento rápido son esenciales para mejorar los resultados.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com A menudo es necesario un desbridamiento extenso durante la reparación quirúrgica urgente en estos pacientes. Existe un alto riesgo de complicaciones infecciosas secundarias y puede que sea necesaria una nueva intervención quirúrgica para nuevas lesiones infecciosas.Deben realizarse cultivos intraoperatorios para orientar con precisión el tratamiento antibiótico posterior; sin embargo, a menudo se administran antibióticos empíricos, ya que los cultivos de sangre periférica y de muestras quirúrgicas son negativos en una gran proporción de pacientes.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com Puede estar indicada una antibioticoterapia prolongada (de 4 a 6 semanas de duración a toda la vida) en función del patógeno específico, el tipo de reparación quirúrgica y el estado inmunológico del paciente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
La aortitis inflamatoria (causada, por ejemplo, por la arteritis de Takayasu o la arteritis de células gigantes) se trata con dosis altas de corticosteroides y cirugía.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [205]Ben Jmaà H, Karray R, Jmal H, et al. Surgical and endoluminal management of the inflammatory aortitis: a Tunisian center experience [in French]. J Med Vasc. 2017 Jul;42(4):213-20. http://www.ncbi.nlm.nih.gov/pubmed/28705339?tool=bestpractice.com
hallazgo incidental: AAA asintomático de pequeño tamaño
vigilancia
Para los aneurismas de aorta abdominal (AAA) detectados de manera incidental, se prefiere la vigilancia para reparar hasta que el riesgo teórico de rotura supere el riesgo estimado de mortalidad quirúrgica.[4]Owens DK, Davidson KW, Krist AH, et al; US Preventive Services Task Force. Screening for abdominal aortic aneurysm: US Preventive Services Task Force recommendation statement. JAMA. 2019 Dec 10;322(22):2211-8. https://jamanetwork.com/journals/jama/fullarticle/2757234 http://www.ncbi.nlm.nih.gov/pubmed/31821437?tool=bestpractice.com
La cirugía abierta temprana para el tratamiento de los AAA más pequeños no reduce la mortalidad por todas las causas o específicas de los AAA.[4]Owens DK, Davidson KW, Krist AH, et al; US Preventive Services Task Force. Screening for abdominal aortic aneurysm: US Preventive Services Task Force recommendation statement. JAMA. 2019 Dec 10;322(22):2211-8.
https://jamanetwork.com/journals/jama/fullarticle/2757234
http://www.ncbi.nlm.nih.gov/pubmed/31821437?tool=bestpractice.com
[132]Ulug P, Powell JT, Martinez MA, et al. Surgery for small asymptomatic abdominal aortic aneurysms. Cochrane Database Syst Rev. 2020 Jul 1;7(7):CD001835.
https://www.doi.org/10.1002/14651858.CD001835.pub5
http://www.ncbi.nlm.nih.gov/pubmed/32609382?tool=bestpractice.com
[  ]
How does immediate surgery compare with surveillance in people with asymptomatic abdominal aortic aneurysms (AAAs)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3227/fullMostrarme la respuesta Una revisión sistemática (4 ensayos, 3314 participantes) encontró evidencia de alta calidad para demostrar que la reparación inmediata del AAA de pequeño tamaño (4 cm a 5.5 cm) no mejoró la supervivencia a largo plazo, en comparación con la vigilancia (cociente de riesgos instantáneos ajustado 0.88; IC del 95%: 0.75 a 1.02; seguimiento medio de 10 años).[132]Ulug P, Powell JT, Martinez MA, et al. Surgery for small asymptomatic abdominal aortic aneurysms. Cochrane Database Syst Rev. 2020 Jul 1;7(7):CD001835.
https://www.doi.org/10.1002/14651858.CD001835.pub5
http://www.ncbi.nlm.nih.gov/pubmed/32609382?tool=bestpractice.com
La falta de beneficio atribuible a la cirugía inmediata fue consistente, independientemente de la edad del paciente, el diámetro del aneurisma pequeño y si la reparación fue endovascular o abierta.[132]Ulug P, Powell JT, Martinez MA, et al. Surgery for small asymptomatic abdominal aortic aneurysms. Cochrane Database Syst Rev. 2020 Jul 1;7(7):CD001835.
https://www.doi.org/10.1002/14651858.CD001835.pub5
http://www.ncbi.nlm.nih.gov/pubmed/32609382?tool=bestpractice.com
]
How does immediate surgery compare with surveillance in people with asymptomatic abdominal aortic aneurysms (AAAs)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3227/fullMostrarme la respuesta Una revisión sistemática (4 ensayos, 3314 participantes) encontró evidencia de alta calidad para demostrar que la reparación inmediata del AAA de pequeño tamaño (4 cm a 5.5 cm) no mejoró la supervivencia a largo plazo, en comparación con la vigilancia (cociente de riesgos instantáneos ajustado 0.88; IC del 95%: 0.75 a 1.02; seguimiento medio de 10 años).[132]Ulug P, Powell JT, Martinez MA, et al. Surgery for small asymptomatic abdominal aortic aneurysms. Cochrane Database Syst Rev. 2020 Jul 1;7(7):CD001835.
https://www.doi.org/10.1002/14651858.CD001835.pub5
http://www.ncbi.nlm.nih.gov/pubmed/32609382?tool=bestpractice.com
La falta de beneficio atribuible a la cirugía inmediata fue consistente, independientemente de la edad del paciente, el diámetro del aneurisma pequeño y si la reparación fue endovascular o abierta.[132]Ulug P, Powell JT, Martinez MA, et al. Surgery for small asymptomatic abdominal aortic aneurysms. Cochrane Database Syst Rev. 2020 Jul 1;7(7):CD001835.
https://www.doi.org/10.1002/14651858.CD001835.pub5
http://www.ncbi.nlm.nih.gov/pubmed/32609382?tool=bestpractice.com
La derivación quirúrgica de los AAA más pequeños generalmente se reserva para el crecimiento rápido, o una vez que se alcanza el diámetro umbral para la reparación del aneurisma en una ecografía repetida.[4]Owens DK, Davidson KW, Krist AH, et al; US Preventive Services Task Force. Screening for abdominal aortic aneurysm: US Preventive Services Task Force recommendation statement. JAMA. 2019 Dec 10;322(22):2211-8. https://jamanetwork.com/journals/jama/fullarticle/2757234 http://www.ncbi.nlm.nih.gov/pubmed/31821437?tool=bestpractice.com
Sin embargo, en pacientes con una causa genética subyacente o un trastorno del tejido conjuntivo, deberá individualizarse el diámetro umbral para considerar la reparación, en función de las características anatómicas y la genética subyacente (el riesgo de ruptura es mayor en diámetros aórticos más pequeños en algunas afecciones, y la reparación quirúrgica es más difícil en determinados trastornos debido al aumento de la fragilidad de la pared arterial y la anatomía).[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
manejo agresivo del riesgo cardiovascular
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
El tratamiento preoperatorio de los factores de riesgo cardiovascular modificables mejora la supervivencia a largo plazo después de la reparación del AAA.[196]Khashram M, Williman JA, Hider PN, et al. Management of modifiable vascular risk factors improves late survival following abdominal aortic aneurysm repair: a systematic review and meta-analysis. Ann Vasc Surg. 2017 Feb;39:301-11. http://www.ncbi.nlm.nih.gov/pubmed/27666804?tool=bestpractice.com
Se debe animar a los pacientes a dejar de fumar y ofrecerles tratamiento farmacológico (tratamiento sustitutivo con nicotina, nortriptilina y bupropión) o asesoramiento para ayudarles a conseguirlo si es necesario.[1]Dehlin JM, Upchurch GR. Management of abdominal aortic aneurysms. Curr Treat Options Cardiovasc Med. 2005 Jun;7(2):119-30.
http://www.ncbi.nlm.nih.gov/pubmed/15935120?tool=bestpractice.com
[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482.
https://www.doi.org/10.1161/CIR.0000000000001106
http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
[13]Zankl AR, Schumacher H, Krumsdorf U, et al. Pathology, natural history and treatment of abdominal aortic aneurysms. Clin Res Cardiol. 2007 Mar;96(3):140-51.
http://www.ncbi.nlm.nih.gov/pubmed/17180573?tool=bestpractice.com
[15]Singh K, Bønaa H, Jacobsen BK, et al. Prevalence of and risk factors for abdominal aortic aneurysms in a population-based study: the Tromsø Study. Am J Epidemiol. 2001 Aug 1;154(3):236-44.
https://academic.oup.com/aje/article/154/3/236/125840
http://www.ncbi.nlm.nih.gov/pubmed/11479188?tool=bestpractice.com
[22]Lederle FA, Johnson GR, Wilson SE, et al; Aneurysm Detection and Management (ADAM) Veterans Affairs Cooperative Study Group. Prevalence and associations of abdominal aortic aneurysm detected through screening. Ann Intern Med. 1997 Mar 15;126(6):441-9.
http://www.ncbi.nlm.nih.gov/pubmed/9072929?tool=bestpractice.com
[23]Wilmink TB, Quick CR, Day NE. The association between cigarette smoking and abdominal aortic aneurysms. J Vasc Surg. 1999 Dec;30(6):1099-105.
http://www.ncbi.nlm.nih.gov/pubmed/10587395?tool=bestpractice.com
[136]Hartmann-Boyce J, Chepkin SC, Ye W, et al. Nicotine replacement therapy versus control for smoking cessation. Cochrane Database Syst Rev. 2018 May 31;5:CD000146.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000146.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/29852054?tool=bestpractice.com
[137]Rigotti NA, Clair C, Munafò MR, et al. Interventions for smoking cessation in hospitalised patients. Cochrane Database Syst Rev. 2012 May 16;(5):CD001837.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001837.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/22592676?tool=bestpractice.com
[138]Howes S, Hartmann-Boyce J, Livingstone-Banks J, et al. Antidepressants for smoking cessation. Cochrane Database Syst Rev. 2020 Apr 22;(4):CD000031.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000031.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/32319681?tool=bestpractice.com
[  ]
What are the effects of adding bupropion or fluoxetine to other treatments compared with using other treatments alone for people trying to quit smoking?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4337/fullMostrarme la respuesta
]
What are the effects of adding bupropion or fluoxetine to other treatments compared with using other treatments alone for people trying to quit smoking?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4337/fullMostrarme la respuesta
El entrenamiento preoperatorio con ejercicios redujo las complicaciones cardíacas posquirúrgicas en un pequeño ensayo aleatorizado controlado (EAC) de pacientes sometidos a reparación abierta o endovascular del AAA, aunque una revisión de la Cochrane y una revisión sistemática independiente de la prehabilitación (entrenamiento con ejercicios) antes de la cirugía del AAA no mostraron ningún beneficio en los resultados.[197]Barakat HM, Shahin Y, Khan JA, et al. Preoperative supervised exercise improves outcomes after elective abdominal aortic aneurysm repair: a randomized controlled trial. Ann Surg. 2016 Jul;264(1):47-53. http://www.ncbi.nlm.nih.gov/pubmed/26756766?tool=bestpractice.com [198]Fenton C, Tan AR, Abaraogu UO, et al. Prehabilitation exercise therapy before elective abdominal aortic aneurysm repair. Cochrane Database Syst Rev. 2021 Jul 8;7(7):CD013662. https://www.doi.org/10.1002/14651858.CD013662.pub2 http://www.ncbi.nlm.nih.gov/pubmed/34236703?tool=bestpractice.com [199]Bonner RJ, Wallace T, Jones AD, et al. The content of pre-habilitative interventions for patients undergoing repair of abdominal aortic aneurysms and their effect on post-operative outcomes: a systematic review. Eur J Vasc Endovasc Surg. 2021 May;61(5):756-65. https://www.doi.org/10.1016/j.ejvs.2021.01.043 http://www.ncbi.nlm.nih.gov/pubmed/33678532?tool=bestpractice.com Aunque el entrenamiento preoperatorio con ejercicios puede ser beneficioso para los pacientes sometidos a reparación de AAA, es necesario realizar pruebas diagnósticas adicionales con EAC antes de recomendarlo de forma más generalizada.[200]Wee IJY, Choong AMTL. A systematic review of the impact of preoperative exercise for patients with abdominal aortic aneurysm. J Vasc Surg. 2020 Jun;71(6):2123-31.e1. https://www.doi.org/10.1016/j.jvs.2018.09.039 http://www.ncbi.nlm.nih.gov/pubmed/30606665?tool=bestpractice.com
El uso perioperatorio de estatinas ralentiza el crecimiento del aneurisma, reduce el riesgo de rotura y disminuye la mortalidad por reparación o rotura del AAA.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com El tratamiento de estatinas debe iniciarse al menos 1 mes antes de la cirugía para reducir la morbilidad y la mortalidad cardiovascular, y continuarse indefinidamente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [141]Risum Ø, Sandven I, Sundhagen JO, et al. Editor's choice - effect of statins on total mortality in abdominal aortic aneurysm repair: a systematic review and meta-analysis. Eur J Vasc Endovasc Surg. 2021 Jan;61(1):114-20. https://www.doi.org/10.1016/j.ejvs.2020.08.007 http://www.ncbi.nlm.nih.gov/pubmed/32928667?tool=bestpractice.com
Los pacientes con AAA presentan un mayor riesgo de sufrir eventos cardiovasculares adversos graves. La evidencia es limitada, pero en ausencia de contraindicaciones, los pacientes con AAA deben recibir un tratamiento antiplaquetario único (ácido acetilsalicílico o clopidogrel).[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [142]Aboyans V, Bauersachs R, Mazzolai L, et al. Antithrombotic therapies in aortic and peripheral arterial diseases in 2021: a consensus document from the ESC working group on aorta and peripheral vascular diseases, the ESC working group on thrombosis, and the ESC working group on cardiovascular pharmacotherapy. Eur Heart J. 2021 Oct 14;42(39):4013-24. https://www.doi.org/10.1093/eurheartj/ehab390 http://www.ncbi.nlm.nih.gov/pubmed/34279602?tool=bestpractice.com Esto debe continuar durante el periodo perioperatorio.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
La hipertensión debe controlarse para reducir la morbilidad y la mortalidad cardiovascular.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
tratamiento de causa infecciosa/inflamatoria
Tratamiento adicional recomendado para ALGUNOS pacientes del grupo seleccionado
Debe abordarse la etiología infecciosa o inflamatoria.
Si se sospecha que el paciente presenta un aneurisma infeccioso, el diagnóstico temprano y el tratamiento rápido con antibióticos y reparación quirúrgica urgente son esenciales para mejorar los resultados.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com A menudo es necesario un desbridamiento extenso durante la reparación quirúrgica urgente en estos pacientes. Existe un alto riesgo de complicaciones infecciosas secundarias y puede que sea necesaria una nueva intervención quirúrgica para nuevas lesiones infecciosas.Deben realizarse cultivos intraoperatorios para orientar con precisión el tratamiento antibiótico posterior; sin embargo, a menudo se administran antibióticos empíricos, ya que los cultivos de sangre periférica y de muestras quirúrgicas son negativos en una gran proporción de pacientes.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com Puede estar indicada una antibioticoterapia prolongada (de 4 a 6 semanas de duración a toda la vida) en función del patógeno específico, el tipo de reparación quirúrgica y el estado inmunológico del paciente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
La aortitis inflamatoria (causada, por ejemplo, por la arteritis de Takayasu o la arteritis de células gigantes) se trata con dosis altas de corticosteroides y cirugía.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [205]Ben Jmaà H, Karray R, Jmal H, et al. Surgical and endoluminal management of the inflammatory aortitis: a Tunisian center experience [in French]. J Med Vasc. 2017 Jul;42(4):213-20. http://www.ncbi.nlm.nih.gov/pubmed/28705339?tool=bestpractice.com
hallazgo incidental: AAA asintomático de gran tamaño
reparación quirúrgica electiva
En general, se indica la reparación en pacientes con AAA asintomático de gran tamaño (p. ej., con un diámetro que excede los 5.5 cm en hombres o >5.0 cm en mujeres en los Estados Unidos, aunque las decisiones de tratamiento basadas en un mayor tamaño pueden diferir en otros países).[78]National Institute for Health and Care Excellence. Abdominal aortic aneurysm: diagnosis and management. Mar 2020 [internet publication]. https://www.nice.org.uk/guidance/ng156 La reparación de un aneurisma ≥5.5 cm ofrece una ventaja en la supervivencia.[1]Dehlin JM, Upchurch GR. Management of abdominal aortic aneurysms. Curr Treat Options Cardiovasc Med. 2005 Jun;7(2):119-30. http://www.ncbi.nlm.nih.gov/pubmed/15935120?tool=bestpractice.com [76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com [106]UK Small Aneurysm Trial Participants. Mortality results for randomized controlled trial of early elective surgery or ultrasonographic surveillance for small abdominal aortic aneurysms. Lancet. 1998 Nov 21;352(9141):1649-55. http://www.ncbi.nlm.nih.gov/pubmed/9853436?tool=bestpractice.com [107]Powell JT, Brady AR, Brown LC, et al; United Kingdom Small Aneurysm Trial Participants. Long-term outcomes of immediate repair compared with surveillance of small abdominal aortic aneurysms. N Engl J Med. 2002 May 9;346(19):1445-52. https://www.nejm.org/doi/full/10.1056/NEJMoa013527 http://www.ncbi.nlm.nih.gov/pubmed/12000814?tool=bestpractice.com [108]Powell JT, Brown LC, Forbes JF, et al. Final 12-year follow-up of surgery versus surveillance in the UK Small Aneurysm Trial. Br J Surg. 2007 Jun;94(6):702-8. http://www.ncbi.nlm.nih.gov/pubmed/17514693?tool=bestpractice.com
Las decisiones relativas a la reparación deben ser individualizadas, teniendo en cuenta la preferencia del paciente, su edad, sexo, factores de riesgo perioperatorio y factores de riesgo anatómicos. Se debe tener cuidado de evaluar la calidad de vida del paciente y de realizar un asesoramiento cuidadoso con respecto a los riesgos de la cirugía y la calidad de vida posterior. Se recomienda un enfoque de toma de decisiones compartida que tenga en cuenta los riesgos y beneficios de los procedimientos.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [132]Ulug P, Powell JT, Martinez MA, et al. Surgery for small asymptomatic abdominal aortic aneurysms. Cochrane Database Syst Rev. 2020 Jul 1;7(7):CD001835. https://www.doi.org/10.1002/14651858.CD001835.pub5 http://www.ncbi.nlm.nih.gov/pubmed/32609382?tool=bestpractice.com
Los datos sugieren que en pacientes con AAA de gran tamaño (≥5.5 cm) sometidos a reparación electiva, la EVAR equivale a la reparación abierta en términos de supervivencia global, aunque la tasa de intervenciones secundarias es más elevada en la EVAR.[143]Greenhalgh RM, Brown LC, Powell JT, et al; United Kingdom EVAR Trial Investigators. Endovascular versus open repair of abdominal aortic aneurysm. N Engl J Med. 2010 May 20;362(20):1863-71. http://www.ncbi.nlm.nih.gov/pubmed/20382983?tool=bestpractice.com [144]Amato B, Fugetto F, Compagna R, et al. Endovascular repair versus open repair in the treatment of ruptured aortic aneurysms: a systematic review. Minerva Chir. 2019 Dec;74(6):472-80. http://www.ncbi.nlm.nih.gov/pubmed/29806754?tool=bestpractice.com La EVAR también reduce la mortalidad relacionada con el AAA (pero no presenta supervivencia global a un plazo más amplio) en pacientes con AAA de gran tamaño (≥5.5 cm) y no aptos para la reparación abierta.[145]Greenhalgh RM, Brown LC, Powell JT, et al; United Kingdom EVAR Trial Investigators. Endovascular repair of aortic aneurysm in patients physically ineligible for open repair. N Engl J Med. 2010 May 20;362(20):1872-80. http://www.ncbi.nlm.nih.gov/pubmed/20382982?tool=bestpractice.com
Los AAA posreparación de mayor tamaño parecen estar asociados a una menor tasa de supervivencia tardía que los aneurismas de menor tamaño (cociente de riesgos instantáneos agrupado de 1.14 por 1 cm de aumento en el diámetro del AAA, IC del 95%: 1.09 a 1.18; seguimiento de 12 a 91.2 meses).[146]Khashram M, Hider PN, Williman JA, et al. Does the diameter of abdominal aortic aneurysm influence late survival following abdominal aortic aneurysm repair? A systematic review and meta-analysis. Vascular. 2016 Dec;24(6):658-67. http://www.ncbi.nlm.nih.gov/pubmed/27189809?tool=bestpractice.com La asociación es más pronunciada para la EVAR que para la reparación abierta.
Para los pacientes con un AAA complejo y riesgo quirúrgico estándar, se debe considerar la apertura o EVAR en función de la aptitud, la anatomía y las preferencias del paciente. Para los pacientes con un AAA complejo y alto riesgo quirúrgico, se debe considerar la EVAR con tecnologías fenestradas y ramificadas como tratamiento de primera línea. Los endoinjertos fenestrados y ramificados se han convertido en el tratamiento de elección de los AAA complejos en la mayoría de los centros de alto volumen.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com Estos procedimientos son alternativas viables a la reparación abierta para los AAA yuxtarrenales y suprarrenales, o para aquellos con AAA en los que un cuello corto o enfermo impide la reparación convencional.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
reducción del riesgo cardiovascular preoperatorio
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
El tratamiento preoperatorio de los factores de riesgo cardiovascular modificables mejora la supervivencia a largo plazo después de la reparación del AAA.[196]Khashram M, Williman JA, Hider PN, et al. Management of modifiable vascular risk factors improves late survival following abdominal aortic aneurysm repair: a systematic review and meta-analysis. Ann Vasc Surg. 2017 Feb;39:301-11. http://www.ncbi.nlm.nih.gov/pubmed/27666804?tool=bestpractice.com
Se debe animar a los pacientes a dejar de fumar y ofrecerles tratamiento farmacológico (tratamiento sustitutivo con nicotina, nortriptilina y bupropión) o asesoramiento para ayudarles a conseguirlo si es necesario.[1]Dehlin JM, Upchurch GR. Management of abdominal aortic aneurysms. Curr Treat Options Cardiovasc Med. 2005 Jun;7(2):119-30.
http://www.ncbi.nlm.nih.gov/pubmed/15935120?tool=bestpractice.com
[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482.
https://www.doi.org/10.1161/CIR.0000000000001106
http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
[13]Zankl AR, Schumacher H, Krumsdorf U, et al. Pathology, natural history and treatment of abdominal aortic aneurysms. Clin Res Cardiol. 2007 Mar;96(3):140-51.
http://www.ncbi.nlm.nih.gov/pubmed/17180573?tool=bestpractice.com
[15]Singh K, Bønaa H, Jacobsen BK, et al. Prevalence of and risk factors for abdominal aortic aneurysms in a population-based study: the Tromsø Study. Am J Epidemiol. 2001 Aug 1;154(3):236-44.
https://academic.oup.com/aje/article/154/3/236/125840
http://www.ncbi.nlm.nih.gov/pubmed/11479188?tool=bestpractice.com
[22]Lederle FA, Johnson GR, Wilson SE, et al; Aneurysm Detection and Management (ADAM) Veterans Affairs Cooperative Study Group. Prevalence and associations of abdominal aortic aneurysm detected through screening. Ann Intern Med. 1997 Mar 15;126(6):441-9.
http://www.ncbi.nlm.nih.gov/pubmed/9072929?tool=bestpractice.com
[23]Wilmink TB, Quick CR, Day NE. The association between cigarette smoking and abdominal aortic aneurysms. J Vasc Surg. 1999 Dec;30(6):1099-105.
http://www.ncbi.nlm.nih.gov/pubmed/10587395?tool=bestpractice.com
[136]Hartmann-Boyce J, Chepkin SC, Ye W, et al. Nicotine replacement therapy versus control for smoking cessation. Cochrane Database Syst Rev. 2018 May 31;5:CD000146.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000146.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/29852054?tool=bestpractice.com
[137]Rigotti NA, Clair C, Munafò MR, et al. Interventions for smoking cessation in hospitalised patients. Cochrane Database Syst Rev. 2012 May 16;(5):CD001837.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001837.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/22592676?tool=bestpractice.com
[138]Howes S, Hartmann-Boyce J, Livingstone-Banks J, et al. Antidepressants for smoking cessation. Cochrane Database Syst Rev. 2020 Apr 22;(4):CD000031.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000031.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/32319681?tool=bestpractice.com
[  ]
What are the effects of adding bupropion or fluoxetine to other treatments compared with using other treatments alone for people trying to quit smoking?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4337/fullMostrarme la respuesta
]
What are the effects of adding bupropion or fluoxetine to other treatments compared with using other treatments alone for people trying to quit smoking?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4337/fullMostrarme la respuesta
El entrenamiento preoperatorio con ejercicios redujo las complicaciones cardíacas posquirúrgicas en un pequeño ensayo aleatorizado controlado (EAC) de pacientes sometidos a reparación abierta o endovascular del AAA, aunque una revisión de la Cochrane y una revisión sistemática independiente de la prehabilitación (entrenamiento con ejercicios) antes de la cirugía del AAA no mostraron ningún beneficio en los resultados.[197]Barakat HM, Shahin Y, Khan JA, et al. Preoperative supervised exercise improves outcomes after elective abdominal aortic aneurysm repair: a randomized controlled trial. Ann Surg. 2016 Jul;264(1):47-53. http://www.ncbi.nlm.nih.gov/pubmed/26756766?tool=bestpractice.com [198]Fenton C, Tan AR, Abaraogu UO, et al. Prehabilitation exercise therapy before elective abdominal aortic aneurysm repair. Cochrane Database Syst Rev. 2021 Jul 8;7(7):CD013662. https://www.doi.org/10.1002/14651858.CD013662.pub2 http://www.ncbi.nlm.nih.gov/pubmed/34236703?tool=bestpractice.com [199]Bonner RJ, Wallace T, Jones AD, et al. The content of pre-habilitative interventions for patients undergoing repair of abdominal aortic aneurysms and their effect on post-operative outcomes: a systematic review. Eur J Vasc Endovasc Surg. 2021 May;61(5):756-65. https://www.doi.org/10.1016/j.ejvs.2021.01.043 http://www.ncbi.nlm.nih.gov/pubmed/33678532?tool=bestpractice.com Aunque el entrenamiento preoperatorio con ejercicios puede ser beneficioso para los pacientes sometidos a reparación de AAA, es necesario realizar pruebas diagnósticas adicionales con EAC antes de recomendarlo de forma más generalizada.[200]Wee IJY, Choong AMTL. A systematic review of the impact of preoperative exercise for patients with abdominal aortic aneurysm. J Vasc Surg. 2020 Jun;71(6):2123-31.e1. https://www.doi.org/10.1016/j.jvs.2018.09.039 http://www.ncbi.nlm.nih.gov/pubmed/30606665?tool=bestpractice.com
El uso perioperatorio de estatinas ralentiza el crecimiento del aneurisma, reduce el riesgo de rotura y disminuye la mortalidad por reparación o rotura del AAA.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com El tratamiento de estatinas debe iniciarse al menos 1 mes antes de la cirugía para reducir la morbilidad y la mortalidad cardiovascular, y continuarse indefinidamente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [141]Risum Ø, Sandven I, Sundhagen JO, et al. Editor's choice - effect of statins on total mortality in abdominal aortic aneurysm repair: a systematic review and meta-analysis. Eur J Vasc Endovasc Surg. 2021 Jan;61(1):114-20. https://www.doi.org/10.1016/j.ejvs.2020.08.007 http://www.ncbi.nlm.nih.gov/pubmed/32928667?tool=bestpractice.com
Los pacientes con AAA presentan un mayor riesgo de sufrir eventos cardiovasculares adversos graves. La evidencia es limitada, pero en ausencia de contraindicaciones, los pacientes con AAA deben recibir un tratamiento antiplaquetario único (ácido acetilsalicílico o clopidogrel).[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [142]Aboyans V, Bauersachs R, Mazzolai L, et al. Antithrombotic therapies in aortic and peripheral arterial diseases in 2021: a consensus document from the ESC working group on aorta and peripheral vascular diseases, the ESC working group on thrombosis, and the ESC working group on cardiovascular pharmacotherapy. Eur Heart J. 2021 Oct 14;42(39):4013-24. https://www.doi.org/10.1093/eurheartj/ehab390 http://www.ncbi.nlm.nih.gov/pubmed/34279602?tool=bestpractice.com Esto debe continuar durante el periodo perioperatorio.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
La hipertensión debe controlarse para reducir la morbilidad y la mortalidad cardiovascular.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
antibioticoterapia perioperatoria
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
Se administra antibioticoterapia perioperatoria. La cobertura con antibióticos de amplio espectro es necesaria y se realiza conforme a los protocolos locales.
tratamiento de causa infecciosa/inflamatoria
Tratamiento adicional recomendado para ALGUNOS pacientes del grupo seleccionado
Debe abordarse la etiología infecciosa o inflamatoria.
Si se sospecha que el paciente presenta un aneurisma infeccioso, el diagnóstico temprano y el tratamiento rápido con antibióticos y reparación quirúrgica urgente son esenciales para mejorar los resultados.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com A menudo es necesario un desbridamiento extenso durante la reparación quirúrgica urgente en estos pacientes. Existe un alto riesgo de complicaciones infecciosas secundarias y puede que sea necesaria una nueva intervención quirúrgica para nuevas lesiones infecciosas.Deben realizarse cultivos intraoperatorios para orientar con precisión el tratamiento antibiótico posterior; sin embargo, a menudo se administran antibióticos empíricos, ya que los cultivos de sangre periférica y de muestras quirúrgicas son negativos en una gran proporción de pacientes.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com Puede estar indicada una antibioticoterapia prolongada (de 4 a 6 semanas de duración a toda la vida) en función del patógeno específico, el tipo de reparación quirúrgica y el estado inmunológico del paciente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
La aortitis inflamatoria (causada, por ejemplo, por la arteritis de Takayasu o la arteritis de células gigantes) se trata con dosis altas de corticosteroides y cirugía.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [205]Ben Jmaà H, Karray R, Jmal H, et al. Surgical and endoluminal management of the inflammatory aortitis: a Tunisian center experience [in French]. J Med Vasc. 2017 Jul;42(4):213-20. http://www.ncbi.nlm.nih.gov/pubmed/28705339?tool=bestpractice.com
fuga de la reparación endovascular que requiere tratamiento
procedimientos correctivos
Una endofuga es un flujo sanguíneo persistente fuera del injerto y dentro del saco del aneurisma.[206]Schurink GW, Aarts NJ, vanBockel JH. Endoleak after stent-graft treatment of abdominal aortic aneurysm: a meta-analysis of clinical studies. Br J Surg. 1999 May;86(5):581-7. http://www.ncbi.nlm.nih.gov/pubmed/10361173?tool=bestpractice.com [207]Veith FJ, Baum RA, Ohki T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg. 2002 May;35(5):1029-35. http://www.ncbi.nlm.nih.gov/pubmed/12021724?tool=bestpractice.com No es una complicación tras una reparación abierta.
La vigilancia posoperatoria puede detectar endofugas importantes y una expansión de la bolsa de aneurisma. El riesgo tras una reparación endovascular del aneurisma (EVAR) es del 24%.[206]Schurink GW, Aarts NJ, vanBockel JH. Endoleak after stent-graft treatment of abdominal aortic aneurysm: a meta-analysis of clinical studies. Br J Surg. 1999 May;86(5):581-7. http://www.ncbi.nlm.nih.gov/pubmed/10361173?tool=bestpractice.com Existen cinco tipos de fugas internas.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
Tipo I: fuga en el lugar de fijación (tipo IA en el extremo proximal del endoinjerto u oclusor ilíaco; tipo IB en el extremo distal); generalmente inmediata, pero pueden producirse fugas retardadas.[Figure caption and citation for the preceding image starts]: Endofuga tipo I en anastomosis distal de la ilíaca izquierda (fuga marcada con un círculo)University of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends]. Debe hacerse todo lo posible para reparar la fuga interna de tipo I antes de completar el procedimiento (p. ej., moldeado con balón de la zona de sellado proximal, colocación de un manguito proximal, endostaples, embolización líquida).[208]van Schaik TG, Meekel JP, Hoksbergen AWJ, et al. Systematic review of embolization of type I endoleaks using liquid embolic agents. J Vasc Surg. 2021 Sep;74(3):1024-32.
https://www.doi.org/10.1016/j.jvs.2021.03.061
http://www.ncbi.nlm.nih.gov/pubmed/33940072?tool=bestpractice.com
La endofuga persistente de tipo IA puede requerir la conversión a reparación abierta, siempre que el riesgo quirúrgico sea aceptable.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331.
https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2.
https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com
[209]Perini P, Bianchini Massoni C, Mariani E, et al. Systematic review and meta-analysis of the outcome of different treatments for type 1a endoleak after EVAR. Ann Vasc Surg. 2019 Oct;60:435-46.e1.
http://www.ncbi.nlm.nih.gov/pubmed/31200054?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Extensión de endoprótesis expandida para la misma endofuga tipo I (marcada con un círculo)University of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].
Debe hacerse todo lo posible para reparar la fuga interna de tipo I antes de completar el procedimiento (p. ej., moldeado con balón de la zona de sellado proximal, colocación de un manguito proximal, endostaples, embolización líquida).[208]van Schaik TG, Meekel JP, Hoksbergen AWJ, et al. Systematic review of embolization of type I endoleaks using liquid embolic agents. J Vasc Surg. 2021 Sep;74(3):1024-32.
https://www.doi.org/10.1016/j.jvs.2021.03.061
http://www.ncbi.nlm.nih.gov/pubmed/33940072?tool=bestpractice.com
La endofuga persistente de tipo IA puede requerir la conversión a reparación abierta, siempre que el riesgo quirúrgico sea aceptable.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331.
https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2.
https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com
[209]Perini P, Bianchini Massoni C, Mariani E, et al. Systematic review and meta-analysis of the outcome of different treatments for type 1a endoleak after EVAR. Ann Vasc Surg. 2019 Oct;60:435-46.e1.
http://www.ncbi.nlm.nih.gov/pubmed/31200054?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Extensión de endoprótesis expandida para la misma endofuga tipo I (marcada con un círculo)University of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].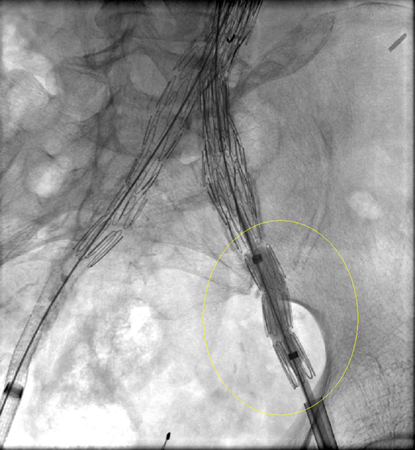 [Figure caption and citation for the preceding image starts]: Resolución de la endofuga tipo I, resuelta con la expansión de la extensiónUniversity of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].
[Figure caption and citation for the preceding image starts]: Resolución de la endofuga tipo I, resuelta con la expansión de la extensiónUniversity of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].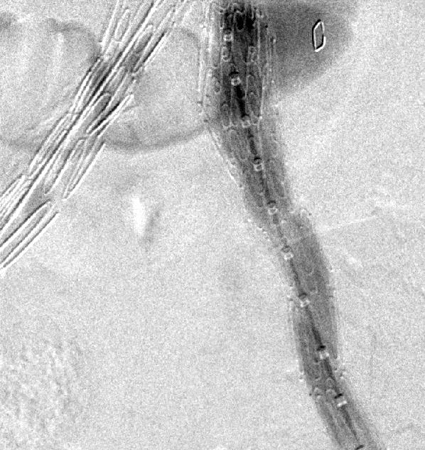
Tipo II: fuga de rama patente.[Figure caption and citation for the preceding image starts]: Fuga interna de tipo II (rodeada) descubierta en tomografía computarizada de seguimientoUniversity of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends]. Puede ocurrir una resolución espontánea, aunque la persistencia puede provocar un crecimiento del saco.[210]Higashiura W, Greenberg RK, Katz E, et al. Predictive factors, morphologic effects, and proposed treatment paradigm for type II endoleaks after repair of infrarenal abdominal aortic aneurysms. J Vasc Interv Radiol. 2007 Aug;18(8):975-81.
http://www.ncbi.nlm.nih.gov/pubmed/17675614?tool=bestpractice.com
Si se observa una endofuga de tipo II u otra alteración preocupante en la imagen por TC con contraste 1 mes después de haber realizado la EVAR, se recomienda realizar un estudio por imágenes postoperatorio a los 6 meses.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2.
https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com
Alrededor del 50% de las fugas internas de tipo II se diagnostican antes de los 30 días de seguimiento; el 40% después de 30 días, y el 8% se diagnostican después de 12 meses de seguimiento.[211]Charisis N, Bouris V, Conway AM, et al. A systematic review and pooled meta-analysis on the incidence and temporal occurrence of type II endoleak following an abdominal aortic aneurysm repair. Ann Vasc Surg. 2021 Aug;75:406-19.
http://www.ncbi.nlm.nih.gov/pubmed/33549794?tool=bestpractice.com
El tratamiento es tema de controversia y se recomienda si persiste a los 6 a 12 meses o si el tamaño de la bolsa de aneurisma aumenta de tal modo que pueden poner en riesgo las zonas de sello proximal y/o distal.[212]Mansueto G, Cenzi D, Scuro A, et al. Treatment of type II endoleak with a transcatheter transcaval approach: results at 1-year follow-up. J Vasc Surg. 2007 Jun;45(6):1120-7.
http://www.ncbi.nlm.nih.gov/pubmed/17543674?tool=bestpractice.com
[213]Baum RA, Stavropoulos SW, Fairman RM, et al. Endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2003 Sep;14(9 Pt 1):1111-7.
http://www.ncbi.nlm.nih.gov/pubmed/14514802?tool=bestpractice.com
[214]Van Marrewijk CJ, Fransen G, Laheij RJ, et al. Is a type II endoleak after EVAR a harbinger of risk? Causes and outcome of open conversion and aneurysm rupture during follow-up. Eur J Vasc Endovasc Surg. 2004 Feb;27(2):128-37.
http://www.ncbi.nlm.nih.gov/pubmed/14718893?tool=bestpractice.com
[215]Harris PL, Vallabhaneni SR, Desgranges P, et al. Incidence and risk factors of late rupture, conversion, and death after endovascular repair of infrarenal aortic aneurysms: the EUROSTAR experience. J Vasc Surg. 2000 Oct;32(4):739-49.
http://www.ncbi.nlm.nih.gov/pubmed/11013038?tool=bestpractice.com
[216]Ultee KHJ, Büttner S, Huurman R, et al. Editor's choice - systematic review and meta-analysis of the outcome of treatment for type II endoleak following endovascular aneurysm repair. Eur J Vasc Endovasc Surg. 2018 Dec;56(6):794-807.
https://www.doi.org/10.1016/j.ejvs.2018.06.009
http://www.ncbi.nlm.nih.gov/pubmed/30104089?tool=bestpractice.com
[217]Smith T, Quencer KB. Best practice guidelines: imaging surveillance after endovascular aneurysm repair. AJR Am J Roentgenol. 2020 May;214(5):1165-74.
https://www.doi.org/10.2214/AJR.19.22197
http://www.ncbi.nlm.nih.gov/pubmed/32130043?tool=bestpractice.com
El tratamiento de elección es la embolización transarterial con espiral, aunque también se han reportado la ligadura laparoscópica de ramas colaterales, la punción translumbar directa del saco, la embolización translumbar y la embolización transcaval transcatéter.[207]Veith FJ, Baum RA, Ohki T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg. 2002 May;35(5):1029-35.
http://www.ncbi.nlm.nih.gov/pubmed/12021724?tool=bestpractice.com
[212]Mansueto G, Cenzi D, Scuro A, et al. Treatment of type II endoleak with a transcatheter transcaval approach: results at 1-year follow-up. J Vasc Surg. 2007 Jun;45(6):1120-7.
http://www.ncbi.nlm.nih.gov/pubmed/17543674?tool=bestpractice.com
[213]Baum RA, Stavropoulos SW, Fairman RM, et al. Endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2003 Sep;14(9 Pt 1):1111-7.
http://www.ncbi.nlm.nih.gov/pubmed/14514802?tool=bestpractice.com
[214]Van Marrewijk CJ, Fransen G, Laheij RJ, et al. Is a type II endoleak after EVAR a harbinger of risk? Causes and outcome of open conversion and aneurysm rupture during follow-up. Eur J Vasc Endovasc Surg. 2004 Feb;27(2):128-37.
http://www.ncbi.nlm.nih.gov/pubmed/14718893?tool=bestpractice.com
[218]Steinmetz E, Rubin BG, Sanchez LA, et al. Type II endoleak after endovascular abdominal aortic aneurysm repair: a conservative approach with selective intervention is safe and cost-effective. J Vasc Surg. 2004 Feb;39(2):306-13.
http://www.ncbi.nlm.nih.gov/pubmed/14743129?tool=bestpractice.com
[219]Baum RA, Cope C, Fairman, et al. Translumbar embolization of type 2 endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2001 Jan;12(1):111-6.
http://www.ncbi.nlm.nih.gov/pubmed/11200344?tool=bestpractice.com
[220]Baum RA, Carpenter JP, Golden MA, et al. Treatment of type 2 endoleaks after endovascular repair of abdominal aortic aneurysms: comparison of transarterial and translumbar techniques. J Vasc Surg. 2002 Jan;35(1):23-9.
http://www.ncbi.nlm.nih.gov/pubmed/11802129?tool=bestpractice.com
[221]Schmid R, Gurke L, Aschwanden M, et al. CT-guided percutaneous embolization of a lumbar artery maintaining a type II endoleak. J Endovasc Ther. 2002 Apr;9(2):198-202.
http://www.ncbi.nlm.nih.gov/pubmed/12010100?tool=bestpractice.com
[222]Chin KM, Lee SQW, Lee HJ, et al. Preservation of stent graft after iatrogenic type III endoleak during open transperitoneal surgical intervention for complicated type II endoleak. Ann Vasc Surg. 2020 Jan;62:496.e1-496.e7.
http://www.ncbi.nlm.nih.gov/pubmed/31394250?tool=bestpractice.com
[223]Li Q, Hou P. Sac embolization and side branch embolization for preventing type II endoleaks after endovascular aneurysm repair: a meta-analysis. J Endovasc Ther. 2020 Feb;27(1):109-16.
https://www.doi.org/10.1177/1526602819878411
http://www.ncbi.nlm.nih.gov/pubmed/31566053?tool=bestpractice.com
[224]Akmal MM, Pabittei DR, Prapassaro T, et al. A systematic review of the current status of interventions for type II endoleak after EVAR for abdominal aortic aneurysms. Int J Surg. 2021 Nov;95:106138.
https://www.doi.org/10.1016/j.ijsu.2021.106138
http://www.ncbi.nlm.nih.gov/pubmed/34637951?tool=bestpractice.com
[225]Yu HYH, Lindström D, Wanhainen A, et al. Systematic review and meta-analysis of prophylactic aortic side branch embolization to prevent type II endoleaks. J Vasc Surg. 2020 Nov;72(5):1783-1792.e1.
https://www.doi.org/10.1016/j.jvs.2020.05.020
http://www.ncbi.nlm.nih.gov/pubmed/32442608?tool=bestpractice.com
[226]Zhang X, Ji L, Chen MY, et al. Transarterial embolization versus translumber embolization for type Ⅱ endoleak after endovascular abdominal aortic aneurysm repair: a meta-analysis. Chin Med Sci J. 2020 Jun 30;35(2):135-41.
https://www.doi.org/10.24920/003618
http://www.ncbi.nlm.nih.gov/pubmed/32684233?tool=bestpractice.com
Puede ocurrir una resolución espontánea, aunque la persistencia puede provocar un crecimiento del saco.[210]Higashiura W, Greenberg RK, Katz E, et al. Predictive factors, morphologic effects, and proposed treatment paradigm for type II endoleaks after repair of infrarenal abdominal aortic aneurysms. J Vasc Interv Radiol. 2007 Aug;18(8):975-81.
http://www.ncbi.nlm.nih.gov/pubmed/17675614?tool=bestpractice.com
Si se observa una endofuga de tipo II u otra alteración preocupante en la imagen por TC con contraste 1 mes después de haber realizado la EVAR, se recomienda realizar un estudio por imágenes postoperatorio a los 6 meses.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2.
https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com
Alrededor del 50% de las fugas internas de tipo II se diagnostican antes de los 30 días de seguimiento; el 40% después de 30 días, y el 8% se diagnostican después de 12 meses de seguimiento.[211]Charisis N, Bouris V, Conway AM, et al. A systematic review and pooled meta-analysis on the incidence and temporal occurrence of type II endoleak following an abdominal aortic aneurysm repair. Ann Vasc Surg. 2021 Aug;75:406-19.
http://www.ncbi.nlm.nih.gov/pubmed/33549794?tool=bestpractice.com
El tratamiento es tema de controversia y se recomienda si persiste a los 6 a 12 meses o si el tamaño de la bolsa de aneurisma aumenta de tal modo que pueden poner en riesgo las zonas de sello proximal y/o distal.[212]Mansueto G, Cenzi D, Scuro A, et al. Treatment of type II endoleak with a transcatheter transcaval approach: results at 1-year follow-up. J Vasc Surg. 2007 Jun;45(6):1120-7.
http://www.ncbi.nlm.nih.gov/pubmed/17543674?tool=bestpractice.com
[213]Baum RA, Stavropoulos SW, Fairman RM, et al. Endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2003 Sep;14(9 Pt 1):1111-7.
http://www.ncbi.nlm.nih.gov/pubmed/14514802?tool=bestpractice.com
[214]Van Marrewijk CJ, Fransen G, Laheij RJ, et al. Is a type II endoleak after EVAR a harbinger of risk? Causes and outcome of open conversion and aneurysm rupture during follow-up. Eur J Vasc Endovasc Surg. 2004 Feb;27(2):128-37.
http://www.ncbi.nlm.nih.gov/pubmed/14718893?tool=bestpractice.com
[215]Harris PL, Vallabhaneni SR, Desgranges P, et al. Incidence and risk factors of late rupture, conversion, and death after endovascular repair of infrarenal aortic aneurysms: the EUROSTAR experience. J Vasc Surg. 2000 Oct;32(4):739-49.
http://www.ncbi.nlm.nih.gov/pubmed/11013038?tool=bestpractice.com
[216]Ultee KHJ, Büttner S, Huurman R, et al. Editor's choice - systematic review and meta-analysis of the outcome of treatment for type II endoleak following endovascular aneurysm repair. Eur J Vasc Endovasc Surg. 2018 Dec;56(6):794-807.
https://www.doi.org/10.1016/j.ejvs.2018.06.009
http://www.ncbi.nlm.nih.gov/pubmed/30104089?tool=bestpractice.com
[217]Smith T, Quencer KB. Best practice guidelines: imaging surveillance after endovascular aneurysm repair. AJR Am J Roentgenol. 2020 May;214(5):1165-74.
https://www.doi.org/10.2214/AJR.19.22197
http://www.ncbi.nlm.nih.gov/pubmed/32130043?tool=bestpractice.com
El tratamiento de elección es la embolización transarterial con espiral, aunque también se han reportado la ligadura laparoscópica de ramas colaterales, la punción translumbar directa del saco, la embolización translumbar y la embolización transcaval transcatéter.[207]Veith FJ, Baum RA, Ohki T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg. 2002 May;35(5):1029-35.
http://www.ncbi.nlm.nih.gov/pubmed/12021724?tool=bestpractice.com
[212]Mansueto G, Cenzi D, Scuro A, et al. Treatment of type II endoleak with a transcatheter transcaval approach: results at 1-year follow-up. J Vasc Surg. 2007 Jun;45(6):1120-7.
http://www.ncbi.nlm.nih.gov/pubmed/17543674?tool=bestpractice.com
[213]Baum RA, Stavropoulos SW, Fairman RM, et al. Endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2003 Sep;14(9 Pt 1):1111-7.
http://www.ncbi.nlm.nih.gov/pubmed/14514802?tool=bestpractice.com
[214]Van Marrewijk CJ, Fransen G, Laheij RJ, et al. Is a type II endoleak after EVAR a harbinger of risk? Causes and outcome of open conversion and aneurysm rupture during follow-up. Eur J Vasc Endovasc Surg. 2004 Feb;27(2):128-37.
http://www.ncbi.nlm.nih.gov/pubmed/14718893?tool=bestpractice.com
[218]Steinmetz E, Rubin BG, Sanchez LA, et al. Type II endoleak after endovascular abdominal aortic aneurysm repair: a conservative approach with selective intervention is safe and cost-effective. J Vasc Surg. 2004 Feb;39(2):306-13.
http://www.ncbi.nlm.nih.gov/pubmed/14743129?tool=bestpractice.com
[219]Baum RA, Cope C, Fairman, et al. Translumbar embolization of type 2 endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2001 Jan;12(1):111-6.
http://www.ncbi.nlm.nih.gov/pubmed/11200344?tool=bestpractice.com
[220]Baum RA, Carpenter JP, Golden MA, et al. Treatment of type 2 endoleaks after endovascular repair of abdominal aortic aneurysms: comparison of transarterial and translumbar techniques. J Vasc Surg. 2002 Jan;35(1):23-9.
http://www.ncbi.nlm.nih.gov/pubmed/11802129?tool=bestpractice.com
[221]Schmid R, Gurke L, Aschwanden M, et al. CT-guided percutaneous embolization of a lumbar artery maintaining a type II endoleak. J Endovasc Ther. 2002 Apr;9(2):198-202.
http://www.ncbi.nlm.nih.gov/pubmed/12010100?tool=bestpractice.com
[222]Chin KM, Lee SQW, Lee HJ, et al. Preservation of stent graft after iatrogenic type III endoleak during open transperitoneal surgical intervention for complicated type II endoleak. Ann Vasc Surg. 2020 Jan;62:496.e1-496.e7.
http://www.ncbi.nlm.nih.gov/pubmed/31394250?tool=bestpractice.com
[223]Li Q, Hou P. Sac embolization and side branch embolization for preventing type II endoleaks after endovascular aneurysm repair: a meta-analysis. J Endovasc Ther. 2020 Feb;27(1):109-16.
https://www.doi.org/10.1177/1526602819878411
http://www.ncbi.nlm.nih.gov/pubmed/31566053?tool=bestpractice.com
[224]Akmal MM, Pabittei DR, Prapassaro T, et al. A systematic review of the current status of interventions for type II endoleak after EVAR for abdominal aortic aneurysms. Int J Surg. 2021 Nov;95:106138.
https://www.doi.org/10.1016/j.ijsu.2021.106138
http://www.ncbi.nlm.nih.gov/pubmed/34637951?tool=bestpractice.com
[225]Yu HYH, Lindström D, Wanhainen A, et al. Systematic review and meta-analysis of prophylactic aortic side branch embolization to prevent type II endoleaks. J Vasc Surg. 2020 Nov;72(5):1783-1792.e1.
https://www.doi.org/10.1016/j.jvs.2020.05.020
http://www.ncbi.nlm.nih.gov/pubmed/32442608?tool=bestpractice.com
[226]Zhang X, Ji L, Chen MY, et al. Transarterial embolization versus translumber embolization for type Ⅱ endoleak after endovascular abdominal aortic aneurysm repair: a meta-analysis. Chin Med Sci J. 2020 Jun 30;35(2):135-41.
https://www.doi.org/10.24920/003618
http://www.ncbi.nlm.nih.gov/pubmed/32684233?tool=bestpractice.com
Tipo III: defecto del injerto con fuga por desgarro del tejido, desconexión del injerto o desintegración del tejido.[206]Schurink GW, Aarts NJ, vanBockel JH. Endoleak after stent-graft treatment of abdominal aortic aneurysm: a meta-analysis of clinical studies. Br J Surg. 1999 May;86(5):581-7. http://www.ncbi.nlm.nih.gov/pubmed/10361173?tool=bestpractice.com [207]Veith FJ, Baum RA, Ohki T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg. 2002 May;35(5):1029-35. http://www.ncbi.nlm.nih.gov/pubmed/12021724?tool=bestpractice.com [227]Kwon J, Dimuzio P, Salvatore D, et al. Incidence of stent graft failure from type IIIB endoleak in contemporary endovascular abdominal aortic aneurysm repair. J Vasc Surg. 2020 Feb;71(2):645-53. https://www.doi.org/10.1016/j.jvs.2019.06.183 http://www.ncbi.nlm.nih.gov/pubmed/31466740?tool=bestpractice.com Se indica la reparación en el momento de su descubrimiento (extensión de la endoprótesis endovascular).[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com [213]Baum RA, Stavropoulos SW, Fairman RM, et al. Endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2003 Sep;14(9 Pt 1):1111-7. http://www.ncbi.nlm.nih.gov/pubmed/14514802?tool=bestpractice.com [217]Smith T, Quencer KB. Best practice guidelines: imaging surveillance after endovascular aneurysm repair. AJR Am J Roentgenol. 2020 May;214(5):1165-74. https://www.doi.org/10.2214/AJR.19.22197 http://www.ncbi.nlm.nih.gov/pubmed/32130043?tool=bestpractice.com [228]Lowe C, Hansrani V, Madan M, et al. Type IIIb endoleak after elective endovascular aneurysm repair: a systematic review. J Cardiovasc Surg (Torino). 2020 Jun;61(3):308-16. http://www.ncbi.nlm.nih.gov/pubmed/29616524?tool=bestpractice.com
Tipo IV: fuga por porosidad de la pared del injerto.[206]Schurink GW, Aarts NJ, vanBockel JH. Endoleak after stent-graft treatment of abdominal aortic aneurysm: a meta-analysis of clinical studies. Br J Surg. 1999 May;86(5):581-7. http://www.ncbi.nlm.nih.gov/pubmed/10361173?tool=bestpractice.com [207]Veith FJ, Baum RA, Ohki T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg. 2002 May;35(5):1029-35. http://www.ncbi.nlm.nih.gov/pubmed/12021724?tool=bestpractice.com Estas fugas son infrecuentes y se autolimitan con endoprótesis más nuevas.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com [213]Baum RA, Stavropoulos SW, Fairman RM, et al. Endoleaks after endovascular repair of abdominal aortic aneurysms. J Vasc Interv Radiol. 2003 Sep;14(9 Pt 1):1111-7. http://www.ncbi.nlm.nih.gov/pubmed/14514802?tool=bestpractice.com
Tipo V (endotensión): la endotensión es un aumento de la presión intracava tras una intervención quirúrgica endovascular sin que se visualice una fuga interna en la tomografía computarizada con contraste diferido. Menos frecuente con los injertos de nueva generación.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com No hay método estandarizado para medir la endotensión ni consenso sobre la terapia indicada en ausencia de agrandamiento de aneurisma; sin embargo, se sugiere realizar un tratamiento de la endotensión para evitar la rotura del aneurisma en pacientes seleccionados con expansión continua de aneurisma.[76]Chaikof EL, Dalman RL, Eskandari MK, et al. The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. J Vasc Surg. 2018 Jan;67(1):2-77.e2. https://www.jvascsurg.org/article/S0741-5214(17)32369-8/fulltext http://www.ncbi.nlm.nih.gov/pubmed/29268916?tool=bestpractice.com [207]Veith FJ, Baum RA, Ohki T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg. 2002 May;35(5):1029-35. http://www.ncbi.nlm.nih.gov/pubmed/12021724?tool=bestpractice.com [217]Smith T, Quencer KB. Best practice guidelines: imaging surveillance after endovascular aneurysm repair. AJR Am J Roentgenol. 2020 May;214(5):1165-74. https://www.doi.org/10.2214/AJR.19.22197 http://www.ncbi.nlm.nih.gov/pubmed/32130043?tool=bestpractice.com
reducción del riesgo cardiovascular preoperatorio
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
El tratamiento preoperatorio de los factores de riesgo cardiovascular modificables mejora la supervivencia a largo plazo después de la reparación del AAA.[196]Khashram M, Williman JA, Hider PN, et al. Management of modifiable vascular risk factors improves late survival following abdominal aortic aneurysm repair: a systematic review and meta-analysis. Ann Vasc Surg. 2017 Feb;39:301-11. http://www.ncbi.nlm.nih.gov/pubmed/27666804?tool=bestpractice.com
Se debe animar a los pacientes a dejar de fumar y ofrecerles tratamiento farmacológico (tratamiento sustitutivo con nicotina, nortriptilina y bupropión) o asesoramiento para ayudarles a conseguirlo si es necesario.[1]Dehlin JM, Upchurch GR. Management of abdominal aortic aneurysms. Curr Treat Options Cardiovasc Med. 2005 Jun;7(2):119-30.
http://www.ncbi.nlm.nih.gov/pubmed/15935120?tool=bestpractice.com
[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482.
https://www.doi.org/10.1161/CIR.0000000000001106
http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
[13]Zankl AR, Schumacher H, Krumsdorf U, et al. Pathology, natural history and treatment of abdominal aortic aneurysms. Clin Res Cardiol. 2007 Mar;96(3):140-51.
http://www.ncbi.nlm.nih.gov/pubmed/17180573?tool=bestpractice.com
[15]Singh K, Bønaa H, Jacobsen BK, et al. Prevalence of and risk factors for abdominal aortic aneurysms in a population-based study: the Tromsø Study. Am J Epidemiol. 2001 Aug 1;154(3):236-44.
https://academic.oup.com/aje/article/154/3/236/125840
http://www.ncbi.nlm.nih.gov/pubmed/11479188?tool=bestpractice.com
[22]Lederle FA, Johnson GR, Wilson SE, et al; Aneurysm Detection and Management (ADAM) Veterans Affairs Cooperative Study Group. Prevalence and associations of abdominal aortic aneurysm detected through screening. Ann Intern Med. 1997 Mar 15;126(6):441-9.
http://www.ncbi.nlm.nih.gov/pubmed/9072929?tool=bestpractice.com
[23]Wilmink TB, Quick CR, Day NE. The association between cigarette smoking and abdominal aortic aneurysms. J Vasc Surg. 1999 Dec;30(6):1099-105.
http://www.ncbi.nlm.nih.gov/pubmed/10587395?tool=bestpractice.com
[136]Hartmann-Boyce J, Chepkin SC, Ye W, et al. Nicotine replacement therapy versus control for smoking cessation. Cochrane Database Syst Rev. 2018 May 31;5:CD000146.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000146.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/29852054?tool=bestpractice.com
[137]Rigotti NA, Clair C, Munafò MR, et al. Interventions for smoking cessation in hospitalised patients. Cochrane Database Syst Rev. 2012 May 16;(5):CD001837.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001837.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/22592676?tool=bestpractice.com
[138]Howes S, Hartmann-Boyce J, Livingstone-Banks J, et al. Antidepressants for smoking cessation. Cochrane Database Syst Rev. 2020 Apr 22;(4):CD000031.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000031.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/32319681?tool=bestpractice.com
[  ]
What are the effects of adding bupropion or fluoxetine to other treatments compared with using other treatments alone for people trying to quit smoking?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4337/fullMostrarme la respuesta
]
What are the effects of adding bupropion or fluoxetine to other treatments compared with using other treatments alone for people trying to quit smoking?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4337/fullMostrarme la respuesta
El entrenamiento preoperatorio con ejercicios redujo las complicaciones cardíacas posquirúrgicas en un pequeño ensayo aleatorizado controlado (EAC) de pacientes sometidos a reparación abierta o endovascular del AAA, aunque una revisión de la Cochrane y una revisión sistemática independiente de la prehabilitación (entrenamiento con ejercicios) antes de la cirugía del AAA no mostraron ningún beneficio en los resultados.[197]Barakat HM, Shahin Y, Khan JA, et al. Preoperative supervised exercise improves outcomes after elective abdominal aortic aneurysm repair: a randomized controlled trial. Ann Surg. 2016 Jul;264(1):47-53. http://www.ncbi.nlm.nih.gov/pubmed/26756766?tool=bestpractice.com [198]Fenton C, Tan AR, Abaraogu UO, et al. Prehabilitation exercise therapy before elective abdominal aortic aneurysm repair. Cochrane Database Syst Rev. 2021 Jul 8;7(7):CD013662. https://www.doi.org/10.1002/14651858.CD013662.pub2 http://www.ncbi.nlm.nih.gov/pubmed/34236703?tool=bestpractice.com [199]Bonner RJ, Wallace T, Jones AD, et al. The content of pre-habilitative interventions for patients undergoing repair of abdominal aortic aneurysms and their effect on post-operative outcomes: a systematic review. Eur J Vasc Endovasc Surg. 2021 May;61(5):756-65. https://www.doi.org/10.1016/j.ejvs.2021.01.043 http://www.ncbi.nlm.nih.gov/pubmed/33678532?tool=bestpractice.com Aunque el entrenamiento preoperatorio con ejercicios puede ser beneficioso para los pacientes sometidos a reparación de AAA, es necesario realizar pruebas diagnósticas adicionales con EAC antes de recomendarlo de forma más generalizada.[200]Wee IJY, Choong AMTL. A systematic review of the impact of preoperative exercise for patients with abdominal aortic aneurysm. J Vasc Surg. 2020 Jun;71(6):2123-31.e1. https://www.doi.org/10.1016/j.jvs.2018.09.039 http://www.ncbi.nlm.nih.gov/pubmed/30606665?tool=bestpractice.com
El uso perioperatorio de estatinas ralentiza el crecimiento del aneurisma, reduce el riesgo de rotura y disminuye la mortalidad por reparación o rotura del AAA.[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com El tratamiento de estatinas debe iniciarse al menos 1 mes antes de la cirugía para reducir la morbilidad y la mortalidad cardiovascular, y continuarse indefinidamente.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [141]Risum Ø, Sandven I, Sundhagen JO, et al. Editor's choice - effect of statins on total mortality in abdominal aortic aneurysm repair: a systematic review and meta-analysis. Eur J Vasc Endovasc Surg. 2021 Jan;61(1):114-20. https://www.doi.org/10.1016/j.ejvs.2020.08.007 http://www.ncbi.nlm.nih.gov/pubmed/32928667?tool=bestpractice.com
Los pacientes con AAA presentan un mayor riesgo de sufrir eventos cardiovasculares adversos graves. La evidencia es limitada, pero en ausencia de contraindicaciones, los pacientes con AAA deben recibir un tratamiento antiplaquetario único (ácido acetilsalicílico o clopidogrel).[5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com [142]Aboyans V, Bauersachs R, Mazzolai L, et al. Antithrombotic therapies in aortic and peripheral arterial diseases in 2021: a consensus document from the ESC working group on aorta and peripheral vascular diseases, the ESC working group on thrombosis, and the ESC working group on cardiovascular pharmacotherapy. Eur Heart J. 2021 Oct 14;42(39):4013-24. https://www.doi.org/10.1093/eurheartj/ehab390 http://www.ncbi.nlm.nih.gov/pubmed/34279602?tool=bestpractice.com Esto debe continuar durante el periodo perioperatorio.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com
La hipertensión debe controlarse para reducir la morbilidad y la mortalidad cardiovascular.[3]Wanhainen A, Van Herzeele I, Bastos Goncalves F, et al. Editor's choice -- European Society for Vascular Surgery (ESVS) 2024 clinical practice guidelines on the management of abdominal aorto-iliac artery aneurysms. Eur J Vasc Endovasc Surg. 2024 Feb;67(2):192-331. https://www.ejves.com/article/S1078-5884(23)00889-4/fulltext http://www.ncbi.nlm.nih.gov/pubmed/38307694?tool=bestpractice.com [5]Isselbacher EM, Preventza O, Hamilton Black J 3rd, et al. 2022 ACC/AHA guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022 Dec 13;146(24):e334-e482. https://www.doi.org/10.1161/CIR.0000000000001106 http://www.ncbi.nlm.nih.gov/pubmed/36322642?tool=bestpractice.com
antibioticoterapia perioperatoria
Se recomienda el tratamiento para TODOS LOS pacientes en el grupo de pacientes seleccionados
Se administra antibioticoterapia perioperatoria. La cobertura con antibióticos de amplio espectro es necesaria y se realiza conforme a los protocolos locales.

Seleccione un grupo de pacientes para consultar nuestras recomendaciones
Tenga en cuenta que las formulaciones/vías y dosis pueden diferir entre los nombres y marcas de los fármacos, las fórmulas de los fármacos o las localizaciones. Las recomendaciones de tratamiento son específicas para cada grupo de pacientes. Véase el descargo de responsabilidad
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad