Etiología
La sepsis es la respuesta sistémica a la infección. Por lo tanto, la etiología primaria puede atribuirse al agente patógeno que provocó la infección y a la respuesta del huésped. Si bien cualquier infección puede provocar sepsis, los agentes patógenos más comunes son las bacterias, los virus o los hongos. El tipo de agente patógeno varía en función de numerosos factores del huésped, incluidas la edad, la comorbilidad y la ubicación geográfica. A continuación se enumeran los agentes patógenos típicos/importantes por grupo de pacientes.
Sepsis neonatal de inicio temprano (SIT):[9][20][21][22]
Se define como sepsis neonatal que se presenta durante las primeras 72 horas de vida.
Los estreptococos del grupo B (EGB) y los bacilos gramnegativos (especialmente Escherichia coli) son, con diferencia, los agentes patógenos causales más comunes en la SIT.
Staphylococcus aureus y los estafilococos coagulasa negativos, Haemophilus influenzae y los enterococos conforman el resto de las etiologías bacterianas en la SIT.
Listeria monocytogenes es una infección poco frecuente, pero tiene una propensión desproporcionada a infectar a mujeres embarazadas y a sus fetos. Puede causar SIT o sepsis neonatal de inicio tardío.
Sepsis neonatal de inicio tardío (SAT):[10][20][23]
Se define como sepsis neonatal que se presenta después de las primeras 72 horas y hasta el primer mes de vida.
Los estafilococos coagulasa-negativos son la causa más común de pérdidas de vidas humanas debido a la alta incidencia en la infección asociada a catéteres vasculares en pacientes neonatales hospitalizados.
También puede ser causada por los mismos organismos responsables de la SIT.
Lactantes y niños pequeños:[4][14][24]
Streptococcus pneumoniae sigue siendo una de las principales causas de infección bacteriana invasiva durante la infancia
Neisseria meningitidis se presenta con una distribución etaria bimodal que afecta a niños pequeños y adolescentes. Es menos común desde la incorporación de la vacunación.
S aureus y los estreptococos del grupo A pueden causar sepsis en niños anteriormente sanos. En la temporada 2022-2023 se informaron en Inglaterra casos de escarlatina y de enfermedad por estreptococos invasivos del grupo A (iGAS) más elevados de lo normal.[25]
H influenzae tipo B es una causa importante de sepsis en el mundo, pero poco frecuente en el mundo desarrollado gracias a la vacunación.
Bordetella pertussis, si bien es poco frecuente, puede causar una enfermedad grave en lactantes pequeños antes de la vacunación primaria.
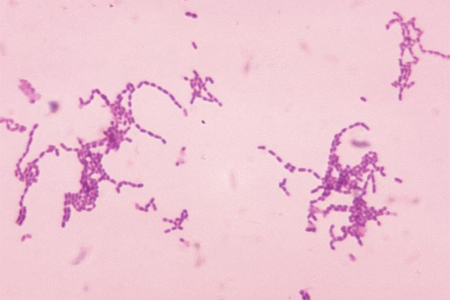
Los datos sobre organismos de infección específicos en entornos con pocos recursos son menos sólidos, pero la diarrea y la neumonía son las infecciones más comunes (y las causas de muerte más comunes).[Figure caption and citation for the preceding image starts]: Microfotografía de tinción de Gram de especies de la bacteria StreptococcusImagen cedida por el Centers for Disease Control and Prevention Image Library de EE. UU. [Citation ends].
Lactantes y niños hospitalizados:[26]
La causa de infección intrahospitalaria dependerá de la epidemiología bacteriana local.
Los estafilococos coagulasa negativos generalmente están asociados a infección del catéter vascular.
S aureus resistente a la meticilina (SARM) es menos frecuente en el Reino Unido en comparación con Estados Unidos
Microorganismos gramnegativos como Pseudomonas aeruginosa, Klebsiella, E coli y especies de Acinetobacter.
Asplénico o asplenia funcional:[27][28]
Sepsis por Salmonella, incluida la osteomielitis por Salmonella en anemia falciforme
Otros microorganismos encapsulados (por ejemplo, S pneumoniae, H influenzae).
Enfermedades transmitidas por los mosquitos y otras enfermedades tropicales:[29]
La malaria (Plasmodium falciparum), el virus del dengue y Burkholderia pseudomallei (meliodosis) son causas importantes de sepsis en zonas endémicas.
Otros microorganismos:[15]
Los agentes patógenos fúngicos (p. ej., especies de Candida, especies de Aspergillus) y virales (p. ej., gripe, virus sincitial respiratorio, metaneumovirus humano, varicela y virus herpes simple) dan cuenta de hasta el 5.3% y el 2.9% de las sepsis en niños.
Fisiopatología
La respuesta normal del huésped a la infección es un proceso inflamatorio destinado a localizar y controlar la infección. La respuesta inflamatoria se desencadena cuando células inmunitarias innatas (p. ej., macrófagos) reconocen el agente patógeno invasor. Por ejemplo, los receptores de las células inmunitarias innatas reconocen los lipopolisacáridos de las bacterias gramnegativas.[30] Después de adherirse a estos sitios, las células inmunitarias se activan y segregan citocinas proinflamatorias, responsables de reclutar células polimorfonucleares al sitio de la infección. Estas células polimorfonucleares liberan citocinas proinflamatorias que producen vasodilatación y permeabilidad vascular (extravasación capilar).[30] En la respuesta normal del huésped, esta respuesta proinflamatoria está regulada y se localiza mediante una respuesta antinflamatoria simultánea.[30] La sepsis se presenta cuando esta respuesta normal proinflamatoria del huésped excede sus restricciones homeostáticas usuales y se convierte en un proceso generalizado, lo que produce inflamación lejos de la fuente de infección.
Aunque este modelo de sepsis es intuitivo, los resultados de las nuevas investigaciones sugieren que puede ser una simplificación excesiva. La fisiopatología puede incluir procesos como la disfunción del endotelio, la muerte celular, el desajuste bioenergético y la inmunoparálisis.
Disfunción endotelial:
El endotelio rodea todo el aparato cardiovascular y es responsable de diversas respuestas fisiológicas (p. ej., control del tono vascular y la regulación de la coagulación) para mantener correctamente el flujo sanguíneo y el suministro de oxígeno a los órganos. Las interrupciones y aberraciones de la función endotelial inciden en muchas de las manifestaciones cardiovasculares de sepsis.[30] Las citocinas inflamatorias y las células efectoras (p. ej., los neutrófilos) se involucran e interaccionan con el endotelio durante la sepsis; el endotelio activado resultante ejecuta entonces muchos de los efectos sistémicos. Estos cambios incluyen extravasación capilar generalizada (es decir, permeabilidad capilar aumentada), que, a su vez, genera edema en los tejidos y una reducción del volumen circulante. Esto puede provocar, o exacerbar, el shock (a causa de la hipovolemia) y la disfunción orgánica.[30] El endotelio es responsable de liberar óxido nítrico, un potente vasodilatador. La función del óxido nítrico en personas sanas es regular el flujo sanguíneo regional de acuerdo a los cambios en la demanda. En la sepsis, el endotelio activado dañado puede liberar grandes cantidades de óxido nítrico sistémicamente y provocar una vasodilatación generalizada, así como disminución de la resistencia vascular.[31] Por lo general, la coagulación se ve afectada por la sepsis, debido a la activación de las vías de coagulación que provoca el endotelio activado.[30] El panorama típico es una coagulación intravascular diseminada (es decir, consumo de plaquetas y coagulación prolongada). La manifestación clínica es una combinación de disfunción orgánica isquémica, a causa de la coagulación intravascular, y sangrado.
Además de los efectos microcirculatorios de la sepsis, un efecto directo sobre el corazón de los mediadores circulantes puede reducir el rendimiento del miocardio, contribuyendo a la disminución del gasto cardíaco y al shock.[32]
Muerte celular:
La naturaleza exacta de la muerte celular en la sepsis es un área de investigación constante y todavía requiere una mayor delineación. En términos generales, la muerte celular se produce durante la sepsis debido a una combinación de necrosis y apoptosis. La contribución exacta de cada uno de estos mecanismos a la muerte celular en la sepsis es materia de debate.[33]
Se han descrito aberraciones de los mecanismos apoptóticos en varios tipos de células en la sepsis. La apoptosis retardada en células inmunitarias innatas (p. ej., neutrófilos y macrófagos) puede causar el retraso de la resolución de las respuestas proinflamatorias. Por el contrario, se describió un aumento en las tasas de apoptosis en los linfocitos en pacientes sépticos, lo que puede resultar en una inmunosupresión adquirida.[33]
Trastorno bioenergético:
La disfunción orgánica en la sepsis no puede atribuirse en su totalidad a los efectos circulatorios descritos anteriormente. Otra característica del shock séptico es la insuficiencia bioenergética generalizada que se produce como consecuencia de un menor consumo de oxígeno por parte de las células. Esto puede ser el resultado de la inhibición directa de la función mitocondrial (es decir, la respiración) a través de mediadores de inflamación, tales como el óxido nítrico.[34]
El origen de esta respuesta no está claro, pero se ha propuesto que la disfunción mitocondrial y la insuficiencia energética resultante de la sepsis constituyen una respuesta adaptativa.[35]
Inmunoparálisis:
Además de la respuesta proinflamatoria sistémica, la respuesta del huésped en la sepsis también incluye una respuesta antinflamatoria concomitante. Esta se conoce como el síndrome de respuesta antinflamatoria compensatoria.[36]
La procedencia evolutiva de esta respuesta puede ser una respuesta contrarregulatoria, o adquirida, que permite restringir y controlar la respuesta proinflamatoria.[37]
Un efecto putativo del síndrome de respuesta antinflamatoria compensatoria es una modulación del sistema inmune del huésped, conocida como inmunoparálisis, que puede aumentar la susceptibilidad del huésped a infecciones secundarias.[38][39]
Los datos sugieren que existe una considerable heterogeneidad en las respuestas del huésped de los pacientes. Esta heterogeneidad se aplica al equilibrio de los procesos pro y antinflamatorios, y la naturaleza de los cambios humorales y celulares.[40]
Clasificación
Clasificación de la sepsis neonatal
La sepsis neonatal se define como un síndrome clínico de la sepsis, y/o aislamiento de un agente patógeno en el flujo sanguíneo, en un lactante durante los primeros 28 días de vida.[8] Los síntomas y signos clínicos con frecuencia son menos evidentes o más sutiles que en niños mayores. La sepsis en recién nacidos generalmente se clasifica en función del momento del inicio en relación con el nacimiento:
Sepsis neonatal de inicio temprano: sepsis neonatal durante las primeras 72 horas de vida[9]
La sepsis neonatal de inicio tardío (SIT): sepsis neonatal que se presenta después de las primeras 72 horas.[10]
Clasificación por grupo etario
A los fines de una clasificación coherente, se utilizan los siguientes grupos etarios para hacer referencia a los rangos normales de variables fisiológicas y valores de laboratorio:[3]
Recién nacido: de 0 días a 1 semana
Neonato: de 0 días a 1 mes
Lactante: de 1 mes a <2 años
Niño pequeño y en edad preescolar: de ≥2 años a <6 años
Niño en edad escolar: de ≥6 años a <13 años
Adolescentes y adultos jóvenes: de ≥13 años <18 años.
Tenga en cuenta que los lactantes prematuros no están clasificados en este esquema de edades.
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad