Etiologia
A etiologia da doença de Crohn (DC) permanece indefinida, com vários estudos sugerindo que fatores genéticos e ambientais estejam envolvidos.
Fatores genéticos
Estudos de associação genômica ampla identificaram mais de 71 diferentes loci de susceptibilidade genética, com as associações mais fortes sendo entre o CARD15 (família de domínio de recrutamento de caspase, membro 15), que codifica a proteína de reconhecimento de patógenos NOD2 (domínio de oligomerização de ligação de nucleotídeos contendo 2) e outros loci, como o locus IBD5, o gene da autofagia ATG16L1 (ATG16 autophagy 16-like 1) e o receptor da interleucina 23.[22][23][24] O genótipo também pode influenciar a distribuição da DC.[25]
Os loci de suscetibilidade e fatores de risco genéticos identificados representam <20% do risco hereditário de doença inflamatória intestinal.[26][27][28]
Fatores ambientais
Incluem tabagismo, pílula contraceptiva oral, anti-inflamatórios não esteroidais, exposição a antibióticos, dieta (poucas frutas, poucos vegetais, baixo teor de fibras, alto teor de açúcar refinado, alimentos ultraprocessados), estilo de vida sedentário e não ter recebido aleitamento materno.[1][19][29][30][31][32][33][34]
Espécie Campylobacter foi associada com a doença inflamatória intestinal incidente e ativa, incluindo DC.[35][36]
Alguns estudos sugerem que a Mycobacterium avium paratuberculosis pode contribuir para o aumento do risco de DC.[37] No entanto, uma associação coincidente não foi descartada.[38]
A deficiência de vitamina D e a deficiência de zinco podem complicar a DC; uma relação causal não foi estabelecida.[32]
Fisiopatologia
Teorias atuais sobre a fisiopatologia da doença de Crohn (DC) indicam que fatores infecciosos, imunológicos, ambientais, alimentares e psicossociais desempenham um papel em um indivíduo suscetível genética e imunologicamente.[18][19][31][32][39][40][41][42]
A lesão inicial começa como um infiltrado inflamatório ao redor das criptas intestinais que, subsequentemente, evolui para ulceração da mucosa superficial. A inflamação evolui comprometendo camadas mais profundas e forma granulomas não caseosos. Esses granulomas afetam todas as camadas da parede intestinal e os linfonodos mesentéricos e regionais. O achado desses granulomas é altamente sugestivo da DC, embora sua ausência não descarte o diagnóstico.[43][44]
Dentre os achados endoscópicos iniciais estão hiperemia e edema da mucosa inflamada. Evolui para úlceras profundas distintas localizadas em direção transversal e longitudinal, criando um aspecto pavimentoso. Essas lesões são separadas pela mucosa intestinal normal de maneira descontínua (lesões descontínuas e segmentares [skip lesion]).[5][Figure caption and citation for the preceding image starts]: vista endoscópica da ileíte de CrohnFornecido pelo Dr. Wissam Bleibel, Dr. Bishal Mainali, Dr. Chandrashekhar Thukral e Dr. Mark A. Peppercorn, os autores anteriores deste tópico [Citation ends].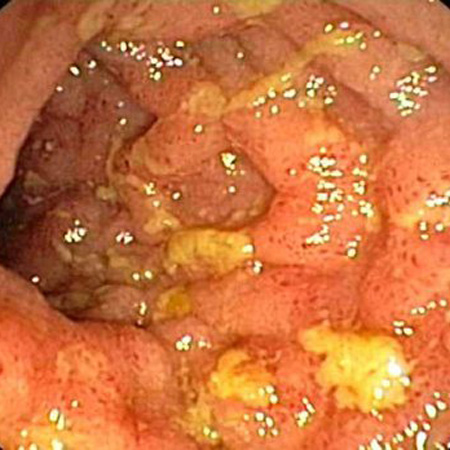 [Figure caption and citation for the preceding image starts]: visão endoscópica de íleo terminal normalDo acervo pessoal de Dr. Charlotte Ford, North Middlesex Hospital Trust, Londres, Reino Unido [Citation ends].
[Figure caption and citation for the preceding image starts]: visão endoscópica de íleo terminal normalDo acervo pessoal de Dr. Charlotte Ford, North Middlesex Hospital Trust, Londres, Reino Unido [Citation ends].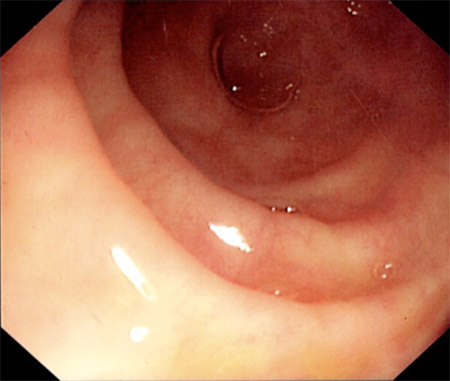
A inflamação transmural aguda resulta em obstrução intestinal devido a edema de mucosa associado a espasmo. A inflamação transmural crônica torna a parede do intestino espessa e causa cicatrização, estreitamento luminal e formação de estenose. Isso pode causar fistulização, formação de tratos sinusais, perfuração e/ou formação de abscesso. A inflamação crônica também danifica a mucosa intestinal, resultando em baixa capacidade absortiva. Isso pode causar desnutrição, desidratação e deficiências de vitaminas e nutrientes.
O envolvimento do íleo terminal interfere na absorção do ácido biliar, que causa esteatorreia, deficiência de vitamina lipossolúvel e formação de cálculos biliares.[45] O excesso de gordura nas fezes liga-se ao cálcio, aumentando a absorção de oxalato e predispondo à formação de nefrolitíase de oxalato.[1][5][41][46][47][48]
Além das manifestações relacionadas ao trato gastrointestinal, a DC pode envolver vários órgãos e sistemas extraintestinais, inclusive pele, articulações, boca, olhos, fígado e ductos biliares.[5][6][7][8] Alguns desses distúrbios têm mecanismos autoimunes.[5][6]
Classificação
Classificação de Viena da doença de Crohn (DC)[3]
Classifica pacientes com DC em 24 subgrupos. Utilizada principalmente para fins de pesquisa.
Idade no diagnóstico - primeira vez em que o diagnóstico é estabelecido definitivamente por radiologia, endoscopia, patologia ou cirurgia.
A1 <40 anos de idade.
A2 40 anos de idade ou mais.
Localização - extensão máxima do envolvimento da doença em qualquer momento antes da primeira ressecção. Com envolvimento mínimo de um local, trata-se de lesão aftosa ou ulceração. É necessário um exame do intestino delgado e do intestino grosso para classificação.
L1 - íleo terminal - limitado ao íleo terminal, com ou sem acometimento de ceco.
L2 - cólon - qualquer localização no cólon entre o ceco e o reto, sem envolvimento do intestino delgado ou do trato gastrointestinal superior.
L3 - ileocolônica - doença do íleo e de qualquer localização entre o cólon ascendente e o reto.
L4 - trato gastrointestinal superior - qualquer doença proximal ao íleo terminal (excluindo a boca), independentemente de envolvimento adicional do íleo terminal ou do cólon.
Comportamento
B1 - sem estenose, não penetrante.
B2 - estenose - estreitamento luminal constante demonstrado por métodos radiológicos, endoscópicos ou cirúrgico-patológicos, com dilatação pré-estenótica ou sinais/sintomas obstrutivos, sem presença de doença penetrante, em qualquer momento na evolução da doença.
B3 - penetrante - ocorrência de fístulas intra-abdominais ou perianais, massas inflamatórias e/ou abscessos em qualquer momento na evolução da doença. Úlceras perianais estão incluídas. Complicações intra-abdominais pós-operatórias e acrocórdons estão descartadas.
Classificação de Montreal da DC[4]
A revisão de Montreal da classificação de Viena não altera os três parâmetros predominantes, mas introduz modificações em cada categoria para possibilitar: início precoce; doença do trato gastrointestinal superior coexistente com doença mais distal; separação da doença perianal em uma subclassificação; um tempo estipulado a ser definido antes que o comportamento da doença seja classificado.
Idade ao diagnóstico
A1 abaixo de 16 anos
A2 entre 17 e 40 anos
A3 acima de 40 anos
Localização
L1 ileal
L2 colônica
L3 ileocolônica
L4 doença superior isolada (L4 é um modificador que pode ser acrescentado a L1 a L3 quando houver doença do trato gastrointestinal superior concomitante).
Comportamento
B1 - sem estenose, não penetrante
B2 - com estenose
B3 - penetrante
P modificador de doença periférica (acrescentado a B1 a B3 quando houver doença perianal concomitante).
O uso deste conteúdo está sujeito ao nosso aviso legal