Câncer de tireoide
- Visão geral
- Teoria
- Diagnóstico
- Tratamento
- ACOMPANHAMENTO
- Recursos
Algoritmo de tratamento
Observe que as formulações/vias e doses podem diferir entre nomes e marcas de medicamentos, formulários de medicamentos ou localidades. As recomendações de tratamento são específicas para os grupos de pacientes:ver aviso legal
papilar, folicular ou oncocítico
vigilância ativa ou cirurgia (lobectomia ou tireoidectomia total ± dissecção da região central do pescoço)
Para pacientes com tumores de risco muito baixo (por exemplo, microcarcinomas papilares unifocais [≤1 cm] sem evidência de extensão extracapsular ou metástases linfonodais), pode ser considerada vigilância ativa com acompanhamento ultrassonográfico da tireoide e linfonodos cervicais a cada 6-12 meses.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [59]National Institute for Health and Care Excellence. Thyroid cancer: assessment and management. Dec 2022 [internet publication]. https://www.nice.org.uk/guidance/ng230 [66]Tuttle RM, Alzahrani AS. Risk stratification in differentiated thyroid cancer: from detection to final follow-up. J Clin Endocrinol Metab. 2019 Mar 15;104(9):4087-100. https://academic.oup.com/jcem/article/104/9/4087/5380478 http://www.ncbi.nlm.nih.gov/pubmed/30874735?tool=bestpractice.com [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer [70]Saravana-Bawan B, Bajwa A, Paterson J, et al. Active surveillance of low-risk papillary thyroid cancer: a meta-analysis. Surgery. 2020 Jan;167(1):46-55. http://www.ncbi.nlm.nih.gov/pubmed/31526581?tool=bestpractice.com
A orientação não recomenda rotineirament aspiração com agulha fina (AAF) para um diagnóstico citológico nos nódulos menores que 1 cm com características de baixo risco; no entanto, essa política varia internacionalmente, com alguns países realizando a AAF e citologia para os nódulos suspeitos antes de oferecerem vigilância ativa.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [71]Ito Y, Miyauchi A, Oda H. Low-risk papillary microcarcinoma of the thyroid: a review of active surveillance trials. Eur J Surg Oncol. 2018 Mar;44(3):307-15. https://www.ejso.com/article/S0748-7983(17)30370-0/fulltext http://www.ncbi.nlm.nih.gov/pubmed/28343733?tool=bestpractice.com
A vigilância ativa pode ser a opção preferencial em pacientes idosos e naqueles com alto risco cirúrgico.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer
A transição para a cirurgia durante a vigilância ativa é indicada se o paciente solicitar cirurgia ou se houver alterações críticas (por exemplo, novas metástases de linfonodos comprovadas por biópsia; metástases à distância; invasão do nervo laríngeo recorrente, traqueia ou esôfago; evidência radiológica de extensão extratireoidiana; crescimento do câncer de 3 mm em qualquer dimensão ou aumento de 50% no volume).[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [71]Ito Y, Miyauchi A, Oda H. Low-risk papillary microcarcinoma of the thyroid: a review of active surveillance trials. Eur J Surg Oncol. 2018 Mar;44(3):307-15. https://www.ejso.com/article/S0748-7983(17)30370-0/fulltext http://www.ncbi.nlm.nih.gov/pubmed/28343733?tool=bestpractice.com
Para todos os outros tipos de câncer de tireoide, a cirurgia geralmente é recomendada para o tratamento inicial.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [59]National Institute for Health and Care Excellence. Thyroid cancer: assessment and management. Dec 2022 [internet publication]. https://www.nice.org.uk/guidance/ng230 [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer A tireoidectomia total é considerada o tratamento cirúrgico padrão. No entanto, em pacientes com tumor entre 1 cm e 4 cm de diâmetro sem extensão extratireoidiana e sem evidência clínica de metástases linfonodais, a lobectomia pode ser considerada como procedimento cirúrgico inicial.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com É importante que os pacientes entendam que os achados intraoperatórios durante a lobectomia podem precisar ser completados por uma tireoidectomia total (tireoidectomia completa).[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
A cirurgia (por exemplo, tireoidectomia total ou lobectomia) é necessária para confirmar (histologicamente) o diagnóstico de carcinoma folicular ou oncocítico porque a citologia por AAF não diferencia, de maneira confiável, entre adenoma (benigno) folicular ou concoítico e carcinoma.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
Caso o carcinoma folicular ou oncocítico invasivo seja diagnosticado após a lobectomia inicial, a tireoidectomia completa subsequente pode ser necessária, dependendo do nível de invasão do tumor.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
A tireoidectomia completa é necessária se os pacientes tiverem carcinoma invasivo folicular ou oncocítico: amplamente invasivo (invasão macroscópica da glândula tireoide com ou sem tecidos moles e vasos sanguíneos adjacentes), ou angioinvasivo encapsulado com envolvimento de ≥4 vasos sanguíneos.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
Normalmente, o monitoramento da doença é preferível em pacientes com carcinoma folicular ou oncocítico invasivo que é: minimamente invasivo (tumor encapsulado com invasão capsular microscópica e sem invasão vascular), ou angioinvasivo encapsulado com envolvimento de <4 vasos sanguíneos.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
As complicações da tireoidectomia total incluem um aumento do risco de dano do nervo laríngeo recorrente ou hipoparatireoidismo.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx O risco de hipoparatireoidismo permanente é maior para tireoidectomia total que para tireoidectomia subtotal. O paciente deve ser encaminhado para um cirurgião experiente.
A dissecção da região central do pescoço terapêutica para pacientes com linfonodos centrais clinicamente envolvidos deve acompanhar a tireoidectomia total para fornecer a eliminação da doença na região central do pescoço.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com A dissecção do pescoço central profilática é controversa.[69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer Em alguns centros é recomendado, mas a redução da recorrência locorregional é acompanhada de aumento da taxa de efeitos adversos pós-operatórios.[74]Chen L, Wu YH, Lee CH, et al. Prophylactic central neck dissection for papillary thyroid carcinoma with clinically uninvolved central neck lymph nodes: a systematic review and meta-analysis. World J Surg. 2018 Sep;42(9):2846-57. http://www.ncbi.nlm.nih.gov/pubmed/29488066?tool=bestpractice.com
Supressão do TSH
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
A tireoidectomia total requer terapia de reposição de hormônio tireoidiano (por exemplo, levotiroxina).
Como o hormônio estimulante da tireoide (TSH) circulante estimula a proliferação em tireócitos normais e na maioria das células de câncer de tireoide, são usadas doses supressoras de TSH na terapia com hormônio tireoidiano.[14]Cabanillas ME, McFadden DG, Durante C. Thyroid cancer. Lancet. 2016 Dec 3;388(10061):2783-95. http://www.ncbi.nlm.nih.gov/pubmed/27240885?tool=bestpractice.com
O uso da supressão do hormônio tireoidiano deve ser baseado no risco inicial da doença e na avaliação contínua do risco do estado da doença (consulte Critérios de diagnóstico para estratificação de risco). A menor quantidade possível de hormônio tireoidiano deve ser usada.[72]Biondi B, Cooper DS. Thyroid hormone suppression therapy. Endocrinol Metab Clin North Am. 2019 Mar;48(1):227-37. http://www.ncbi.nlm.nih.gov/pubmed/30717904?tool=bestpractice.com
Em pacientes com doença de alto risco, recomenda-se manter um nível sérico de TSH <0.1 mUI/L.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com Manter um nível de TSH sérico <0.1 mUI/L (mas não necessariamente indetectável) também é recomendado em pacientes com doença estrutural residual ou resposta bioquimicamente incompleta se forem jovens ou com apresentarem baixo risco de complicações, como hipertireoidismo subclínico exógeno.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [72]Biondi B, Cooper DS. Thyroid hormone suppression therapy. Endocrinol Metab Clin North Am. 2019 Mar;48(1):227-37. http://www.ncbi.nlm.nih.gov/pubmed/30717904?tool=bestpractice.com
Em pacientes com doença de risco intermediário, recomenda-se manter um nível sérico de TSH de 0.1 a 0.5 mUI/L.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com
Em pacientes com doença de baixo risco, os níveis séricos de TSH devem ser mantidos na faixa de baixo a normal (0.5 a 2.0 mUI/L).[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer
Pacientes com doença de baixo risco submetidos a lobectomia podem não necessitar de terapia de reposição de hormônio tireoidiano se o TSH sérico for mantido em uma faixa-alvo baixa a normal.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com
Doses supressoras de TSH na terapia de reposição da tireoide podem resultar em hipertireoidismo subclínico exógeno, que por sua vez pode resultar em desfechos adversos, como osteoporose, fraturas e doenças cardiovasculares, incluindo fibrilação atrial.[72]Biondi B, Cooper DS. Thyroid hormone suppression therapy. Endocrinol Metab Clin North Am. 2019 Mar;48(1):227-37. http://www.ncbi.nlm.nih.gov/pubmed/30717904?tool=bestpractice.com A perda óssea é uma preocupação particular para a supressão de TSH em mulheres menopausadas não tratadas com estrogênio, mas o efeito da supressão de TSH na taxa de fraturas não é claro.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [73]Brancatella A, Marcocci C. TSH suppressive therapy and bone. Endocr Connect. 2020 Jul;9(7):R158-72. https://ec.bioscientifica.com/view/journals/ec/9/7/EC-20-0167.xml http://www.ncbi.nlm.nih.gov/pubmed/32567550?tool=bestpractice.com
Opções primárias
levotiroxina: consulte um especialista para obter orientação quanto à dose
terapia com iodo radioativo
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
A avaliação de risco (com base em achados cirúrgicos e patológicos) e avaliação do estado da doença pós-operatório (inclusive medições de tireoglobulina [Tg] sérica e ultrassonografia do pescoço) são necessárias para orientar a seleção de pacientes para terapia com iodo radioativo.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [54]Webb RC, Howard RS, Stojadinovic A, et al. The utility of serum thyroglobulin measurement at the time of remnant ablation for predicting disease-free status in patients with differentiated thyroid cancer: a meta-analysis involving 3947 patients. J Clin Endocrinol Metab. 2012 Aug;97(8):2754-63. https://academic.oup.com/jcem/article/97/8/2754/2823340 http://www.ncbi.nlm.nih.gov/pubmed/22639291?tool=bestpractice.com [75]Tuttle RM, Ahuja S, Avram AM, et al. Controversies, consensus, and collaboration in the use of (131)I therapy in differentiated thyroid cancer: a joint statement from the American Thyroid Association, the European Association of Nuclear Medicine, the Society of Nuclear Medicine and Molecular Imaging, and the European Thyroid Association. Thyroid. 2019 Apr;29(4):461-70. https://www.liebertpub.com/doi/10.1089/thy.2018.0597 http://www.ncbi.nlm.nih.gov/pubmed/30900516?tool=bestpractice.com [76]Pacini F, Fuhrer D, Elisei R, et al. 2022 ETA consensus statement: what are the indications for post-surgical radioiodine therapy in differentiated thyroid cancer? Eur Thyroid J. 2022 Jan 1;11(1):e210046. https://etj.bioscientifica.com/view/journals/etj/11/1/ETJ-21-0046.xml http://www.ncbi.nlm.nih.gov/pubmed/34981741?tool=bestpractice.com
O uso de terapia com iodo radioativo é recomendado após tireoidectomia total em pacientes com doença de alto risco e em pacientes selecionados com doença de risco intermediário.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [76]Pacini F, Fuhrer D, Elisei R, et al. 2022 ETA consensus statement: what are the indications for post-surgical radioiodine therapy in differentiated thyroid cancer? Eur Thyroid J. 2022 Jan 1;11(1):e210046. https://etj.bioscientifica.com/view/journals/etj/11/1/ETJ-21-0046.xml http://www.ncbi.nlm.nih.gov/pubmed/34981741?tool=bestpractice.com
A terapia com iodo radioativo não é recomendada rotineiramente para pacientes com doença de baixo risco, mas as características que afetam o risco de recorrência, as implicações do acompanhamento da doença e as preferências do paciente devem ser consideradas.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [77]Leboulleux S, Bournaud C, Chougnet CN, et al. Thyroidectomy without radioiodine in patients with low-risk thyroid cancer. N Engl J Med. 2022 Mar 10;386(10):923-32. https://www.nejm.org/doi/10.1056/NEJMoa2111953 http://www.ncbi.nlm.nih.gov/pubmed/35263518?tool=bestpractice.com
A seleção da dose ideal de iodo radioativo terapêutico pode ser desafiadora e deve basear-se na avaliação de risco, além de ser individualizada (por exemplo, orientada por fatores do paciente e meta de tratamento).[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [75]Tuttle RM, Ahuja S, Avram AM, et al. Controversies, consensus, and collaboration in the use of (131)I therapy in differentiated thyroid cancer: a joint statement from the American Thyroid Association, the European Association of Nuclear Medicine, the Society of Nuclear Medicine and Molecular Imaging, and the European Thyroid Association. Thyroid. 2019 Apr;29(4):461-70. https://www.liebertpub.com/doi/10.1089/thy.2018.0597 http://www.ncbi.nlm.nih.gov/pubmed/30900516?tool=bestpractice.com [76]Pacini F, Fuhrer D, Elisei R, et al. 2022 ETA consensus statement: what are the indications for post-surgical radioiodine therapy in differentiated thyroid cancer? Eur Thyroid J. 2022 Jan 1;11(1):e210046. https://etj.bioscientifica.com/view/journals/etj/11/1/ETJ-21-0046.xml http://www.ncbi.nlm.nih.gov/pubmed/34981741?tool=bestpractice.com Consulte a orientação local.
Níveis aumentados de hormônio estimulante da tireoide (TSH) são necessários para se induzir a captação de iodo radioativo nas células tireoidianas.[76]Pacini F, Fuhrer D, Elisei R, et al. 2022 ETA consensus statement: what are the indications for post-surgical radioiodine therapy in differentiated thyroid cancer? Eur Thyroid J. 2022 Jan 1;11(1):e210046. https://etj.bioscientifica.com/view/journals/etj/11/1/ETJ-21-0046.xml http://www.ncbi.nlm.nih.gov/pubmed/34981741?tool=bestpractice.com A administração de TSH humano recombinante exógeno (rhTSH) é o método preferencial de preparação para a terapia com iodo radioativo para a maioria dos pacientes.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
Após a terapia com iodo radioativo, um exame de imagem de corpo inteiro com iodo radioativo deve ser obtido para estadiar a doença e documentar a avidez de iodo radioativo de quaisquer lesões estruturais.[78]Gulec SA, Ahuja S, Avram AM, et al. A joint statement from the American Thyroid Association, the European Association of Nuclear Medicine, the European Thyroid Association, the Society of Nuclear Medicine and Molecular Imaging on current diagnostic and theranostic approaches in the management of thyroid cancer. Thyroid. 2021 Jul;31(7):1009-19. https://www.liebertpub.com/doi/10.1089/thy.2020.0826 http://www.ncbi.nlm.nih.gov/pubmed/33789450?tool=bestpractice.com
O uso de um exame de imagem "diagnóstico" com iodo radioativo após a cirurgia, mas antes da terapia com iodo radioativo, é controversa.[75]Tuttle RM, Ahuja S, Avram AM, et al. Controversies, consensus, and collaboration in the use of (131)I therapy in differentiated thyroid cancer: a joint statement from the American Thyroid Association, the European Association of Nuclear Medicine, the Society of Nuclear Medicine and Molecular Imaging, and the European Thyroid Association. Thyroid. 2019 Apr;29(4):461-70.
https://www.liebertpub.com/doi/10.1089/thy.2018.0597
http://www.ncbi.nlm.nih.gov/pubmed/30900516?tool=bestpractice.com
[76]Pacini F, Fuhrer D, Elisei R, et al. 2022 ETA consensus statement: what are the indications for post-surgical radioiodine therapy in differentiated thyroid cancer? Eur Thyroid J. 2022 Jan 1;11(1):e210046.
https://etj.bioscientifica.com/view/journals/etj/11/1/ETJ-21-0046.xml
http://www.ncbi.nlm.nih.gov/pubmed/34981741?tool=bestpractice.com
Uma cintilografia diagnóstica com iodo radioativo pode fornecer informações relevantes para a tomada de decisão clínica apenas em pacientes selecionados.[78]Gulec SA, Ahuja S, Avram AM, et al. A joint statement from the American Thyroid Association, the European Association of Nuclear Medicine, the European Thyroid Association, the Society of Nuclear Medicine and Molecular Imaging on current diagnostic and theranostic approaches in the management of thyroid cancer. Thyroid. 2021 Jul;31(7):1009-19.
https://www.liebertpub.com/doi/10.1089/thy.2020.0826
http://www.ncbi.nlm.nih.gov/pubmed/33789450?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Aumento da captação de radioiodo nos dois campos pulmonares e no mediastino devido a metástase pulmonar miliar do carcinoma papilar da tireoideGkountouvas A, Chatjimarkou F, Thomas D, et al. Miliary lung metastasis due to papillary thyroid carcinoma. BMJ Case Reports. 2009; doi:10.1136/bcr.06.2008.0322 [Citation ends].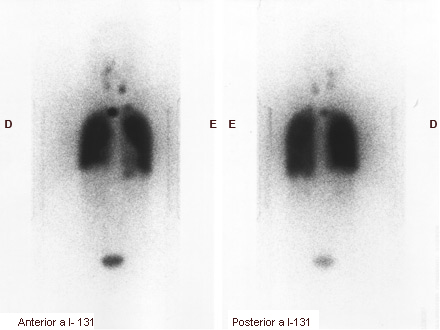
observação e vigilância ± cirurgia ± terapia com iodo radioativo ± terapias locais direcionadas (por exemplo, radioterapia por feixe externo, ablação térmica)
O risco de recorrência é determinado no momento do diagnóstico e reavaliado continuamente em resposta às terapias iniciais.[66]Tuttle RM, Alzahrani AS. Risk stratification in differentiated thyroid cancer: from detection to final follow-up. J Clin Endocrinol Metab. 2019 Mar 15;104(9):4087-100. https://academic.oup.com/jcem/article/104/9/4087/5380478 http://www.ncbi.nlm.nih.gov/pubmed/30874735?tool=bestpractice.com Os ensaios de tireoglobulina sérica e a ultrassonografia do pescoço são os pilares do acompanhamento do câncer de tireoide diferenciado.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer
A recorrência pode ser bioquímica ou estrutural.
O tratamento dos pacientes que podem desenvolver recorrência bioquímica (ou seja, níveis de tireoglobulina em ascensão ou recém-elevados), sem evidências de doença estrutural, compreende observação e vigilância com estudos de imagem apropriados realizados a intervalos de tempo guiados pelo tempo de duplicação da tireoglobulina.[79]Scharpf J, Tuttle M, Wong R, et al. Comprehensive management of recurrent thyroid cancer: an American Head and Neck Society consensus statement. Head Neck. 2016 Dec;38(12):1862-9. https://onlinelibrary.wiley.com/doi/10.1002/hed.24513 http://www.ncbi.nlm.nih.gov/pubmed/27717219?tool=bestpractice.com
Pacientes com suspeita de recorrência estrutural no pescoço (doença persistente ou recorrente comprovada por biópsia) pode necessitar de terapias adicionais ou pode ser tratada com observação e imagens transversais seriadas (por exemplo, tomografia computadorizada com contraste [TC] ou ressonância nuclear magnética [RNM]) em uma frequência suficiente para identificar a progressão de uma doença clinicamente significativa.[79]Scharpf J, Tuttle M, Wong R, et al. Comprehensive management of recurrent thyroid cancer: an American Head and Neck Society consensus statement. Head Neck. 2016 Dec;38(12):1862-9. https://onlinelibrary.wiley.com/doi/10.1002/hed.24513 http://www.ncbi.nlm.nih.gov/pubmed/27717219?tool=bestpractice.com Uma doença estrutural recorrente que mede 8-10 mm ou mais em imagens anatômicas nas regiões central e lateral do pescoço, respectivamente, é considerada para cirurgia de revisão.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com [79]Scharpf J, Tuttle M, Wong R, et al. Comprehensive management of recurrent thyroid cancer: an American Head and Neck Society consensus statement. Head Neck. 2016 Dec;38(12):1862-9. https://onlinelibrary.wiley.com/doi/10.1002/hed.24513 http://www.ncbi.nlm.nih.gov/pubmed/27717219?tool=bestpractice.com
Metástases são observadas com mais frequência em pacientes com subtipos histológicos agressivos e podem ocorrer em até 10% dos pacientes com câncer de tireoide diferenciado.[69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer [80]Tumino D, Frasca F, Newbold K. Updates on the management of advanced, metastatic, and radioiodine refractory differentiated thyroid cancer. Front Endocrinol (Lausanne). 2017 Nov 20;8:312. https://www.frontiersin.org/articles/10.3389/fendo.2017.00312/full http://www.ncbi.nlm.nih.gov/pubmed/29209273?tool=bestpractice.com Para o manejo do câncer de tireoide metastático diferenciado, a American Thyroid Association recomenda uma hierarquia preferencial de excisão cirúrgica da doença locorregional, terapia com iodo radioativo para a doença com resposta clínica ao iodo radioativo (com terapia supressora de hormônio estimulante da tireoide [TSH]), terapias locais direcionadas (por exemplo, radioterapia por feixe externo, ablação térmica) e terapia sistêmica com inibidores de quinases.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com
Para pacientes com doença metastática assintomática estável ou lentamente progressiva, a terapia com hormônio tireoidiano supressor de TSH pode ser usada isoladamente.[1]Haugen BR, Alexander EK, Bible KC, et al; American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2016 Jan;26(1):1-133. https://www.liebertpub.com/doi/10.1089/thy.2015.0020 http://www.ncbi.nlm.nih.gov/pubmed/26462967?tool=bestpractice.com
Se as metástases à distância apresentarem resposta clínica ao iodo radioativo, a terapia com iodo radioativo é repetida a cada 6-12 meses, dependendo da taxa de crescimento e da resposta.[81]Verburg FA, Hänscheid H, Luster M. Radioactive iodine (RAI) therapy for metastatic differentiated thyroid cancer. Best Pract Res Clin Endocrinol Metab. 2017 Jun;31(3):279-90. http://www.ncbi.nlm.nih.gov/pubmed/28911724?tool=bestpractice.com À medida que os tumores evoluem, eles podem perder a capacidade de concentrar iodo radioativo.[33]Fugazzola L, Elisei R, Fuhrer D, et al. 2019 European Thyroid Association guidelines for the treatment and follow-up of advanced radioiodine-refractory thyroid cancer. Eur Thyroid J. 2019 Oct;8(5):227-45. https://etj.bioscientifica.com/view/journals/etj/8/5/ETJ502229.xml http://www.ncbi.nlm.nih.gov/pubmed/31768334?tool=bestpractice.com
terapia específica
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
O tratamento com inibidores da quinase, ou outras terapias direcionadas, pode ser considerado para pacientes com câncer de tireoide diferenciado progressivo que não são adequados ou não apresentam resposta ao tratamento local (inclusive cirurgia e terapia com iodo radioativo).
O teste genético para identificar potenciais mutações/alterações acionáveis (por exemplo, NTRK, BRAF, RET, deficiência no reparo de erro de pareamento [dMMR], instabilidade de microssatélite [IMS], carga mutacional tumoral [TMB]) é recomendado antes de iniciar a terapia.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [46]Filetti S, Durante C, Hartl DM, et al. ESMO clinical practice guideline update on the use of systemic therapy in advanced thyroid cancer. Ann Oncol. 2022 Jul;33(7):674-84. https://www.annalsofoncology.org/article/S0923-7534(22)00694-9/fulltext http://www.ncbi.nlm.nih.gov/pubmed/35491008?tool=bestpractice.com [82]Shonka DC Jr, Ho A, Chintakuntlawar AV, et al. American Head and Neck Society Endocrine Surgery Section and International Thyroid Oncology Group consensus statement on mutational testing in thyroid cancer: defining advanced thyroid cancer and its targeted treatment. Head Neck. 2022 Jun;44(6):1277-300. http://www.ncbi.nlm.nih.gov/pubmed/35274388?tool=bestpractice.com
Se a terapia sistêmica for indicada, os seguintes inibidores de quinase são recomendados como opções de primeira linha: lenvatinibe ou sorafenibe.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
Inibidores de quinase alternativos que podem ser considerados incluem: cabozantinibe (se a progressão ocorrer após lenvatinibe e/ou sorafenibe); larotrectinibe ou entrectinibe ou repotrectinibe (para tumores sólidos avançados positivos para fusão gênica de NTRK); selpercatinibe ou pralsetinibe (para tumores positivos para fusão gênica de RET).[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
As terapias direcionadas que podem ser consideradas para pacientes com tumores sólidos metastáticos ou recorrentes irressecáveis, que evoluíram após o tratamento prévio sem opções de tratamento alternativas satisfatórias incluem: Pembrolizumabe (um anticorpo monoclonal bloqueador do receptor da proteína 1 de morte celular programada [PD-1] para tumores com TMB alta [≥10 mutações/megabase], ou tumores com IMS alta ou dMMR); ou dabrafenibe associado a trametinibe (para pacientes com mutação BRAF V600E).[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
A sequência ideal de terapia sistêmica nesse caso não é clara. A tomada de decisão deve basear-se em fatores que incluem resposta esperada ao tratamento, perfil de segurança do medicamento e preferências do paciente.
Consulte o protocolo clínico e de diretrizes terapêuticas local para obter mais informações sobre dosagens.
Opções primárias
sorafenibe
ou
lenvatinibe
Opções secundárias
cabozantinibe
ou
larotrectinibe
ou
entrectinibe
ou
Repotrectinibe
ou
selpercatinibe
ou
pralsetinibe
Opções terciárias
pembrolizumabe
ou
dabrafenibe
e
trametinibe
anaplásico
cirurgia + quimiorradiação
O câncer de tireoide anaplásico geralmente é diagnosticado em estágio avançado (normalmente com metástases à distância), exibe comportamento extremamente agressivo e está associado a um prognóstico desfavorável.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer
Um envolvimento multidisciplinar precoce, incluindo a equipe de cuidados paliativos, é importante para dar suporte à tomada de decisão do paciente.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com Determinar a extensão da doença e avaliar as mutações influencia as opções de tratamento (inclusive elegibilidade para ensaios clínicos) e os objetivos do cuidado.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com
A combinação de múltiplas modalidades terapêuticas (cirurgia, radioterapia, terapia sistêmica [quimioterapia, terapia direcionada]) é a abordagem mais eficaz para tratar o câncer de tireoide anaplásico, mas precisa ser individualizada para equilibrar bem os riscos e benefícios.
A terapia com iodo radioativo não é usada porque tumores anaplásicos não captam radioiodo.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
Se possível, uma tireoidectomia total é realizada. Determinar se um paciente é candidato à cirurgia depende da ressecabilidade do tumor, da extensão da invasão local, da necessidade de traqueostomia urgente, da presença de metástases à distância e da capacidade funcional e objetivos de tratamento do paciente.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com A reposição do hormônio tireoidiano é necessária após a tireoidectomia total.
Independentemente do status cirúrgico, a radioterapia deve ser considerada precocemente no tratamento do câncer de tireoide anaplásico.[83]Rao SN, Smallridge RC. Anaplastic thyroid cancer: an update. Best Pract Res Clin Endocrinol Metab. 2022 May 27;101678. http://www.ncbi.nlm.nih.gov/pubmed/35668021?tool=bestpractice.com
A quimioterapia com paclitaxel, docetaxel ou tratamentos combinados (por exemplo, carboplatina/paclitaxel, docetaxel/doxorrubicina) está associada com taxas de resposta muito baixas e toxicidades significativas. No entanto, a quimioterapia pode ser considerada por seu efeito radiossensibilizante quando combinada com radioterapia ou como uma ponte para a terapia direcionada para pacientes que aguardam os resultados do perfil molecular.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com
Siga as diretrizes do protocolo dos especialistas locais para dosagem da quimioterapia.
Opções primárias
paclitaxel
ou
docetaxel
ou
paclitaxel
e
carboplatina
ou
docetaxel
e
doxorrubicina
terapia específica
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
O uso de terapia direcionada em pacientes com câncer de tireoide anaplásico depende dos resultados dos testes genéticos.[13]Bible KC, Kebebew E, Brierley J, et al. 2021 American Thyroid Association guidelines for management of patients with anaplastic thyroid cancer. Thyroid. 2021 Mar;31(3):337-86. https://www.liebertpub.com/doi/10.1089/thy.2020.0944 http://www.ncbi.nlm.nih.gov/pubmed/33728999?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [46]Filetti S, Durante C, Hartl DM, et al. ESMO clinical practice guideline update on the use of systemic therapy in advanced thyroid cancer. Ann Oncol. 2022 Jul;33(7):674-84. https://www.annalsofoncology.org/article/S0923-7534(22)00694-9/fulltext http://www.ncbi.nlm.nih.gov/pubmed/35491008?tool=bestpractice.com [84]Maniakas A, Zafereo M, Cabanillas ME. Anaplastic thyroid cancer: new horizons and challenges. Endocrinol Metab Clin North Am. 2022 Jun;51(2):391-401. http://www.ncbi.nlm.nih.gov/pubmed/35662448?tool=bestpractice.com [85]Wang JR, Zafereo ME, Dadu R, et al. Complete surgical resection following neoadjuvant dabrafenib plus trametinib in BRAF(V600E)-mutated anaplastic thyroid carcinoma. Thyroid. 2019 Aug;29(8):1036-43. https://pmc.ncbi.nlm.nih.gov/articles/PMC6707029 http://www.ncbi.nlm.nih.gov/pubmed/31319771?tool=bestpractice.com
Dabrafenibe associado a trametinibe: pode ser considerado antes da cirurgia (para melhorar a ressecabilidade) em pacientes com mutação BRAF V600E e doença locorregional.
Larotrectinibe ou entrectinibe ou repotrectinibe: para pacientes com tumores sólidos avançados positivos para fusão gênica de NTRK.
Selpercatinibe ou pralsetinibe: para pacientes com tumores positivos para fusão gênica de RET.
Imunoterapia; por exemplo, pembrolizumabe, para pacientes com tumores com carga mutacional tumoral alta (TMB-H; ≥10 mutações/megabase).
Consulte o protocolo clínico e de diretrizes terapêuticas local para obter mais informações sobre dosagens.
Opções primárias
dabrafenibe
e
trametinibe
ou
larotrectinibe
ou
entrectinibe
ou
Repotrectinibe
ou
selpercatinibe
ou
pralsetinibe
Opções secundárias
pembrolizumabe
medular
cirurgia
A cirurgia para os pacientes com câncer de tireoide medular esporádico ou hereditário é a tireoidectomia total e a dissecção linfonodal do compartimento central, cuja extensão depende dos níveis séricos de calcitonina e dos achados ultrassonográficos.[4]Wells SA Jr, Asa SL, Dralle H, et al. Revised American Thyroid Association guidelines for the management of medullary thyroid carcinoma. Thyroid. 2015 Jun;25(6):567-610. https://www.liebertpub.com/doi/10.1089/thy.2014.0335 http://www.ncbi.nlm.nih.gov/pubmed/25810047?tool=bestpractice.com [53]Viola D, Elisei R. Management of medullary thyroid cancer. Endocrinol Metab Clin North Am. 2019 Mar;48(1):285-301. http://www.ncbi.nlm.nih.gov/pubmed/30717909?tool=bestpractice.com [69]European Society for Medical Oncology. Clinical practice guidelines - thyroid cancer. 2019 [internet publication]. https://www.esmo.org/guidelines/guidelines-by-topic/endocrine-and-neuroendocrine-cancers/thyroid-cancer [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx
reposição do hormônio tireoidiano
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
A reposição de hormônio tireoidiano (por exemplo, levotiroxina) é necessária após a tireoidectomia total para manter os níveis de hormônio estimulante da tireoide (TSH) sérico na faixa eutireoidiana.[4]Wells SA Jr, Asa SL, Dralle H, et al. Revised American Thyroid Association guidelines for the management of medullary thyroid carcinoma. Thyroid. 2015 Jun;25(6):567-610. https://www.liebertpub.com/doi/10.1089/thy.2014.0335 http://www.ncbi.nlm.nih.gov/pubmed/25810047?tool=bestpractice.com
O câncer de tireoide medular não é sensível ao TSH; portanto, as doses supressivas de TSH não são necessárias.
Opções primárias
levotiroxina: consulte um especialista para obter orientação quanto à dose
cirurgia ± radioterapia por feixe externo ± tratamentos focais
As recorrências são tratadas com cirurgia adicional, associada a radioterapia por feixe externo caso o controle local não seja possível.[86]Hadoux J, Pacini F, Tuttle RM, et al. Management of advanced medullary thyroid cancer. Lancet Diabetes Endocrinol. 2016 Jan;4(1):64-71. http://www.ncbi.nlm.nih.gov/pubmed/26608066?tool=bestpractice.com
Na doença metastática, a cirurgia pode ser indicada para os pacientes nos quais uma única ou algumas metástases estiverem localizadas no cérebro, pulmões ou fígado.[86]Hadoux J, Pacini F, Tuttle RM, et al. Management of advanced medullary thyroid cancer. Lancet Diabetes Endocrinol. 2016 Jan;4(1):64-71. http://www.ncbi.nlm.nih.gov/pubmed/26608066?tool=bestpractice.com Tratamentos focais, incluindo radioterapia por feixe externo, radiocirurgia estereotáxica, ablação por radiofrequência ou quimioembolização, são usados a depender do local das metástases.[4]Wells SA Jr, Asa SL, Dralle H, et al. Revised American Thyroid Association guidelines for the management of medullary thyroid carcinoma. Thyroid. 2015 Jun;25(6):567-610. https://www.liebertpub.com/doi/10.1089/thy.2014.0335 http://www.ncbi.nlm.nih.gov/pubmed/25810047?tool=bestpractice.com [86]Hadoux J, Pacini F, Tuttle RM, et al. Management of advanced medullary thyroid cancer. Lancet Diabetes Endocrinol. 2016 Jan;4(1):64-71. http://www.ncbi.nlm.nih.gov/pubmed/26608066?tool=bestpractice.com
terapia específica
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
Os inibidores da quinase produziram altas taxas de resposta em pacientes com câncer de tireoide medular metastático.[86]Hadoux J, Pacini F, Tuttle RM, et al. Management of advanced medullary thyroid cancer. Lancet Diabetes Endocrinol. 2016 Jan;4(1):64-71. http://www.ncbi.nlm.nih.gov/pubmed/26608066?tool=bestpractice.com
Os inibidores de multiquinase cabozantinibe e vandetanibe são recomendados como terapia sistêmica de primeira linha para os pacientes com câncer de tireoide medular metastático e progressivo.[4]Wells SA Jr, Asa SL, Dralle H, et al. Revised American Thyroid Association guidelines for the management of medullary thyroid carcinoma. Thyroid. 2015 Jun;25(6):567-610. https://www.liebertpub.com/doi/10.1089/thy.2014.0335 http://www.ncbi.nlm.nih.gov/pubmed/25810047?tool=bestpractice.com [37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [46]Filetti S, Durante C, Hartl DM, et al. ESMO clinical practice guideline update on the use of systemic therapy in advanced thyroid cancer. Ann Oncol. 2022 Jul;33(7):674-84. https://www.annalsofoncology.org/article/S0923-7534(22)00694-9/fulltext http://www.ncbi.nlm.nih.gov/pubmed/35491008?tool=bestpractice.com [82]Shonka DC Jr, Ho A, Chintakuntlawar AV, et al. American Head and Neck Society Endocrine Surgery Section and International Thyroid Oncology Group consensus statement on mutational testing in thyroid cancer: defining advanced thyroid cancer and its targeted treatment. Head Neck. 2022 Jun;44(6):1277-300. http://www.ncbi.nlm.nih.gov/pubmed/35274388?tool=bestpractice.com
Os inibidores de RET selpercatinibe e pralsetinibe são recomendados para pacientes com câncer medular de tireoide recorrente ou metastático com mutação em RET.[37]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: thyroid carcinoma [internet publication]. https://www.nccn.org/professionals/physician_gls/default.aspx [46]Filetti S, Durante C, Hartl DM, et al. ESMO clinical practice guideline update on the use of systemic therapy in advanced thyroid cancer. Ann Oncol. 2022 Jul;33(7):674-84. https://www.annalsofoncology.org/article/S0923-7534(22)00694-9/fulltext http://www.ncbi.nlm.nih.gov/pubmed/35491008?tool=bestpractice.com
Consulte o protocolo clínico e de diretrizes terapêuticas local para obter mais informações sobre dosagens.
Opções primárias
cabozantinibe
ou
vandetanibe
Opções secundárias
selpercatinibe
ou
pralsetinibe
reposição do hormônio tireoidiano
Tratamento adicional recomendado para ALGUNS pacientes no grupo de pacientes selecionado
A reposição de hormônio tireoidiano (por exemplo, levotiroxina) é necessária após a tireoidectomia total para manter os níveis de hormônio estimulante da tireoide (TSH) sérico na faixa eutireoidiana.[4]Wells SA Jr, Asa SL, Dralle H, et al. Revised American Thyroid Association guidelines for the management of medullary thyroid carcinoma. Thyroid. 2015 Jun;25(6):567-610. https://www.liebertpub.com/doi/10.1089/thy.2014.0335 http://www.ncbi.nlm.nih.gov/pubmed/25810047?tool=bestpractice.com
O câncer de tireoide medular não é sensível ao TSH; portanto, as doses supressivas de TSH não são necessárias.
Opções primárias
levotiroxina: consulte um especialista para obter orientação quanto à dose

Escolha um grupo de pacientes para ver nossas recomendações
Observe que as formulações/vias e doses podem diferir entre nomes e marcas de medicamentos, formulários de medicamentos ou localidades. As recomendações de tratamento são específicas para os grupos de pacientes. Ver aviso legal
O uso deste conteúdo está sujeito ao nosso aviso legal