Una evaluación y diagnóstico rápidos son la piedra angular de una terapia exitosa en el ictus isquémico. Hay que priorizar la estabilización del paciente mediante el manejo de la vía aérea o de cualquier insuficiencia respiratoria o circulatoria que requiera un tratamiento urgente, manteniendo los cuidados de soporte necesarios (véase la sección "Cuidados de soporte"). Los objetivos del tratamiento son los siguientes:
Restaurar el flujo sanguíneo
Se debe proporcionar soporte al metabolismo de la energía en el tejido isquémico
Se debe tratar las complicaciones de edema asociado al accidente cerebrovascular
Se deben prevenir las complicaciones médicas agudas frecuentes.
Trombólisis intravenosa
Véase la sección "Candidatos para la trombólisis intravenosa con alteplasa" más adelante para conocer las recomendaciones sobre qué pacientes son aptos para el tratamiento con trombólisis intravenosa.
Hay tres formulaciones intravenosas del activador del plasminógeno tisular recombinante (r-tPA) disponibles en EE. UU.: alteplasa, tenecteplasa y reteplasa. Actualmente, solo la alteplasa está aprobada para su uso en el ictus isquémico agudo. Los otros dos están aprobados solo para el uso en el infarto agudo de miocardio.
La alteplasa favorece la trombólisis y por lo tanto, la recanalización y la reperfusión. Se recomienda la administración precoz de alteplasa intravenosa en los pacientes adecuados que cumplan los criterios definidos para la trombólisis.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
El inicio temprano de la trombólisis intravenosa (es decir, dentro de las 4.5 horas posteriores al inicio de los síntomas, si no está contraindicada) se asocia a una mejora en los resultados funcionales.[143]Wardlaw JM, Murray V, Berge E, et al. Thrombolysis for acute ischaemic stroke. Cochrane Database Syst Rev. 2014 Jul 29;(7):CD000213.
https://www.doi.org/10.1002/14651858.CD000213.pub3
http://www.ncbi.nlm.nih.gov/pubmed/25072528?tool=bestpractice.com
[144]Man S, Xian Y, Holmes DN, et al. Association between thrombolytic door-to-needle time and 1-year mortality and readmission in patients with acute ischemic stroke. JAMA. 2020 Jun 2;323(21):2170-84.
https://www.doi.org/10.1001/jama.2020.5697
http://www.ncbi.nlm.nih.gov/pubmed/32484532?tool=bestpractice.com
En un estudio de cohortes retrospectivo de más de 61000 pacientes de 65 años o más con ictus isquémico agudo, un tiempo puerta-aguja más corto se asoció con una menor mortalidad por cualquier causa y con un menor número de reingresos por cualquier causa al año.[144]Man S, Xian Y, Holmes DN, et al. Association between thrombolytic door-to-needle time and 1-year mortality and readmission in patients with acute ischemic stroke. JAMA. 2020 Jun 2;323(21):2170-84.
https://www.doi.org/10.1001/jama.2020.5697
http://www.ncbi.nlm.nih.gov/pubmed/32484532?tool=bestpractice.com
La administración de la alteplasa no debe retrasarse con pruebas adicionales, a menos que se sospeche una contraindicación específica y deba descartarse. La glucemia debe normalizarse antes de iniciar el tratamiento con alteplasa.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
El edema orolingual es una complicación poco frecuente pero potencialmente grave.
En la frecuente situación en que no se presenció el inicio de los síntomas, debe presumirse que el momento del inicio es el momento en que consta que el paciente estuvo bien por última vez.
Los ensayos de alteplasa para la trombólisis en pacientes con un accidente cerebrovascular isquémico agudo y sin contraindicaciones sugieren que la ventana de oportunidad ideal para el tratamiento es hasta 4.5 horas después del inicio de los síntomas neurológicos.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[145]Hacke W, Kaste M, Bluhmki E, et al; ECASS Investigators. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke. N Engl J Med. 2008 Sep 25;359(13):1317-29.
https://www.nejm.org/doi/10.1056/NEJMoa0804656
http://www.ncbi.nlm.nih.gov/pubmed/18815396?tool=bestpractice.com
En el caso de los pacientes con un accidente cerebrovascular agudo grave, el tiempo objetivo desde la llegada al servicio de urgencias hasta la iniciación de la alteplasa intravenosa (si está indicada) es de 60 minutos.[117]Alberts MJ, Latchaw RE, Jagoda A, et al. Revised and updated recommendations for the establishment of primary stroke centers: a summary statement from the brain attack coalition. Stroke. 2011 Sep;42(9):2651-65.
https://www.ahajournals.org/doi/full/10.1161/strokeaha.111.615336
http://www.ncbi.nlm.nih.gov/pubmed/21868727?tool=bestpractice.com
[146]Whiteley WN, Emberson J, Lees KR, et al. Risk of intracerebral haemorrhage with alteplase after acute ischaemic stroke: a secondary analysis of an individual patient data meta-analysis. Lancet Neurol. 2016 Aug;15(9):925-33.
http://www.ncbi.nlm.nih.gov/pubmed/27289487?tool=bestpractice.com
La alteplasa está aprobada en los EE. UU. para su uso dentro de las 3 horas posteriores al inicio de los síntomas del ictus y en Europa para el uso dentro de las 4.5 horas posteriores.
La tenecteplasa es al menos tan eficaz y segura como la alteplasa.[147]Alamowitch S, Turc G, Palaiodimou L, et al. European Stroke Organisation (ESO) expedited recommendation on tenecteplase for acute ischaemic stroke. Eur Stroke J. 2023 Mar;8(1):8-54.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10069183
http://www.ncbi.nlm.nih.gov/pubmed/37021186?tool=bestpractice.com
[148]Kheiri B, Osman M, Abdalla A, et al. Tenecteplase versus alteplase for management of acute ischemic stroke: a pairwise and network meta-analysis of randomized clinical trials. J Thromb Thrombolysis. 2018 Nov;46(4):440-50.
http://www.ncbi.nlm.nih.gov/pubmed/30117036?tool=bestpractice.com
[149]Burgos AM, Saver JL. Evidence that tenecteplase Is noninferior to alteplase for acute ischemic stroke: meta-analysis of 5 randomized trials. Stroke. 2019 Aug;50(8):2156-62.
https://www.doi.org/10.1161/STROKEAHA.119.025080
http://www.ncbi.nlm.nih.gov/pubmed/31318627?tool=bestpractice.com
[150]American College of Emergency Physicians Clinical Policies Subcommittee (Writing Committee) on Acute Ischemic Stroke, Lo BM, Carpenter CR, et al. Clinical policy: critical issues in the management of adult patients presenting to the emergency department with acute ischemic stroke. Ann Emerg Med. 2023 Aug;82(2):e17-e64.
https://www.acep.org/patient-care/clinical-policies/acute-ischemic-stroke
http://www.ncbi.nlm.nih.gov/pubmed/37479410?tool=bestpractice.com
La American Heart Association/American Stroke Association (AHA/ASA) recomienda considerar la tenecteplasa como una alternativa a la alteplasa en pacientes con déficit neurológico menor y sin una oclusión intracraneal mayor.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
La información sobre los beneficios y riesgos de la trombólisis intravenosa debe darse al paciente, si es competente, o a un sustituto que tome las decisiones, si está presente. Si es posible, se deberá obtener el consentimiento verbal o por escrito. En la frecuente situación en la que el paciente no es competente para tomar decisiones médicas, y no se puede identificar a la familia o a un representante para la toma de decisiones ni se puede contactar con él a tiempo, está justificado proceder con la administración de alteplasa en un paciente adulto, apto por lo demás, con un ictus isquémico discapacitante.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Si un paciente carece de capacidad de decisión, no tiene una directriz anticipada determinante (que ofrezca orientación en esta situación generalmente imprevista) y no se dispone de un sustituto autorizado, las intervenciones pueden realizarse basándose en la presunción ética y de derecho común del consentimiento; es decir, el fundamento de que las personas razonables consentirían el tratamiento si se les pudiera preguntar. El riesgo inminente de discapacidad significativa también justifica el tratamiento de urgencia en estas circunstancias.[151]Sattin JA, Chiong W, Bonnie RJ, et al. Consent issues in the management of acute ischemic stroke: AAN position statement. Neurology. 2022 Jan 11;98(2):73-9.
https://www.doi.org/10.1212/WNL.0000000000013040
http://www.ncbi.nlm.nih.gov/pubmed/35312627?tool=bestpractice.com
Se debe informar a los encargados de la toma de decisiones de que el tratamiento con r-tPA se asocia con un mejor resultado en alrededor de 1 de cada 3 personas tratadas, y con un peor resultado en alrededor de 3 de cada 100 personas tratadas.[152]Saver JL. Number needed to treat estimates incorporating effects over the entire range of clinical outcomes: novel derivation method and application to thrombolytic therapy for acute stroke. Arch Neurol. 2004 Jul;61(7):1066-70.
https://jamanetwork.com/journals/jamaneurology/fullarticle/786159
http://www.ncbi.nlm.nih.gov/pubmed/15262737?tool=bestpractice.com
En general, 1 de cada 8 personas tratadas con r-tPA presentan una recuperación completa o casi completa, que, de otra manera, habrían quedado discapacitadas.[153]National Institute of Neurological Disorders and Stroke rt-PA Stroke Study Group. Tissue plasminogen activator for acute ischemic stroke. N Engl J Med. 1995 Dec 14;333(24):1581-7.
https://www.nejm.org/doi/full/10.1056/NEJM199512143332401
http://www.ncbi.nlm.nih.gov/pubmed/7477192?tool=bestpractice.com
La ausencia de evidencia definitiva sobre la eficacia de la trombólisis y la terapia endovascular en pacientes con discapacidad previa o demencia da lugar a decisiones difíciles sobre el uso de estas terapias. Se recomienda un enfoque pragmático individualizado en estos pacientes.[154]Ganesh A, Fraser JF, Gordon Perue GL, et al. Endovascular treatment and thrombolysis for acute ischemic stroke in patients with premorbid disability or dementia: a scientific statement from the American Heart Association/American Stroke Association. Stroke. 2022 May;53(5):e204-e217.
https://www.doi.org/10.1161/STR.0000000000000406
http://www.ncbi.nlm.nih.gov/pubmed/35343235?tool=bestpractice.com
Contraindicaciones de la trombólisis intravenosa con alteplasa
Las siguientes son contraindicaciones para el tratamiento con alteplasa según las guías de la AHA/ASA:[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Contraindicaciones absolutas:
Inicio de los síntomas >9 horas[155]Ma H, Campbell BC, Parsons MW, et al; EXTEND Investigators. Thrombolysis guided by perfusion imaging up to 9 hours after onset of stroke. N Engl J Med. 2019 May 9;380(19):1795-803.
https://www.nejm.org/doi/full/10.1056/NEJMoa1813046
http://www.ncbi.nlm.nih.gov/pubmed/31067369?tool=bestpractice.com
La TC revela una hemorragia intracraneal aguda
Antecedentes de traumatismo craneal grave
Síntomas que sugieran una hemorragia subaracnoidea
Pacientes con plaquetas <100,000/mm3, índice normalizado internacional (INR) >1.7, TTP activada (TTPa) >40 segundos, o tiempo de protrombina >15 segundos
El paciente ha recibido una dosis de heparina de bajo peso molecular en las últimas 24 horas
Evidencia de sangrado activo en la exploración
Síntomas congruentes con endocarditis infecciosa
Sospecha o conocimiento de la asociación entre el ictus isquémico agudo y la disección del arco aórtico.
Contraindicaciones relativas:
Antecedentes de ictus previo en los 3 meses anteriores
Antecedentes de hemorragia intracraneal previa
Antecedentes de cirugía intracraneal/intraespinal en los últimos 3 meses
El paciente está tomando fármacos antiplaquetarios que inhiben el receptor de la glicoproteína IIb/IIIa
Antecedentes de neoplasia intra-axial intracraneal
Antecedentes de neoplasia maligna gastrointestinal o evento reciente de sangrado en los 21 días anteriores
Antecedentes de cirugías mayores o traumatismos graves en los 14 días anteriores
El paciente está tomando inhibidores directos de la trombina o inhibidores directos del factor Xa, a menos que los análisis clínicos, tales como TTPa, INR, recuento de plaquetas, tiempo de coagulación de ecarina, tiempo de trombina o los análisis adecuados de la actividad directa del factor Xa, sean normales o que el paciente no haya recibido una dosis de estos fármacos durante más de 48 horas (suponiendo una función de metabolización renal normal).
Deberá consultar en su guía farmacológica local las contraindicaciones para el uso de tenecteplasa.
Candidatos para trombólisis intravenosa con alteplasa
Las guías de práctica clínica de la AHA/ASA establecen que las recomendaciones de elegibilidad para el tratamiento con alteplasa son:[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Dentro de las 3 horas siguientes a la aparición de los síntomas del ictus o desde que consta que el paciente estuvo bien por última vez o en su situación basal:
Pacientes elegibles médicamente de ≥18 años (igualmente recomendado para pacientes de <80 y >80 años)
Pacientes con síntomas graves de accidente cerebrovascular o síntomas leves de accidente cerebrovascular pero incapacitantes
En un plazo de 3.0 a 4.5 horas desde la aparición de los síntomas del ictus o desde que consta que el paciente ha estado bien por última vez:
Pacientes con edad ≤80 años
Aquellos sin antecedentes de diabetes mellitus, ni de accidente cerebrovascular
Las personas con una puntuación inicial en National Institutes of Health Stroke Scale (NIHSS) ≤25
Aquellos que no toman anticoagulantes orales
Aquellos donde no hay evidencia en estudios por imágenes de lesión isquémica que involucre a más de un tercio del área de la arteria cerebral media.
Pacientes cuya presión arterial puede reducirse de forma segura a <185/110 mmHg con fármacos antihipertensivos.
Pacientes con niveles iniciales de glucosa >2.8 mmol/L (>50 mg/dL)
Los pacientes con cambios isquémicos tempranos en una TC sin contraste de grado leve a moderado (aparte de la hipodensidad franca)
Pacientes que han recibido monoterapia antiplaquetaria o tratamiento combinado antes del accidente cerebrovascular, siempre que el beneficio de la alteplasa supere el posible aumento del riesgo de hemorragia intracerebral sintomática.
Pacientes con enfermedad renal terminal en hemodiálisis y TTPa normal.
En las guías de práctica clínica de la AHA/ASA se pueden encontrar recomendaciones adicionales para el tratamiento con alteplasa.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Normalizar la glucemia
La glucemia debe ser >2.8 mmol/L (>50 mg/dL) antes de iniciar el tratamiento con alteplasa intravenosa. Para obtener más información, consulte la sección "Cuidados de soporte" a continuación.
Reducir la presión arterial
La presión sanguínea debe ser <185/110 mmHg antes de iniciar el tratamiento de alteplasa intravenosa.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Para obtener más información, consulte la sección "Cuidados de soporte" a continuación.
Los pacientes con grandes déficits y los pacientes de edad avanzada
Cuando se trata a un paciente con déficits importantes, se reduce la probabilidad de un resultado favorable y existe mayor riesgo de hemorragia después de la trombólisis.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Las guías de práctica clínica de la AHA/ASA afirman que para los pacientes ≥18 años de edad que, por lo demás, son médicamente aptos, la administración de alteplasa en las primeras 3 horas se recomienda igualmente para los pacientes de <80 y >80 años de edad.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[156]Berge E, Whiteley W, Audebert H, et al. European Stroke Organisation (ESO) guidelines on intravenous thrombolysis for acute ischaemic stroke. Eur Stroke J. 2021 Mar;6(1):I-LXII.
https://www.doi.org/10.1177/2396987321989865
http://www.ncbi.nlm.nih.gov/pubmed/33817340?tool=bestpractice.com
Aunque el uso de alteplasa ha estado previamente restringido a personas menores de 80 años, las evidencias demuestran que los pacientes mayores de 80 años obtienen tantos beneficios (reducción de muerte o dependencia, mejores resultados funcionales) de la alteplasa como aquellos menores de 80 años, especialmente si se tratan en las primeras 3 horas tras el ictus.[143]Wardlaw JM, Murray V, Berge E, et al. Thrombolysis for acute ischaemic stroke. Cochrane Database Syst Rev. 2014 Jul 29;(7):CD000213.
https://www.doi.org/10.1002/14651858.CD000213.pub3
http://www.ncbi.nlm.nih.gov/pubmed/25072528?tool=bestpractice.com
[157]Bluhmki E, Danays T, Biegert G, et al. Alteplase for acute ischemic stroke in patients aged >80 years: pooled analyses of individual patient data. Stroke. 2020 Aug;51(8):2322-31.
https://www.doi.org/10.1161/STROKEAHA.119.028396
http://www.ncbi.nlm.nih.gov/pubmed/32611284?tool=bestpractice.com
[158]Hacke W, Lyden P, Emberson J, et al. Effects of alteplase for acute stroke according to criteria defining the European Union and United States marketing authorizations: individual-patient-data meta-analysis of randomized trials. Int J Stroke. 2018 Feb;13(2):175-s89.
https://www.doi.org/10.1177/1747493017744464
http://www.ncbi.nlm.nih.gov/pubmed/29171359?tool=bestpractice.com
Ácido acetilsalicílico y terapia antiplaquetaria doble
Las guías de práctica clínica recomiendan que los pacientes con accidente cerebrovascular isquémico reciban ácido acetilsalicílico, independientemente de que sean o no aptos para la alteplasa.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Sin embargo, si se administra alteplasa, no se debe comenzar a tomar ácido acetilsalicílico durante 24 horas, y solo después de que una tomografía computarizada de la cabeza muestre la ausencia de hemorragia intracraneal.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[159]Zinkstok SM, Roos YB; ARTIS investigators. Early administration of aspirin in patients treated with alteplase for acute ischaemic stroke: a randomised controlled trial. Lancet. 2012 Aug 25;380(9843):731-7.
http://www.ncbi.nlm.nih.gov/pubmed/22748820?tool=bestpractice.com
La administración temprana (es decir, en un plazo de las 24 horas) de ácido acetilsalicílico en pacientes con accidente cerebrovascular isquémico agudo que recibieron alteplasa no mostró ninguna mejora significativa en los resultados a los 3 meses.[159]Zinkstok SM, Roos YB; ARTIS investigators. Early administration of aspirin in patients treated with alteplase for acute ischaemic stroke: a randomised controlled trial. Lancet. 2012 Aug 25;380(9843):731-7.
http://www.ncbi.nlm.nih.gov/pubmed/22748820?tool=bestpractice.com
Pacientes con accidente cerebrovascular menor
Para los pacientes con ictus isquémico no cardioembólico o accidente isquémico transitorio (AIT), las guías de la AHA/ASA recomiendan aspirina, clopidogrel o la combinación de aspirina más dipiridamol de liberación prolongada en la prevención secundaria del ictus isquémico.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
En los pacientes con un ictus isquémico menor no cardioembólico reciente (puntuación NIHSS ≤3) o con un AIT de alto riesgo (puntuación ABCD2 ≥4), la AHA/ASA recomienda iniciar un tratamiento antiagregante doble de forma precoz (idealmente en las 12-24 horas siguientes al inicio de los síntomas y al menos en los 7 días siguientes al inicio) y mantenerlo durante 21-90 días, seguido de un tratamiento antiagregante único, para reducir el riesgo de ictus isquémico recurrente.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[160]Wang Y, Johnston SC, Bath PM, et al. Acute dual antiplatelet therapy for minor ischaemic stroke or transient ischaemic attack. BMJ. 2019 Feb 28;364:l895.
https://www.bmj.com/content/364/bmj.l895.long
http://www.ncbi.nlm.nih.gov/pubmed/30819687?tool=bestpractice.com
[161]Kennedy J, Hill MD, Ryckborst KJ, et al. Fast assessment of stroke and transient ischaemic attack to prevent early recurrence (FASTER): a randomised controlled pilot trial. Lancet Neurol. 2007 Nov;6(11):961-9.
http://www.ncbi.nlm.nih.gov/pubmed/17931979?tool=bestpractice.com
El régimen de terapia antiplaquetaria doble de ticagrelor más ácido acetilsalicílico ha recibido la aprobación de la Administración de Medicamentos y Alimentos (FDA) en EE.UU. para reducir el riesgo de accidente cerebrovascular en pacientes con accidente cerebrovascular isquémico agudo con una puntuación NIHSS de ≤5 o AIT de alto riesgo. En Europa, en diciembre de 2021 se retiró una solicitud a la Agencia Europea del Medicamento (EMA) para cambiar la autorización de comercialización del ticagrelor con el fin de incluir la prevención del accidente cerebrovascular en adultos que han sufrido un accidente cerebrovascular isquémico de leve a moderado o un AIT de alto riesgo. Basándose en los datos de los ensayos y en la respuesta de la empresa a sus preguntas, la EMA expresó su preocupación por el hecho de que los beneficios del tratamiento a corto plazo con ticagrelor más ácido acetilsalicílico para prevenir el accidente cerebrovascular en estos pacientes no superaran claramente los riesgos de sangrados mortales y no mortales.
Evidencia que respalda la terapia antiplaquetaria doble
Un metanálisis encontró que la terapia antiplaquetaria doble con clopidogrel más ácido acetilsalicílico dentro de las 24 horas después de un accidente cerebrovascular isquémico menor (puntuación del NIHSS de ≤3; pacientes no candidatos a la trombólisis intravenosa) o AIT de alto riesgo redujo el riesgo absoluto de un accidente cerebrovascular posterior en un 2%, en comparación con el ácido acetilsalicílico en solitario.[162]Hao Q, Tampi M, O'Donnell M, et al. Clopidogrel plus aspirin versus aspirin alone for acute minor ischaemic stroke or high risk transient ischaemic attack: systematic review and meta-analysis. BMJ. 2018 Dec 18;363:k5108.
https://www.bmj.com/content/363/bmj.k5108.long
http://www.ncbi.nlm.nih.gov/pubmed/30563866?tool=bestpractice.com
La mortalidad por todas las causas no difirió entre los grupos de tratamiento; clopidogrel más ácido acetilsalicílico se asoció con un pequeño aumento absoluto del riesgo de sangrado extracraneal moderado o grave (0.2%).[162]Hao Q, Tampi M, O'Donnell M, et al. Clopidogrel plus aspirin versus aspirin alone for acute minor ischaemic stroke or high risk transient ischaemic attack: systematic review and meta-analysis. BMJ. 2018 Dec 18;363:k5108.
https://www.bmj.com/content/363/bmj.k5108.long
http://www.ncbi.nlm.nih.gov/pubmed/30563866?tool=bestpractice.com
En un segundo metanálisis, el riesgo de accidente cerebrovascular isquémico recurrente en pacientes con accidente cerebrovascular isquémico agudo o AIT se redujo significativamente con un tratamiento a corto plazo (≤1 mes; RR 0.53, IC del 95%: 0.37 a 0.78) y a medio plazo (≤3 meses; RR 0. 72, IC del 95% 0.58 a 0.90) de ácido acetilsalicílico más clopidogrel, en comparación con ácido acetilsalicílico en solitario, pero el tratamiento combinado a largo plazo (>3 meses) no redujo el riesgo de accidente cerebrovascular isquémico recurrente (RR 0.81, IC del 95% 0.63 a 1.04).[163]Rahman H, Khan SU, Nasir F, et al. Optimal duration of aspirin plus clopidogrel after ischemic stroke or transient ischemic attack. Stroke. 2019 Apr;50(4):947-53.
https://www.ahajournals.org/doi/full/10.1161/STROKEAHA.118.023978
http://www.ncbi.nlm.nih.gov/pubmed/30852971?tool=bestpractice.com
El tratamiento combinado a mediano plazo (RR 2.58; IC del 95%: 1.19 a 5.60) y a largo plazo (RR 1.87; IC del 95%: 1.36 a 2.56) aumentó significativamente el riesgo de sangrado grave, pero el tratamiento a corto plazo no lo hizo (RR 1.82; IC del 95%: 0.91 a 3.62).[163]Rahman H, Khan SU, Nasir F, et al. Optimal duration of aspirin plus clopidogrel after ischemic stroke or transient ischemic attack. Stroke. 2019 Apr;50(4):947-53.
https://www.ahajournals.org/doi/full/10.1161/STROKEAHA.118.023978
http://www.ncbi.nlm.nih.gov/pubmed/30852971?tool=bestpractice.com
El ensayo THALES con 11016 pacientes (ninguno de los cuales recibió trombólisis o trombectomía o requirió anticoagulación) demostró que en comparación con la aspirina sola, el tratamiento doble con ticagrelor más ácido acetilsalicílico reducía el riesgo de ictus con discapacidad o muerte en un plazo de 30 días (4.0% frente a 4.7%).[164]Johnston SC, Amarenco P, Denison H, et al. Ticagrelor and aspirin or aspirin alone in acute ischemic stroke or TIA. N Engl J Med. 2020 Jul 16;383(3):207-17.
https://www.doi.org/10.1056/NEJMoa1916870
http://www.ncbi.nlm.nih.gov/pubmed/32668111?tool=bestpractice.com
La hemorragia grave fue más frecuente con ticagrelor más ácido acetilsalicílico que con el ácido acetilsalicílico solo (0.5% vs. 0.1%), incluida la hemorragia intracraneal (0.4% vs. 0.1%). Para los pacientes con ictus reciente con una puntuación NIHSS <5, el ticagrelor más ácido acetilsalicílico durante 30 días fue más eficaz para prevenir el ictus isquémico recurrente que el ácido acetilsalicílico solo.[164]Johnston SC, Amarenco P, Denison H, et al. Ticagrelor and aspirin or aspirin alone in acute ischemic stroke or TIA. N Engl J Med. 2020 Jul 16;383(3):207-17.
https://www.doi.org/10.1056/NEJMoa1916870
http://www.ncbi.nlm.nih.gov/pubmed/32668111?tool=bestpractice.com
Para los pacientes con un ictus isquémico agudo y una puntuación NIHSS <5, el uso de ticagrelor más aspirina durante 30 días redujo los eventos isquémicos recurrentes en un ensayo aleatorizado, doble ciego, controlado con placebo. Sin embargo, las hemorragias graves fueron más frecuentes con ticagrelor más aspirina que con aspirina sola.[164]Johnston SC, Amarenco P, Denison H, et al. Ticagrelor and aspirin or aspirin alone in acute ischemic stroke or TIA. N Engl J Med. 2020 Jul 16;383(3):207-17.
https://www.doi.org/10.1056/NEJMoa1916870
http://www.ncbi.nlm.nih.gov/pubmed/32668111?tool=bestpractice.com
En pacientes chinos con ictus menor y AIT de alto riesgo (puntuación NIHSS <3) que son portadores del alelo de pérdida de función del CYP2C19, el uso de ticagrelor más aspirina redujo moderadamente el riesgo de ictus a los 90 días en comparación con clopidogrel más aspirina. El tratamiento combinado se mantuvo durante 21 días, seguido de ticagrelor o clopidogrel solo durante un máximo de 90 días.[165]Wang Y, Meng X, Wang A, et al. Ticagrelor versus clopidogrel in CYP2C19 loss-of-function carriers with stroke or TIA. N Engl J Med. 2021 Dec 30;385(27):2520-30.
https://www.doi.org/10.1056/NEJMoa2111749
http://www.ncbi.nlm.nih.gov/pubmed/34708996?tool=bestpractice.com
Intervenciones endovasculares
Al igual que la alteplasa, el inicio de las intervenciones endovasculares debe realizarse lo antes posible.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
La trombólisis intravenosa con alteplasa dentro de las 4.5 horas del inicio de los síntomas más la trombectomía mecánica dentro de las 6 horas del inicio de los síntomas es la norma de atención estándar para tratar los accidentes cerebrovasculares provocados por la oclusión de los grandes vasos (OGV) en aquellos pacientes que cumplen los criterios de elegibilidad.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[132]National Institute for Health and Care Excellence. Stroke and transient ischaemic attack in over 16s: diagnosis and initial management. April 2022 [internet publication].
https://www.nice.org.uk/guidance/ng128
[166]Sacks D, Baxter B, Campbell BCV, et al. Multisociety consensus quality improvement revised consensus statement for endovascular therapy of acute ischemic stroke: from the American Association of Neurological Surgeons (AANS), American Society of Neuroradiology (ASNR), Cardiovascular and Interventional Radiology Society of Europe (CIRSE), Canadian Interventional Radiology Association (CIRA), Congress of Neurological Surgeons (CNS), European Society of Minimally Invasive Neurological Therapy (ESMINT), European Society of Neuroradiology (ESNR), European Stroke Organization (ESO), Society for Cardiovascular Angiography and Interventions (SCAI), Society of Interventional Radiology (SIR), Society of NeuroInterventional Surgery (SNIS), and World Stroke Organization (WSO). J Vasc Interv Radiol. 2018 Apr;29(4):441-53.
https://www.jvir.org/article/S1051-0443(17)31073-4/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/29478797?tool=bestpractice.com
[167]Turc G, Bhogal P, Fischer U, et al. European Stroke Organisation (ESO) - European Society for Minimally Invasive Neurological Therapy (ESMINT) guidelines on mechanical thrombectomy in acute ischaemic stroke: endorsed by Stroke Alliance for Europe (SAFE). Eur Stroke J. 2019 Mar;4(1):6-12.
https://journals.sagepub.com/doi/pdf/10.1177/2396987319832140
http://www.ncbi.nlm.nih.gov/pubmed/31165090?tool=bestpractice.com
[168]Campbell BC, Donnan GA, Mitchell PJ, et al. Endovascular thrombectomy for stroke: current best practice and future goals. Stroke Vasc Neurol. 2016 Feb 16;1(1):16-22.
https://svn.bmj.com/content/1/1/16
http://www.ncbi.nlm.nih.gov/pubmed/28959994?tool=bestpractice.com
Los ensayos clínicos y los datos de registro han demostrado la eficacia de este enfoque.[169]Rodrigues FB, Neves JB, Caldeira D, et al. Endovascular treatment versus medical care alone for ischaemic stroke: systematic review and meta-analysis. BMJ. 2016 Apr 18;353:i1754.
https://www.bmj.com/content/353/bmj.i1754.long
http://www.ncbi.nlm.nih.gov/pubmed/27091337?tool=bestpractice.com
[170]Mueller-Kronast NH, Zaidat OO, Froehler MT, et al; STRATIS Investigators. Systematic evaluation of patients treated with neurothrombectomy devices for acute ischemic stroke: primary results of the STRATIS Registry. Stroke. 2017 Oct;48(10):2760-8.
https://www.ahajournals.org/doi/full/10.1161/STROKEAHA.117.016456
http://www.ncbi.nlm.nih.gov/pubmed/28830971?tool=bestpractice.com
[171]Vidale S, Agostoni E. Endovascular treatment of ischemic stroke: an updated meta-analysis of efficacy and safety. Vasc Endovascular Surg. 2017 May;51(4):215-9.
http://www.ncbi.nlm.nih.gov/pubmed/28424039?tool=bestpractice.com
[172]Roaldsen MB, Jusufovic M, Berge E, et al. Endovascular thrombectomy and intra-arterial interventions for acute ischaemic stroke. Cochrane Database Syst Rev. 2021 Jun 14;6:CD007574.
https://www.doi.org/10.1002/14651858.CD007574.pub3
http://www.ncbi.nlm.nih.gov/pubmed/34125952?tool=bestpractice.com
Aún no se ha determinado el papel de la trombectomía por sí sola sin trombólisis intravenosa (por ejemplo, cuando hay contraindicaciones para la trombólisis). La trombectomía intrarterial puede considerarse sin trombólisis intravenosa para:
Los pacientes que se presentan entre 4.5 y 6.0 horas después del inicio del accidente cerebrovascular[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Los pacientes que se presentan 6-24 horas después del inicio del accidente cerebrovascular (último estado conocido normal) que cumplen con los criterios específicos de elegibilidad.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Las intervenciones endovasculares incluyen dispositivos mecánicos de eliminación de coágulos, como los stent retrievers y la trombólisis intrarterial. Las guías de práctica clínica de la AHA/ASA recomiendan el uso de stents retrievers, en lugar de la trombólisis intrarterial y otros dispositivos mecánicos de trombectomía (p. ej., los retrievers concéntricos) como tratamiento endovascular de primera línea para el accidente cerebrovascular isquémico agudo; sin embargo, también pueden ser útiles otros dispositivos distintos de los stents retrievers en algunas circunstancias.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
El uso de un catéter proximal de balón con guía o de catéter distal de calibre grueso, en lugar del catéter cervical con guía solo, en conjunto con stent retrievers, también puede ser útil en determinados pacientes seleccionados cuidadosamente.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Además, podría estar justificada una intervención complementaria (p. ej., la trombólisis intrarterial) para lograr una reperfusión aceptable, si se utiliza dentro de las seis horas siguientes al inicio de los síntomas.
Una revisión sistemática determinó que, incluso en los pacientes con ictus leves debidos a oclusión de grandes vasos (OGV) que no reunían los requisitos para la trombólisis intravenosa con alteplasa, la trombectomía mecánica daba lugar a mejores resultados funcionales a los 90 días y sugería que este tratamiento puede desempeñar un papel importante en los pacientes que no reúnen los requisitos para recibir alteplasa intravenosa.[173]Griessenauer CJ, Medin C, Maingard J, et al. Endovascular mechanical thrombectomy in large-vessel occlusion ischemic stroke presenting with low National Institutes of Health Stroke Scale: systematic review and meta-analysis. World Neurosurg. 2018 Feb;110:263-9.
http://www.ncbi.nlm.nih.gov/pubmed/29174232?tool=bestpractice.com
El análisis de tres ensayos clínicos aleatorizados controlados (1092 pacientes) no detectó diferencias en los resultados funcionales de los pacientes que cumplían criterios para la trombólisis intravenosa con una OGV aguda que recibieron tratamiento endovascular directo en comparación con el tratamiento endovascular precedido de trombólisis intravenosa.[174]Katsanos AH, Turc G, Psychogios M, et al. Utility of intravenous alteplase prior to endovascular stroke treatment: a systematic review and meta-analysis of RCTs. Neurology. 2021 Aug 24;97(8):e777-e784.
http://www.ncbi.nlm.nih.gov/pubmed/34144996?tool=bestpractice.com
Los autores señalaron que, dado que la incertidumbre para la mayoría de los criterios de valoración sigue siendo grande y que los datos disponibles no permiten excluir la posibilidad de un beneficio o un daño global, se necesitan más ensayos controlados aleatorizados.[174]Katsanos AH, Turc G, Psychogios M, et al. Utility of intravenous alteplase prior to endovascular stroke treatment: a systematic review and meta-analysis of RCTs. Neurology. 2021 Aug 24;97(8):e777-e784.
http://www.ncbi.nlm.nih.gov/pubmed/34144996?tool=bestpractice.com
Un ensayo aleatorizado posterior (539 pacientes) encontró que el tratamiento endovascular por sí solo no era superior ni no-inferior a la alteplasa intravenosa seguida del tratamiento endovascular directo en lo que respecta al resultado de discapacidad a los 90 días después del ictus, sin diferencias en la tasa de hemorragia.[175]LeCouffe NE, Kappelhof M, Treurniet KM, et al. A randomized trial of intravenous alteplase before endovascular treatment for stroke. N Engl J Med. 2021 Nov 11;385(20):1833-44.
https://www.doi.org/10.1056/NEJMoa2107727
http://www.ncbi.nlm.nih.gov/pubmed/34758251?tool=bestpractice.com
Se ha estimado que el riesgo de complicaciones con secuelas para los pacientes de la trombectomía mecánica es de alrededor del 15%; es necesario reducir al mínimo esas complicaciones y manejarlas eficazmente para maximizar los beneficios de la trombectomía.[176]Balami JS, White PM, McMeekin PJ, et al. Complications of endovascular treatment for acute ischemic stroke: prevention and management. Int J Stroke. 2018 Jun;13(4):348-61.
http://www.ncbi.nlm.nih.gov/pubmed/29171362?tool=bestpractice.com
La anestesia general durante la trombectomía endovascular se asocia con peores resultados para los pacientes, en comparación con la ausencia de anestesia general (con o sin sedación).[177]Campbell BC, van Zwam WH, Goyal M, et al; HERMES collaborators. Effect of general anaesthesia on functional outcome in patients with anterior circulation ischaemic stroke having endovascular thrombectomy versus standard care: a meta-analysis of individual patient data. Lancet Neurol. 2018 Jan;17(1):47-53.
http://www.ncbi.nlm.nih.gov/pubmed/29263006?tool=bestpractice.com
Candidatos para intervenciones endovasculares
Las guías de práctica clínica de la AHA/ASA establecen que los pacientes que son elegibles para la alteplasa deben tratarse con alteplasa, incluso si son candidatos potenciales para la terapia endovascular con un stent retriever.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
No se debe realizarse una observación de los pacientes en busca de respuesta clínica a la alteplasa intravenosa previo al uso del tratamiento endovascular.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Las guías de práctica clínica de la AHA y la ASA sugieren que se deben tratar con un stent retriever los pacientes que cumplan con los siguientes criterios:[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Presentar una puntuación en la Modified Rankin Disability Scale previa al accidente cerebrovascular de 0-1
Tener una oclusión causal de la arteria carótida interna o de la arteria cerebral media proximal (M1).
Tener ≥18 años de edad.
Tener una puntuación en la NIHSS ≥6
Tener una puntuación ≥6 en la escala Alberta Stroke Program Early CT score (ASPECTS).
Poder comenzar la terapia endovascular (punción inguinal) dentro de las 6 horas a partir del inicio de los síntomas.
Aunque hay falta de evidencias para los stent retrievers en pacientes con accidente cerebrovascular isquémico que quedan fuera de estos criterios, pueden considerarse para su uso en pacientes con oclusión arterial de la circulación anterior que no pueden tratarse con trombólisis intravenosa, o en pacientes con oclusión de otros vasos, como la porción M2 o M3 de la arteria cerebral media, las arterias cerebrales anteriores, las arterias vertebrales, la arteria basilar o las arterias cerebrales posteriores. También pueden considerarse en pacientes <18 años de edad, o con una puntuación >1 en la Modified Rankin Disability Scale, o con una puntuación <6 en ASPECTS, si se inicia dentro de las 6 horas del inicio de los síntomas, pero los beneficios potenciales no son claros debido a que existe una falta de evidencia en dichos pacientes.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
En cuanto a la trombectomía, las guías de práctica clínica de la AHA/ASA establecen:[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
La trombectomía se recomienda dentro de las 6-16 horas desde que se conoce que el paciente haya estado bien por última vez en pacientes seleccionados con un accidente cerebrovascular isquémico agudo que presentan OGV en la circulación anterior y que cumplen otros criterios de elegibilidad de DAWN o DEFUSE 3 (ver tabla)
La trombectomía es rasonable dentro de las 16-24 horas desde que se conoce que el paciente haya estado bien por última vez en pacientes seleccionados con un accidente cerebrovascular isquémico agudo que presentan OGV en la circulación anterior y que cumplen otros criterios de elegibilidad de DAWN (ver tabla).
El ensayo DAWN utilizó la falta de coincidencia de los estudios clínicos por imágenes (combinación de la puntuación del NIHSS y los hallazgos de las imágenes de la perfusión por TC o de la IRM ponderada en difusión) como criterio de elegibilidad para seleccionar a los pacientes con OGV en la circulación anterior para la trombectomía mecánica a 6-24 horas desde que consta que el paciente ha estado bien por última vez.[178]Nogueira RG, Jadhav AP, Haussen DC, et al; DAWN Trial Investigators. Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct. N Engl J Med. 2018 Jan 4;378(1):11-21.
https://www.nejm.org/doi/10.1056/NEJMoa1706442
http://www.ncbi.nlm.nih.gov/pubmed/29129157?tool=bestpractice.com
El ensayo DEFUSE 3 usó el desajuste del núcleo de perfusión y el tamaño máximo del núcleo como criterio de imagen para seleccionar a los pacientes con OGV en la circulación anterior para la trombectomía mecánica a 6-16 horas desde que consta que el paciente ha estado bien por última vez.[179]Albers GW, Marks MP, Kemp S, et al; DEFUSE 3 Investigators. Thrombectomy for stroke at 6 to 16 hours with selection by perfusion imaging. N Engl J Med. 2018 Feb 22;378(8):708-18.
https://www.nejm.org/doi/10.1056/NEJMoa1713973
http://www.ncbi.nlm.nih.gov/pubmed/29364767?tool=bestpractice.com
Para los pacientes que, por lo demás, cumplen los criterios para la trombectomía mecánica, se recomienda la obtención de imágenes vasculares no invasivas de las arterias intracraneales durante la evaluación por imagen inicial.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Es fundamental que se observe una zona de penumbra adecuada en la perfusión por TC o en la perfusión por resonancia magnética antes de la trombectomía.
El tratamiento inicial con trombolisis intrarterial puede considerarse para pacientes cuidadosamente seleccionados con accidentes cerebrovasculares isquémicos graves de <6 horas de duración con una oclusión causal de la circulación anterior, incluida la arteria cerebral anterior, la arteria cerebral media o la arteria carótida interna distal, o aquellos con contraindicaciones o una respuesta incompleta a la trombolisis intravenosa.[180]Furlan A, Higashida R, Wechsler L, et al. Intra-arterial prourokinase for acute ischemic stroke: the PROACT II study: a randomized controlled trial. JAMA. 1999 Dec 1;282(21):2003-11.
https://jamanetwork.com/journals/jama/fullarticle/192156
http://www.ncbi.nlm.nih.gov/pubmed/10591382?tool=bestpractice.com
Sin embargo, las evidencias de eficacia son débiles y no hay intervenciones trombolíticas intrarteriales aprobadas para su uso en los accidentes cerebrovasculares.
[Figure caption and citation for the preceding image starts]: Dartos de los ensayos DAWN y DEFUSE-3 (flujo sanguíneo cerebral [CBF]; tiempo máximo [Tmax]; arteria carótida interna [ICA]; arteria cerebral media [MCA])Creado por BMJ Knowledge Centre usando datos de Dawn-Nogueira et al. N Engl J Med. 2018 378(1):11-21 and Defuse-Albers et al. N Engl J Med. 2018 22;378(8):708-18 [Citation ends].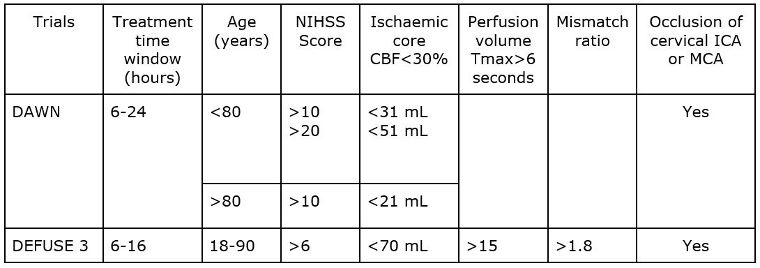
Anticoagulación
En general, no se recomienda la anticoagulación urgente en pacientes no seleccionados con accidente cerebrovascular isquémico para mejorar los resultados de la apoplejía aguda.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
En los metanálisis no se ha observado ninguna reducción de la incapacidad derivada del accidente cerebrovascular en pacientes con accidente cerebrovascular isquémico tratados con anticoagulantes, pero se ha observado un aumento del riesgo de transformación hemorrágica del accidente cerebrovascular, particularmente en pacientes con un mayor volumen sistólico.[181]Sandercock PA, Counsell C, Kane EJ. Anticoagulants for acute ischaemic stroke. Cochrane Database Syst Rev. 2015 Mar 12;(3):CD000024.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000024.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/25764172?tool=bestpractice.com
[  ]
Is there randomized controlled trial evidence to support the use of anticoagulants after acute ischemic stroke?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3899/fullMostrarme la respuesta
]
Is there randomized controlled trial evidence to support the use of anticoagulants after acute ischemic stroke?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3899/fullMostrarme la respuesta
Aunque en un ensayo no se encontró un beneficio significativo de la heparina de bajo peso molecular (HBPM) sobre el ácido acetilsalicílico en pacientes con enfermedad oclusiva de grandes arterias, los análisis de subgrupos y un ensayo controlado aleatorizado no ciego sugieren que la HBPM puede prevenir el deterioro neurológico temprano en subgrupos de pacientes, como los pacientes de edad avanzada, y en pacientes con enfermedad arterial de la circulación posterior sintomática.[182]Yi X, Lin J, Wang C, et al. Low-molecular-weight heparin is more effective than aspirin in preventing early neurologic deterioration and improving six-month outcome. J Stroke Cerebrovasc Dis. 2014 Jul;23(6):1537-44.
http://www.ncbi.nlm.nih.gov/pubmed/24656240?tool=bestpractice.com
[183]Wang QS, Chen C, Chen XY, et al. Low-molecular-weight heparin versus aspirin for acute ischemic stroke with large artery occlusive disease: subgroup analyses from the Fraxiparin in Stroke Study for the treatment of ischemic stroke (FISS-tris) study. Stroke. 2012 Feb;43(2):346-9.
https://www.ahajournals.org/doi/full/10.1161/STROKEAHA.111.628347
http://www.ncbi.nlm.nih.gov/pubmed/22076004?tool=bestpractice.com
Pacientes con fibrilación auricular
El momento óptimo para iniciar la anticoagulación en pacientes con fibrilación auricular después de un ictus isquémico agudo o un AIT no está claro. Las guías de práctica clínica de la AHA/ASA recomiendan iniciar la anticoagulación oral a los 4-14 días después del inicio de los síntomas del ictus.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
En pacientes con fibrilación auricular no valvular y un ictus o AIT, se recomienda la anticoagulación oral (p. ej., apixabán, edoxabán, rivaroxabán, dabigatrán o warfarina) para reducir el riesgo de ictus recurrente, independientemente de si el patrón de fibrilación auricular es paroxístico, persistente o permanente.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
Se recomiendan anticoagulantes orales de acción directa (ACOD) como apixabán, edoxabán, rivaroxabán o dabigatrán por encima de warfarina en pacientes con ictus o AIT y fibrilación auricular que no tengan estenosis mitral moderada a grave o una válvula cardíaca mecánica.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
Grandes ensayos aleatorizados han demostrado que los ACODs reducen clínicamente el riesgo de ictus trombótico con un menor riesgo de sangrado en comparación con los antagonistas de la vitamina K (p. ej., warfarina).[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
El rango del índice internacional normalizado (INR) para los pacientes que reciben warfarina es de 2.0 a 3.0.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
[184]Lip GY, Banerjee A, Boriani G, et al. Antithrombotic therapy for atrial fibrillation: CHEST guideline and expert panel report. Chest. 2018 Nov;154(5):1121-201.
https://journal.chestnet.org/article/S0012-3692(18)32244-X/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/30144419?tool=bestpractice.com
Debe utilizarse un sistema de puntuación validado para evaluar el riesgo hemorrágico del paciente; si es alto, debe realizarse un seguimiento más estrecho.[185]Lane DA, Lip GY. Use of the CHA(2)DS(2)-VASc and HAS-BLED scores to aid decision making for thromboprophylaxis in nonvalvular atrial fibrillation. Circulation. 2012 Aug 14;126(7):860-5.
https://www.ahajournals.org/doi/full/10.1161/circulationaha.111.060061
http://www.ncbi.nlm.nih.gov/pubmed/22891166?tool=bestpractice.com
[186]Feldman W. Treatment of occult bacteremia. Pediatrics. 1984 Dec;74(6):1131-3.
http://www.ncbi.nlm.nih.gov/pubmed/6504638?tool=bestpractice.com
Véase Fibrilación auricular de reciente comienzo.
Ictus o AIT con estenosis de una arteria intracraneal mayor
En pacientes con un ictus o AIT causado por una estenosis del 50% al 99% de una arteria intracraneal mayor, se recomienda la aspirina en lugar de la warfarina para reducir el riesgo de ictus isquémico recurrente y de muerte de causa vascular.[24]Turan TN, Zaidat OO, Gronseth GS, et al. Stroke prevention in symptomatic large artery intracranial atherosclerosis practice advisory: report of the AAN guideline subcommittee. Neurology. 2022 Mar 22;98(12):486-98.
https://www.doi.org/10.1212/WNL.0000000000200030
http://www.ncbi.nlm.nih.gov/pubmed/35314513?tool=bestpractice.com
[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
En los pacientes con accidente cerebrovascular o AIT en un plazo de 30 días atribuibles a una estenosis grave (entre el 70% y el 99%) de una arteria intracraneal principal, se recomienda añadir clopidogrel al ácido acetilsalicílico durante un máximo de 90 días para reducir aún más el riesgo de accidente cerebrovascular recurrente en los pacientes con bajo riesgo de transformación hemorrágica.[24]Turan TN, Zaidat OO, Gronseth GS, et al. Stroke prevention in symptomatic large artery intracranial atherosclerosis practice advisory: report of the AAN guideline subcommittee. Neurology. 2022 Mar 22;98(12):486-98.
https://www.doi.org/10.1212/WNL.0000000000200030
http://www.ncbi.nlm.nih.gov/pubmed/35314513?tool=bestpractice.com
[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
En pacientes con accidente cerebrovascular menor (dentro de 24 horas) o AIT de alto riesgo y estenosis ipsilateral concomitante >30% de una arteria intracraneal mayor, se puede considerar el agregado de ticagrelor al ácido acetilsalicílico hasta 30 días para reducir aún más el riesgo de accidente cerebrovascular recurrente.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
El régimen de terapia antiplaquetaria doble de ticagrelor más ácido acetilsalicílico está aprobado en EE.UU. por la FDA para reducir el riesgo de accidente cerebrovascular en pacientes con accidente cerebrovascular isquémico agudo con una puntuación NIHSS de ≤5 o AIT de alto riesgo. En Europa, en diciembre de 2021 se ha retirado una solicitud a la EMA para cambiar la autorización de comercialización del ticagrelor con el fin de incluir la prevención del accidente cerebrovascular en adultos que han sufrido un accidente cerebrovascular isquémico de leve a moderado o un AIT de alto riesgo. Basándose en los datos de los ensayos y en la respuesta de la empresa a sus preguntas, la EMA expresó su preocupación por el hecho de que los beneficios del tratamiento a corto plazo con ticagrelor más ácido acetilsalicílico para prevenir el accidente cerebrovascular en estos pacientes no superaran claramente los riesgos de sangrados mortales y no mortales.
Endarterectomía carotídea (CEA) y colocación de stents en la arteria carótida (CAS)
En los pacientes con estenosis carotídea sintomática (es decir, AIT o ictus no discapacitante) en los últimos 6 meses y estenosis carotídea ipsilateral grave (del 70% al 99%), se recomienda la endarterectomía carotídea (CEA) para reducir el riesgo de ictus futuro. Eso es adecuado siempre que el riesgo de morbilidad y mortalidad perioperatoria se estime en <6%.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
En los pacientes menores de 68 años y con estenosis carotídea sintomática (es decir, AIT o ictus no discapacitante), se prefiere la CAS en lugar de la CEA si el grado de estenosis está entre el 50% y el 69% (según lo determinado por la angiografía por sustracción digital). Eso es adecuado siempre que el riesgo de morbilidad y mortalidad perioperatoria sea <6%. La CEA o la CAS es beneficiosa para pacientes con estenosis del 70% al 99% sin "casi oclusión carotídea" (del inglés near-occlusion). No se ha encontrado evidencia de beneficio en pacientes con estenosis de <50% o con casi oclusión carotídea.[45]Barnett HJ, Taylor DW, Haynes RB, et al; North American Symptomatic Carotid Endarterectomy Trial Collaborators. Beneficial effect of carotid endarterectomy in symptomatic patients with high-grade carotid stenosis. N Engl J Med. 1991 Aug 15;325(7):445-53.
https://www.nejm.org/doi/10.1056/NEJM199108153250701
http://www.ncbi.nlm.nih.gov/pubmed/1852179?tool=bestpractice.com
[46]Barnett HJ, Taylor DW, Eliasziw M, et al; North American Symptomatic Carotid Endarterectomy Trial Collaborators. Benefit of carotid endarterectomy in patients with symptomatic moderate or severe stenosis. N Engl J Med. 1998 Nov 12;339(20):1415-25.
https://www.nejm.org/doi/10.1056/NEJM199811123392002
http://www.ncbi.nlm.nih.gov/pubmed/9811916?tool=bestpractice.com
[187]Rerkasem A, Orrapin S, Howard DP, et al. Carotid endarterectomy for symptomatic carotid stenosis. Cochrane Database Syst Rev. 2020 Sep 12;9:CD001081.
https://www.doi.org/10.1002/14651858.CD001081.pub4
http://www.ncbi.nlm.nih.gov/pubmed/32918282?tool=bestpractice.com
En los pacientes mayores de 68 años con AIT o ictus isquémico y estenosis carotídea ipsilateral moderada (del 50% al 69%) (documentada mediante imágenes por catéter o estudios de imagen no invasivos), se recomienda la endarterectomía carotídea (CEA) para reducir el riesgo de un ictus futuro. Eso es adecuado, siempre que el riesgo de morbilidad y mortalidad perioperatoria sea <6%. Los factores específicos del paciente, como la edad, el sexo y las comorbilidades, también afectarán a la idoneidad de la CEA.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
La endarterectomía carotídea y la colocación de stents en la arteria carótida mostraron beneficios similares en la prevención del ictus en un ensayo controlado aleatorizado. La colocación de stents tendía a ser más eficaz en pacientes menores de 68 años, mientras que la endarterectomía era más eficaz en pacientes mayores de 68 años. La colocación de stents se asoció con un número ligeramente más elevado de ictus y la endarterectomía se asoció con un número ligeramente más elevado de infartos de miocardio y daños en el XII nervio craneal.[188]Brott TG, Hobson RW 2nd, Howard G, et al; CREST Investigators. Stenting versus endarterectomy for treatment of carotid-artery stenosis. N Engl J Med. 2010 Jul 1;363(1):11-23.
https://www.nejm.org/doi/10.1056/NEJMoa0912321
http://www.ncbi.nlm.nih.gov/pubmed/20505173?tool=bestpractice.com
La durabilidad de la colocación de stents en la arteria carótida se demostró a los 10 años de seguimiento; la tasa de supervivencia fue ligeramente inferior en el grupo de colocación de stents que en el de endarterectomía (probablemente debido a las diferencias de riesgo peri-procedimiento).[189]Brott TG, Howard G, Roubin GS, et al; CREST Investigators. Long-term results of stenting versus endarterectomy for carotid-artery stenosis. N Engl J Med. 2016 Mar 17;374(11):1021-31.
https://www.nejm.org/doi/10.1056/NEJMoa1505215
http://www.ncbi.nlm.nih.gov/pubmed/26890472?tool=bestpractice.com
Véase Estenosis de la arteria carótida.
Foramen oval permeable (FOP)
El cierre del FOP (con terapia antiagregante), la terapia antiagregante en solitario o los anticoagulantes solos son opciones para la prevención secundaria del ictus en pacientes con ictus isquémico criptogénico secundario al FOP.[190]Messé SR, Gronseth GS, Kent DM, et al. Practice advisory update summary: patent foramen ovale and secondary stroke prevention: report of the guideline subcommittee of the American Academy of Neurology. Neurology. 2020 May 19;94(20):876-85.
https://www.doi.org/10.1212/WNL.0000000000009443
http://www.ncbi.nlm.nih.gov/pubmed/32350058?tool=bestpractice.com
Las opciones antiagregantes incluyen aspirina o clopidogrel.[191]Kuijpers T, Spencer FA, Siemieniuk RA, et al. Patent foramen ovale closure, antiplatelet therapy or anticoagulation therapy alone for management of cryptogenic stroke? A clinical practice guideline. BMJ. 2018 Jul 25;362:k2515.
https://www.bmj.com/content/362/bmj.k2515.long
http://www.ncbi.nlm.nih.gov/pubmed/30045912?tool=bestpractice.com
En pacientes con una puntuación alta en la escala de riesgo de embolia paradójica (RoPE), el cierre del FOP reduce la recurrencia de ictus en comparación con el tratamiento médico en solitario.[192]Ahmed N, Steiner T, Caso V, et al; ESO-KSU session participants. Recommendations from the ESO-Karolinska Stroke Update Conference, Stockholm 13-15 November 2016. Eur Stroke J. 2017 Jun;2(2):95-102.
http://journals.sagepub.com/doi/full/10.1177/2396987317699144
[193]Ahmad Y, Howard JP, Arnold A, et al. Patent foramen ovale closure vs. medical therapy for cryptogenic stroke: a meta-analysis of randomized controlled trials. Eur Heart J. 2018 May 7;39(18):1638-49.
https://academic.oup.com/eurheartj/article/39/18/1638/4944510
http://www.ncbi.nlm.nih.gov/pubmed/29590333?tool=bestpractice.com
[194]Lattanzi S, Brigo F, Cagnetti C, et al. Patent foramen ovale and cryptogenic stroke or transient ischemic attack: to close or not to close? A systematic review and meta-analysis. Cerebrovasc Dis. 2018;45(5-6):193-203.
https://www.karger.com/Article/FullText/488401
http://www.ncbi.nlm.nih.gov/pubmed/29649819?tool=bestpractice.com
[195]Ntaios G, Papavasileiou V, Sagris D, et al. Closure of patent foramen ovale versus medical therapy in patients with cryptogenic stroke or transient ischemic attack: updated systematic review and meta-analysis. Stroke. 2018 Feb;49(2):412-8.
https://www.ahajournals.org/doi/full/10.1161/STROKEAHA.117.020030
http://www.ncbi.nlm.nih.gov/pubmed/29335335?tool=bestpractice.com
[196]Vidale S, Russo F, Campana C, et al. Patent foramen ovale closure versus medical therapy in cryptogenic strokes and transient ischemic attacks: a meta-analysis of randomized trials. Angiology. 2019 Apr;70(4):325-31.
http://www.ncbi.nlm.nih.gov/pubmed/30270651?tool=bestpractice.com
En pacientes menores de 60 años con un FOP y un infarto de apariencia embólica y ningún otro mecanismo de ictus identificado, los médicos pueden recomendar el cierre. Esta decisión siempre debe incluir una exposición de los beneficios potenciales (reducción absoluta del riesgo de ictus recurrente del 3.4% a los 5 años) y los riesgos (tasa de complicaciones periprocedimiento del 3.9% y aumento de la tasa absoluta de fibrilación auricular no periprocedimiento del 0.33% anual).[190]Messé SR, Gronseth GS, Kent DM, et al. Practice advisory update summary: patent foramen ovale and secondary stroke prevention: report of the guideline subcommittee of the American Academy of Neurology. Neurology. 2020 May 19;94(20):876-85.
https://www.doi.org/10.1212/WNL.0000000000009443
http://www.ncbi.nlm.nih.gov/pubmed/32350058?tool=bestpractice.com
El cierre del FOP se puede considerar en otras poblaciones, como en un paciente de 60 a 65 años con un grado muy limitado de factores de riesgo vasculares tradicionales (es decir, hipertensión, diabetes, hiperlipidemia o tabaquismo) y ningún otro mecanismo de ictus detectado después de una evaluación exhaustiva, incluida la monitorización prolongada para detectar fibrilación auricular.[190]Messé SR, Gronseth GS, Kent DM, et al. Practice advisory update summary: patent foramen ovale and secondary stroke prevention: report of the guideline subcommittee of the American Academy of Neurology. Neurology. 2020 May 19;94(20):876-85.
https://www.doi.org/10.1212/WNL.0000000000009443
http://www.ncbi.nlm.nih.gov/pubmed/32350058?tool=bestpractice.com
Todos los pacientes con un accidente cerebrovascular previo deben ser tratados con una medicación antitrombótica de forma indefinida si no existe una contraindicación hemorrágica, independientemente de que exista un FOP o de que esté cerrado.
Es probable que en el caso de pacientes menores de 60 años, el cierre del FOP sumado a la terapia antiagregante sea beneficioso para la prevención secundaria de ictus, en comparación con la terapia anticoagulante.[191]Kuijpers T, Spencer FA, Siemieniuk RA, et al. Patent foramen ovale closure, antiplatelet therapy or anticoagulation therapy alone for management of cryptogenic stroke? A clinical practice guideline. BMJ. 2018 Jul 25;362:k2515.
https://www.bmj.com/content/362/bmj.k2515.long
http://www.ncbi.nlm.nih.gov/pubmed/30045912?tool=bestpractice.com
El cierre del FOP más la terapia antiplaquetaria es preferible a la terapia antiplaquetaria en solitario, si la anticoagulación está contraindicada o se ha rechazado.[191]Kuijpers T, Spencer FA, Siemieniuk RA, et al. Patent foramen ovale closure, antiplatelet therapy or anticoagulation therapy alone for management of cryptogenic stroke? A clinical practice guideline. BMJ. 2018 Jul 25;362:k2515.
https://www.bmj.com/content/362/bmj.k2515.long
http://www.ncbi.nlm.nih.gov/pubmed/30045912?tool=bestpractice.com
[197]Mir H, Siemieniuk RA, Ge L, et al. Patent foramen ovale closure, antiplatelet therapy or anticoagulation in patients with patent foramen ovale and cryptogenic stroke: a systematic review and network meta-analysis incorporating complementary external evidence. BMJ Open. 2018 Jul 25;8(7):e023761.
https://bmjopen.bmj.com/content/8/7/e023761.long
http://www.ncbi.nlm.nih.gov/pubmed/30049703?tool=bestpractice.com
La fibrilación auricular es más frecuente en los pacientes que tienen su FOP cerrado, pero es mayormente transitoria.[195]Ntaios G, Papavasileiou V, Sagris D, et al. Closure of patent foramen ovale versus medical therapy in patients with cryptogenic stroke or transient ischemic attack: updated systematic review and meta-analysis. Stroke. 2018 Feb;49(2):412-8.
https://www.ahajournals.org/doi/full/10.1161/STROKEAHA.117.020030
http://www.ncbi.nlm.nih.gov/pubmed/29335335?tool=bestpractice.com
[197]Mir H, Siemieniuk RA, Ge L, et al. Patent foramen ovale closure, antiplatelet therapy or anticoagulation in patients with patent foramen ovale and cryptogenic stroke: a systematic review and network meta-analysis incorporating complementary external evidence. BMJ Open. 2018 Jul 25;8(7):e023761.
https://bmjopen.bmj.com/content/8/7/e023761.long
http://www.ncbi.nlm.nih.gov/pubmed/30049703?tool=bestpractice.com
Véase Foramen oval permeable.
Pacientes con trombosis de los senos venosos cerebrales (TSVC)
La TSVC puede provocar una hemorragia venosa cerebral, un ictus isquémico, edema cerebral, desplazamiento de la línea media y una elevación de la presión intracraneal. El tratamiento con anticoagulación debe comenzar tan pronto como se confirme el diagnóstico de la TSVC.[8]Saposnik G, Bushnell C, Coutinho JM, et al. Diagnosis and management of cerebral venous thrombosis: a scientific statement from the American Heart Association. Stroke. 2024 Mar;55(3):e77-90.
https://www.doi.org/10.1161/STR.0000000000000456
http://www.ncbi.nlm.nih.gov/pubmed/38284265?tool=bestpractice.com
[83]Ulivi L, Squitieri M, Cohen H, et al. Cerebral venous thrombosis: a practical guide. Pract Neurol. 2020 Oct;20(5):356-67.
https://www.doi.org/10.1136/practneurol-2019-002415
http://www.ncbi.nlm.nih.gov/pubmed/32958591?tool=bestpractice.com
Debe buscarse la orientación de un especialista para saber si se debe elegir la heparina de bajo peso molecular (HBPM) o la heparina no fraccionada. La American Heart Association y la Organización Europea de Accidentes Cerebrovasculares sugieren preferentemente una HBPM en lugar de la heparina no fraccionada debido a la administración más práctica, el efecto anticoagulante más predecible, el menor riesgo de trombocitopenia, la eficacia de la HBPM y las tasas más bajas de complicaciones hemorrágicas.[8]Saposnik G, Bushnell C, Coutinho JM, et al. Diagnosis and management of cerebral venous thrombosis: a scientific statement from the American Heart Association. Stroke. 2024 Mar;55(3):e77-90.
https://www.doi.org/10.1161/STR.0000000000000456
http://www.ncbi.nlm.nih.gov/pubmed/38284265?tool=bestpractice.com
[198]Ferro JM, Bousser MG, Canhão P, et al. European Stroke Organization guideline for the diagnosis and treatment of cerebral venous thrombosis - endorsed by the European Academy of Neurology. Eur J Neurol. 2017 Oct;24(10):1203-13.
https://www.doi.org/10.1111/ene.13381
http://www.ncbi.nlm.nih.gov/pubmed/28833980?tool=bestpractice.com
La presencia de hemorragia venosa no constituye una contraindicación para la anticoagulación.[8]Saposnik G, Bushnell C, Coutinho JM, et al. Diagnosis and management of cerebral venous thrombosis: a scientific statement from the American Heart Association. Stroke. 2024 Mar;55(3):e77-90.
https://www.doi.org/10.1161/STR.0000000000000456
http://www.ncbi.nlm.nih.gov/pubmed/38284265?tool=bestpractice.com
[199]Zuurbier SM, Arnold M, Middeldorp S, et al. Risk of cerebral venous thrombosis in obese women. JAMA Neurol. 2016 May 1;73(5):579-84.
https://www.doi.org/10.1001/jamaneurol.2016.0001
http://www.ncbi.nlm.nih.gov/pubmed/26974867?tool=bestpractice.com
[200]Fan Y, Yu J, Chen H, et al. Chinese Stroke Association guidelines for clinical management of cerebrovascular disorders: executive summary and 2019 update of clinical management of cerebral venous sinus thrombosis. Stroke Vasc Neurol. 2020 Jun;5(2):152-8.
https://www.doi.org/10.1136/svn-2020-000358
http://www.ncbi.nlm.nih.gov/pubmed/32409571?tool=bestpractice.com
Para la prevención posterior de la TSVC, la duración del tratamiento depende del número de episodios de TSVC y de si se ha identificado una causa subyacente conocida. Se debe hablar sobre la duración del tratamiento con un hematólogo. Los anticoagulantes orales utilizados para la TSVC incluyen los antagonistas de la vitamina K, como la warfarina (rango de INR de 2.0 a 3.0), y los ACOD. Los ACOD parecen ser una opción alternativa segura y eficaz a los AVK según estudios aleatorizados retrospectivos y prospectivos abiertos.[8]Saposnik G, Bushnell C, Coutinho JM, et al. Diagnosis and management of cerebral venous thrombosis: a scientific statement from the American Heart Association. Stroke. 2024 Mar;55(3):e77-90.
https://www.doi.org/10.1161/STR.0000000000000456
http://www.ncbi.nlm.nih.gov/pubmed/38284265?tool=bestpractice.com
[201]Ferro JM, Coutinho JM, Dentali F, et al. Safety and efficacy of dabigatran etexilate vs dose-adjusted warfarin in patients with cerebral venous thrombosis: a randomized clinical trial. JAMA Neurol. 2019 Dec 1;76(12):1457-65.
https://www.doi.org/10.1001/jamaneurol.2019.2764
http://www.ncbi.nlm.nih.gov/pubmed/31479105?tool=bestpractice.com
[202]Field TS, Dizonno V, Almekhlafi MA, et al. Study of rivaroxaban for cerebral venous thrombosis: a randomized controlled feasibility trial comparing anticoagulation with rivaroxaban to standard-of-care in symptomatic cerebral venous thrombosis. Stroke. 2023 Nov;54(11):2724-36.
https://www.doi.org/10.1161/STROKEAHA.123.044113
http://www.ncbi.nlm.nih.gov/pubmed/37675613?tool=bestpractice.com
[203]Yaghi S, Shu L, Bakradze E, et al. Direct oral anticoagulants versus warfarin in the treatment of cerebral venous thrombosis (ACTION-CVT): a multicenter international study. Stroke. 2022 Mar;53(3):728-38.
https://www.doi.org/10.1161/STROKEAHA.121.037541
http://www.ncbi.nlm.nih.gov/pubmed/35143325?tool=bestpractice.com
[204]Yaghi S, Saldanha IJ, Misquith C, et al. Direct oral anticoagulants versus vitamin K antagonists in cerebral venous thrombosis: a systematic review and meta-analysis. Stroke. 2022 Oct;53(10):3014-24.
https://www.doi.org/10.1161/STROKEAHA.122.039579
http://www.ncbi.nlm.nih.gov/pubmed/35938419?tool=bestpractice.com
En casos seleccionados de TSVC, las terapias endovasculares (trombectomía directa o trombólisis intracoágulo con r-tPA) pueden ser consideradas por un equipo multidisciplinario.[83]Ulivi L, Squitieri M, Cohen H, et al. Cerebral venous thrombosis: a practical guide. Pract Neurol. 2020 Oct;20(5):356-67.
https://www.doi.org/10.1136/practneurol-2019-002415
http://www.ncbi.nlm.nih.gov/pubmed/32958591?tool=bestpractice.com
Dada la falta de ensayos controlados (y desenlaces más desfavorables en los metanálisis), las terapias endovasculares se reservan para pacientes con evidencia de propagación del trombo, para individuos con deterioro neurológico a pesar del tratamiento médico o para aquellos con contraindicaciones para la anticoagulación.[8]Saposnik G, Bushnell C, Coutinho JM, et al. Diagnosis and management of cerebral venous thrombosis: a scientific statement from the American Heart Association. Stroke. 2024 Mar;55(3):e77-90.
https://www.doi.org/10.1161/STR.0000000000000456
http://www.ncbi.nlm.nih.gov/pubmed/38284265?tool=bestpractice.com
Estatinas
Se recomienda el tratamiento con estatinas con efectos hipolipemiantes intensivos en pacientes con accidente cerebrovascular isquémico o AIT, a fin de reducir el riesgo de accidente cerebrovascular y de eventos cardiovasculares.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
[205]Grundy SM, Stone NJ, Bailey AL, et al. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA guideline on the management of blood cholesterol: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019 Jun 18;139(25):e1082-143.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000000625
http://www.ncbi.nlm.nih.gov/pubmed/30586774?tool=bestpractice.com
El tratamiento con estatinas no debe iniciarse inmediatamente. Existe consenso en que es seguro comenzar con estatinas después de 48 horas.[132]National Institute for Health and Care Excellence. Stroke and transient ischaemic attack in over 16s: diagnosis and initial management. April 2022 [internet publication].
https://www.nice.org.uk/guidance/ng128
El tratamiento con estatinas debe mantenerse en las personas que ya están recibiendo estatinas.[132]National Institute for Health and Care Excellence. Stroke and transient ischaemic attack in over 16s: diagnosis and initial management. April 2022 [internet publication].
https://www.nice.org.uk/guidance/ng128
Existe evidencia de que la tasa de eventos cardiovasculares recurrentes o ictus es menor en pacientes con lipoproteína de baja densidad (LDL) controlada en <70 mg/dL en comparación con aquellos con LDL entre 90 y 110 mg/dL.[24]Turan TN, Zaidat OO, Gronseth GS, et al. Stroke prevention in symptomatic large artery intracranial atherosclerosis practice advisory: report of the AAN guideline subcommittee. Neurology. 2022 Mar 22;98(12):486-98.
https://www.doi.org/10.1212/WNL.0000000000200030
http://www.ncbi.nlm.nih.gov/pubmed/35314513?tool=bestpractice.com
[206]Amarenco P, Kim JS, Labreuche J, et al. A Comparison of two LDL cholesterol targets after ischemic stroke. N Engl J Med. 2020 Jan 2;382(1):9.
https://www.doi.org/10.1056/NEJMoa1910355
http://www.ncbi.nlm.nih.gov/pubmed/31738483?tool=bestpractice.com
Se recomienda la monitorización de las enzimas hepáticas en los pacientes que toman estatinas. Debe tenerse precaución al recetar estatinas de alta intensidad a pacientes con antecedentes de hemorragia intracerebral.
En pacientes con ictus isquémico sin cardiopatía coronaria conocida, sin fuentes cardíacas mayores de embolismo y colesterol LDL (LDL-C) >100 mg/dL, está indicada la atorvastatina para reducir el riesgo de recurrencia de ictus.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
En pacientes con ictus o AIT e hiperlipidemia, se debe evaluar la adherencia a los cambios en el estilo de vida y los efectos del tratamiento reductor del colesterol LDL mediante la medición de los lípidos en ayunas y los indicadores de seguridad adecuados a las 4-12 semanas después del inicio de la estatina o del ajuste de la dosis. Esta evaluación debe repetirse cada 3-12 meses a partir de entonces, según la necesidad de evaluar la adherencia o la seguridad.[102]Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke. 2021 Jul;52(7):e364-467.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000375
http://www.ncbi.nlm.nih.gov/pubmed/34024117?tool=bestpractice.com
Cuidados de soporte
Al mismo tiempo que la evaluación aguda para la trombólisis y/o la trombectomía, se deben tomar las siguientes medidas:
Apoyar la oxigenación de la sangre. Se deberá proporcionar oxigenoterapia solo cuando la saturación de oxígeno en sangre sea <94%. El uso amplio de oxígeno se asocia con un aumento de la mortalidad en pacientes gravemente enfermos.[207]Chu DK, Kim LH, Young PJ, et al. Mortality and morbidity in acutely ill adults treated with liberal versus conservative oxygen therapy (IOTA): a systematic review and meta-analysis. Lancet. 2018 Apr 28;391(10131):1693-705.
http://www.ncbi.nlm.nih.gov/pubmed/29726345?tool=bestpractice.com
[208]Siemieniuk RAC, Chu DK, Kim LH, et al. Oxygen therapy for acutely ill medical patients: a clinical practice guideline. BMJ. 2018 Oct 24;363:k4169.
https://www.bmj.com/content/363/bmj.k4169.long
http://www.ncbi.nlm.nih.gov/pubmed/30355567?tool=bestpractice.com
Puede ser necesario intubar con ventilación mecánica a los pacientes con un nivel de consciencia disminuido o hipoxemia refractaria.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[209]Rønning OM, Guldvog B. Should stroke victims routinely receive supplemental oxygen? A quasi-randomized controlled trial. Stroke. 1999 Oct;30(10):2033-7.
https://www.ahajournals.org/doi/full/10.1161/01.str.30.10.2033
http://www.ncbi.nlm.nih.gov/pubmed/10512903?tool=bestpractice.com
Tratamiento de soporte de la presión arterial sistémica. El manejo de la presión arterial en casos de ictus isquémico agudo es un tema controvertido, ya que existe evidencia contradictoria y una falta de grandes ensayos clínicos controlados.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Muchos pacientes con ictus isquémico presentan una presión arterial elevada en el momento de la presentación. El hecho de disminuir la presión arterial podría reducir la presión de perfusión cerebral y promover la extensión del ictus.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[213]Ahmed N, Näsman P, Wahlgren NG. Effect of intravenous nimodipine on blood pressure and outcome after acute stroke. Stroke. 2000 Jun;31(6):1250-5.
https://www.ahajournals.org/doi/full/10.1161/01.str.31.6.1250
http://www.ncbi.nlm.nih.gov/pubmed/10835440?tool=bestpractice.com
Sin embargo, las guías de práctica clínica de la AHA/ASA recomiendan el tratamiento precoz de la hipertensión cuando sea necesario por sus comorbilidades. Entre las comorbilidades particulares se encuentran el evento coronario agudo concomitante, la insuficiencia cardíaca aguda, la disección aórtica, sICH [hemorragia intracerebral sintomática] postfibrinolisis o la preeclampsia/eclampsia. El manejo de estos pacientes debe individualizarse, pero en general, la reducción de la presión arterial en un 15% de la inicial es un objetivo razonable.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Se requiere una presión sanguínea de <185/110 mmHg antes de iniciar la alteplasa intravenosa. Se ha encontrado que la reducción intensiva de la presión sanguínea sistólica a 130-140 mmHg 1 hora antes del tratamiento con alteplasa es segura, pero no parece mejorar los resultados clínicos, en comparación con un objetivo de <180 mmHg.[214]Anderson CS, Huang Y, Lindley RI, et al; ENCHANTED Investigators and Coordinators. Intensive blood pressure reduction with intravenous thrombolysis therapy for acute ischaemic stroke (ENCHANTED): an international, randomised, open-label, blinded-endpoint, phase 3 trial. Lancet. 2019 Mar 2;393(10174):877-88.
http://www.ncbi.nlm.nih.gov/pubmed/30739745?tool=bestpractice.com
[215]Sandset EC, Anderson CS, Bath PM, et al. European Stroke Organisation (ESO) guidelines on blood pressure management in acute ischaemic stroke and intracerebral haemorrhage. Eur Stroke J. 2021 Jun;6(2):XLVIII-LXXXIX.
https://www.doi.org/10.1177/23969873211012133
http://www.ncbi.nlm.nih.gov/pubmed/34780578?tool=bestpractice.com
Normalizar los niveles de glucemia (necesario antes de iniciar la alteplasa intravenosa).
La hipoglucemia puede causar lesiones cerebrales y debe evitarse. Un ensayo aleatorizado mostró que en los pacientes con un ictus isquémico agudo e hiperglucemia, el control agresivo de la glucemia mediante infusión de insulina intravenosa no produjo una diferencia significativa en un resultado funcional favorable a los 90 días en comparación con el control glucémico estándar, pero se asoció con episodios de hipoglucemia grave en más pacientes (2.6%).[216]Johnston KC, Bruno A, Pauls Q, et al; Neurological Emergencies Treatment Trials Network and the SHINE Trial Investigators. Intensive vs standard treatment of hyperglycemia and functional outcome in patients with acute ischemic stroke: the SHINE randomized clinical trial. JAMA. 2019 Jul 23;322(4):326-35.
https://jamanetwork.com/journals/jama/fullarticle/2738553
http://www.ncbi.nlm.nih.gov/pubmed/31334795?tool=bestpractice.com
La hipoglucemia se puede controlar adecuadamente mediante inyecciones subcutáneas de insulina frecuentes basadas en una escala móvil.[217]Fuentes B, Ntaios G, Putaala J, et al. European Stroke Organisation (ESO) guidelines on glycaemia management in acute stroke. Eur Stroke J. 2018 Mar;3(1):5-21.
https://journals.sagepub.com/doi/full/10.1177/2396987317742065
http://www.ncbi.nlm.nih.gov/pubmed/31008333?tool=bestpractice.com
Se ha asociado la hiperglucemia con un desenlace desfavorable y con el riesgo de que el accidente cerebrovascular isquémico se transforme en uno hemorrágico.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[138]Baird TA, Parsons MW, Phanh T, et al. Persistent poststroke hyperglycemia is independently associated with infarct expansion and worse clinical outcome. Stroke. 2003 Sep;34(9):2208-14.
https://www.ahajournals.org/doi/full/10.1161/01.str.0000085087.41330.ff
http://www.ncbi.nlm.nih.gov/pubmed/12893952?tool=bestpractice.com
[139]Kase CS, Furlan AJ, Wechsler LR, et al. Cerebral hemorrhage after intra-arterial thrombolysis for ischemic stroke: the PROACT II trial. Neurology. 2001 Nov 13;57(9):1603-10.
http://www.ncbi.nlm.nih.gov/pubmed/11706099?tool=bestpractice.com
[140]Demchuk AM, Morgenstern LB, Krieger DW, et al. Serum glucose level and diabetes predict tissue plasminogen activator-related intracerebral hemorrhage in acute ischemic stroke. Stroke. 1999 Jan;30(1):34-9.
https://www.ahajournals.org/doi/full/10.1161/01.str.30.1.34
http://www.ncbi.nlm.nih.gov/pubmed/9880385?tool=bestpractice.com
Se recomienda el tratamiento de la glucemia significativamente elevada, ya que la evidencia indica que la hiperglucemia intrahospitalaria persistente durante las primeras 24 horas después de un ictus isquémico agudo se asocia con peores resultados que la normoglucemia.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Reducir la fiebre. La fiebre puede asociarse con peores resultados tras el ictus.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[218]Saxena M, Young P, Pilcher D, et al. Early temperature and mortality in critically ill patients with acute neurological diseases: trauma and stroke differ from infection. Intensive Care Med. 2015 May;41(5):823-32.
https://www.doi.org/10.1007/s00134-015-3676-6
http://www.ncbi.nlm.nih.gov/pubmed/25643903?tool=bestpractice.com
Por lo tanto, es razonable tratar la fiebre, aunque todavía no se ha demostrado que sea eficaz en ensayos controlados.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[219]Krieger DW, Yenari MA. Therapeutic hypothermia for acute ischemic stroke: what do laboratory studies teach us? Stroke. 2004 Jun;35(6):1482-9.
https://www.ahajournals.org/doi/full/10.1161/01.str.0000126118.44249.5c
http://www.ncbi.nlm.nih.gov/pubmed/15073396?tool=bestpractice.com
[220]Den Hertog HM, van der Worp HB, Tseng MC, et al. Cooling therapy for acute stroke. Cochrane Database Syst Rev. 2009 Jan 21;(1):CD001247.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001247.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/19160194?tool=bestpractice.com
[221]Ntaios G, Dziedzic T, Michel P, et al. European Stroke Organisation (ESO) guidelines for the management of temperature in patients with acute ischemic stroke. Int J Stroke. 2015 Aug;10(6):941-9.
http://journals.sagepub.com/doi/full/10.1111/ijs.12579
http://www.ncbi.nlm.nih.gov/pubmed/26148223?tool=bestpractice.com
Aunque no se ha observado en ensayos clínicos que estos pasos sean eficaces, pueden retrasar el avance del accidente cerebrovascular o prevenir su extensión, ya que optimizan la administración de sustrato de energía y el metabolismo de energía del tejido.
Después de la evaluación y el tratamiento en el servicio de urgencias, se deberán trasladar los pacientes con accidente cerebrovascular isquémico a una unidad especializada en accidentes cerebrovasculares.[132]National Institute for Health and Care Excellence. Stroke and transient ischaemic attack in over 16s: diagnosis and initial management. April 2022 [internet publication].
https://www.nice.org.uk/guidance/ng128
Estas unidades mejoran el resultado funcional de los accidentes cerebrovasculares y la supervivencia.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[222]Langhorne P, Ramachandra S, Stroke Unit Trialists' Collaboration. Organised inpatient (stroke unit) care for stroke: network meta-analysis. Cochrane Database Syst Rev. 2020 Apr 23;(4):CD000197.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000197.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/32324916?tool=bestpractice.com
[223]Adeoye O, Nyström KV, Yavagal DR, et al. Recommendations for the establishment of stroke systems of care: a 2019 update. Stroke. 2019 Jul;50(7):e187-210.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000173
http://www.ncbi.nlm.nih.gov/pubmed/31104615?tool=bestpractice.com
[  ]
How does organized inpatient care compare with care on a general medical ward for people with stroke/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3108/fullMostrarme la respuesta Las unidades de accidentes cerebrovasculares tienen equipos multidisciplinarios que incluyen médicos, personal de enfermería y especialistas en rehabilitación con conocimientos especializados en accidentes cerebrovasculares.[224]National Institute for Health and Care Excellence. Stroke rehabilitation in adults. Jun 2013 [internet publication].
https://www.nice.org.uk/guidance/cg162
Los cuidados de soporte mejorados, la prevención de complicaciones como la infección y la iniciación más temprana del tratamiento de rehabilitación se encuentran entre los mecanismos por los que se cree que las unidades de accidentes cerebrovasculares producen mejores resultados.
]
How does organized inpatient care compare with care on a general medical ward for people with stroke/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3108/fullMostrarme la respuesta Las unidades de accidentes cerebrovasculares tienen equipos multidisciplinarios que incluyen médicos, personal de enfermería y especialistas en rehabilitación con conocimientos especializados en accidentes cerebrovasculares.[224]National Institute for Health and Care Excellence. Stroke rehabilitation in adults. Jun 2013 [internet publication].
https://www.nice.org.uk/guidance/cg162
Los cuidados de soporte mejorados, la prevención de complicaciones como la infección y la iniciación más temprana del tratamiento de rehabilitación se encuentran entre los mecanismos por los que se cree que las unidades de accidentes cerebrovasculares producen mejores resultados.
En la fase subaguda del cuidado hospitalario, es necesario proporcionar soporte nutricional, terapia de rehabilitación (física, ocupacional y/o terapia del habla, según se indique), prevención de la aspiración (evaluación de la deglución) y prevención de la trombosis venosa profunda (TVP)/tromboembolismo venoso (TEV).
[  ]
In people with aphasia following stroke, how does the use of speech and language therapy affect outcomes?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1384/fullMostrarme la respuesta
[
]
In people with aphasia following stroke, how does the use of speech and language therapy affect outcomes?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1384/fullMostrarme la respuesta
[  ]
Does electromechanical and robot‐assisted arm training improve generic activities of daily living, arm function, and arm strength in patients who have had a stroke?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2317/fullMostrarme la respuesta
]
Does electromechanical and robot‐assisted arm training improve generic activities of daily living, arm function, and arm strength in patients who have had a stroke?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2317/fullMostrarme la respuesta
El deterioro de la deglución es frecuente en casos de accidente cerebrovascular y se asocia con un mayor riesgo de neumonía por aspiración y muerte.[225]Martino R, Foley N, Bhogal S, et al. Dysphagia after stroke: incidence, diagnosis, and pulmonary complications. Stroke. 2005 Dec;36(12):2756-63.
https://www.ahajournals.org/doi/full/10.1161/01.str.0000190056.76543.eb
http://www.ncbi.nlm.nih.gov/pubmed/16269630?tool=bestpractice.com
[226]Mann G, Hankey GJ, Cameron D. Swallowing function after stroke: prognosis and prognostic factors at 6 months. Stroke. 1999 Apr;30(4):744-8.
https://www.ahajournals.org/doi/full/10.1161/01.str.30.4.744
http://www.ncbi.nlm.nih.gov/pubmed/10187872?tool=bestpractice.com
Las guías de práctica clínica respaldan el uso de una prueba de la deglución a pie de cama antes de comer o beber, pero no proporcionan datos específicos sobre la administración y la interpretación de la prueba.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Un método razonable es suspender la ingesta oral si hay tos o voz húmeda después de la deglución de un vaso de agua de pequeño tamaño. Los pacientes que no pueden alimentarse por vía oral deben recibir líquidos isotónicos (para disminuir el riesgo de edema cerebral) y recibir alimentación enteral por sonda nasogástrica, nasoduodenal o de gastrostomía percutánea.
[  ]
How does percutaneous endoscopic gastrostomy compare with nasogastric tube feeding in people with swallowing disturbances?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1134/fullMostrarme la respuesta
]
How does percutaneous endoscopic gastrostomy compare with nasogastric tube feeding in people with swallowing disturbances?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1134/fullMostrarme la respuesta
Profilaxis para la TEV
La tromboembolia venosa (TEV) es la causante de cerca del 10% de las muertes por accidente cerebrovascular.[227]Wijdicks EF, Scott JP. Pulmonary embolism associated with acute stroke. Mayo Clin Proc. 1997 Apr;72(4):297-300.
http://www.ncbi.nlm.nih.gov/pubmed/9121173?tool=bestpractice.com
Se recomienda la compresión neumática intermitente de las piernas para reducir el riesgo de TVP/TEV en pacientes con accidente cerebrovascular no ambulatorio.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[228]Dennis M, Caso V, Kappelle LJ, et al; European Stroke Organisation. European Stroke Organisation (ESO) guidelines for prophylaxis for venous thromboembolism in immobile patients with acute ischaemic stroke. Eur Stroke J. 2016 Mar;1(1):6-19.
https://journals.sagepub.com/doi/full/10.1177/2396987316628384
http://www.ncbi.nlm.nih.gov/pubmed/31008263?tool=bestpractice.com
[229]Dennis M, Sandercock P, Reid J, et al; CLOTS (Clots in Legs Or sTockings after Stroke) Trials Collaboration. Effectiveness of intermittent pneumatic compression in reduction of risk of deep vein thrombosis in patients who have had a stroke (CLOTS 3): a multicentre randomised controlled trial. Lancet. 2013 Aug 10;382(9891):516-24.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(13)61050-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/23727163?tool=bestpractice.com
No se recomiendan las medias de compresión elástica.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[228]Dennis M, Caso V, Kappelle LJ, et al; European Stroke Organisation. European Stroke Organisation (ESO) guidelines for prophylaxis for venous thromboembolism in immobile patients with acute ischaemic stroke. Eur Stroke J. 2016 Mar;1(1):6-19.
https://journals.sagepub.com/doi/full/10.1177/2396987316628384
http://www.ncbi.nlm.nih.gov/pubmed/31008263?tool=bestpractice.com
Los beneficios de la heparina subcutánea profiláctica en pacientes con un accidente cerebrovascular isquémico agudo no están bien establecidos; disminuye las tasas de trombosis venosa profunda y embolia pulmonar, pero también se asocia con un aumento significativo de la tasa de hemorragia, sin efectos significativos en la mortalidad o el estado funcional en el seguimiento final.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
En las guías de práctica clínica se señala que puede haber un subgrupo de pacientes para los que los beneficios de la reducción del riesgo de TEV con heparina superan el mayor riesgo de sangrado intracraneal y extracraneal.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[228]Dennis M, Caso V, Kappelle LJ, et al; European Stroke Organisation. European Stroke Organisation (ESO) guidelines for prophylaxis for venous thromboembolism in immobile patients with acute ischaemic stroke. Eur Stroke J. 2016 Mar;1(1):6-19.
https://journals.sagepub.com/doi/full/10.1177/2396987316628384
http://www.ncbi.nlm.nih.gov/pubmed/31008263?tool=bestpractice.com
No existe una herramienta de predicción para identificar a estos pacientes, pero los pacientes que se consideran con un riesgo particularmente alto de TEV incluyen aquellos con parálisis completa de la pierna, TEV anterior, deshidratación o comorbilidades (como neoplasia maligna o sepsis), o bien pacientes fumadores o que lo han sido recientemente.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[132]National Institute for Health and Care Excellence. Stroke and transient ischaemic attack in over 16s: diagnosis and initial management. April 2022 [internet publication].
https://www.nice.org.uk/guidance/ng128
[228]Dennis M, Caso V, Kappelle LJ, et al; European Stroke Organisation. European Stroke Organisation (ESO) guidelines for prophylaxis for venous thromboembolism in immobile patients with acute ischaemic stroke. Eur Stroke J. 2016 Mar;1(1):6-19.
https://journals.sagepub.com/doi/full/10.1177/2396987316628384
http://www.ncbi.nlm.nih.gov/pubmed/31008263?tool=bestpractice.com
Se recomienda la movilización temprana para los pacientes con accidente cerebrovascular, pero no se debe realizar una movilización muy temprana e intensa (p. ej.o, múltiples sesiones fuera de la cama) dentro de las 24 horas del inicio del accidente cerebrovascular.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
[132]National Institute for Health and Care Excellence. Stroke and transient ischaemic attack in over 16s: diagnosis and initial management. April 2022 [internet publication].
https://www.nice.org.uk/guidance/ng128
[230]AVERT Trial Collaboration group. Efficacy and safety of very early mobilisation within 24 h of stroke onset (AVERT): a randomised controlled trial. Lancet. 2015 Jul 4;386(9988):46-55.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(15)60690-0/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/25892679?tool=bestpractice.com
La movilización temprana puede disminuir el riesgo de TEV al reducir la estasis venosa, pero esto no se ha demostrado en los ensayos controlados.[228]Dennis M, Caso V, Kappelle LJ, et al; European Stroke Organisation. European Stroke Organisation (ESO) guidelines for prophylaxis for venous thromboembolism in immobile patients with acute ischaemic stroke. Eur Stroke J. 2016 Mar;1(1):6-19.
https://journals.sagepub.com/doi/full/10.1177/2396987316628384
http://www.ncbi.nlm.nih.gov/pubmed/31008263?tool=bestpractice.com
Véase Profilaxis del tromboembolismo venoso.
Rehabilitación
Después de un accidente cerebrovascular se recomienda la rehabilitación temprana.[231]Winstein CJ, Stein J, Arena R, et al. Guidelines for adult stroke rehabilitation and recovery: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2016 Jun;47(6):e98-169.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000098
http://www.ncbi.nlm.nih.gov/pubmed/27145936?tool=bestpractice.com
Sin embargo, no se debe realizar una movilización muy temprana y de alta intensidad dentro de las 24 horas posteriores al inicio del ictus, ya que puede reducir las probabilidades de un resultado favorable a los 3 meses.[119]Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-418.
https://www.ahajournals.org/doi/full/10.1161/STR.0000000000000211
http://www.ncbi.nlm.nih.gov/pubmed/31662037?tool=bestpractice.com
Debido a las lesiones neurológicas, muchos pacientes con accidente cerebrovascular presentan una limitación de sus capacidades de deambulación y movilidad, lo que reduce su calidad de vida.
El objetivo de la rehabilitación es permitir que la persona pueda reiniciar una vida social y/o laboral aceptable.
La logopedia es crucial para aumentar el grado de comunicación funcional.[224]National Institute for Health and Care Excellence. Stroke rehabilitation in adults. Jun 2013 [internet publication].
https://www.nice.org.uk/guidance/cg162
Alrededor de un tercio de los pacientes que sufren un ictus desarrollan afasia.[232]Pedersen PM, Vinter K, Olsen TS. Aphasia after stroke: type, severity and prognosis. The Copenhagen aphasia study. Cerebrovasc Dis. 2004;17(1):35-43.
https://www.doi.org/10.1159/000073896
http://www.ncbi.nlm.nih.gov/pubmed/14530636?tool=bestpractice.com
Se están investigando las diferencias en el resultado funcional cuando se comparan regímenes de tratamiento específicos (es decir, la intensidad, la dosis y la duración). Se sabe que las personas que se someten a tratamientos muy intensivos tienen una mayor incidencia de abandono temprano de la terapia.[233]Brady MC, Kelly H, Godwin J, et al. Speech and language therapy for aphasia following stroke. Cochrane Database Syst Rev. 2016 Jun 1;(6):CD000425.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000425.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/27245310?tool=bestpractice.com
La práctica mental describe un método de entrenamiento que utiliza el ensayo cognitivo de actividades para mejorar el desempeño de esas actividades: un individuo ensaya mentalmente de forma repetida una acción o tarea en su imaginación (p. ej., coger una taza o extender el brazo) sin realizar físicamente la acción o tarea. Los ensayos controlados aleatorizados respaldan el uso de la práctica mental, además del tratamiento convencional de rehabilitación física, para mejorar el deterioro de las extremidades superiores después del ictus.[234]Barclay RE, Stevenson TJ, Poluha W, et al. Mental practice for treating upper extremity deficits in individuals with hemiparesis after stroke. Cochrane Database Syst Rev. 2020 May 25;5:CD005950.
https://www.doi.org/10.1002/14651858.CD005950.pub5
http://www.ncbi.nlm.nih.gov/pubmed/32449959?tool=bestpractice.com
La realidad virtual y los videojuegos interactivos han surgido como enfoques de tratamiento novedosos en la rehabilitación de accidentes cerebrovasculares. En un metanálisis se determinó que la realidad virtual puede mejorar la función de las extremidades superiores y las actividades de la vida diaria cuando se utiliza como complemento de la atención habitual (para aumentar el tiempo total de la terapia); sin embargo, la realidad virtual y los videojuegos interactivos no presentan más beneficios que la terapia convencional. No había evidencias suficientes para llegar a conclusiones sobre el efecto de la realidad virtual y los videojuegos interactivos en la velocidad de marcha, el equilibrio, la participación o la calidad de vida.[235]Laver KE, Lange B, George S, et al. Virtual reality for stroke rehabilitation. Cochrane Database Syst Rev. 2017 Nov 20;(11):CD008349.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD008349.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/29156493?tool=bestpractice.com
El robot de asistencia para el ejercicio de la marcha (GEAR) puede producir mejoras clínicamente significativas en el equilibrio y en la función de las extremidades inferiores en pacientes con accidente cerebrovascular infratentorial.[236]Tomida K, Sonoda S, Hirano S, et al. Randomized controlled trial of gait training using Gait Exercise Assist Robot (GEAR) in stroke patients with hemiplegia. J Stroke Cerebrovasc Dis. 2019 Sep;28(9):2421-8.
http://www.ncbi.nlm.nih.gov/pubmed/31307899?tool=bestpractice.com

 ]
]
 ]
Las unidades de accidentes cerebrovasculares tienen equipos multidisciplinarios que incluyen médicos, personal de enfermería y especialistas en rehabilitación con conocimientos especializados en accidentes cerebrovasculares.[224] Los cuidados de soporte mejorados, la prevención de complicaciones como la infección y la iniciación más temprana del tratamiento de rehabilitación se encuentran entre los mecanismos por los que se cree que las unidades de accidentes cerebrovasculares producen mejores resultados.
]
Las unidades de accidentes cerebrovasculares tienen equipos multidisciplinarios que incluyen médicos, personal de enfermería y especialistas en rehabilitación con conocimientos especializados en accidentes cerebrovasculares.[224] Los cuidados de soporte mejorados, la prevención de complicaciones como la infección y la iniciación más temprana del tratamiento de rehabilitación se encuentran entre los mecanismos por los que se cree que las unidades de accidentes cerebrovasculares producen mejores resultados. ]
[
]
[  ]
]
 ]
]