Abordagem
Os fatores de risco importantes para a infecção incluem a exposição a picadas de flebotomíneos, pouco conhecimento sobre a doença, desnutrição, imunossupressão e, em alguns casos, a proximidade com pacientes infectados. Levantar a história e fazer o exame clínico são medidas cruciais para se determinar o grau de suspeita clínica de leishmaniose cutânea (LC) e leishmaniose visceral (LV). A confirmação laboratorial é obrigatória, uma vez que outras doenças podem apresentar um quadro clínico semelhante.
História
Tanto na LV quanto na LC, o paciente pode apresentar história de:
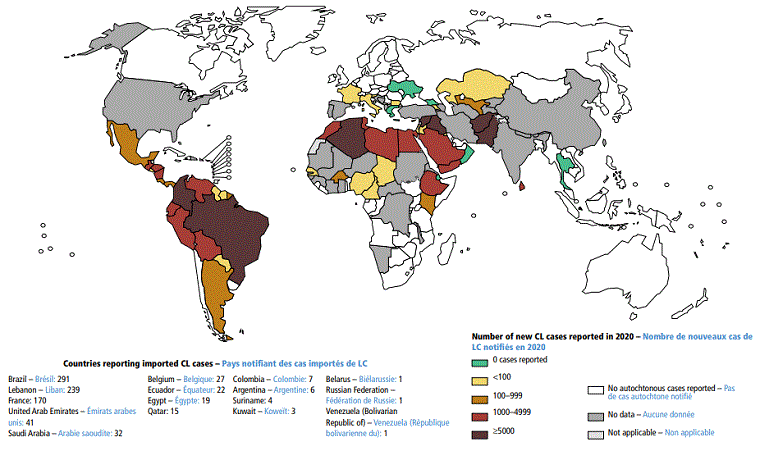
Permanência prévia em área endêmica[Figure caption and citation for the preceding image starts]: Status mundial da endemicidade da leishmaniose cutânea (LC), 2020Vigilância global da leishmaniose: 2019–2020, uma linha basal para o roteiro de 2030: Organização Mundial da Saúde; 2021. Licença: CC BY-NC-SA 3.0 IGO (https://creativecommons.org/licenses/by-nc-sa/3.0/igo/) [Citation ends].
 [Figure caption and citation for the preceding image starts]: Status mundial da endemicidade da leishmaniose visceral (LV), 2020Vigilância global da leishmaniose: 2019–2020, uma linha basal para o roteiro de 2030: Organização Mundial da Saúde; 2021. Licença: CC BY-NC-SA 3.0 IGO (https://creativecommons.org/licenses/by-nc-sa/3.0/igo/) [Citation ends].
[Figure caption and citation for the preceding image starts]: Status mundial da endemicidade da leishmaniose visceral (LV), 2020Vigilância global da leishmaniose: 2019–2020, uma linha basal para o roteiro de 2030: Organização Mundial da Saúde; 2021. Licença: CC BY-NC-SA 3.0 IGO (https://creativecommons.org/licenses/by-nc-sa/3.0/igo/) [Citation ends].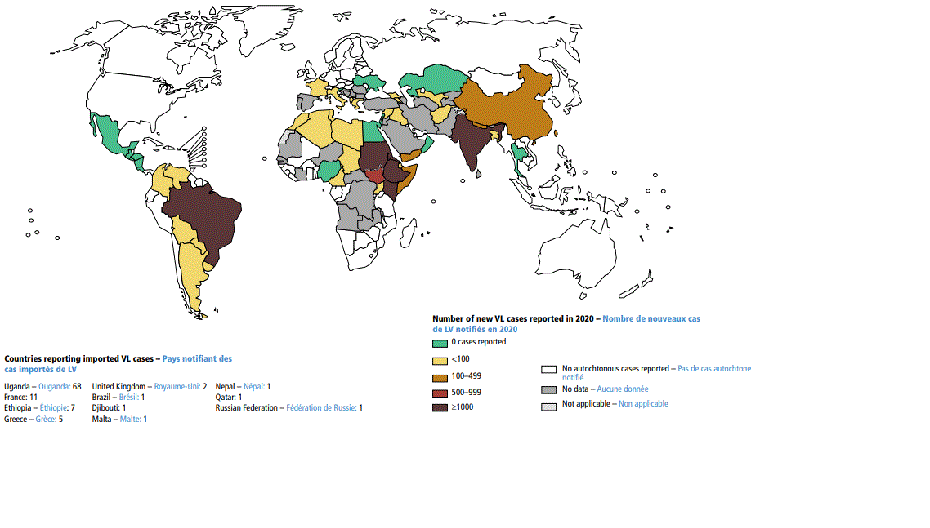
Imunossupressão do tipo mediada por células, incluindo o sistema imunológico menos maduro
Tratamento prévio antileishmaniose (levanta a suspeita de recidiva).
Os sintomas manifestos na LV incluem:
Febre prolongada
Fadiga
Anorexia
Perda de peso
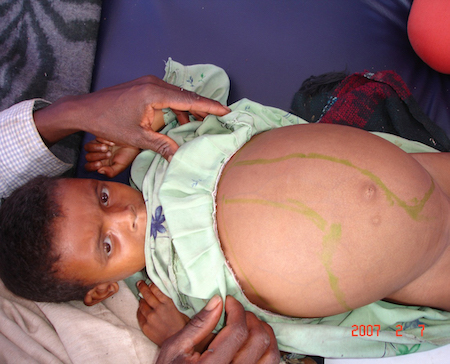
Distensão abdominal.[Figure caption and citation for the preceding image starts]: Hepatoesplenomegalia em um paciente etíope com leishmaniose visceralImagem cortesia da Organização Mundial da Saúde [Citation ends].
Os sintomas menos comuns na LV incluem:
Tosse
Diarreia
Arrepios
Sangramentos, incluindo epistaxe.
Exame físico clínico
Os sinais apresentados na LC incluem:
Lesões cutâneas ulcerativas, nodulares, semelhantes a placas ou verrucosas no local da picada (LC localizada). As lesões geralmente afetam a pele facilmente exposta, incluindo o rosto, os braços e os membros inferiores. Uma única lesão ulcerativa envolvendo a pina é conhecida como úlcera "chiclero" no sudeste do México e na América Latina, quando causada por Leishmania mexicana.[10]
Lesões em locais distantes da picada do flebotomíneo, como áreas de trauma menor.
Múltiplos nódulos cutâneos não ulcerativos (leishmaniose cutânea difusa).
Várias lesões ulcerativas e papulonodulares na pele (leishmaniose disseminada).
Lesões nódulo-ulcerativas ao redor de uma cicatriz de leishmaniose curada (leishmaniose recidivante).
Pequenos nódulos subcutâneos (linfangite nodular), geralmente em padrão esporotricoide, bem como linfadenopatia regional em alguns casos.
A inflamação da mucosa granulomatosa, ulcerativa e/ou destrutiva ocorre mais comumente no nariz, mas também pode envolver a orofaringe ou laringe (leishmaniose mucosa [LM]).[Figure caption and citation for the preceding image starts]: Lesão ulcerativa por Leishmania braziliensis de um estudante que viajou ao PeruDo acervo do Dr. N. Aronson; usado com permissão [Citation ends].
 [Figure caption and citation for the preceding image starts]: Injeção intralesional para o tratamento da leishmaniose cutâneaImagem cortesia da Organização Mundial da Saúde [Citation ends].
[Figure caption and citation for the preceding image starts]: Injeção intralesional para o tratamento da leishmaniose cutâneaImagem cortesia da Organização Mundial da Saúde [Citation ends].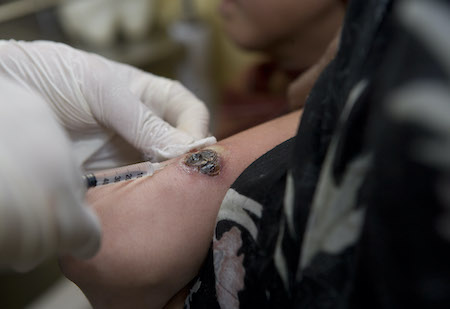
Na leishmaniose visceral [LV], pode ser detectado o seguinte:
Enfraquecimento
Linfadenopatia (comum no Sudão, incomum em outros locais)
Esplenomegalia
Hepatomegalia
Hiperpigmentação (no sul da Ásia).
Na maioria dos casos, o quadro clínico da leishmaniose visceral (LV) em pacientes imunossuprimidos é semelhante ao de pacientes imunocompetentes. No entanto, uma minoria de pacientes imunossuprimidos apresenta características atípicas (por exemplo, sinais de comprometimento do trato digestivo ou respiratório, ausência de esplenomegalia).
Investigações
Recomenda-se um hemograma completo na leishmaniose visceral (LV) para identificar e monitorar a anemia, a leucopenia e a trombocitopenia. Alguns medicamentos usados no tratamento da leishmaniose (por exemplo, paromomicina, medicamentos de antimônio pentavalente, anfotericina B e miltefosina) podem causar disfunção hepática ou renal, levando à necessidade de análise dos testes da função hepática e da ureia basais. Um teste de gravidez baseado na quantificação da gonadotrofina coriônica humana (hCG) é essencial antes de escolherem as opções de tratamento, uma vez que vários medicamentos são tóxicos para o feto. É prudente realizar um ECG antes de se usarem medicamentos de antimônio pentavalente ou pentamidina para avaliar o intervalo QT basal.
O diagnóstico é confirmado pelo exame microscópico de amostras relevantes (histopatologia), isolamento do parasita por cultura de sangue ou tecido e detecção molecular do DNA do parasita por reação em cadeia da polimerase; os exames complementares incluem a testagem sorológica na LV.[76][77][78] A escolha do exame depende do tipo da leishmaniose e da disponibilidade do exame. Múltiplos testes são recomendados, se possível, para maximizar a probabilidade de um resultado positivo.[8]
Avaliação laboratorial na leishmaniose cutânea
A lesão na pele deve ser limpa ou desbridada, se necessário, antes de se coletar a amostra. Se possível, devem ser realizados vários tipos de testes para maximizar o rendimento diagnóstico.[79]
Se houver disponibilidade, o diagnóstico parasitológico molecular (ou seja, ensaios com base na reação em cadeia da polimerase) deve ser realizado em caso de suspeita de leishmaniose cutânea (LC). Tal abordagem é particularmente útil nas amostras com baixa carga parasitária (por exemplo, de pacientes com LM).[78] O diagnóstico parasitológico molecular é realizado usando-se amostras de tecido obtidas de raspagens cutâneas (coletando tecido do tamanho de um grão de arroz), swabs de úlceras, aspirados ou esfregaços da pele. A biópsia por punção cutânea ou por raspagem pode ter um rendimento menor, pois é encontrada uma carga parasitária maior na epiderme e na derme superior.[80] Métodos moleculares também são usados para determinar as espécies de Leishmania.
Se o diagnóstico parasitológico molecular não estiver disponível, use um exame microscópico de aspirados de biópsia, esfregaços, raspagens ou esfregaços da pele, coloração de Giemsa ou hematoxilina-eosina.[77] O exame microscópico é, provavelmente, a abordagem diagnóstica mais comum nos países onde a leishmaniose cutânea (LC) é endêmica. Um cinetoplasto em forma de bacilo deve ser visualizado.[1] O parasita pode ser mais bem visto usando-se a microscopia por imersão em óleo, com um aumento de 100 vezes.
O isolamento do parasita por cultura de amostras de tecido ou biópsia pode ser útil e é aproximadamente 95% específico; no entanto, essa abordagem não é muito sensível (geralmente <50%), exige muito trabalho e requer laboratórios especializados. A determinação das espécies pode ser feita bioquimicamente (por eletroforese de isoenzimas), por espectroscopia de massas (MALDI) ou usando teste de amplificação de ácido nucleico. O conhecimento das espécies de Leishmania responsáveis pela infecção ajuda a direcionar a terapia, especialmente quando várias espécies circulam em uma determinada área, e ajuda a determinar se o tratamento sistêmico pode ser necessário (por exemplo, infecção adquirida na região amazônica, onde o risco de LM é maior).[8]
A sorologia não é usada no diagnóstico da leishmaniose cutânea (LC) devido à sua baixa sensibilidade e sua incapacidade de distinguir entre infecções pregressas e presentes.
Avaliação laboratorial de leishmaniose visceral em pacientes imunocompetentes
A leishmaniose visceral (LV) pode ser sugerida por um dos testes sorológicos altamente sensíveis e específicos (ensaio de imunoadsorção enzimática [ELISA], teste de anticorpo fluorescente indireto, Western blot, teste de aglutinação direta, tira reagente rK39 baseada em antígeno). A escolha do exame depende, principalmente, da disponibilidade e da competência laboratoriais.[2] No entanto, a sensibilidade e a especificidade desses ensaios imunológicos podem variar de acordo com a localização geográfica, a resposta imune do hospedeiro e o tipo de teste. Além disso, um resultado positivo pode persistir por anos após o tratamento.
Em pacientes com quadro clínico típico e sorologia positiva para LV, é aconselhável fazer a confirmação parasitológica, pois os achados e a quantificação dos parasitas confirmam o diagnóstico e podem ajudar na avaliação da resposta ao tratamento. Nos pacientes com sorologia positiva, mas com doença clinicamente atípica, o diagnóstico parasitológico é necessário. Amostras parasitológicas podem ser obtidas por aspiração do tecido esplênico, apesar do risco de hemorragia fatal; da medula óssea, que é o método de preferência; do fígado; ou dos linfonodos. A sensibilidade do exame microscópico de medula óssea ou de tecido linfonodal pode ser <50%; portanto, um resultado negativo não descarta a infecção por leishmaniose. Uma amostra de aspirado deve ser enviada para cultura e/ou reação em cadeia da polimerase, que são exames mais sensíveis que a microscopia por esfregaço.[78]
Nos pacientes com sorologia negativa, um diagnóstico alternativo deve ser pesquisado.[2] No entanto, se a suspeita clínica de leishmaniose visceral (LV) permanecer alta, recomendam-se exames parasitológicos.
Avaliação laboratorial da leishmaniose visceral em pacientes imunossuprimidos
Em pacientes imunossuprimidos, o diagnóstico parasitológico é a abordagem de primeira linha, pois a sorologia é menos sensível nessa coorte. Além disso, o diagnóstico parasitológico normalmente é mais sensível porque os pacientes imunossuprimidos têm uma carga parasitária maior no sangue e nos tecidos. A análise do esfregaço de sangue periférico ou da camada leucoplaquetária por microscopia direta, cultura ou reação em cadeia da polimerase (o método mais sensível) são os testes não invasivos de primeira linha. Se os resultados forem negativos, os mesmos procedimentos devem ser aplicados em um aspirado de medula óssea. Dependendo do quadro clínico, as lesões em outros locais do corpo (por exemplo, trato digestivo, pele) podem ser submetidas a amostragem.
O diagnóstico sorológico é uma medida adjuvante devido à sensibilidade variável e tipicamente menor desse método de teste nos pacientes imunossuprimidos. Além disso, um atraso no diagnóstico e no tratamento subsequente tem potencial para causar ainda mais danos a esse grupo de pacientes vulneráveis.[19][81]
Diagnóstico de recidiva de leishmaniose visceral
Na recidiva da LV, os pacientes geralmente apresentam o mesmo quadro clínico que no episódio inicial. A recidiva deve ser confirmada parasitologicamente. O diagnóstico parasitológico por exame direto ou cultura de tecido é o teste de escolha. O valor diagnóstico da reação em cadeia da polimerase é incerto, já que ela pode permanecer positiva em pacientes clinicamente curados; no entanto, a reação em cadeia da polimerase quantitativa pode mostrar níveis elevados do DNA na recidiva.[8][82] O diagnóstico da recidiva não pode ser baseado em testes sorológicos, uma vez que os anticorpos contra Leishmania donovani ou Leishmania infantum (sinônimo: L chagasi) geralmente permanecem detectáveis por anos após o diagnóstico inicial.[83][84]
Leishmaniose dérmica pós-calazar
Para dar início ao tratamento da Leishmaniose dérmica pós-calazar é suficiente ter a história (tratamento atual ou passado da LV) e o exame clínico (presença de lesão macular, maculopapular ou nodular em locais típicos). O diagnóstico pode ser confirmado por exame direto, cultura ou reação em cadeia da polimerase de biópsias das lesões cutâneas. A sensibilidade do diagnóstico parasitológico é aumentada se as amostras forem retiradas de lesões grandes ou nodulares.[6] O diagnóstico sorológico não é útil, uma vez que os anticorpos contra a L donovani geralmente permanecem detectáveis por anos após o tratamento da LV.[83][84]
O uso deste conteúdo está sujeito ao nosso aviso legal