Abordagem
O diagnóstico de pré-eclâmpsia deve ser realizado quando existe novo episódio de hipertensão persistente, geralmente com proteinúria depois de 20 semanas de gestação.[1][2][16][53] A ausência de hipertensão descarta o diagnóstico, apesar de haver condições relacionadas, como a síndrome HELLP, que podem se apresentar com ou sem hipertensão. A síndrome HELLP é um subtipo de pré-eclâmpsia grave caracterizada por hemólise (H), enzimas hepáticas elevadas (EHE) e plaquetopenia (LP).[2][16] Porém, a presença de proteinúria não é mais obrigatória no diagnóstico da pré-eclâmpsia.[2] Um diagnóstico de pré-eclâmpsia pode ser feito na ausência de proteinúria se a hipertensão se apresentar com envolvimento sistêmico materno, geralmente complicações hepáticas ou hematológicas, ou com restrição do crescimento fetal.[1][2] Após o diagnóstico, a avaliação fetal deve ser realizada com outros exames maternos para avaliar o envolvimento sistêmico.
Se houver sinais e sintomas de pré-eclâmpsia grave ou complicações, o tratamento imediato é necessário. Com a confirmação do diagnóstico, ou se houver preocupação em relação à saúde da mãe ou do feto, a mulher deve ser internada em uma unidade de cuidados obstétricos para manejo.[1][16]
História
A pré-eclâmpsia geralmente ocorre em gestantes após as 20 semanas de gestação.[1][16][54] Os principais fatores de risco incluem nuliparidade, história materna prévia ou história familiar, índice de massa corporal >30, idade materna >40 anos, gravidez múltipla (gemelar), subfertilidade, hipertensão gestacional (hipertensão que se desenvolve após 20 semanas de gestação na ausência de proteinúria e sintomas sistêmicos), diabetes preexistente, síndrome do ovário policístico, doença autoimune, doença renal, doença cardiovascular preexistente e hipertensão crônica.
As mulheres podem ser assintomáticas e diagnosticadas em uma consulta clínica de rotina ou podem apresentar de forma aguda os sintomas a seguir.
Cefaleia: geralmente frontal; a presença desse sintoma classifica a pré-eclâmpsia como grave.[1] Ocorre em aproximadamente 40% das mulheres com doença grave e é um dos poucos sintomas que predizem um aumento do risco de eclâmpsia.[8]
Dor na parte superior do abdome: geralmente dor no quadrante superior direito; ocorre em cerca de 16% das mulheres com doença grave e é um sintoma clínico da síndrome HELLP.[8]
Distúrbios visuais: fotopsia (percepção de luzes piscantes nos campos visuais), escotoma e vasoespasmo retiniano são relativamente raros, mas indicam um aumento do risco de eclâmpsia. A cegueira cortical deve alertar o médico para edema cerebral subjacente.
Dispneia: em decorrência do edema pulmonar, podendo complicar a pré-eclâmpsia. Se ocorrer depois do parto, é uma das principais causas de mortalidade materna.
Convulsões: exigem internação na unidade de terapia intensiva, estabilização e parto.[1]
Oligúria: pode estar associada a um edema crescente. As mulheres correm maior risco pós-parto, quando há maior probabilidade de edema pulmonar.
A presença desses sintomas, além de hipertensão com ou sem proteinúria, classifica a pré-eclâmpsia como grave.[1] Se as movimentações fetais estiverem reduzidas, uma avaliação imediata do bem-estar fetal será necessária.
[  ]
]
Exame físico
Hipertensão (definida como pressão arterial sistólica [PA] ≥140 mmHg e/ou PA diastólica ≥90 mmHg) em uma mulher previamente normotensa é diagnóstica.[1][16][54] É necessário fazer pelo menos duas medições, com um intervalo mínimo de 4 horas.[1]
Edema é muito comum, mas não discriminatório, de modo que não deve ser usado no diagnóstico. Hiper-reflexia e/ou clônus são raros e têm pouco valor na avaliação clínica. A fundoscopia raramente é anormal, mas, se for, a hipertensão crônica subjacente está implícita.
Se a altura do fundo do útero for pequena, isso indicará que o volume do líquido amniótico está reduzido, o que pode significar restrição de crescimento, e a avaliação fetal por ultrassonografia será necessária.
[  ]
A restrição do crescimento fetal ocorre em aproximadamente 30% das mulheres com pré-eclâmpsia.[8]
]
A restrição do crescimento fetal ocorre em aproximadamente 30% das mulheres com pré-eclâmpsia.[8]
Urinálise
O teste da tira reagente pode ser usado para fazer a triagem da presença de proteína na urina. O teste da tira reagente com leitores automáticos é mais preciso que a análise visual.
Proteinúria associada à pressão arterial elevada na faixa de pré-eclâmpsia requer o encaminhamento para uma unidade especializada ou internação hospitalar para avaliação. Na ausência de proteinúria ou sinais sistêmicos de pré-eclâmpsia, um diagnóstico alternativo deve ser procurado.
A proteína urinária pode ser estimada em uma coleta de urina de 24 horas, com um nível diagnóstico considerado como excreção urinária de ≥300 mg de proteína/24 horas.[1][2][34]
No entanto, completar uma coleta de urina de 24 horas é difícil para as mulheres, e o National Institute for Health and Care Excellence (NICE) do Reino Unido recomenda não usar rotineiramente a coleta de urina de 24 horas para quantificar a proteinúria em gestantes.[16] Se disponível, há preferência por um teste pontual alternativo, como a relação proteína/creatinina (RPC, para a qual um resultado ≥30 mg/mmol é diagnóstico).[1][16][34][54]l Se a medição da proteinúria estiver acima do limiar diagnóstico, mas ainda houver incerteza diagnóstica, considere testar novamente em uma nova amostra, além de uma revisão clínica.
Como o nível de proteinúria não está correlacionado ao desfecho, não há benefícios ao repetir rotineiramente a urinálise após o diagnóstico.[16]
Avaliação fetal
A avaliação imediata por ultrassonografia fetal é necessária caso a movimentação fetal seja reduzida ou haja suspeita de restrição do crescimento fetal.
[  ]
A biometria fetal deve ser usada para diagnosticar ou descartar a restrição do crescimento fetal, embora o crescimento só possa ser totalmente avaliado por exames realizados com 2 semanas de intervalo.
]
A biometria fetal deve ser usada para diagnosticar ou descartar a restrição do crescimento fetal, embora o crescimento só possa ser totalmente avaliado por exames realizados com 2 semanas de intervalo.
Outros métodos de avaliação fetal devem ser utilizados em todos os pacientes inicialmente com os seguintes exames:[1][16][54]
A velocimetria da artéria umbilical por Doppler é a principal ferramenta de avaliação. Ela reduz a mortalidade perinatal e permite tomar decisões melhores e mais apropriadas sobre o parto. Deve ser realizada no início da internação e, se estiver normal, repetida duas vezes por semana. Se estiver anormal, o monitoramento mais intenso talvez seja necessário usando outros meios, incluindo avaliação por Doppler de outros vasos fetais e cardiotocografia fetal. [
 ]
O parto pode ser necessário dentro de alguns dias.[Figure caption and citation for the preceding image starts]: Velocimetria da artéria umbilical por Doppler: (1) padrão normal; (2) fluxo diastólico final reduzido; (3) fluxo diastólico final ausente; (4) fluxo diastólico final inversoDo acervo pessoal do Dr. James J. Walker; usado com permissão [Citation ends].
]
O parto pode ser necessário dentro de alguns dias.[Figure caption and citation for the preceding image starts]: Velocimetria da artéria umbilical por Doppler: (1) padrão normal; (2) fluxo diastólico final reduzido; (3) fluxo diastólico final ausente; (4) fluxo diastólico final inversoDo acervo pessoal do Dr. James J. Walker; usado com permissão [Citation ends].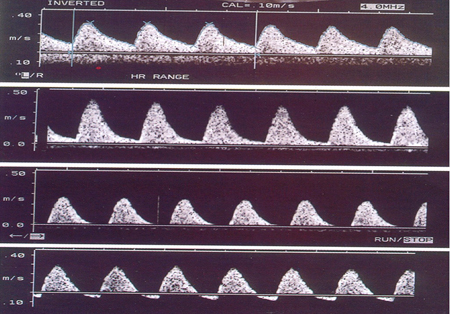
A cardiotocografia fetal é recomendada para avaliar o bem-estar do feto, mas tem pouco valor prognóstico. Deve ser realizada inicialmente e, no máximo, duas vezes por semana, a não ser que haja alguma preocupação como sangramento vaginal, movimentações fetais reduzidas ou aumento da gravidade da doença. [
 ]
]
Avaliação do líquido amniótico, com a técnica de medição de bolsa vertical única mais profunda sendo preferível em vez do índice de líquido amniótico. Pode ser facilmente combinada com a velocimetria da artéria umbilical por Doppler.
Outras investigações maternas
Hemograma completo, creatinina sérica e testes da função hepática (TFHs) são indicadores úteis da progressão da doença e, portanto, são recomendados em todas as mulheres após a urinálise inicial e a avaliação fetal.
A creatinina sérica elevada indica doença renal subjacente. Embora o ácido úrico sérico elevado esteja associado a pré-eclâmpsia grave, ele não oferece valor diagnóstico adicional. A redução do número de plaquetas e aumento dos níveis de transaminase são parcialmente diagnósticos da síndrome HELLP. A contagem plaquetária é o principal critério usado na classificação da gravidade da síndrome HELLP. Se a contagem plaquetária for <100,000/microlitros, deverão ser realizados um coagulograma completo e TFHs. Se a contagem plaquetária for ≥100,000/microlitros, geralmente não são recomendados outros testes de coagulação.
O teste do fator de crescimento placentário (PlGF) ajuda a avaliar o risco de pré-eclâmpsia e a planejar um parto precoce e seguro, se indicado. O teste também ajuda a identificar as mulheres que não correm risco de pré-eclâmpsia, reduzindo assim acompanhamentos e atendimentos hospitalares desnecessários. Os testes permitem, portanto, que as equipes clínicas direcionem recursos para manter estas mulheres sob acompanhamento adequado. O NICE defende o uso do teste do PlGF em uma ocasião para auxiliar na decisão sobre os cuidados (para ajudar a descartar ou confirmar pré-eclâmpsia) se houver suspeita de pré-eclâmpsia em mulheres que se apresentam entre 20 semanas e 34 semanas e 6 dias de gestação.[16][55][56] Um resultado baixo no teste de PlGF (<100 pg/mL) nem sempre significa que uma mulher tem pré-eclâmpsia, porque o resultado pode estar associado a outras condições que afetam a placenta. No entanto, os resultados dos testes baseados em PlGF são úteis para a tomada de decisões juntamente com o julgamento clínico, particularmente para as mulheres que tiveram hipertensão ou proteinúria antes de engravidar e aquelas com maior risco de desfechos adversos graves na gravidez (por exemplo, mulheres de famílias africanas, caribenhas ou asiáticas). Um ensaio clínico randomizado e controlado de clusters (o estudo PARROT) constatou menos tempo até o diagnóstico e menor incidência de desfechos adversos maternos graves em maternidades nas quais os resultados do PIGF estavam disponíveis, em comparação com unidades em que os resultados do PIGF estavam ocultos (controle).[57] O tempo mediano até o diagnóstico da pré-eclâmpsia foi de 4.1 dias para as mulheres com testes ocultos e de 1.9 dia para as mulheres com testes revelados (relação de tempo de 0.36, intervalo de confiança [IC] de 95%: 0.15 a 0.87; p = 0.027). Desfechos adversos maternos graves foram relatados em 24 (5%) das 447 mulheres do grupo de teste oculto em comparação com 22 (4%) das 573 mulheres do grupo de teste revelado (razão de chances ajustada 0.32, IC de 95% 0.11 a 0.96; P = 0.043). Os desfechos perinatais não foram afetados.[57] O NICE também recomenda a razão entre fator solúvel similar à tirosina-quinase-I (sFlt-1) no soro materno e o PlGF como uma alternativa ao teste do PlGF somente, embora a necessidade da anamnese e do exame físico tradicional permaneça fundamental.[55] O ensaio clínico randomizado, prospectivo, intervencionista e de grupos paralelos INSPIRE revelou que o uso da razão sFlt-1/PlGF em mulheres com suspeita de pré-eclâmpsia melhorou significativamente a acurácia clínica sem afetar a taxa de internações hospitalares.[58] O número de internações não foi significativamente diferente entre os grupos. No entanto, o braço com resultados revelados (resultado sFlt-1/PlGF conhecido pelos médicos) internou 100% das mulheres que desenvolveram pré-eclâmpsia até 7 dias após o teste, enquanto o braço não revelado (com resultados desconhecidos) internou 83% das mulheres (P =0.038). O uso da razão sFlt-1/PlGF produziu uma sensibilidade de 100% (IC de 95%: 85.8 a 100) e um valor preditivo negativo de 100% (IC de 95%: 97.1 a 100) em comparação com uma sensibilidade de 83.3% (IC de 95%: 58.6 a 96.4) e um valor preditivo negativo de 97.8% (IC de 95%: 93.7 a 99.5) com a prática clínica isoladamente. Uma análise estratificada dos dados do PARROT também demonstrou que uma proporção maior de mulheres com um resultado do teste do PlGF muito baixo (<12 pg/mL) recebeu corticosteroides pré-natais: 38.6% no grupo dos testes revelados em comparação com 15.8% no grupo dos testes ocultos.[59] Isto pode ser clinicamente útil na redução das taxas de síndrome do desconforto respiratório e de hemorragia intraventricular em bebês prematuros. No entanto, não está claro se o uso dessas investigações traz algum benefício para os desfechos perinatais. Embora houvesse a preocupação de que os testes do PlGF levassem a um aumento e a um número desnecessário de partos prematuros, a proporção de nascimentos antes de 37 semanas de gestação nos braços de teste e de controle foi a mesma nos ensaios PARROT e INSPIRE. O NICE não recomenda a utilização de testes baseados no PlGF para a tomada de decisões sobre a possibilidade de oferecer um parto antecipado planejado a mulheres com pré-eclâmpsia pré-termo, o que deve se basear na avaliação clínica.[16][55]
Embora a Food and Drug Administration (FDA) dos EUA tenha aprovado o teste de sFlt-1/PlGF para auxiliar na avaliação do risco de progressão para pré-eclâmpsia com características graves, o American College of Obstetricians and Gynecologists não recomenda nenhum teste de biomarcador único (por exemplo, teste de PlGF ou relação de sFlt-1/PlGF) para a predição da pré-eclâmpsia, diagnóstico ou exclusão da pré-eclâmpsia com características graves ou determinação da abordagem de tratamento após um resultado de teste positivo ou negativo.[1][60]
Como colher uma amostra de sangue venoso da fossa antecubital usando uma agulha a vácuo.
O uso deste conteúdo está sujeito ao nosso aviso legal