Abordaje
Orientación de confianza
ebpracticenet le insta a dar prioridad a las siguientes guías de práctica clínica locales:
Évaluation du risque cardiovasculaire en première lignePublicado por: Domus MedicaPublicado por última vez: 2010Cardiovasculaire risicobepaling in de eerste lijnPublicado por: Domus MedicaPublicado por última vez: 2020Existen diversas opciones de tratamiento para la hipercolesterolemia, que se pueden establecer de manera individual o combinada. Estas opciones incluyen cambios en el estilo de vida relacionados con la dieta y el ejercicio, medicamentos y suplementos dietéticos. Rara vez se pueden aplicar tratamientos experimentales o intervenciones procedimentales.
Las guías de práctica clínica internacionales han reforzado el papel del tratamiento farmacológico para reducir el colesterol en función del riesgo de eventos cardiovasculares.[44][51][53][54] A pesar de la existencia de algunas diferencias en las herramientas de estratificación del riesgo y los objetivos de colesterol sugeridos, las guías de práctica clínica son unánimes a la hora de recomendar un tratamiento farmacológico intensivo y, por consiguiente, en cuanto a la fuerte disminución del colesterol con estatinas en pacientes de alto riesgo, principalmente en aquellos con enfermedad cardiovascular ateroesclerótica (cardiopatía coronaria o formas no coronarias de la enfermedad ateroesclerótica, como enfermedad arterial periférica, aneurisma aórtico abdominal, enfermedad de las arterias carótidas [p. ej., accidentes isquémicos transitorios, accidente cerebrovascular de origen carotídeo u obstrucción >50% de una arteria carótida]). Sin embargo, en los pacientes de menor riesgo pueden instaurarse regímenes menos intensivos.
Las recomendaciones de tratamiento en este tema se basan en las guías de práctica clínica de la American Heart Association/American College of Cardiology; puede que las guías de práctica clínica locales sean diferentes.[44]
El manejo de los pacientes diagnosticados con hipercolesterolemia familiar requiere una consulta con un especialista.
Estratificación del riesgo
El beneficio neto que cada paciente recibe de las terapias preventivas está directamente asociado al riesgo cardiovascular inicial (es decir, los que tienen el riesgo más alto obtendrán las mayores reducciones en el riesgo absoluto de las intervenciones preventivas). Por lo tanto, es fundamental realizar una estratificación adecuada del riesgo que sirva de base para el debate y un marco para decidir sobre la intensidad de las estrategias de prevención. Los individuos con enfermedad cardiovascular secundaria a aterosclerosis (ECVSA) clínica presentan un alto riesgo de eventos recurrentes. Dentro de este estrato, aquellos con eventos mayores recurrentes de ECVSA (enfermedad arterial periférica sintomática, apoplejía isquémica, infarto de miocardio o síndrome coronario agudo reciente) presentan mayor riesgo de eventos repetidos.
En pacientes adultos sin ECVSA previa, se pueden utilizar puntuaciones de riesgo para la estimación del riesgo. Hay varios disponibles, como Framingham, QRISK, PROCAM, las ecuaciones a partir de estudios de cohortes agrupados, y SCORE2 y SCORE2-OP. [ Evaluación del riesgo cardiovascular en los hombres (10 años, información para el paciente, Framingham 2008) Opens in new window ] [ Evaluación del riesgo cardiovascular en mujeres (10 años, información para pacientes, Framingham 2008) Opens in new window ] [ Evaluación del riesgo cardiovascular (a 10 años, Puntaje PROCAM, Munster Heart Study) Opens in new window ] [ SCORE2 y SCORE2-OP Opens in new window ] QRISK risk calculator Opens in new window Pooled Cohort Equations CV Risk Calculator Opens in new window Otra herramienta, desarrollada por la American Heart Association, la calculadora de la Herramienta de Evaluación de Riesgos de Prevención Primaria (PREVENT), ayuda a los profesionales de salud a evaluar el riesgo de una persona de desarrollar ECVSA a 10 años teniendo en cuenta varios factores clínicos y de estilo de vida. [ Calculadora en línea PREVENT™ Opens in new window ] [55] Cuando se aplican a grupos similares de población a su cohorte de derivación, estas herramientas funcionan bien. Por lo tanto, los proveedores de salud deben estar familiarizados con la mejor herramienta de predicción de riesgos en su grupo de población de pacientes.[56][57]
Cuando se utilizan las ecuaciones a partir de estudios de cohortes agrupados, los pacientes pueden clasificarse de acuerdo con su riesgo pronosticado de 10 años de eventos graves de ECVSA (infarto de miocardio fatal y no fatal o accidente cerebrovascular) en: riesgo bajo (<5%), riesgo límite (5.0% a <7.5%), riesgo intermedio (≥7.5% a <20%), y riesgo alto (>20%). En pacientes de riesgo límite e intermedio, se pueden considerar factores clínicos y de laboratorio que aumentan el riesgo para decidir el uso de tratamientos hipolipemiantes. Estos factores incluyen: antecedentes familiares de ECVSA prematura (hombres de <55 años, mujeres de <65 años), hipercolesterolemia primaria (colesterol LDL ≥4.1 mmol/L [≥160 mg/dL] o colesterol no HDL ≥4.9 mmol/L [≥190 mg/dL]), síndrome metabólico, tasa de filtración glomerular (TFG) estimada 15-59 mL/min/1.73 m², afecciones inflamatorias crónicas (psoriasis, artritis reumatoide, VIH/SIDA), menopausia prematura, preeclampsia, ascendencia sudasiática, proteína C-reactiva elevada de alta sensibilidad ≥19.1 nmol/L (≥2 mg/L), lipoproteína (a) elevada (>50 mg/dL o >125 nmol/L), apolipoproteína B elevada (≥1.3 g/L [≥130 mg/dL])], o un índice tobillo/brazo <0.9.[44][57][58]
En pacientes con riesgo límite o intermedio después del uso de puntuaciones de riesgo y potenciadores de riesgo (si están presentes), el calcio en las arterias coronarias (CAC) puede utilizarse como ayuda para la toma de decisiones, cuando afecta a la intensidad de las estrategias preventivas, en particular las terapias hipolipemiantes.[44][57]
Los pacientes con manifestación clínica o en alto riesgo de enfermedad cardiovascular se deberán tratar con un tratamiento modificador de lípidos (generalmente, una estatina, si no existe contraindicación), además de con modificaciones del estilo de vida. En personas con un riesgo menor, el tratamiento farmacológico se indica generalmente si los cambios en el estilo de vida no resultan eficaces a corto plazo (3-6 meses). Existen evidencias de que el tratamiento con estatinas reduce los episodios cardiovasculares y la mortalidad en personas sin enfermedad cardiovascular clínica pero con factores de riesgo cardiovascular presentes.[59][60] Además, existen evidencias de que la reducción del riesgo es similar en hombres y mujeres con un riesgo comparable de enfermedad cardiovascular.[61]
El grupo de investigadores Cholesterol Treatment Trialists (CTT) ha demostrado una reducción de la mortalidad y la enfermedad cardiovascular mediante la reducción del colesterol de las lipoproteína de baja densidad (LDL), independientemente de la presencia de enfermedad cardiovascular.[59] Este metanálisis evaluó los efectos de las estatinas frente al placebo, de las estatinas más potentes frente a las menos potentes y de las estatinas de dosis más altas frente a las de dosis más bajas durante aproximadamente 5 años. Este trabajo demostró claramente los beneficios de la reducción de las LDL en la prevención de las enfermedades cardiovasculares y la mortalidad, incluso en personas sin hipercolesterolemia manifiesta y únicamente en presencia de factores de riesgo de enfermedad cardiovascular. Un metanálisis de la US Preventive Services Task Force (USPSTF) confirmó los resultados del CTT, incluidos los beneficios sobre la mortalidad.[60] En la era actual, la rentabilidad del tratamiento con estatinas es ampliamente aplicable a casi todas las poblaciones de riesgo primario y secundario.[62]
En pacientes con trastornos inflamatorios crónicos, como artritis reumatoide o VIH, las guías de práctica clínica de la American Heart Association/American College of Cardiology recomiendan un lipidograma en ayunas y una evaluación de los factores de riesgo de ASCVD antes y 4-12 semanas después de iniciar la terapia modificadora de la enfermedad inflamatoria o el tratamiento antirretroviral, para ayudar a la toma de decisiones sobre el inicio y el ajuste de la terapia hipolipemiante[44]
Modificación del estilo de vida
Se recomiendan cambios en el estilo de vida de todos los pacientes. Existen evidencias claras de que la reducción de las grasas totales y saturadas de la dieta, la pérdida de peso en pacientes con sobrepeso, el ejercicio aeróbico y la adición de estanoles/esteroles vegetales a la dieta conducen a una disminución del colesterol LDL y a un aumento del colesterol HDL.[30][63][64][65]
La implementación de cambios en la dieta puede resultar difícil para muchos pacientes, por lo que puede ser útil incluir un nutricionista en el plan de atención al paciente. Se deberá recomendar una ingesta reducida de colesterol y grasas saturadas, así como el aumento del consumo de fibra dietética, carbohidratos complejos y grasas no saturadas.[14][31]
Un amplio estudio realizado en el Reino Unido con más de 2500 pacientes reveló que solo con la dieta, se pudo reducir el colesterol LDL entre un 5% y un 7% en el 60% de los pacientes, que también experimentaron una reducción media del peso corporal de un 1.8%.[66] Un metanálisis de 37 estudios en los que se evaluaron la fase I y la fase II de las dietas (concentración de grasas saturadas <10% y <7%, respectivamente) demostró una reducción promedio del 13% del colesterol LDL Un metanálisis de 23 ensayos controlados reveló una disminución del 7% del colesterol LDL con suplementos de soja y una disminución del 19% del colesterol LDL con una dieta mediterránea. Las dietas ricas en fibra soluble reducen el colesterol LDL un 2% por gramo de fibra ingerida al día.[67] Las dietas basadas en plantas se han asociado con la reducción del LDL-C, el colesterol total y la apolipoproteína B.[68][69]
El efecto del ejercicio aeróbico y de la dieta se ha estudiado en 377 hombres y mujeres con niveles bajos de colesterol HDL y niveles altos de colesterol LDL. Se observaron reducciones significativas de LDL en el grupo de dieta y ejercicio en comparación con el grupo de control o el de dieta sola.[70]
Los pacientes con un riesgo cardiovascular medio o bajo se pueden tratar con una modificación del estilo de vida durante 3 a 6 meses antes de considerar el tratamiento con fármacos hipolipemiantes.[71] No obstante, este periodo de tiempo sigue siendo tema de controversia; se deberán coordinar 2 a 3 visitas de seguimiento en un plazo de 2 a 3 meses para evaluar la motivación y el cumplimiento terapéutico.
Tratamiento farmacológico: estatinas
Cuando los cambios en el estilo de vida por sí solos no son adecuados para reducir el colesterol a los niveles indicados por las guías de práctica clínica, se recomienda el tratamiento farmacológico con estatinas como opción de primera línea. En pacientes con colesterol LDL extremadamente elevado (> 4.9 mmol/L [>190 mg/dL]) y las personas con alto riesgo cardiovascular, el tratamiento farmacológico debe acompañar a la dieta y el ejercicio como enfoque terapéutico inicial.[44][48][51]
La colaboración CTT ha demostrado que por cada 1 mmol/L (39 mg/dL) de reducción del colesterol LDL, se produce una reducción del riesgo relativo del 10% de mortalidad por cualquier causa, del 20% de muertes por enfermedad coronaria, del 27% de infarto de miocardio no mortal, del 25% de revascularización coronaria y del 21% de accidente cerebrovascular isquémico.[59]
Un metanálisis ampliado del USPSTF y una revisión de la Cochrane confirman una reducción de la mortalidad por todas las causas y de los principales episodios cardiovasculares.[60][72][73]
[  ]
El USPSTF recomienda que los adultos de 40-75 años que presenten uno o más factores de riesgo cardiovascular (es decir, dislipidemia, diabetes, hipertensión o tabaquismo) y un riesgo estimado de enfermedad cardiovascular a 10 años igual o superior al 10% empiecen a tomar una estatina. A las personas con un riesgo a 10 años entre el 7.5% y menos del 10% se les puede ofrecer selectivamente una estatina.[72] Los datos de los ensayos apoyan el uso de estatinas en individuos de riesgo intermedio étnicamente diversos sin enfermedad cardiovascular.[74] En los pacientes con síndrome coronario agudo se utilizan dosis más altas debido al papel que desempeñan las estatinas en la estabilización de la placa.
]
El USPSTF recomienda que los adultos de 40-75 años que presenten uno o más factores de riesgo cardiovascular (es decir, dislipidemia, diabetes, hipertensión o tabaquismo) y un riesgo estimado de enfermedad cardiovascular a 10 años igual o superior al 10% empiecen a tomar una estatina. A las personas con un riesgo a 10 años entre el 7.5% y menos del 10% se les puede ofrecer selectivamente una estatina.[72] Los datos de los ensayos apoyan el uso de estatinas en individuos de riesgo intermedio étnicamente diversos sin enfermedad cardiovascular.[74] En los pacientes con síndrome coronario agudo se utilizan dosis más altas debido al papel que desempeñan las estatinas en la estabilización de la placa.
Las estatinas inhiben 3-hidroxi-3-metilglutaril-coenzima (HMG-CoA) reductasa, una enzima clave en la síntesis del colesterol que permite la regulación ascendente de los receptores de LDL y una depuración de LDL mejorada. Las reducciones del colesterol LDL con estatinas oscila entre un 20% y un 55%, en función del tipo y la dosis de la estatina elegida.[75]
La American College of Cardiology/American Heart Association han definido como estatinas de intensidad moderada como una que generalmente reduce el nivel de colesterol LDL en un 30-49%, mientras que las dosis de estatinas de alta intensidad son las que reducen el nivel de colesterol LDL en ≥50%.[44]
La terapia con estatinas se deberá iniciar en pacientes que pertenezcan a los siguientes grupos:
Guías de práctica clínica del American College of Cardiology y la American Heart Association (Estados Unidos):[44]
Presencia de ECVSA, no en muy alto riesgo de eventos futuros: trate a los pacientes de ≤75 años de edad con estatina de alta intensidad (la dosis diaria disminuye el colesterol LDL en ≥50%) o con estatina de intensidad moderada (la dosis diaria disminuye el colesterol LDL en un 30% a <50%) si no se tolera el tratamiento de alta intensidad; trate a los pacientes de edad >75 años con estatinas de intensidad moderada o alta.
Presencia de ECVSA, con un riesgo muy alto de eventos futuros: trate con terapia de alta intensidad o el máximo tratamiento con estatinas. El riesgo muy alto se define como un historial de múltiples eventos mayores de ECVSA (síndrome coronario agudo reciente [en los últimos 12 meses], infarto de miocardio distinto del síndrome coronario agudo reciente, accidente cerebrovascular isquémico, enfermedad arterial periférica sintomática[claudicación con índice tobillo/brazo <0.85], revascularización previa, o amputación]) o un evento mayor de ECVSA y múltiples afecciones de alto riesgo (edad ≥65 años, antecedentes familiares heterocigóticos, antecedentes de injerto de bypass de arteria coronaria previo o intervención coronaria percutánea, diabetes mellitus, hipertensión, enfermedad renal crónica, tabaquismo actual, colesterol LDL persistentemente elevado (≥2.6 mmol/L (≥100 mg/dL)]) a pesar del máximo tratamiento tolerado, antecedentes de insuficiencia cardíaca congestiva).
Personas entre 20 y 75 años con aumentos primarios de colesterol LDL >4.9 mmol/L (>190 mg/dL): este grupo incluye pacientes que presentan hipercolesterolemia familiar y son de alto riesgo teniendo en cuenta solo el nivel de colesterol LDL; en este grupo no se estima el riesgo a los 10 años; se tratan con una estatina de alta intensidad o una estatina de intensidad moderada si no son candidatos para el tratamiento con estatinas de alta intensidad.
Personas de 40-75 años con diabetes mellitus: comenzar con estatinas de intensidad moderada en aquellos que tengan un riesgo estimado de enfermedad cardiovascular aterosclerótica (ECVSA) a 10 años <7.5% y sin factores de riesgo elevados adicionales. Empezar a administrar estatinas de alta intensidad a los pacientes de mayor riesgo.
Las personas sin ECVSA o diabetes de entre 40 y 75 años de edad con colesterol LDL de 1.8 a 4.9 mmol/L (70-189 mg/dL): estiman un riesgo de 10 años y si hay riesgo límite, de 5.0% a <7.5%, y hay presentes potenciadores de riesgo, después mantenga una discusión sobre la terapia con estatinas de intensidad moderada; la discusión entre el paciente y el médico debe considerar el potencial de los beneficios de la reducción de riesgo de la ECVSA y los efectos adversos, las interacciones farmacológicas y las preferencias del paciente respecto al tratamiento. Los potenciadores de riesgo incluyen: antecedentes familiares de ECVSA prematura; colesterol LDL persistentemente elevado de ≥4.1 mmol/L (≥160 mg/dL); enfermedad renal crónica; síndrome metabólico; afecciones específicas de las mujeres (p. ej., preeclampsia, menopausia prematura); enfermedades inflamatorias (especialmente artritis reumatoide, psoriasis, VIH); factores de etnicidad (p. ej., ascendencia del sur de Asia); proteína C-reactiva elevada de alta sensibilidad ≥19.1 nmol/L (≥2 mg/dL); lipoproteína (a) elevada >50 mg/dL o >125 nmol/L, apolipoproteína B elevada ≥1.3 g/L (≥130 mg/dL), índice tobillo/brazo <0.9. Si existe riesgo intermedio, ≥7.5% a <20%, y están presentes los potenciadores de riesgo, se debe iniciar la terapia con estatinas de intensidad moderada; si no está seguro, puede usar el índice de calcio en las arterias coronarias (CAC=0: menor riesgo; no considere el uso de estatinas a menos que haya diabetes, antecedentes familiares de cardiopatías congénitas (CC) prematuras, tabaquismo; CAC=1-99: favorece el uso de estatinas, especialmente si la edad es superior a los 55 años; CAC=100+ y/o ≥percentil 75: empiece con estatinas). Si es de alto riesgo, ≥20%, comience el tratamiento con estatinas de alta intensidad.
Personas con insuficiencia cardíaca: no iniciar de manera rutinaria la terapia con estatinas en pacientes que requieran hemodiálisis o que padezcan insuficiencia cardíaca de clase III o IV.
Guías de práctica clínica del National Institute for Health and Care Excellence:[51]
Presencia de ECVSA o prevención secundaria: iniciar atorvastatina a dosis altas en ausencia de contraindicaciones. Para la prevención secundaria de las ECV, el objetivo es lograr que el colesterol LDL sea ≤2,0 mmol/L (<77 mg/dL) o el colesterol no HDL ≤2,6 mmol/L (<100 mg/dL). Se recomiendan dosis altas de atorvastatina para las personas con ECV, con independencia de su nivel de colesterol, a menos que se aplique alguna de las siguientes condiciones: posibles interacciones farmacológicas (p. ej., con claritromicina, azoles sistémicos u otros fármacos antimicóticos); un alto riesgo de efectos adversos (p. ej., en personas de edad avanzada, personas con baja masa muscular o alteraciones en la función renal); o la preferencia del paciente por una dosis más baja.[Evidencia A][Evidencia B]
Ofrecer atorvastatina para la prevención primaria de las enfermedades cardiovasculares (ECV) a las personas que tengan un riesgo de 10 años de desarrollar ECV igual o superior al 10% (estimado con QRISK3). QRISK risk calculator Opens in new window
Ofrecer atorvastatina para la prevención primaria de la ECV a las personas con diabetes tipo 1 que tengan más de 40 años, más de 10 años de diabetes, nefropatía establecida u otros factores de riesgo de ECV.
Ofrecer atorvastatina para la prevención primaria de la ECV a las personas con diabetes tipo 2 que tengan un riesgo ≥10% a 10 años de desarrollar ECV (estimado con QRISK3). QRISK risk calculator Opens in new window
Ofrecer atorvastatina para la prevención primaria o secundaria de la ECV a personas con enfermedad renal crónica. Se debe aumentar la dosis si no se logra una disminución del colesterol no HDL > 40% y la tasa de filtración glomerular (TFG) estimada es ≥30 mL/minuto/1.73 m². Discutir el uso de dosis más altas con un especialista renal si la TFG estimada es <30 ml/minuto/1.73 m².
Seguimiento tras el inicio de tratamiento con estatina: el colesterol total, el colesterol HDL y el colesterol no HDL en todas las personas que hayan comenzado un tratamiento con estatinas de alta intensidad a los 3 meses del inicio del tratamiento con el objetivo de lograr una reducción del colesterol no HDL superior al 40%. Si no se consigue una reducción >40% del colesterol no HDL: discutir la adherencia y el momento de administración de la dosis; optimizar la adherencia a las medidas dietéticas y de estilo de vida; considerar el aumento de la dosis si se ha empezado con menos de 80 mg/día de atorvastatina y se considera que la persona tiene un riesgo mayor debido a comorbilidades, puntuación de riesgo o utilizando el juicio clínico.
Recomendaciones de la International Atherosclerosis Society (IAS):[53]
La IAS no establece específicamente "objetivos del tratamiento" para los niveles de lipoproteínas aterogénicas por distintas circunstancias. En su lugar, identifica niveles óptimos de colesterol aterogénico y establece, de manera general, que la intensidad del tratamiento para reducir el colesterol se deberá ajustar conforme al riesgo a largo plazo.
Es recomendable que la mayoría de los pacientes con enfermedad cardiovascular ateroesclerótica (ECVSA) reciba un tratamiento con estatinas de máxima intensidad, siempre que este se tolere. El nivel óptimo de colesterol LDL en pacientes con ECVSA ateroesclerótica establecida es <1.8 mmol/L (<70 mg/dL) (o colesterol no HDL <2.6 mmol/L [<100 mg/dL]). En muchos pacientes, es posible que sea necesario un tratamiento adyuvante con otros medicamentos hipolipemiantes (p. ej., ezetimiba, fármacos de secuestro de ácidos biliares, fibratos) para alcanzar los valores recomendados. [
 ]
]
La International Atherosclerosis Society (IAS) sugiere que un nivel óptimo de colesterol LDL para la prevención primaria es < 2.6 mmol/L (<100 mg/dL) o colesterol no HDL <3.4 mmol/L (<130 mg/dL). Se recomienda utilizar un tratamiento con estatinas ajustado conforme al riesgo de por vida de enfermedad cardiovascular (desde los 50 a los 80 años de edad) con los siguientes niveles de riesgo: alto (≥45%), moderadamente alto (30%-44%), moderado (15%-29%), y bajo (<15%). La mayoría de pacientes de alto riesgo requieren tratamiento con estatinas para alcanzar un nivel de colesterol LDL <2.6 mmol/L (<100 mg/dL) (o de colesterol no HDL <3.4 mmol/L [<130 mg/dL]); por lo tanto, se recomienda el uso de estos fármacos. El uso de estatinas también se deberá considerar en personas con un riesgo moderadamente alto y como tratamiento opcional en personas con un riesgo moderado.
En personas más jóvenes, especialmente aquellas con un nivel alto de colesterol LDL (hipercolesterolemia familiar), los algoritmos clínicos de tabaquismo y diabetes generalmente subestiman el riesgo y se deben tratar esos factores de riesgo. El tratamiento con estatinas se debe considerar en función de la gravedad de las elevaciones de colesterol LDL y si no se han controlado adecuadamente otros factores de riesgo.
El riesgo de por vida se puede estimar como:[Figure caption and citation for the preceding image starts]: Riesgo de morbilidad de enfermedad cardiovascular (ECV) a los 80 años de edadPanel de Expertos en Dislipidemia. Un documento de posición de la sociedad internacional de aterosclerosis: recomendaciones globales para el manejo de la dislipidemia: resumen ejecutivo. Atherosclerosis. 2014 Feb;232(2):410-3; usado con autorización [Citation ends].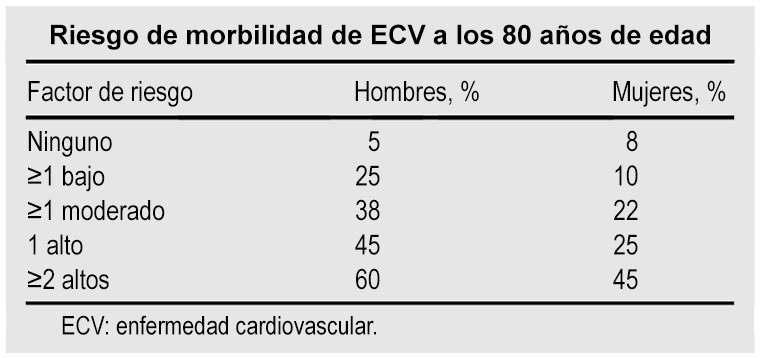 [Figure caption and citation for the preceding image starts]: Algoritmo de riesgo de Lloyd-Jones/FraminghamPanel de Expertos en Dislipidemia. Un documento de posición de la sociedad internacional de aterosclerosis: recomendaciones globales para el manejo de la dislipidemia: resumen ejecutivo. Atherosclerosis. 2014 Feb;232(2):410-3; usado con autorización [Citation ends].
[Figure caption and citation for the preceding image starts]: Algoritmo de riesgo de Lloyd-Jones/FraminghamPanel de Expertos en Dislipidemia. Un documento de posición de la sociedad internacional de aterosclerosis: recomendaciones globales para el manejo de la dislipidemia: resumen ejecutivo. Atherosclerosis. 2014 Feb;232(2):410-3; usado con autorización [Citation ends].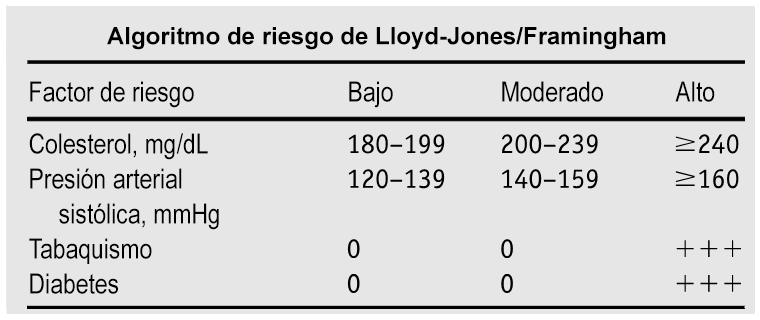
Guía de práctica clínica de European Society of Cardiology/European Atherosclerosis Society:[41]
Para pacientes con un riesgo cardiovascular muy alto (enfermedad cardiovascular documentada o inequívoca en los estudios por imágenes; diabetes mellitus con daño de órgano objetivo (microalbuminuria, retinopatía, neuropatía), o al menos tres factores de riesgo principales, o diabetes mellitus tipo 1 de larga duración [>20 años]; enfermedad renal crónica grave [TFG <30 mL/minuto/1.73 m²]; un nivel calculado de SCORE ≥10% para un riesgo a 10 años de ECV fatal), una reducción de colesterol LDL a partir de la línea inicial de ≥50% y se recomienda un objetivo de colesterol LDL de <1.4 mmol/L (<55 mg/dL). European Society of Cardiology SCORE risk charts Opens in new window
Para pacientes con alto riesgo cardiovascular (factores de riesgo individuales marcadamente elevados [en particular colesterol total >8 mmol/L (>310 mg/dL) o presión arterial ≥180/110 mmHg], personas con diabetes mellitus que no cumplen con los criterios de riesgo muy altos y presentan un factor de riesgo adicional o duración de la diabetes mellitus ≥10 años, enfermedad renal crónica moderada [TFG 30-59 mL/minuto/1.73 m²], un SCORE calculado entre el 5% y el 9% para un riesgo de 10 años de CVD fatal), una reducción del colesterol LDL-a partir del nivel inicial de ≥50% y se recomienda un objetivo de colesterol LDL de <1.8 mmol/L (<70 mg/dL). European Society of Cardiology SCORE risk charts Opens in new window
Para las personas en riesgo moderado (pacientes jóvenes con diabetes mellitus [<35 años para el tipo 1 y <50 años para el tipo 2] con una duración <10 años, sin factores de riesgo adicionales, un nivel de PUNTUACION entre 1% y 4% para un riesgo de 10 años de ECV fatal) se debe considerar una meta de colesterol LDL <2.6 mmol/L (<100 mg/dL). European Society of Cardiology SCORE risk charts Opens in new window
Para las personas en bajo riesgo (nivel de SCORE <1% para un riesgo de CVD fatal a 10 años) un objetivo de lipoproteína de baja densidad (LDL) <3.0 mmol/L debe considerarse (<116 mg/dL). European Society of Cardiology SCORE risk charts Opens in new window
Recomendación para el uso de estatinas: recetar estatinas hasta la dosis más alta o dosis máxima tolerable para lograr la meta.
Mientras que las directrices sobre dislipidemia de la Society of Cardiology (ESC)/European Atherosclerosis Society (EAS) de 2019 hacen referencia al sistema de evaluación del riesgo SCORE, las directrices de la ESC de 2021 sobre prevención de enfermedades cardiovasculares recomiendan la evaluación actualizada del riesgo SCORE2.[56] Es probable que las futuras interaciones de las directrices sobre lípidos actualicen las recomendaciones a este sistema de puntuación.
Los efectos adversos de las estatinas son infrecuentes, pero incluyen elevaciones de las enzimas hepáticas y miositis o rabdomiólisis. También se han registrado casos de toxicidad muscular sin elevación de enzimas. Esto parece ocurrir con mayor frecuencia cuando se utilizan algunas de las estatinas con fármacos que inhiben la isoenzima 3A4 del citocromo P-450 (p. ej., antibióticos macrólidos, inhibidores de la proteasa del VIH, antimicóticos azólicos y ciclosporina). Algunas estatinas (lovastatina, simvastatina, rosuvastatina, fluvastatina) pueden elevar los niveles de digoxina y potenciar el efecto de la warfarina. Se aconseja tener precaución cuando se utilicen estatinas con estos fármacos y es posible que sean necesarias dosis inferiores de estatinas (o del fármaco que interactúe). Además, la Administración de Medicamentos y Alimentos de EE. UU. (FDA) recomienda actualmente que la dosis de simvastatina no exceda los 40 mg/día, debido a que la dosis de 80 mg/día implica mayor riesgo de miopatía. Recomienda utilizar la dosis de 80 mg/día solo en pacientes que hayan recibido esta dosis durante 12 meses o más sin experimentar reacciones adversas. Para pacientes que no respondan a la dosis de 40 mg/día, la FDA recomienda cambiar a una estatina distinta, en lugar de aumentar la dosis.
Dos metanálisis, uno que compara las estatinas con un placebo y otro que compara una terapia con estatinas más intensiva con otra menos intensiva, demuestran que el uso de estatinas está asociado a un mayor riesgo de diabetes de tipo 2 de inicio reciente.[76][77] Otro estudio, que analizó 3 ensayos de gran tamaño muestral, reveló que existe un ligero mayor riesgo de desarrollar diabetes de tipo 2 de inicio reciente con dosis altas de atorvastatina y que el nivel inicial de glucosa en ayunas y las características del síndrome metabólico son predictivos de diabetes de tipo 2 de inicio reciente.[78] Un ensayo a gran escala sobre la rosuvastatina demostró que, aunque el tratamiento con estatinas aumentaba el riesgo de diabetes mellitus, este peligro era superado por los beneficios cardiovasculares de las estatinas, con 134 eventos vasculares o muertes evitadas por cada 54 nuevos casos de diabetes diagnosticados.[79]
En pacientes con enfermedad renal crónica (ERC), un estudio en el que se evaluó la asociación de la simvastatina y la ezetimiba y un metanálisis de los principales ensayos sobre tratamientos hipolipemiantes en pacientes con ERC confirmaron la importancia de reducir el colesterol para prevenir la enfermedad cardiovascular en estas personas.[80]
Los efectos adversos son más frecuentes en pacientes de edad avanzada, aquellos con varias enfermedades y en los que reciben varios fármacos. En algunas personas, cambiar de una estatina a otra o reducir la dosis puede mejorar los efectos negativos.
Estudios más antiguos han sugerido que la reducción agresiva de lípidos puede tener efectos adversos en el cerebro, al provocar trastorno cognitivo, demencia y accidente cerebrovascular hemorrágico. Sin embargo, una revisión de la evidencia actual y la declaración científica de la American Heart Association concluye que no existe ninguna asociación. Se considera que el riesgo de accidente cerebrovascular hemorrágico con tratamiento hipolipemiante entre pacientes con antecedentes de accidente cerebrovascular hemorrágico no es sólido y requiere más estudios.[81]
Han surgido datos de algunos de los ensayos iniciales sobre estatinas que documentan la seguridad y eficacia a largo plazo del tratamiento con estatinas. En el ensayo de prevención primaria de West of Scotland Coronary Prevention Study, el tratamiento con estatinas llevó a una reducción sustancial en el resultado de la enfermedad cardiovascular en dos décadas, sin ninguna inquietud nueva relativa a la seguridad.[82] Se documentaron hallazgos similarmente favorables en relación con la eficacia del tratamiento con estatinas en el ensayo de seguimiento por 16 años de Long-term Intervention with Pravastatin in Ischemic Disease, un ensayo de prevención secundaria.[83] En relación con la seguridad a largo plazo, no hubo ningún impacto de las estatinas en mortalidad por cáncer o no cardiovascular durante el seguimiento a largo plazo.
Tratamiento farmacológico: opciones sin estatinas
Las estatinas son una clase de fármacos muy segura. Sin embargo, muchos pacientes no logran una reducción adecuada del colesterol LDL y hasta un 10% de las personas es intolerante, especialmente cuando se trata de síntomas musculares.[84] No existe consenso sobre el tratamiento de los pacientes intolerantes a las estatinas. El cambio de una estatina a otra o la reducción de la dosis/intensidad pueden mejorar la tolerancia. Además, para estos pacientes se ha propuesto un tratamiento de administración de estatinas en días alternos con o sin ezetimiba a diario. Una revisión sistemática de la administración de estatinas en días alternos sugiere que cuando se utilizan estatinas más potentes, como la atorvastatina y la rosuvastatina, se obtienen reducciones del colesterol LDL similares a las obtenidas con el tratamiento diario.[84] No obstante, la tolerancia no se evaluó adecuadamente en la mayoría de estos estudios. Además, los estudios se ven obstaculizados por el número reducido de sujetos y el seguimiento a corto plazo. Finalmente, el tratamiento en días alternos puede conducir a la omisión de dosis o la administración de dosis adicionales.
La intolerancia completa a las estatinas es rara; sin embargo, para estos pacientes, puede considerarse un ensayo de fármacos no estatínicos para reducir el colesterol LDL como alternativa a las estatinas, con derivación a un especialista en lípidos.[41][54]
Para los pacientes que no consiguen una reducción adecuada del colesterol LDL con el tratamiento máximo tolerado con estatinas, puede considerarse la adición de tratamientos sin estatinas.[41][44][54]
1. Ezetimiba
Afecta a la absorción del colesterol dietario y biliar en las microvellosidades intestinales al interactuar con receptores específicos y, a diferencia de las resinas secuestradoras de ácidos biliares, resulta en una exposición sistémica.
Se puede administrar además solo o junto al tratamiento con estatinas y cambios en el estilo de vida. Eficaz para reducir los lípidos en pacientes con aumentos leves a moderados de colesterol LDL; sin embargo, con un promedio de reducción del colesterol LDL del 20% puede no ser suficiente para pacientes que necesiten una reducción mayor del colesterol LDL. Si se usa sola, se han registrado reducciones de LDL de entre un 15% a un 20%.[85] En combinación con la simvastatina, logró reducir el nivel de LDL un 14% adicional por encima del efecto obtenido solo con la simvastatina.[86]
El ensayo IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial) demostró que el tratamiento con ezetimiba más simvastatina redujo los riesgos absolutos y relativos de eventos cardiovasculares graves en personas con cardiopatía coronaria de riesgo alto, en comparación con la simvastatina sola.[87] El beneficio de la ezetimiba es proporcional a su habilidad de reducción del colesterol LDL.[88]
El ensayo EWTOPIA 75, en el que se asignó aleatoriamente a pacientes de 75 años o más sin ASCVD a ezetimiba frente a placebo, mostró una reducción significativa de los episodios cardiovasculares y la revascularización coronaria en el brazo de ezetimiba en comparación con el de placebo.[89]
2. Inhibidores de la proteína convertasa subtilisina/kexina tipo 9 (PCSK9) (anticuerpos monoclonales)
PCSK9 se fija a los receptores de LDL, facilitando su degradación. Cuando está en exceso, PCSK9 es una causa de hipercolesterolemia familiar. Las mutaciones de pérdida de funcionalidad se asocian a niveles de colesterol LDL más bajos y a un menor riesgo de eventos cardiovasculares.[90]
Los anticuerpos monoclonales humanos dirigidos contra PCSK9 (p. ej., evolocumab y alirocumab) proporcionan tres veces el efecto de la ezetimiba (disminución del 60% del colesterol LDL).
Los inhibidores del PCSK9 reducen significativamente el colesterol LDL en aproximadamente un 50% a 60% y esto da como resultado un mayor logro del objetivo de colesterol LDL cuando se añade a las estatinas en una variedad de grupos de población, incluidos aquellos que presentan hipercolesterolemia familiar heterocigótica.[91]
Los ensayos FOURIER y ODYSSEY que evaluaron el evolocumab y el alirocumab, respectivamente, han demostrado que la inhibición del PCSK9 reduce los eventos cardiovasculares en individuos con alto riesgo de padecer enfermedad cardiovascular.[92][93][94][95]
En FOURIER (n = 27,564; pacientes con manifestaciones anteriores de enfermedad cardiovascular aterosclerótica) la adición de evolocumab al tratamiento con estatinas, en comparación con el tratamiento con estatinas solo, resultó en una reducción del 15% del riesgo relativo de eventos cardiovasculares importantes y una reducción del 20% del riesgo relativo en el objetivo final secundario combinado de infarto de miocardio, accidente cerebrovascular y mortalidad. La mediana inicial del colesterol LDL fue de 2.3 mmol/L (90 mg/dL) y se redujo a una mediana de 0.8 mmol/L (30 mg/dL) con evolocumab. Para prevenir un evento clínico de los criterios de evaluación primarios y secundarios, 66 y 50 individuos, respectivamente, deberían ser tratados durante 2 años. El uso de evolocumab en el ensayo condujo a una reducción del riesgo relativo del 20% al 25% en el número total de infartos de miocardio, accidentes cerebrovasculares y revascularizaciones coronarias durante el período de estudio.[96] Un análisis preestablecido encontró una asociación directa continua de la disminución del colesterol LDL con la reducción de los eventos cardiovasculares con beneficios de hasta 0.25 mmol/L (10 mg/dL) y con los mayores beneficios en aquellas personas que alcanzaron un colesterol LDL <0.5 mmol/L (<20 mg/dL).[97] El evolocumab se toleró bien, no hubo diferencias significativas entre los grupos en cuanto a los eventos adversos (incluidos eventos de diabetes de inicio reciente y eventos neurocognitivos), excepto en las reacciones en el sitio de la inyección, que fueron más frecuentes con evolocumab (el 2.1% frente al 1.6%).
En el estudio abierto de extensión de FOURIER, 6635 pacientes del estudio FOURIER recibieron evolocumab y fueron seguidos durante una mediana de 5 años (algunos, por tanto, recibieron evolocumab durante más de 8 años en total). En dicho estudio de extensión se observó que los pacientes asignados inicialmente al azar a evolocumab en el ensayo FOURIER tenían un menor riesgo de sufrir eventos cardiovasculares que los asignados inicialmente al azar a placebo, y que las tasas de eventos adversos seguían siendo bajas.[98][99]
En un nuevo análisis de los datos de mortalidad del ensayo FOURIER original, en el que se utilizaron documentos reglamentarios para abordar las discrepancias y restaurar los datos completos de mortalidad, se comunicó que el beneficio de mortalidad de evolocumab puede ser menos significativo de lo que se informó inicialmente.[100] Este nuevo análisis ha desatado polémica. Los críticos argumentan que el nuevo análisis del estudio de FOURIER es fundamentalmente defectuoso debido al uso que hace de datos incompletos y a un proceso post hoc y no ciego. Afirman que el ensayo FOURIER original siguió un riguroso proceso de adjudicación de eventos preespecificados y ciegos por parte de cardiólogos y neurólogos experimentados, de conformidad con las definiciones y la normativa de la FDA. Enfatizan que la metodología y los resultados del ensayo original fueron sólidos y que el nuevo análisis reclasificó incorrectamente las muertes, lo que condujo a una conclusión errónea sobre la eficacia de evolocumab.[100]
EBBINGHAUS, un subestudio de FOURIER, no halló ninguna asociación entre el tratamiento con evolocumab y los acontecimientos adversos neurocognitivos evaluados objetivamente mediante la Batería Automatizada de Pruebas Neuropsicológicas de Cambridge (CANTAB).[101] Un análisis adicional de los datos del ensayo FOURIER encontró que el evolocumab redujo los niveles de colesterol de lipoproteínas de baja densidad en un 50% o más en el 90.5% de los pacientes y en un 30% o más en el 99.8% de los pacientes.[102]
En ODYSSEY OUTCOMES, un ensayo controlado aleatorizado doble ciego multicéntrico de 18,924 pacientes, el alirocumab redujo el riesgo de eventos cardiovasculares isquémicos recurrentes (incluida la mortalidad por todas las causas y el infarto de miocardio) en comparación con el placebo en pacientes que tenían un síndrome coronario agudo previo y estaban recibiendo tratamiento con estatinas de alta intensidad.[94][95][103][104]
En un metanálisis de 11 ensayos aleatorizados que comparaban los inhibidores de la PCSK9 con el placebo, y que incluían a 38,235 personas tratadas durante al menos 48 semanas, los inhibidores de la PCSK9 redujeron los infartos de miocardio en un 27% y los accidentes cerebrovasculares en un 19%, sin una diferencia significativa en la mortalidad cardiovascular. Sin embargo, es importante destacar que la población del estudio incluía tanto pacientes en prevención secundaria con episodios vasculares previos como individuos con hipercolesterolemia familiar pero sin episodios cardiovasculares previos. La heterogeneidad del riesgo inicial limita la interpretación de estos resultados.[105] Una revisión de la Cochrane que evaluó la eficacia y la seguridad de los inhibidores de la PCSK9 para la prevención de enfermedades cardiovasculares descubrió que tanto el alirocumab como el evolocumab disminuían el riesgo de enfermedad cardiovascular cuando se añadían a otros medicamentos que reducen el colesterol LDL (p. ej., estatinas o ezetimiba) y existe una sólida base probatoria para los inhibidores de la PCSK9 en personas que podrían no ser aptas para otros fármacos hipolipemiantes o en aquellas que no puedan alcanzar los objetivos lipídicos con otros tratamientos. Existen datos limitados sobre los beneficios de los inhibidores de la PCSK9 en comparación con otras terapias, y evidencias limitadas sobre los posibles problemas de seguridad.[106] [
 ]
[
]
[  ]
]
En algunos países, el alirocumab está aprobado como complemento de la dieta, solo o en combinación con otros tratamientos hipolipemiantes (p. ej., estatinas, ezetimiba), para el tratamiento de adultos con hiperlipidemia primaria (incluida la hipercolesterolemia familiar heterocigótica) para reducir el colesterol LDL, estatinas, ezetimiba), para el tratamiento de adultos con hiperlipidemia primaria (incluida la hipercolesterolemia familiar heterocigótica) para reducir el colesterol LDL; como complemento de otras terapias reductoras del LDL en pacientes con hipercolesterolemia familiar homocigótica para reducir el colesterol LDL; y para reducir el riesgo de infarto de miocardio, ictus y angina inestable que requiera ingreso hospitalario en adultos con enfermedad cardiovascular establecida.
En algunos países, el evolocumab está aprobado: como complemento de la dieta, solo o en combinación con otros tratamientos reductores de lípidos (p. ej., estatinas, ezetimiba), para el tratamiento de adultos con hiperlipidemia primaria (incluida la hipercolesterolemia familiar heterocigótica) con el fin de reducir el colesterol LDL; como complemento de la dieta y de otros tratamientos reductores de LDL (p. ej., los medicamentos para la diabetes), estatinas, ezetimiba, aféresis de LDL) en pacientes con hipercolesterolemia familiar homocigótica que requieren una reducción adicional del colesterol LDL; y para reducir el riesgo de infarto de miocardio, accidente cerebrovascular y revascularización coronaria en adultos con enfermedad cardiovascular establecida.
3. Secuestradores de ácidos biliares
Son eficaces en pacientes con elevaciones leves a moderadas del colesterol LDL.
Los fármacos secuestradores de ácidos biliares, como la colestiramina y el colesevelam se pueden utilizar como terapias adyuvantes a las estatinas y la ezetimiba en casos de hipercolesterolemia grave, en pacientes en alto riesgo de cardiopatía coronaria, cuando no se alcanzan los objetivos de colesterol LDL y, generalmente, en pacientes con hipercolesterolemia familiar. La ezetimiba bloquea aproximadamente el 50% de la absorción del colesterol y los fármacos secuestradores de ácidos biliares pueden ocuparse del colesterol restante presente en el lumen intestinal. Existe evidencia de que tanto el colesevelam como la colestiramina potencian el efecto reductor de la ezetimiba en los niveles de colesterol. Además, en caso de sitosterolemia (una afección poco frecuente), se pueden añadir fármacos secuestradores de ácidos biliares a la ezetimiba para reducir los niveles de fitosterol y colesterol.
Los inhibidores de los ácidos biliares actúan fijándolos en el intestino e impidiendo su reabsorción. A través de este proceso, se logra extraer aproximadamente el 90% de los ácidos biliares. La pérdida de ácidos biliares ricos en colesterol conduce a una disminución del colesterol intrahepático y a la regulación ascendente de los receptores de LDL. El aumento de la densidad de los receptores en el hígado permite reducir aún más el colesterol en sangre. En función de la dosis utilizada, se pueden obtener reducciones de LDL que van de un 10% a un 24%.[107]
La mayoría de los efectos adversos están relacionados con el tracto gastrointestinal e incluyen náuseas, distensión, cólicos y transaminasas hepáticas aumentadas. Para muchos pacientes, estos efectos adversos son muy limitantes.
La absorción de otros fármacos se puede ver considerablemente alterada. Cualquier otro fármaco se debe tomar 1 hora antes o 4 horas después de los fármacos secuestradores de ácidos biliares.
Están formalmente contraindicados en pacientes con niveles de triglicéridos >5.65 mmol/L (>500 mg/dL).
El umbral para considerar un tratamiento adicional sin estatinas varía en función del riesgo. Si el objetivo de reducción del colesterol LDL no se alcanza con el tratamiento máximo tolerado con estatinas, puede considerarse la posibilidad de utilizar tratamientos adicionales sin estatinas, como ezetimiba y/o un inhibidor de PCSK9 (anticuerpo monoclonal).[41][44][54] También hay aprobados nuevos tratamientos sin estatinas (p. ej., ácido bempedoico, inclisirán); puede que aún no estén incluidos en las guías de práctica clínica y se deberá consultar los protocolos locales.[54] Consulte el apartado de Tratamientos emergentes para más información.
La decisión de añadir tratamientos sin estatinas debe ser compartida entre el paciente y el médico tras una discusión sobre los riesgos, los beneficios y las preferencias del paciente. Deben optimizarse las modificaciones del estilo de vida, además de revisar la adherencia a las estatinas.[54]
Tratamiento de pacientes de edad avanzada
Existe controversia en la literatura acerca de si los pacientes mayores deben ser tratados con terapia modificadora de lípidos. En comparación con los pacientes más jóvenes, los individuos de mayor edad tienen un mayor riesgo de sufrir una ECVSA. El colesterol pierde su impacto como factor de riesgo en pacientes de edad avanzada y no existe consenso con respecto a si las estatinas se deberán prescribir para pacientes asintomáticos de edad avanzada con hipercolesterolemia. El estudio PROSPER (Prospective Study of Pravastatin in the Elderly at Risk), que evaluó los efectos del tratamiento con pravastatina en personas de 70 a 82 años de edad, determinó que, en la prevención primaria, el tratamiento con estatinas solo era eficaz en personas con un nivel de colesterol HDL <1.15 mmol/L (<45 mg/dL), para los que se obtuvo una reducción relativa de un 33%.[108] Un metanálisis de 8 estudios que incluyó a 24,674 personas de prevención primaria mayores de 65 años (42.7% mujeres; edad promedio 73.0 ± 2.9 años; seguimiento promedio 3.5 ± 1.5 años) mostraron que las estatinas, comparadas con el placebo, redujeron el riesgo de infarto de miocardio en un 39.4% (riesgo relativo: 0.606; IC del 95%: 0.434 a 0.847; p = 0.003) y el riesgo de accidente cerebrovascular en un 23.8% (riesgo relativo: 0.762; IC del 95%: 0.626 a 0.926; p = 0.006).[109] No obstante, no se observó beneficio alguno en cuanto a la mortalidad.
En los datos de cohortes de gran tamaño muestral se ha observado un aumento de los acontecimientos cardiovasculares adversos graves en adultos de 75 años o más a los que se les han retirado las estatinas, en comparación con los que las siguen tomando, tanto en cohortes de prevención primaria como secundaria.[110]
Un metanálisis de la colaboración CTT mostró una reducción relativa similar en el riesgo de eventos de ASCVD por mmol/L de reducción en el colesterol LDL con terapia de estatinas en individuos mayores de 75 años, en comparación con pacientes más jóvenes.[111]
Por lo tanto, tanto las guías de práctica clínica de la ESC/EAS como las del American College of Cardiology/American Heart Association recomiendan el tratamiento con estatinas para los pacientes mayores de 75 años con un episodio previo de ECVSA. En prevención primaria, las directrices recomiendan considerar el tratamiento con estatinas en este grupo de edad. Las guías de práctica clínica también destacan la necesidad de aumentar la concienciación sobre los eventos adversos en esta población, especialmente en presencia de comorbilidades, deterioro de la función renal o hepática y polifarmacia.[41][44]
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad