Abordagem
O principal objetivo do tratamento é garantir a hidratação, o equilíbrio eletrolítico e a nutrição durante o período de adaptação intestinal. O principal objetivo é que o paciente volte a ter um estilo de vida o mais normal possível, reduzindo e idealmente eliminando a necessidade de NP.
O tratamento depende da extensão e da anatomia da ressecção do intestino e envolve alteração alimentar (incluindo a necessidade de um aumento de ingestão de energia), suplementação de nutriente e fluidos, e medicamentos para minimizar as perdas de fluidos e controlar a diarreia.[4] Em pacientes com insuficiência intestinal irreversível, as capacidades de absorção do intestino delgado nunca são recuperadas, e esses pacientes necessitem de NP de longa duração.[1] Tais pacientes apresentarão recorrência de perda de peso, depleção de volume, desequilíbrio eletrolítico ou desnutrição ao tentar um desmame da NP.
Intervenções cirúrgicas são usadas para auxiliar a adaptação intestinal. Uma anastomose colônica funcionante é essencial para a adaptação; dessa forma, a reanastomose do cólon é uma intervenção cirúrgica primordial.
Quando houver falha da NP em um paciente, é necessário realizar uma terapia de resgate com transplante intestinal ou transplante combinado de intestino e fígado.
Pacientes com anastomose jejunoileocólica
O manejo depende principalmente do comprimento do intestino delgado residual.
Pacientes com intestino delgado residual com >100 cm (ou >150 cm se o cólon for parcialmente removido) podem não precisar de suporte com NP, podendo ser manejados somente com dieta. Caso não se consiga atingir o estado nutricional adequado, pode-se iniciar o suporte com NP parcial e desmame.
Pacientes com intestino delgado residual ≤100 cm (ou ≤150 cm se o cólon for parcialmente removido) geralmente precisam de suporte com NP parcial combinado com dieta oral. Os pacientes com anastomose jejunoileocólica têm as maiores probabilidades de desmame da NP.[4]
Todos os pacientes requerem monitoramento de eletrólitos/micronutrientes e reposição com reidratação oral. Caso haja hipersecreção de ácido gástrico e diarreia, elas devem ser controladas.[4]
Os pacientes devem ser encorajados a consumir uma dieta rica em carboidratos complexos, amidos e fibras solúveis, que podem ser sintetizados no cólon em ácidos graxos de cadeia curta, fornecendo uma fonte extra de energia.[27] Como o cólon está em continuidade, esses pacientes têm risco de nefrolitíase de oxalato, e também devem ser instruídos a iniciarem uma dieta baixa em oxalato.[4] A suplementação com cálcio oral pode ser benéfica.
Pacientes com anastomose jejunoileal com ressecção total do cólon
O cólon desempenha um papel essencial na absorção da água e de nutrientes, que é perdido nesse grupo de pacientes. Além disso, a síntese da vitamina K pela flora intestinal colônica (que poderia compensar parcialmente a má absorção intestinal da vitamina K) também é perdida, causando o risco de deficiência grave de vitamina K.
A maioria dos pacientes requer NP. Pacientes com 100 cm a 200 cm de intestino delgado residual geralmente precisam de suporte com NP parcial combinado com dieta oral. Todos os pacientes também requerem o monitoramento de eletrólitos/micronutrientes e reposição com reidratação oral. Caso haja hipersecreção de ácido gástrico e diarreia, elas devem ser controladas.[2][4]
Deve-se tentar o desmame da NP, mas ele pode não ser bem-sucedido. É quase certo que pacientes com ≤100 cm de intestino delgado residual terão dependência da NP.
Pacientes com jejunostomia terminal ou duodenostomia
Esses pacientes têm o risco mais elevado de insuficiência intestinal crônica, a menos que seja realizada uma reanastomose primária para o cólon. Além disso, esses pacientes têm um risco de deficiência de vitaminas hidrossolúveis e lipossolúveis.
Sempre que possível, deve-se realizar uma reanastomose primária do intestino delgado com o cólon em todos os pacientes. Isso permite que o intestino se beneficie das habilidades do cólon durante a adaptação e aumente muito as chances do paciente de desmame da NP.
Os pacientes requerem suporte com NP total pelos primeiros 7 a 10 dias após a cirurgia, após os quais deve-se iniciar suporte com NP parcial em combinação com dieta oral. Os pacientes com intestino delgado residual >100 cm (ou >150 cm se o cólon for parcialmente removido) podem ser transferidos para a dieta oral com relativa rapidez, enquanto aqueles com intestino delgado residual ≤100 cm (ou ≤150 cm, se o cólon for parcialmente removido) podem precisar de NP por mais tempo.
Todos os pacientes necessitam de monitoramento de eletrólitos/micronutrientes e reposição com reidratação oral.[2] Caso haja hipersecreção de ácido gástrico e diarreia, elas devem ser controladas.[2][4]
Os pacientes devem ser encorajados a consumir uma dieta rica em carboidratos complexos, amidos e fibras solúveis, que podem ser sintetizados no cólon em ácidos graxos de cadeia curta, fornecendo uma fonte extra de energia.[27] A criação de uma anastomose colônica traz ao paciente um risco de nefrolitíase de oxalato; por isso, os pacientes devem ser instruídos a iniciarem uma dieta baixa em oxalato.[4]
Nutrição parenteral
Terapia com NP
A decisão de iniciar a NP é orientada inicialmente pela extensão e anatomia da ressecção intestinal e revisada de acordo com a resposta clínica. A maioria dos pacientes apresenta ressecções intestinais extensas, e não limitadas, e irão precisar inicialmente de NP.
A nutrição necessária é dada em um período de 24 horas, com esforços para infundir os requisitos nutricionais diários em um período curto, para que o paciente possa ficar livre da bomba de infusão por um período do dia (chamado ciclagem). O objetivo é fazer a transição do paciente para um cronograma de alimentação noturno de 10 a 12 horas, para que o estímulo hipotalâmico da fome possa ser preservado durante o dia. Ao final do período de alimentação, a NP deve ser diminuída em 30 a 60 minutos, para evitar hipoglicemia.
As instruções de segurança do cateter são essenciais para a prevenção de complicações, como a sepse associada ao cateter e a trombose venosa.
Desmame da NP
Isso é determinado pela taxa de adaptação intestinal e pode levar até 2 anos. Em alguns casos, entretanto, pode demorar mais. Há poucos dados disponíveis para confirmar o período de adaptação maior e mais completo ou máximo.
Atinge-se o desmame aumentando gradativamente a ingestão oral em alimentações pequenas e frequentes, conforme tolerado. Isso é acompanhado de: ajuste correspondente da frequência e do conteúdo da NP; monitoramento dos estados hídrico e nutricional; controle da diarreia; e uso de soluções de reidratação oral. Os pacientes devem ter como objetivo o consumo de 2 a 3 vezes sua ingestão calórica normal durante o desmame. Assim que o desmame for completado com êxito, deve-se continuar com a ingestão calórica elevada com reidratação oral e alterações alimentares.
Dependência de NP e falha da NP
Dependência da NP
Os pacientes com insuficiência intestinal verdadeira apresentarão recorrência de perda de peso, depleção de volume, desequilíbrio eletrolítico ou desnutrição toda vez que se tentar uma redução da NP. Esses pacientes são dependentes de NP e necessitam de NP de longa duração. A função hepática deve ser monitorada para prevenir e detectar a insuficiência hepática, uma complicação conhecida da insuficiência intestinal de longa duração.[2]
A teduglutida, um análogo humano do peptídeo semelhante ao glucagon 2 (GLP-2) administrado por via subcutânea, mostrou melhorar a absorção intestinal e reduzir a necessidade de NP em pacientes dependentes de NP com SIC.[28][29] Pode-se tentar o desmame após 4 semanas de tratamento com teduglutida. Se o desmame for bem-sucedido será necessário tratamento contínuo por toda a vida. No entanto, há incertezas quanto à dosagem de manutenção ideal. Há risco de aceleração do crescimento neoplásico com a teduglutida. A neoplasia do intestino delgado foi constatada em estudos com animais, e há risco teórico de câncer colorretal em seres humanos.[30] Portanto, pacientes com cólon intacto precisam de fazer uma colonoscopia antes de iniciar o tratamento e, depois disso, em intervalos regulares durante o tratamento (pelo menos, a cada 5 anos). Deve-se descontinuar o tratamento em pacientes com malignidade gastrointestinal, tendo cautela em pacientes com malignidade não gastrointestinais.
Falha na NP
Considera-se que os pacientes não estão respondendo à terapia de NP caso apresentem um ou mais dos seguintes fatores:[2][15]
Insuficiência hepática iminente ou evidente devido à doença hepática associada à insuficiência intestinal (DHAII)
Pelo menos duas tromboses dos principais vasos venosos centrais
Sepse frequente associada ao acesso venoso central (>2 infecções bacterianas por ano ou 1 fungemia em toda a vida)
Depleção de volume grave frequente.
A composição da NP deve ser ajustada em pacientes que desenvolverem DHAII. Deve-se evitar o excesso de alimentação com dextrose (>40 kcal/kg/dia) e reduzir a administração de lipídios intravenosos para menos de 1 g/kg/dia, se possível.[2] No entanto, as emulsões lipídicas intravenosas a base de óleo de soja devem continuar fornecendo pelo menos 4% a 8% da energia total, a fim de evitar a deficiência de ácidos graxos essenciais. Isso geralmente requer uma redução geral da ingestão calórica, já que se deve evitar o excesso de alimentação. Emulsões lipídicas alternativas, contendo óleo de peixe ou uma combinação de óleo de peixe e de oliva, podem ser usadas como fonte de energia em pacientes com DHAII.[31][32]
Caso não haja melhora clínica após o ajuste da NP, ou se ocorrer falha da NP devida a tromboses recorrentes dos canais venosos centrais ou depleção de volume grave frequente, o paciente deve ser encaminhado para um centro de transplante intestinal para fazer um transplante de intestino delgado. O NHS da Inglaterra oferece serviços de transplante do intestino delgado para pacientes adultos e pediátricos em centros de transplante especializados. Esse serviço cobre a avaliação pré-transplante, o transplante, o manejo de complicações e um acompanhamento imediato e de longo prazo após o transplante.[33]
A ocorrência de sepse frequente associada ao acesso venoso central é um critério controverso para a falha da NP, e que não é amplamente aceito devido à alta incidência de infecção pós-transplante.[15] Além disso, casos de sepse relacionada ao cateter estão geralmente associados ao uso inadequado da técnica de cuidado com o cateter. A opinião do autor é a de que infecções frequentes do cateter são um fator de risco para a infecção pós-transplante, e que instruções mais claras sobre cuidados com o cateter, que incluam demonstração, podem ser uma opção mais adequada para o paciente que um transplante intestinal. O transplante intestinal fica reservado como opção final, devido ao risco associado de alta morbidade e mortalidade. Os pacientes com doença hepática em estágio terminal precisarão de transplante combinado de intestino e de fígado. Idealmente, o transplante precoce isolado de intestino delgado evita a necessidade de transplante de fígado/intestino. Em razão de considerações anatômicas, o transplante multivisceral é raramente necessário.
Cirurgia de alongamento/estreitamento intestinal em caso de dependência de NP
Pacientes dependentes de NP, com segmentos intestinais dilatados, podem submeter-se ao procedimento cirúrgico de alongamento/estreitamento intestinal, como o procedimento de Bianchi ou o procedimento de enteroplastia transversa seriada (STEP), que pode auxiliar na adaptação intestinal e no desmame da NP.
O procedimento de Bianchi usa um segmento imóvel do intestino delgado, realiza uma transecção do segmento e reconecta as metades pelas extremidades, dobrando, assim, o comprimento do intestino e ajudando na motilidade. Os critérios de inclusão incluem: diâmetro intestinal >3 cm; comprimento do intestino delgado residual >40 cm com ≥20 cm de intestino delgado dilatado; dependência de NP; e ausência de doença hepática, doença de Crohn e enterite por radiação. Em um estudo, 14 de 16 crianças obtiveram êxito no desmame da NP com este procedimento; ocorreram estenoses anastomóticas, uma importante complicação, em aproximadamente 10% dos pacientes.[15][34][35]
O procedimento STEP envolve a aplicação de grampos lineares ao longo do intestino delgado em direções alternadas e opostas, a fim de dividir de forma incompleta o intestino dilatado. Isso tem o mesmo efeito do procedimento de Bianchi, mas com a vantagem de evitar a formação de estenoses pós-operatórias.[36]
Não há nenhum ensaio clínico randomizado e controlado que tenha comparado o procedimento de Bianchi com a STEP; logo, não se sabe ao certo qual procedimento é superior, embora a STEP seja tecnicamente menos desafiadora para os cirurgiões.
Pacientes com SIC e dilatação de segmentos não funcionais do intestino podem apresentar supercrescimento bacteriano no intestino. Se persistente, é preciso tratá-lo antes da realização desses procedimentos.
Ingestão oral
Hidratação
Quando os pacientes ficarem com sede, eles devem ser incentivados a tomar uma solução de reidratação oral (SRO) em vez de água, suco ou bebidas esportivas.[16][37][38] A SRO foi desenvolvida pela Organização Mundial de Saúde (OMS) e é composta de 2.5 g NaCl, 1.5 g KCl, 2.5 g de bicarbonato de sódio e 1.5 g de sacarose em 1 litro de água. Essa composição se beneficia do mecanismo de cotransporte de sódio e glicose do intestino para maximizar a absorção de água. Estão disponíveis preparações comerciais em pó ou prontas para uso. O débito urinário deve ser mantido em um mínimo de 1000 mL em 24 horas.
Pode ser preciso preparar uma SRO formulada especificamente para atender às necessidades de determinados pacientes, de acordo com os protocolos locais: por exemplo, uma solução sem potássio para um paciente com hipercalemia ou com risco de desenvolvê-la.
Instruções alimentares
Os pacientes devem ser encorajados a comer 2 a 3 vezes a quantidade de calorias consumidas antes de adquirir a SIC. Isso pode produzir mais diarreia, mas ajuda na adaptação do intestino e no desmame da NP.
Alimentos contendo lactose são uma rica fonte de cálcio e devem ser estimulados, a menos que o paciente seja intolerante à lactose, ou caso tenha sido submetido a uma ressecção jejunal maciça.[39]
Pacientes com ressecção ileal têm má absorção de gordura e de sais biliares, bem como deficiência de magnésio, vitamina B12 e cálcio. A deficiência de vitaminas lipossolúveis (A, D, E, K) pode também se desenvolver em consequência da má absorção de gordura. Embora a gordura seja um micronutriente com alta concentração de energia, ela pode causar diarreia em pacientes com cólon em continuidade. Os triglicerídeos de cadeia média (TCM) podem ser suplementados como fonte de gordura pois são absorvidos diretamente na circulação portal, sem a necessidade de ligação com sais biliares do estômago, intestino delgado e cólon; no entanto, eles têm um gosto ruim e um baixo ponto de fumaça ao serem utilizados na culinária. Os TCM não fornecem ácidos graxos essenciais.
Um pequeno corpo de evidências mostrou que as fórmulas enterais baseadas em peptídeos não são superiores a outras fórmulas, e não devem, por isso, ser prescritas em rotina.[40][41]
Prescrição de medicamentos orais
Não se pode prever como os medicamentos orais serão absorvidos em cada paciente, e deve-se buscar alternativas para a dosagem oral.
São preferíveis medicamentos sublinguais.
Geralmente, deve-se evitar as formulações intravenosas, se possível, já que o acesso frequente do cateter pode predispor a infecções.
Sempre que possível, deve-se realizar o monitoramento da concentração sérica de medicamentos a fim de garantir que a dose não será tóxica ou subterapêutica.[38]
Manejo da perda de fluidos
Os pacientes com SIC têm duas fontes principais de perda de fluido. A primeira é a hipersecreção de ácido gástrico estimulado por hipergastrinemia. A segunda é diarreia, que é multifatorial.
Redução de ácido: é necessário administrar um inibidor da bomba de prótons (IBP), como omeprazol ou lansoprazol, nos 6 primeiros meses, a fim de reduzir a hipersecreção gástrica compensatória temporária que ocorre após uma cirurgia gastrointestinal extensa.[2][4][42][43][44][45][46] Cirurgias menos extensas, como ressecções segmentais pequenas para doença de Crohn, podem não causar hipersecreção gástrica, e a terapia de inibidor da bomba de prótons (IBP) não é necessária nesses casos. Pode-se usar a concentração de gastrina sérica para orientar a necessidade da terapia com IBP. Os IBPs podem induzir diarreia em alguns pacientes, por isso é importante monitorar os volumes de diarreia antes e depois do início do tratamento com IBP.
Controle da diarreia: a loperamida e o difenoxilato/atropina são agentes de primeira linha para o manejo da diarreia.[16] Os opioides, como a codeína ou a tintura de ópio, são de segunda linha.[2] As alternativas de terceira linha incluem os medicamentos de ligação do ácido biliar colestiramina e colestipol, que ajudam a prevenir a diarreia causada por ácidos biliares não absorvidos, mas podem aumentar a má absorção de medicamentos e de vitaminas lipossolúveis e aumentar a diarreia. A octreotida pode controlar a diarreia desacelerando o trânsito intestinal e aumentando a absorção de água e de sódio, mas pode induzir a colelitíase e inibir a adaptação intestinal, prolongando o tempo necessário de NP.[47][48] A clonidina pode reduzir o volume de diarreia em pacientes com cólon residual em continuidade devido a seus efeitos na absorção de cloreto, mas pode produzir efeitos colaterais significativos de hipotensão e efeitos centrais, como torpor.[49]
Monitoramento e reposição de eletrólitos/micronutrientes
Todos os pacientes requerem monitoramento e reposição de eletrólitos/micronutrientes.
A suplementação de cálcio é recomendada para todos os pacientes. A deficiência de potássio, bicarbonato, fósforo e quaisquer vitaminas ou nutrientes deve ser suplementada conforme necessário. Deve-se tomar cuidado com suplementos de magnésio oral, já que eles podem induzir diarreia e piorar a absorção. O gluconato de magnésio pode causar menos diarreia que os sais de óxido, sulfato ou citrato. O manejo da má absorção de vitamina B12 e gordura é requerido por toda a vida em pacientes com ressecção ileal terminal superior a 60 cm, já que a adaptação intestinal não consegue compensar as funções exclusivas do íleo terminal.
É preciso verificar frequentemente os níveis durante a suplementação, já que a absorção é diferente para cada paciente.[Figure caption and citation for the preceding image starts]: Manejo da síndrome do intestino curto. TCM, triglicerídeos de cadeia média; IBP, inibidor da bomba de prótons; NP, nutrição parenteralAdaptado de Buchman AL, et al. Gastroenterology. 2003;124:1111-1134; usado com permissão. [Citation ends].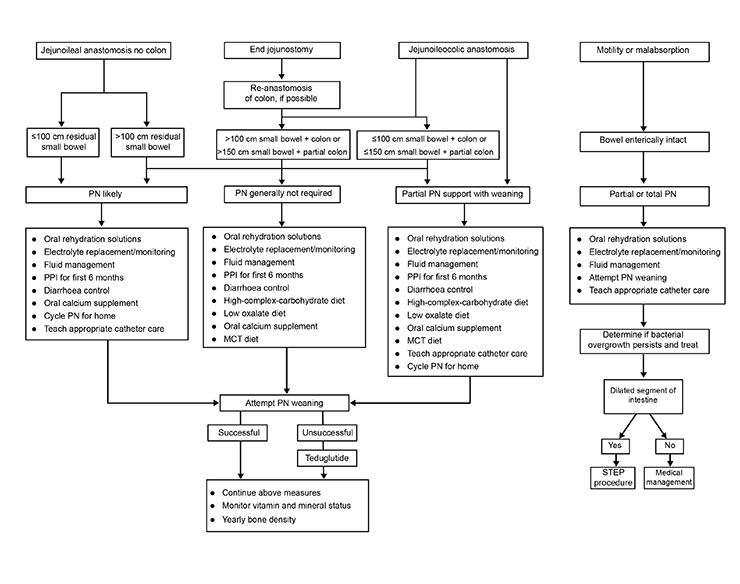
O uso deste conteúdo está sujeito ao nosso aviso legal