Etiologia
Geralmente, os distúrbios alimentares têm etiologia multifatorial. O possíveis fatores contribuintes são indicados a seguir.
Transtornos neurológicos, neuromusculares e do neurodesenvolvimento: encefalopatia hipóxica isquêmica, paralisia cerebral, atrofia muscular espinhal, distrofia miotônica congênita, miastenia grave e distrofias musculares). Lactentes com atraso no desenvolvimento são pelo menos duas vezes mais propensos a apresentarem dificuldades alimentares do que crianças com desenvolvimento normal. Até 80% das crianças com distúrbios alimentares complexos apresentam atraso no desenvolvimento.[4][7]
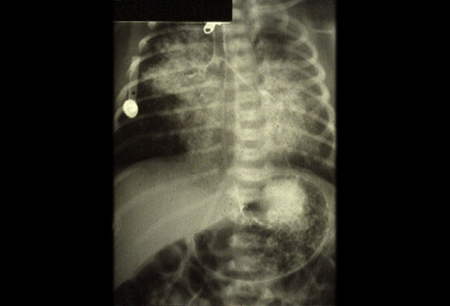
Anomalias anatômicas: fenda labial/palatina, anquiloglossia, fístula traqueoesofágica, gastrosquise (fissura congênita da parede abdominal) e estenose/atresia esofágica. As anormalidades estruturais foram responsáveis por 60% dos encaminhamentos para uma grande equipe norte-americana especializada em alimentação pediátrica.[4][Figure caption and citation for the preceding image starts]: Fístula traqueoesofágica tipo H. Radiografia torácica/tubograma demonstrando dispersão do corante radiopaco no campo pulmonar quando injetado na sonda nasogástrica posicionada no esôfago. Corante também observado no estômagoDo acervo da Dra. Stephanie Gill [Citation ends].
 [Figure caption and citation for the preceding image starts]: Manejo imediato da gastrosquise (fissura congênita da parede abdominal): alça intestinal contida em uma bolsa de silo pré-formada. Apesar da correção cirúrgica precoce, estes bebês apresentam um risco elevado de alteração da motilidade e de problemas alimentaresDo acervo da Dra. Stephanie Gill [Citation ends].
[Figure caption and citation for the preceding image starts]: Manejo imediato da gastrosquise (fissura congênita da parede abdominal): alça intestinal contida em uma bolsa de silo pré-formada. Apesar da correção cirúrgica precoce, estes bebês apresentam um risco elevado de alteração da motilidade e de problemas alimentaresDo acervo da Dra. Stephanie Gill [Citation ends].
Problemas cirúrgicos: formação de estoma, síndrome do intestino curto e hérnia de hiato. Podem ocorrer distúrbios alimentares após a cirurgia: por exemplo, alteração da motilidade esofágica após reparo de atresia esofágica ou gastrosquise, ou síndrome do intestino curto após ressecção do intestino para enterocolite necrosante grave.[10][11][12]
Distúrbios gastrointestinais:
Doença do refluxo gastroesofágico (DRGE): foram relatados sintomas de DRGE em 25.5% dos lactentes com 1 mês de idade, caindo para 2.9% aos 6 meses.[13] A incidência é ainda maior em lactentes prematuros, principalmente se houver presença de sonda de alimentação.[14][15]
Cólica: relatada em 5% a 19% dos lactentes nos primeiros meses de vida.[16]
Alergia à proteína do leite de vaca: afeta aproximadamente 2% dos lactentes.[17][18]
Doença celíaca: tem prevalência geral de aproximadamente 1%.[19] Os sintomas se desenvolvem após a introdução do glúten na dieta durante o desmame.
Intolerância à lactose: a intolerância à lactose primária raramente causa sintomas antes dos 5 anos de idade, embora os níveis de lactase diminuam logo após o desmame. Os lactentes prematuros têm atividade de lactase muito mais baixa que os lactentes nascidos a termo, o que pode causar uma intolerância à lactose transitória. A deficiência de lactase congênita é rara. A intolerância à lactose secundária pode ser causada por gastroenterite viral, giardíase, alergia à proteína do leite de vaca, doença celíaca ou doença de Crohn.[20]
Esofagite eosinofílica: os dados sobre a incidência são escassos, mas essa doença é relatada em lactentes.
Afecções genéticas (incluindo síndrome de Down e sequência de Pierre Robin): responsáveis por 9% dos pacientes encaminhados para uma equipe europeia de especialistas em alimentação.[3]
Cardiopatia congênita: os lactentes com cardiopatia congênita passam por hospitalização prolongada com intubação, início tardio da alimentação enteral e maior incidência de DRGE que, em conjunto, podem comprometer a aquisição e o desenvolvimento de habilidades alimentares.[1] Os lactentes submetidos a cirurgia cardíaca, principalmente para reparos em um único ventrículo, apresentam aumento do risco de enterocolite necrosante e disfunção alimentar subsequente, incluindo manipulação dos alimentos, sufocamento e vômitos, comportamento agressivo durante as refeições e aversão à alimentação.[21][22] Em um estudo retrospectivo realizado com lactentes submetidos a cirurgias cardíacas no período neonatal, 22% apresentaram distúrbios alimentares, definidos como ingestão inadequada para a idade, retardo do crescimento pôndero-estatural e necessidade de alimentação nasogástrica.[23]
Displasia broncopulmonar (doença pulmonar crônica da prematuridade): interrompe a capacidade do lactente de coordenar os estágios de sucção/deglutição/respiração da alimentação.[2] Os lactentes se cansam facilmente durante a alimentação e realizam a sucção com menos eficiência.[24]
Prematuridade e restrição do crescimento intrauterino: um terço dos pacientes encaminhados com distúrbios alimentares nasceu com <37 semanas de gestação.[3] Os lactentes prematuros apresentam comprometimento da coordenação de sucção, deglutição e respiração; trânsito intestinal lento; atividade de lactase reduzida; aumento do risco de DRGE; e aumento do risco de cirurgia (por exemplo, formação de estoma ou ressecção intestinal para enterocolite necrosante). A prematuridade aumenta a probabilidade de manipulação clínica da orofaringe (ventilação com colocação de tubo endotraqueal, sondas alimentares, sucção orofaríngea), que provavelmente aumenta a aversão sensorial e causa dificuldades alimentares comportamentais.[3] Lactentes encaminhados para centros de atenção terciária para manejo de distúrbios alimentares apresentam um peso ao nascer significativamente mais baixo para sua idade gestacional, implicando que problemas alimentares estão associados à restrição do crescimento intrauterino.[3]
Fatores psicossociais: uma equipe norte-americana especializada em alimentação relatou que 80% das crianças observadas apresentavam problemas alimentares complicados por questões comportamentais.[4] A resposta aprendida do lactente à alimentação e as ações subsequentes do cuidador podem ter impacto considerável nos distúrbios alimentares.
Fisiopatologia
O trânsito efetivo de líquido da cavidade oral ao estômago requer que o lactente coordene a sucção, a deglutição e a respiração. O lactente deve posicionar a língua e a mandíbula ao redor do mamilo ou mama e realizar a sucção para extrair o líquido para sua boca. A presença de líquido na faringe indica deglutição. Pausas para respiração durante cada deglutição para prevenir a aspiração dos conteúdos faríngeos.
A coordenação desse processo é comprometida pela prematuridade, por condições neurológicas e neuromusculares, por transtornos do neurodesenvolvimento, por anormalidades anatômicas da orofaringe ou do esôfago e por doenças cardíacas e respiratórias que aumentam o esforço de respiração. Os lactentes prematuros são neurologicamente imaturos e, geralmente, não conseguem coordenar a sequência sucção-deglutição- respiração antes de 34 semanas de idade gestacional corrigida.[25] Problemas neurológicos, neuromusculares e do neurodesenvolvimento podem causar má coordenação da sequência sucção, deglutição e respiração. Isso pode causar aumento do tempo gasto na alimentação (com impacto sobre a saciedade, a digestão e a fome), aumentar o risco de aspiração e comprometer o desenvolvimento das capacidades oromotoras necessárias para uma alimentação independente.[3][8][25] Problemas anatômicos como micrognatia, fenda labial e fenda palatina comprometem a anatomia craniofacial normal, deixando o lactente incapaz de sugar efetivamente. Uma frequência respiratória elevada e um maior trabalho de respiração em repouso prejudicam a capacidade de alimentação.[8] Esses lactentes se cansam com facilidade durante a alimentação. Má coordenação, sucção fraca e sucção curta são descritas nos lactentes com displasia broncopulmonar grave.[24]
O movimento dos alimentos e líquidos da faringe ao estômago requer peristaltismo esofágico efetivo e relaxamento transitório do esfíncter esofágico inferior. A alteração da motilidade esofágica está associada a múltiplas causas de distúrbios alimentares em lactentes, incluindo afecções neurológicas e neuromusculares, atraso no desenvolvimento e gastrosquise.
Afecções gastrointestinais podem causar náuseas ou desconforto durante a alimentação, contribuindo para o desenvolvimento de distúrbios alimentares.
Em muitos casos, a causa do distúrbio alimentar é multifatorial. Por exemplo, lactentes prematuros têm dificuldade com a coordenação neurológica da deglutição e têm um trato digestivo imaturo, com atividade de lactase reduzida, o que diminui a absorção de nutrientes dos alimentos.
Questões comportamentais como recusa alimentar foram vinculados à aversão oral atribuída a estímulos desagradáveis dos tubos orogástricos e tubos endotraqueais que passam pela boca.[3]
Classificação
Foi proposto um termo diagnóstico unificado de "distúrbios alimentares pediátricos", utilizando a estrutura de classificação internacional de funcionalidade, incapacidade e saúde da Organização Mundial da Saúde.[1] Essa classificação descreve o efeito de um distúrbio alimentar nas funcionalidades da criança, unificando capacidades clínicas, nutricionais e alimentares, e as questões psicossociais associadas ao distúrbio, justificando a avaliação da doença subjacente e das limitações funcionais para orientar sobre os planos de cuidados ideal.
Anteriormente, problemas clínicos, cirúrgicos e nutricionais que causam distúrbios alimentares tinham sido classificados como orgânicos, enquanto os problemas comportamentais e psicológicos tinham sido denominados de não orgânicos.[3] Entretanto, muitos autores criticam essa classificação como muito simplista. A maioria dos distúrbios alimentares é multifatorial por natureza, e os sintomas clínicos são semelhantes em ambos os grupos.[5][6] Além disso, essa classificação não auxilia o diagnóstico nem o manejo, pois muitos distúrbios exigirão o apoio de uma equipe multidisciplinar para o alcance de resultados ideais.
O uso deste conteúdo está sujeito ao nosso aviso legal