Abordaje
Se debe diagnosticar la preeclampsia en casos de hipertensión de inicio reciente y persistente con proteinuria después de la semana 20 de gestación.[1][2][16][53] La ausencia de hipertensión descarta el diagnóstico, aunque existen enfermedades relacionadas, tales como el síndrome HELLP, que pueden presentarse con y sin hipertensión. El síndrome HELLP es un subtipo de preeclampsia grave, caracterizado por hemólisis (H), enzimas hepáticas elevadas (EL) y plaquetas bajas (LP).[2][16] Sin embargo, la presencia de proteinuria ya no es obligatoria en el diagnóstico de la preeclampsia.[2] Se puede hacer un diagnóstico de preeclampsia en ausencia de proteinuria si la hipertensión se presenta con afectación sistémica materna, generalmente complicaciones hepáticas o hematológicas, o restricción del crecimiento fetal.[1][2]Después del diagnóstico, se debe realizar una evaluación fetal y pruebas maternas adicionales para evaluar la afectación sistémica.
Si existen signos y síntomas de preeclampsia grave o complicaciones, se requiere tratamiento inmediato. Una vez confirmado el diagnóstico, o si existen preocupaciones sobre la salud de la madre o del feto, la mujer debe ser ingresada en un centro de atención obstétrica para su tratamiento.[1][16]
Antecedentes
La preeclampsia suele aparecer en las mujeres embarazadas después de las 20 semanas de gestación.[1][16][54] Los factores de riesgo clave son la nuliparidad, los antecedentes maternos o familiares, el índice de masa corporal >30, la edad materna >40 años, el embarazo múltiple (gemelar), la subfertilidad, la hipertensión gestacional (hipertensión que se desarrolla después de las 20 semanas de gestación en ausencia de proteinuria y síntomas sistémicos), la diabetes preexistente, el síndrome de ovario poliquístico, la enfermedad autoinmunitaria, la enfermedad renal, la enfermedad cardiovascular preexistente y la hipertensión crónica.
La paciente puede ser asintomática y se le puede diagnosticar la enfermedad durante una consulta clínica de rutina, o bien puede presentar los siguientes síntomas agudos.
Cefalea: normalmente frontal; la presencia de este síntoma clasifica la preeclampsia como grave.[1] Se produce en aproximadamente el 40% de las pacientes con enfermedad grave y es uno de los pocos síntomas que pronostican un mayor riesgo de eclampsia.[8]
Dolor abdominal superior: por lo general, dolor en el cuadrante superior derecho; se produce en, aproximadamente, el 16% de las pacientes con enfermedad grave y es un síntoma clínico del síndrome HELLP.[8]
Alteraciones visuales: la fotopsia (luces intermitentes percibidas en los campos visuales), los escotomas y el vasoespasmo retiniano son relativamente infrecuentes, pero pronostican un mayor riesgo de eclampsia. La ceguera cortical debe alertar al médico en cuanto a la posibilidad de edema cerebral subyacente.
Dificultad respiratoria: se debe a edema pulmonar y puede complicar la preeclampsia. Si se produce tras el parto, es una de las causas principales de mortalidad materna.
Convulsiones: requiere el ingreso de la paciente en una unidad de cuidados intensivos para su estabilización y el parto.[1]
Oliguria: puede estar asociada con un aumento de edema. Las mujeres corren un mayor riesgo después del parto, cuando es más probable que se produzca un edema pulmonar.
Si se presentan estos síntomas, además de hipertensión con o sin proteinuria, la preeclampsia se clasifica como grave.[1] Si los movimientos fetales son reducidos, es necesario realizar una evaluación del bienestar fetal de inmediato.
[  ]
]
Exploración física
La hipertensión (definida como presión arterial sistólica [PA] ≥140 mmHg y/o PA diastólica ≥90 mmHg) en una mujer previamente normotensa es diagnóstica.[1][16][54] Deben realizarse al menos dos mediciones, con un intervalo mínimo de 4 horas.[1]
La presencia de edema es muy común, pero no excluyente, por lo que no se debe usar en el diagnóstico. La presencia de hiperreflexia y/o clonus es rara y de poco valor para la evaluación clínica. La fundoscopia rara vez es anormal, pero si lo es, implica hipertensión crónica subyacente.
Si el útero es pequeño para la fecha, implica que el volumen del líquido amniótico es reducido, lo cual puede indicar retraso del crecimiento y requerir una evaluación fetal por ecografía.
[  ]
Retraso de crecimiento fetal: en aproximadamente un 30% de las mujeres, se observa retraso del crecimiento fetal.[8]
]
Retraso de crecimiento fetal: en aproximadamente un 30% de las mujeres, se observa retraso del crecimiento fetal.[8]
Análisis de orina
La prueba de la tira reactiva puede usarse para detectar la presencia de proteínas en la orina. La prueba de la tira reactiva con lectores automatizados es más precisa que el análisis visual.
La proteinuria asociada con una presión sanguínea elevada en el rango de la preeclampsia requiere la derivación a una unidad especializada o el ingreso hospitalario para su evaluación. Ante la ausencia de proteinuria o de signos sistémicos de preeclampsia, se debe buscar un diagnóstico alternativo.
La proteína urinaria puede estimarse en una recogida de orina de 24 horas, considerándose un nivel diagnóstico la excreción urinaria de ≥300 mg de proteína/24 horas.[1][2][34]
Sin embargo, completar una recogida de orina de 24 horas es incómodo para las mujeres y el National Institute for Health and Care Excellence (NICE) del Reino Unido recomienda no utilizar de forma rutinaria la recogida de orina de 24 horas para cuantificar la proteinuria en las mujeres embarazadas.[16] Si está disponible, se prefiere una prueba puntual alternativa, como la relación proteína:creatinina (RPC, para la cual un resultado de ≥30 mg/mmol es diagnóstico).[1][16][34][54] Si la medición de la proteinuria está por encima del umbral de diagnóstico pero sigue habiendo duda diagnóstica, considere la posibilidad de volver a realizar la prueba en una nueva muestra, además de la revisión clínica.
Debido a que el nivel de proteinuria no se correlaciona con el resultado, no hay beneficio en repetir rutinariamente el análisis de orina una vez que se ha realizado un diagnóstico.[16]
Evaluación fetal
Se requiere una evaluación inmediata mediante una ecografía fetal si se reducen los movimientos fetales o se sospecha una restricción del crecimiento fetal.
[  ]
La biometría fetal se debe usar para diagnosticar o descartar el retraso del crecimiento fetal, aunque el crecimiento solo se puede evaluar por completo mediante exploraciones realizadas con 2 semanas de diferencia.
]
La biometría fetal se debe usar para diagnosticar o descartar el retraso del crecimiento fetal, aunque el crecimiento solo se puede evaluar por completo mediante exploraciones realizadas con 2 semanas de diferencia.
En todas las mujeres deben utilizarse inicialmente otros métodos de evaluación fetal mediante las siguientes pruebas:[1][16][54]
La velocimetría Doppler de la arteria umbilical es la principal herramienta de evaluación. Reduce la mortalidad perinatal y respalda la toma de mejores decisiones, lo cual conduce a decisiones más adecuadas sobre el parto. Se debe llevar a cabo en el ingreso hospitalario y, si este es normal, se debe repetir dos veces a la semana. En caso de ser anormal, se puede requerir una monitorización más intensa por otros medios, entre ellos la evaluación Doppler de otros vasos sanguíneos fetales y la cardiotocografía fetal. [
 ]
Puede ser necesario provocar el parto en pocos días.[Figure caption and citation for the preceding image starts]: Velocimetría Doppler de la arteria umbilical: (1) patrón normal; (2) flujo telediastólico reducido; (3) flujo telediastólico ausente; (4) flujo telediastólico reversoDe la colección personal del Dr. James J. Walker; usado con autorización [Citation ends].
]
Puede ser necesario provocar el parto en pocos días.[Figure caption and citation for the preceding image starts]: Velocimetría Doppler de la arteria umbilical: (1) patrón normal; (2) flujo telediastólico reducido; (3) flujo telediastólico ausente; (4) flujo telediastólico reversoDe la colección personal del Dr. James J. Walker; usado con autorización [Citation ends].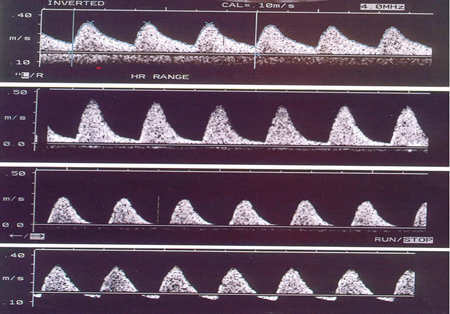
La cardiotocografía fetal se recomienda para evaluar el bienestar del feto, pero tiene poco valor pronóstico. Se debe realizar inicialmente y luego no más de dos veces a la semana, a menos que haya motivo de preocupación, como sangrado vaginal, movimientos fetales reducidos o mayor gravedad de la enfermedad. [
 ]
]
La evaluación del líquido amniótico, preferiblemente del bolsillo vertical único más profundo en lugar del índice amniótico. Se combina fácilmente con la velocimetría Doppler de la arteria umbilical.
Otras pruebas diagnósticas maternas
El hemograma completo, la creatinina sérica y las pruebas de función hepática (PFH) son indicadores útiles del avance de la enfermedad, por lo que se recomiendan para todas las pacientes después del análisis de orina y de la evaluación fetal inicial.
El aumento de la creatinina sérica implica enfermedad renal subyacente. Aunque el ácido úrico sérico elevado se asocia a la preeclampsia grave, no ofrece un valor diagnóstico adicional. La disminución de los niveles de plaquetas y el aumento de los niveles de transaminasas son parcialmente diagnósticos para el síndrome HELLP. El recuento de plaquetas es el criterio principal que se usa para clasificar la gravedad del síndrome HELLP. Si el recuento de plaquetas es <100,000/microlitro, debe realizarse un examen completo de coagulación y pruebas de función hepática (PFH): Si el recuento de plaquetas es ≥100,000/microlitro, no suelen recomendarse más pruebas de coagulación.
La prueba del factor de crecimiento placentario (PlGF, por sus siglas en inglés) ayuda a evaluar el riesgo de preeclampsia y a planificar un parto temprano y seguro, si está indicado. La prueba también ayuda a identificar a las mujeres que no están en riesgo de preeclampsia, lo que reduce el monitoreo innecesario y las asistencias hospitalarias. Por lo tanto, las pruebas permiten a los equipos clínicos orientar los recursos para mantener a estas mujeres bajo un seguimiento adecuado. El NICE aboga por el uso de la prueba PlGF en una ocasión para ayudar a decidir sobre la atención (para ayudar a descartar o descartar la preeclampsia) si existe una sospecha de preeclampsia en mujeres que se presentan entre las semanas 20 y las 34 semanas más 6 días de gestación.[16][55][56] Un resultado bajo de la prueba de PlGF (<100 pg/mL) no siempre significa que una mujer tenga preeclampsia, ya que el resultado puede estar asociado con otras afecciones que afectan a la placenta. Sin embargo, los resultados de las pruebas basadas en PlGF son útiles para la toma de decisiones junto con el juicio clínico, especialmente para las mujeres que tenían hipertensión o proteinuria antes de quedar embarazadas y aquellas con mayor riesgo de resultados adversos graves del embarazo (p. ej., mujeres de origen familiar africano, caribeño o asiático). Un ensayo controlado aleatorizado por conglomerados (el estudio PARROT) informó que el tiempo transcurrido hasta el diagnóstico fue más rápido y con una menor incidencia de resultados adversos maternos graves en las unidades de maternidad en las que se disponía de los resultados de los PIGF, en comparación con las unidades en las que los resultados de los PIGF estaban ocultos (control).[57] La mediana de tiempo hasta el diagnóstico de preeclampsia fue de 4.1 días con pruebas ocultas frente a 1.9 días con pruebas reveladas (relación de tiempo 0.36; intervalo de confianza [IC] del 95%: 0.15 a 0.87; P=0.027). Se notificaron resultados adversos graves para la madre en 24 (5%) de 447 mujeres en el grupo de prueba oculta frente a 22 (4%) de 573 mujeres en el grupo de prueba revelada (odds-ratio ajustado 0.32; IC del 95%: 0.11 a 0.96; P = 0.043). Los resultados perinatales no se vieron afectados.[57] El NICE también recomienda la relación tirosina quinasa 1 similar al fms soluble (sFlt-1) en suero materno a PlGF como alternativa a las pruebas de PlGF solamente, aunque sigue siendo primordial la necesidad de realizar la entrevista clínica y una exploración física.[55] El ensayo clínico prospectivo, intervencionista, de grupos paralelos y aleatorizado INSPIRE encontró que el uso de la relación sFlt-1/PlGF en mujeres que presentaban sospecha de preeclampsia mejoró significativamente la precisión clínica sin afectar la tasa de ingreso hospitalario.[58] El número de ingresos no fue significativamente diferente entre los grupos. Sin embargo, el grupo de revelación (resultado de sFlt-1/PlGF conocido por los médicos) admitió al 100% de las mujeres que desarrollaron preeclampsia dentro de los 7 días posteriores a la prueba, mientras que el grupo de no revelación (resultado desconocido) admitió al 83% de las mujeres (p = 0.038). El uso de la relación sFlt-1/PlGF produjo una sensibilidad del 100% (IC del 95%: 85.8 a 100) y un valor predictivo negativo del 100% (IC del 95%: 97.1 a 100) en comparación con una sensibilidad del 83.3% (IC del 95%: 58.6 a 96.4) y un valor predictivo negativo del 97.8% (IC del 95%: 93.7 a 99.5) con la práctica clínica sola. Un análisis estratificado de los datos de PARROT también mostró que una mayor proporción de mujeres con un resultado muy bajo de la prueba de PlGF (<12 pg/mL) recibieron corticosteroides prenatales: 38.6% en el grupo de prueba revelado en comparación con 15.8% en el grupo de prueba oculta.[59] Esto puede ser clínicamente útil para reducir la tasa de síndrome de dificultad respiratoria y hemorragia intraventricular en recién nacidos prematuros. Sin embargo, no está claro si estas pruebas diagnósticas suponen algún beneficio para los resultados perinatales. Aunque existía la preocupación de que las pruebas de PlGF condujeran a un aumento e innecesario de partos prematuros, la proporción de nacimientos antes de las 37 semanas de gestación en los grupos de prueba y control fue la misma en los ensayos PARROT e INSPIRE. El NICE recomienda no utilizar las pruebas basadas en PlGF para tomar decisiones sobre si se debe ofrecer un parto prematuro planificado en mujeres con preeclampsia prematura, que debe basarse en una evaluación clínica.[16][55]
Aunque la Administración de Medicamentos y Alimentos de EE. UU. (FDA) ha aprobado la prueba sFlt-1/PlGF para ayudar en la evaluación del riesgo de avance a preeclampsia con características graves, el American College of Obstetricians and Gynecologists no recomienda ninguna prueba de biomarcadores (por ejemplo, la prueba PlGF o la relación sFlt-1/PlGF) para la predicción de la preeclampsia, el diagnóstico o la exclusión de la preeclampsia con características graves o la determinación del enfoque de gestión después de un resultado positivo o negativo de la prueba.[1][60]
Cómo tomar una muestra de sangre venosa de la fosa antecubital utilizando una aguja de vacío.
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad