A pancreatite aguda tem duas fases distintas que necessitam de diferentes abordagens de manejo: a fase inicial (1 semana), caracterizada por síndrome da resposta inflamatória sistêmica (SRIS) e/ou falência de órgãos e a fase tardia (>1 semana), caracterizada por complicações locais, incluindo necrose pancreática estéril ou infectada e pseudocistos.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Na maioria dos pacientes, a doença é leve e melhora rapidamente em 3-7 dias com ressuscitação fluídica, controle da dor e das náuseas e alimentação oral precoce, enquanto cerca de 20% a 30% dos pacientes desenvolvem doença grave, com uma taxa de mortalidade hospitalar de cerca de 15%.[28]Leppäniemi A, Tolonen M, Tarasconi A, et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg. 2019 Jun 13;14:27.
https://wjes.biomedcentral.com/articles/10.1186/s13017-019-0247-0
http://www.ncbi.nlm.nih.gov/pubmed/31210778?tool=bestpractice.com
Manejo inicial
Todos os pacientes precisam ser tratados com hidratação intravenosa nas primeiras 24 horas e rigorosamente monitorados quanto a perdas iniciais de líquidos, choque hipovolêmico e sintomas sugestivos de falência orgânica nas primeiras 48-72 horas após a apresentação.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[70]de-Madaria E, Buxbaum JL, Maisonneuve P, et al. Aggressive or moderate fluid resuscitation in acute pancreatitis. N Engl J Med. 2022 Sep 15;387(11):989-1000.
http://www.ncbi.nlm.nih.gov/pubmed/36103415?tool=bestpractice.com
Recomenda-se uma taxa constante para a ressuscitação inicial, com um monitoramento rigoroso e adição de fluido em bolus apenas se houver evidências de hipovolemia.[70]de-Madaria E, Buxbaum JL, Maisonneuve P, et al. Aggressive or moderate fluid resuscitation in acute pancreatitis. N Engl J Med. 2022 Sep 15;387(11):989-1000.
http://www.ncbi.nlm.nih.gov/pubmed/36103415?tool=bestpractice.com
[71]Gardner TB. Fluid resuscitation in acute pancreatitis - going over the WATERFALL. N Engl J Med. 2022 Sep 15;387(11):1038-9. Os médicos devem reconhecer que os pacientes com pancreatite aguda podem desenvolver hipovolemia rapidamente após a internação e precisam de fluidos em bolus e/ou aumentos no índice de hidratação.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Antes, a reidratação precoce agressiva era recomendada para todos os pacientes com pancreatite aguda, mas agora há evidências que dão suporte a uma abordagem moderada com atenção especial aos sinais vitais, principalmente a frequência cardíaca, com avaliação da ureia e hematócritos a intervalos frequentes (até 6 horas após a apresentação e pelas 24-48 horas seguintes).[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[70]de-Madaria E, Buxbaum JL, Maisonneuve P, et al. Aggressive or moderate fluid resuscitation in acute pancreatitis. N Engl J Med. 2022 Sep 15;387(11):989-1000.
http://www.ncbi.nlm.nih.gov/pubmed/36103415?tool=bestpractice.com
[72]Li XW, Wang CH, Dai JW, et al. Comparison of clinical outcomes between aggressive and non-aggressive intravenous hydration for acute pancreatitis: a systematic review and meta-analysis. Crit Care. 2023 Mar 22;27(1):122.
https://www.doi.org/10.1186/s13054-023-04401-0
http://www.ncbi.nlm.nih.gov/pubmed/36949459?tool=bestpractice.com
Pode não ser possível predizer quais pacientes com pancreatite aguda desenvolverão doença grave: as ferramentas de escore da gravidade, como a APACHE II e a Glasgow, têm valor limitado no início da evolução da doença. Embora os testes laboratoriais iniciais do hematócrito e da função renal sejam importantes para determinar as perdas de fluido intravascular e a insuficiência renal precoce, nenhum exame laboratorial demonstrou ser consistentemente acurado na predição da gravidade posterior da doença.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[73]Baillie J, ed. Advances in endoscopy: current developments in diagnostic and therapeutic endoscopy. Gastroenterol Hepatol (N Y). 2010 Jan;6(1):16-8.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2886440
http://www.ncbi.nlm.nih.gov/pubmed/20567534?tool=bestpractice.com
Nenhum paciente deve ser classificado como tendo doença leve até pelo menos 48 horas após o início dos sintomas, pois alguns pacientes que desenvolvem doença grave se apresentam sem sinais de falência orgânica ou de complicações locais.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
É fundamental reconhecer a importância da falência orgânica na determinação da gravidade da doença.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Na presença de disfunção orgânica associada à SRIS, podem ser necessários monitoramento e suporte orgânico adicionais (por exemplo, suplementação de oxigênio e/ou suporte ventilatório para insuficiência respiratória). Podem estar presentes sinais de disfunção cardiovascular, respiratória ou renal. Pacientes com falência de órgãos e/ou SRIS persistente devem ser internados em uma unidade de terapia intensiva sempre que possível.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[28]Leppäniemi A, Tolonen M, Tarasconi A, et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg. 2019 Jun 13;14:27.
https://wjes.biomedcentral.com/articles/10.1186/s13017-019-0247-0
http://www.ncbi.nlm.nih.gov/pubmed/31210778?tool=bestpractice.com
A definição de SRIS é atendida pela presença de pelo menos dois dos seguintes critérios:[49]Levy MM, Fink MP, Marshall JC, et al. 2001 SCCM/ESICM/ACCP/ATS/SIS international sepsis definitions conference. Crit Care Med. 2003 Apr;31(4):1250-6.
http://www.ncbi.nlm.nih.gov/pubmed/12682500?tool=bestpractice.com
Frequência de pulso >90 batimentos por minuto
Frequência respiratória >20 por minuto ou pressão parcial de dióxido de carbono (PaCO₂) <32 mmHg
Temperatura >38 ºC ou <36 ºC
Contagem leucocitária >12,000 ou <4000 células/mm³, ou >10% de neutrófilos imaturos (bastonetes)
A presença de falência persistente (> 48 horas) de um único órgão ou de múltiplos órgãos define a pancreatite aguda como grave de acordo com os critérios de Atlanta revisados.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[28]Leppäniemi A, Tolonen M, Tarasconi A, et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg. 2019 Jun 13;14:27.
https://wjes.biomedcentral.com/articles/10.1186/s13017-019-0247-0
http://www.ncbi.nlm.nih.gov/pubmed/31210778?tool=bestpractice.com
Na prática clínica diária, os seguintes critérios (critérios originais de Atlanta) podem ser usados para se estabelecer a falência de órgãos:[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Choque: pressão arterial sistólica <90 mmHg
Insuficiência pulmonar: pressão parcial de oxigênio (PaO₂) ≤60%
Insuficiência renal: creatinina >176.8 micromoles/L (≥2 mg/dL)
Hemorragia digestiva: sangramento de >500 mL em 24 horas
Hidratação intravenosa precoce
O tratamento inicial da pancreatite aguda requer hidratação intravenosa precoce.[1]Nirula R. Chapter 9: Diseases of the pancreas. High yield surgery. Philadelphia, PA: Lippincott Williams & Wilkins; 2000.[5]Way LW, Doherty GM. Chapter 27: Pancreas. In: Current surgical diagnosis & treatment. 11th ed. New York, NY: McGraw-Hill; 2003.[70]de-Madaria E, Buxbaum JL, Maisonneuve P, et al. Aggressive or moderate fluid resuscitation in acute pancreatitis. N Engl J Med. 2022 Sep 15;387(11):989-1000.
http://www.ncbi.nlm.nih.gov/pubmed/36103415?tool=bestpractice.com
[74]Darvas K, Futo J, Okros I, et al. Principles of intensive care in severe acute pancreatitis in 2008 [in Hungarian]. Orv Hetil. 2008 Nov 23;149(47):2211-20.
http://www.ncbi.nlm.nih.gov/pubmed/19004743?tool=bestpractice.com
[75]Curtis CS, Kudsk KA. Nutrition support in pancreatitis. Surg Clin North Am. 2007 Dec;87(6):1403-15.
http://www.ncbi.nlm.nih.gov/pubmed/18053838?tool=bestpractice.com
[76]Thomson A. Nutritional support in acute pancreatitis. Curr Opin Clin Nutr Metab Care. 2008 May;11(3):261-6.
http://www.ncbi.nlm.nih.gov/pubmed/18403922?tool=bestpractice.com
[77]Marik PE. What is the best way to feed patients with pancreatitis? Curr Opin Crit Care. 2009 Apr;15(2):131-8.
http://www.ncbi.nlm.nih.gov/pubmed/19300086?tool=bestpractice.com
[78]Kumari R, Sadarat F, Luhana S, et al. Evaluating the efficacy of different volume resuscitation strategies in acute pancreatitis patients: a systematic review and meta-analysis. BMC Gastroenterol. 2024 Mar 25;24(1):119.
https://www.doi.org/10.1186/s12876-024-03205-y
http://www.ncbi.nlm.nih.gov/pubmed/38528470?tool=bestpractice.com
Os médicos devem se concentrar em uma taxa constante de ressuscitação inicial (não mais que 1.5 mL/kg/hora) e devem administrar um bolus de 10 mL/kg somente se houver sinais de hipovolemia.[71]Gardner TB. Fluid resuscitation in acute pancreatitis - going over the WATERFALL. N Engl J Med. 2022 Sep 15;387(11):1038-9. Os médicos devem se concentrar em uma taxa constante de ressuscitação inicial (não mais que 1.5 mL/kg/hora) e devem administrar um bolus de 10 mL/kg somente se houver sinais de hipovolemia inicial.[71]Gardner TB. Fluid resuscitation in acute pancreatitis - going over the WATERFALL. N Engl J Med. 2022 Sep 15;387(11):1038-9.
Um cristaloide balanceado (como Ringer lactato [solução de Hartmann] ou Plasma-Lyte®) pode ter benefícios em comparação com o soro fisiológico, e as diretrizes geralmente recomendam o uso de um cristaloide balanceado para os pacientes com pancreatite aguda.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[28]Leppäniemi A, Tolonen M, Tarasconi A, et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg. 2019 Jun 13;14:27.
https://wjes.biomedcentral.com/articles/10.1186/s13017-019-0247-0
http://www.ncbi.nlm.nih.gov/pubmed/31210778?tool=bestpractice.com
[46]Wu D, Wan J, Xia L, et al. The efficiency of aggressive hydration with lactated ringer solution for the prevention of post-ERCP pancreatitis: a systematic review and meta-analysis. J Clin Gastroenterol. 2017 Sep;51(8):e68-76.
http://www.ncbi.nlm.nih.gov/pubmed/28609383?tool=bestpractice.com
[47]Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidence-based guidelines for the management of acute pancreatitis. Pancreatology. 2013 Jul-Aug;13(4 Suppl 2):e1-15.
https://www.sciencedirect.com/science/article/pii/S1424390313005255?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/24054878?tool=bestpractice.com
[79]Choosakul S, Harinwan K, Chirapongsathorn S, et al. Comparison of normal saline versus lactated Ringer's solution for fluid resuscitation in patients with mild acute pancreatitis, a randomized controlled trial. Pancreatology. 2018 Jul;18(5):507-12.
http://www.ncbi.nlm.nih.gov/pubmed/29754857?tool=bestpractice.com
[80]Hong J, Li Q, Wang Y, et al. Comparison of fluid resuscitation with lactate ringer's versus normal saline in acute pancreatitis: an updated meta-analysis. Dig Dis Sci. 2024 Jan;69(1):262-74.
https://www.doi.org/10.1007/s10620-023-08187-7
http://www.ncbi.nlm.nih.gov/pubmed/38015322?tool=bestpractice.com
O soro fisiológico administrado em grandes volumes pode levar ao desenvolvimento de uma acidose metabólica hiperclorêmica sem anion gap.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Isso tem particular relevância na pancreatite aguda, onde o pH baixo pode desencadear a ativação prematura do tripsinogênio e exacerbar o sintoma de dor abdominal. No entanto, faltam evidências de alta qualidade sobre a escolha do fluido específico para os pacientes com pancreatite aguda, e os resultados de ensaios clínicos randomizados e controlados em pacientes criticamente enfermos em geral (não especificamente pessoas com pancreatite aguda) chegaram a conclusões conflitantes.[81]Semler MW, Self WH, Wanderer JP, et al. Balanced crystalloids versus saline in critically ill adults. N Engl J Med. 2018 Mar 1;378(9):829-39.
https://www.nejm.org/doi/10.1056/NEJMoa1711584
http://www.ncbi.nlm.nih.gov/pubmed/29485925?tool=bestpractice.com
[82]Zampieri FG, Machado FR, Biondi RS, et al. Effect of intravenous fluid treatment with a balanced solution vs 0.9% saline solution on mortality in critically ill patients: the BaSICS randomized clinical trial. JAMA. 2021 Aug 10;326(9):1-12.
https://jamanetwork.com/journals/jama/fullarticle/2783039
http://www.ncbi.nlm.nih.gov/pubmed/34375394?tool=bestpractice.com
[83]Finfer S, Micallef S, Hammond N, et al. Balanced multielectrolyte solution versus saline in critically ill adults. N Engl J Med. 2022 Jan 18 [Epub ahead of print].
http://www.ncbi.nlm.nih.gov/pubmed/35041780?tool=bestpractice.com
Um aumento de ureia e/ou hematócrito nas primeiras 24-48 horas indica uma reidratação inadequada e tem sido associado ao risco de desenvolvimento de falência orgânica e necrose pancreática. Uma hidratação intravenosa rápida suficiente para diminuir o hematócrito (ou seja, a hemodiluição) e/ou a ureia (ou seja, o aumento da perfusão renal) demonstrou diminuir a morbidade e a mortalidade.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[56]Brown A, Orav J, Banks PA. Hemoconcentration is an early marker for organ failure and necrotizing pancreatitis. Pancreas. 2000 May;20(4):367-72.
http://www.ncbi.nlm.nih.gov/pubmed/10824690?tool=bestpractice.com
[84]Crockett SD, Wani S, Gardner TB, et al. American Gastroenterological Association Institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018 Mar;154(4):1096-101. Estudos demonstraram que esses benefícios aparecem em 24 horas.[85]Buxbaum JL, Quezada M, Da B, et al. Early aggressive hydration hastens clinical improvement in mild acute pancreatitis. Am J Gastroenterol. 2017 May;112(5):797-803.
http://www.ncbi.nlm.nih.gov/pubmed/28266591?tool=bestpractice.com
[86]Fisher JM, Gardner TB. The "golden hours" of management in acute pancreatitis. Am J Gastroenterol. 2012 Aug;107(8):1146-50.
http://www.ncbi.nlm.nih.gov/pubmed/22858994?tool=bestpractice.com
A medição da ureia e do hematócrito em até 6-8 horas após a internação é, portanto, recomendada para que ajustes oportunos na taxa de hidratação possam ser realizados.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Por outro lado, a observação estrita de parâmetros clínicos como frequência cardíaca, pressão arterial e débito urinário, é necessária para prevenir o risco de hidratação intravenosa excessiva, particularmente em determinados grupos de pacientes como idosos e aqueles com história de doença cardíaca e/ou renal.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
A ressuscitação com grandes volumes pode agravar as perdas para o terceiro espaço características da pancreatite aguda, agravando o edema pulmonar e/ou causando síndrome compartimental abdominal.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Um ensaio clínico randomizado, controlado e multicêntrico publicado em 2022 mostrou que a hidratação precoce agressiva resultou em maior incidência de sobrecarga hídrica em comparação com a hidratação moderada, sem melhora nos desfechos clínicos.[70]de-Madaria E, Buxbaum JL, Maisonneuve P, et al. Aggressive or moderate fluid resuscitation in acute pancreatitis. N Engl J Med. 2022 Sep 15;387(11):989-1000.
http://www.ncbi.nlm.nih.gov/pubmed/36103415?tool=bestpractice.com
A justificativa para a hidratação precoce surge de múltiplos fatores que causam hipovolemia, incluindo vômitos, menor ingestão oral, “perda para o terceiro espaço” de líquidos, aumento das perdas respiratórias e sudorese. Uma combinação de efeitos microangiopáticos e edema no pâncreas inflamado pode impedir o fluxo sanguíneo, causando o aumento da morte celular, necrose tecidual e liberação contínua de enzimas pancreáticas, ativando ainda mais as cascatas inflamatórias. A inflamação aumenta a permeabilidade vascular, causando o aumento das perdas de líquido para o terceiro espaço e agravamento da hipoperfusão pancreática. A hipoperfusão do pâncreas causa necrose adicional. A ressuscitação fluídica intravenosa precoce fornece suporte micro e macrocirculatório para prevenir a necrose pancreática e reduzir o risco de outras complicações graves.[84]Crockett SD, Wani S, Gardner TB, et al. American Gastroenterological Association Institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018 Mar;154(4):1096-101.
Pancreatite biliar
Os pacientes com pancreatite biliar leve devem ser submetidos à colecistectomia durante a internação inicial, após a remissão dos sintomas agudos. A colecistectomia é tipicamente protelada para os pacientes com doença grave; esses pacientes necessitam da tomada de decisões complexas entre o cirurgião e o gastroenterologista.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[47]Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidence-based guidelines for the management of acute pancreatitis. Pancreatology. 2013 Jul-Aug;13(4 Suppl 2):e1-15.
https://www.sciencedirect.com/science/article/pii/S1424390313005255?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/24054878?tool=bestpractice.com
Os pacientes com pancreatite biliar complicada por colangite concomitante se beneficiam da colangiopancreatografia retrógrada endoscópica (CPRE) precoce. O benefício é observado nos pacientes com sepse e falência orgânica que se submetem ao procedimento nas primeiras 24 horas da internação.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[47]Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidence-based guidelines for the management of acute pancreatitis. Pancreatology. 2013 Jul-Aug;13(4 Suppl 2):e1-15.
https://www.sciencedirect.com/science/article/pii/S1424390313005255?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/24054878?tool=bestpractice.com
[87]van Dijk SM, Hallensleben NDL, van Santvoort HC, et al. Acute pancreatitis: recent advances through randomised trials. Gut. 2017 Nov;66(11):2024-32.
http://www.ncbi.nlm.nih.gov/pubmed/28838972?tool=bestpractice.com
[88]Moretti A, Papi C, Aratari A, et al. Is early endoscopic retrograde cholangiopancreatography useful in the management of acute biliary pancreatitis? A meta-analysis of randomized controlled trials. Dig Liver Dis. 2008 May;40(5):379-85.
http://www.ncbi.nlm.nih.gov/pubmed/18243826?tool=bestpractice.com
Embora os cálculos biliares no ducto colédoco sejam uma causa comum de pancreatite aguda, a maioria dos cálculos biliares passa facilmente para o duodeno e é perdida nas fezes. A coledocolitíase persistente pode causar obstrução persistente do ducto pancreático e/ou da árvore biliar, causando necrose e/ou colangite. A remoção de cálculos biliares obstrutivos da árvore biliar em pacientes com pancreatite aguda deve reduzir a probabilidade de complicações.
Deve-se suspeitar de colangite na presença da tríade de Charcot (icterícia, febre e calafrios, e dor no quadrante superior direito). A CPRE não é indicada para a pancreatite biliar leve ou grave sem colangite.[63]Fogel EL, Sherman S. ERCP for gallstone pancreatitis. N Engl J Med. 2014 Jan 9;370(2):150-7.[84]Crockett SD, Wani S, Gardner TB, et al. American Gastroenterological Association Institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018 Mar;154(4):1096-101. Os riscos do procedimento superam quaisquer possíveis benefícios nesta população de pacientes.
Analgesia e anti-êmese
O controle da dor com opioides pode reduzir a necessidade de analgesia multimodal.[89]Basurto Ona X, Rigau Comas D, Urrútia G. Opioids for acute pancreatitis pain. Cochrane Database Syst Rev. 2013 Jul 26;(7):CD009179.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD009179.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/23888429?tool=bestpractice.com
[  ]
How do opioids compare with non-opioid analgesics for the management of acute pancreatitis pain?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.515/fullMostre-me a resposta[Evidência C]88504fba-1da0-4e1d-ab84-9d91ed5df3cbccaCQuais as diferenças entre analgésicos opioides e não opioides para o manejo da dor por pancreatite aguda?
]
How do opioids compare with non-opioid analgesics for the management of acute pancreatitis pain?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.515/fullMostre-me a resposta[Evidência C]88504fba-1da0-4e1d-ab84-9d91ed5df3cbccaCQuais as diferenças entre analgésicos opioides e não opioides para o manejo da dor por pancreatite aguda?
Fentanila ou morfina podem ser usadas, seja para dor súbita ou como analgesia controlada pelo paciente. Nos casos leves, pode ser usada a escada analgésica padrão da Organização Mundial da Saúde (OMS) para informar a seleção, monitoramento e ajuste da analgesia. O cetorolaco, um anti-inflamatório não esteroidal (AINE), pode ser usado nos pacientes com função renal intacta. Ele não deve ser utilizado em pacientes idosos devido ao risco de efeitos gastrointestinais adversos.[90]American Geriatrics Society 2012 Beers Criteria Update Expert Panel. American Geriatrics Society updated Beers Criteria for potentially inappropriate medication use in older adults. J Am Geriatr Soc. 2012 Apr;60(4):616-31.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3571677
http://www.ncbi.nlm.nih.gov/pubmed/22376048?tool=bestpractice.com
Náuseas e/ou vômitos são sintomas apresentados em 70% a 80% dos pacientes. A ondansetrona é o antiemético mais comumente usado.
Nutrição
Nutrição na pancreatite aguda leve a moderada
Na pancreatite aguda leve, a ingestão oral deve ser restaurada rapidamente e geralmente não é necessária nenhuma intervenção nutricional. Embora o momento da realimentação permaneça controverso, estudos recentes mostraram que a alimentação oral imediata nos pacientes com doença leve parece segura.[91]Ramírez-Maldonado E, López Gordo S, Pueyo EM, et al. Immediate oral refeeding in patients with mild and moderate acute pancreatitis: a multicenter, randomized controlled trial (PADI trial). Ann Surg. 2021 Aug 1;274(2):255-63.
http://www.ncbi.nlm.nih.gov/pubmed/33196485?tool=bestpractice.com
Tanto o American College of Gastroenterology quanto a American Gastroenterological Association recomendam alimentação oral dentro de 24 horas, se tolerada, nos pacientes com pancreatite aguda.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[84]Crockett SD, Wani S, Gardner TB, et al. American Gastroenterological Association Institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018 Mar;154(4):1096-101.
Diretrizes anteriores recomendavam a suspensão da alimentação oral ("repouso pancreático") até a resolução da dor e/ou normalização das enzimas pancreáticas ou evidência de remissão da inflamação por imagens. No entanto, as evidências atuais mostram que a alimentação oral precoce leva a melhores desfechos.[92]Vaughn VM, Shuster D, Rogers MAM, et al. Early versus delayed feeding in patients with acute pancreatitis: a systematic review. Ann Intern Med. 2017 Jun 20;166(12):883-92.
http://www.ncbi.nlm.nih.gov/pubmed/28505667?tool=bestpractice.com
[93]Bakker OJ, van Brunschot S, van Santvoort HC, et al. Early versus on-demand nasoenteric tube feeding in acute pancreatitis. N Engl J Med. 2014 Nov 20;371(21):1983-93.
http://www.nejm.org/doi/full/10.1056/NEJMoa1404393#t=article
http://www.ncbi.nlm.nih.gov/pubmed/25409371?tool=bestpractice.com
[94]Liang XY, Wu XA, Tian Y, et al. Effects of early versus delayed feeding in patients with acute pancreatitis: a systematic review and meta-analysis. J Clin Gastroenterol. 2024 May-Jun 01;58(5):522-30.
https://www.doi.org/10.1097/MCG.0000000000001886
http://www.ncbi.nlm.nih.gov/pubmed/37428071?tool=bestpractice.com
Uma revisão sistemática de 11 estudos randomizados não mostrou uma associação entre alimentação precoce (≤48 horas após a hospitalização; os estudos avaliaram as vias oral, nasogástrica e nasojejunal) e aumento do risco de eventos adversos em comparação com a alimentação tardia; e os pacientes com pancreatite leve a moderada recebendo alimentação precoce se beneficiaram de uma redução no tempo de internação.[92]Vaughn VM, Shuster D, Rogers MAM, et al. Early versus delayed feeding in patients with acute pancreatitis: a systematic review. Ann Intern Med. 2017 Jun 20;166(12):883-92.
http://www.ncbi.nlm.nih.gov/pubmed/28505667?tool=bestpractice.com
Nutrição na pancreatite aguda grave
Nos pacientes impossibilitados de se alimentar por via oral, deve-se utilizar nutrição por sonda enteral; a nutrição parenteral deve ser evitada.[95]Arvanitakis M, Ockenga J, Bezmarevic M, et al. ESPEN guideline on clinical nutrition in acute and chronic pancreatitis. Clin Nutr. 2020 Mar;39(3):612-31.
https://www.clinicalnutritionjournal.com/article/S0261-5614(20)30009-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/32008871?tool=bestpractice.com
Houve vários ensaios randomizados mostrando que a nutrição parenteral total está associada a complicações infecciosas e outras relacionadas à sonda. A alimentação enteral mantém a barreira da mucosa intestinal, previne a ruptura e previne a translocação de bactérias para semear uma necrose pancreática.[96]Yi F, Ge L, Zhao J, et al. Meta-analysis: total parenteral nutrition versus total enteral nutrition in predicted severe acute pancreatitis. Intern Med. 2012;51(6):523-30.
https://www.jstage.jst.go.jp/article/internalmedicine/51/6/51_6_523/_pdf
http://www.ncbi.nlm.nih.gov/pubmed/22449657?tool=bestpractice.com
[97]Mirtallo JM, Forbes A, McClave SA, et al. International consensus guidelines for nutrition therapy in pancreatitis. JPEN J Parenter Enteral Nutr. 2012 May;36(3):284-91.
http://www.ncbi.nlm.nih.gov/pubmed/22457421?tool=bestpractice.com
[98]Petrov MS, Zagainov V. Influence of enteral versus parenteral nutrition on blood glucose control in acute pancreatitis: a systematic review. Clin Nutr. 2007 Oct;26(5):514-23.
http://www.ncbi.nlm.nih.gov/pubmed/17559987?tool=bestpractice.com
A infusão enteral contínua é preferível à administração cíclica ou em bolus.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
As fórmulas de triglicerídeos de cadeia média à base de pequenos peptídeos podem ser usadas se as fórmulas padrão não forem toleradas.[95]Arvanitakis M, Ockenga J, Bezmarevic M, et al. ESPEN guideline on clinical nutrition in acute and chronic pancreatitis. Clin Nutr. 2020 Mar;39(3):612-31.
https://www.clinicalnutritionjournal.com/article/S0261-5614(20)30009-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/32008871?tool=bestpractice.com
A alimentação por sonda nasogástrica é recomendada de preferência à via nasojejunal para a maioria dos pacientes.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[95]Arvanitakis M, Ockenga J, Bezmarevic M, et al. ESPEN guideline on clinical nutrition in acute and chronic pancreatitis. Clin Nutr. 2020 Mar;39(3):612-31.
https://www.clinicalnutritionjournal.com/article/S0261-5614(20)30009-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/32008871?tool=bestpractice.com
Uma revisão sistemática que descreveu 92 pacientes de 4 estudos sobre alimentação por sonda nasogástrica constatou que ela foi segura e bem tolerada em pacientes com pancreatite aguda grave predita.[99]Petrov MS, Kukosh MV, Emelyanov NV. A randomized controlled trial of enteral versus parenteral feeding in patients with predicted severe acute pancreatitis shows a significant reduction in mortality and in infected pancreatic complications with total enteral nutrition. Dig Surg. 2006;23(5-6):336-44; discussion 344-5.
http://www.ncbi.nlm.nih.gov/pubmed/17164546?tool=bestpractice.com
Os pacientes com aumento do risco de aspiração devem ser colocados em uma posição mais ereta e colocados em precauções de aspiração.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
A colocação de sonda nasojejunal requer radiologia intervencionista ou endoscopia e, portanto, tem implicações de recursos, mas não tem maior benefício comprovado em relação à alimentação por sonda nasogástrica em termos de segurança ou eficácia.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[100]Dutta AK, Goel A, Kirubakaran R, et al. Nasogastric versus nasojejunal tube feeding for severe acute pancreatitis. Cochrane Database Syst Rev. 2020 Mar 26;(3):CD010582.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010582.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/32216139?tool=bestpractice.com
[101]Hsieh PH, Yang TC, Kang EY, et al. Impact of nutritional support routes on mortality in acute pancreatitis: a network meta-analysis of randomized controlled trials. J Intern Med. 2024 Jun;295(6):759-73.
https://www.doi.org/10.1111/joim.13782
http://www.ncbi.nlm.nih.gov/pubmed/38561603?tool=bestpractice.com
A nutrição oral deve ser retomada logo que a dor e qualquer náusea/vômito começar a remitir. Um estudo randomizado demonstrou que uma dieta oral após 72 horas foi tão efetiva quanto a alimentação por sonda nasoenteral precoce na redução da taxa de infecção ou das mortes em pacientes com pancreatite aguda com alto risco de complicações.[93]Bakker OJ, van Brunschot S, van Santvoort HC, et al. Early versus on-demand nasoenteric tube feeding in acute pancreatitis. N Engl J Med. 2014 Nov 20;371(21):1983-93.
http://www.nejm.org/doi/full/10.1056/NEJMoa1404393#t=article
http://www.ncbi.nlm.nih.gov/pubmed/25409371?tool=bestpractice.com
Nenhuma formulação de nutrição enteral específica se provou melhor que a outra em pacientes com pancreatite aguda.[102]Poropat G, Giljaca V, Hauser G, et al. Enteral nutrition formulations for acute pancreatitis. Cochrane Database Syst Rev. 2015 Mar 23;(3):CD010605.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010605.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/25803695?tool=bestpractice.com
Complicações infecciosas
Muitos pacientes com pancreatite aguda que desenvolvem doença grave apresentam complicações infecciosas, incluindo colangite, infecções do trato urinário, pseudocistos infectados, coleçõea de fluidos e necrose pancreática infectada. A febre, a taquicardia, a taquipneia e a leucocitose estão associadas à SRIS que pode ocorrer precocemente na evolução da pancreatite aguda. Esse quadro clínico pode ser indistinguível da sepse. Quando há suspeita de infecção, antibióticos devem ser administrados enquanto a fonte da infecção estiver sendo investigada. No entanto, uma vez que a cultura de sangue e outras culturas forem negativas e nenhuma fonte de infecção for identificada, os antibióticos devem ser descontinuados. Apesar do risco de complicações infecciosas, o American College of Gastroenterology e a American Gastroenterology Association não recomendam o uso de antibióticos profiláticos em pacientes com pancreatite aguda grave (ou pancreatite aguda grave predita).[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[84]Crockett SD, Wani S, Gardner TB, et al. American Gastroenterological Association Institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018 Mar;154(4):1096-101.
Necrose pancreática
Na maioria dos pacientes, a necrose está associada à doença moderadamente grave ou grave.[84]Crockett SD, Wani S, Gardner TB, et al. American Gastroenterological Association Institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018 Mar;154(4):1096-101. A necrose pancreática é definida como áreas difusas ou focais de parênquima pancreático não viável >3 cm de tamanho ou >30% do pâncreas.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Necrose estéril
No início da evolução da doença, áreas de pâncreas necrótico formam uma massa inflamatória difusa sólida/semissólida. A intervenção endoscópica, cirúrgica e/ou radiológica deve ser evitada nas primeiras 4 semanas, a menos que o paciente esteja piorando. Após aproximadamente 4 semanas, uma parede fibrosa se desenvolve ao redor da área necrótica, tornando-a mais passível de intervenção. Nesta fase, a drenagem ou a necrosectomia/desbridamento podem ser consideradas.[47]Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidence-based guidelines for the management of acute pancreatitis. Pancreatology. 2013 Jul-Aug;13(4 Suppl 2):e1-15.
https://www.sciencedirect.com/science/article/pii/S1424390313005255?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/24054878?tool=bestpractice.com
Não são recomendados antibióticos profiláticos para prevenir infecção para os pacientes com necrose estéril (mesmo para aqueles com predição de doença grave).[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Embora os primeiros estudos não cegos tenham sugerido que a administração de antibióticos pode prevenir complicações infecciosas nos pacientes com necrose estéril, estudos subsequentes de alta qualidade consistentemente falharam em confirmar uma vantagem.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[103]Dellinger EP, Tellado JM, Soto NE, et al. Early antibiotic treatment for severe acute necrotizing pancreatitis: a randomized, double-blind, placebo-controlled study. Ann Surg. 2007 May;245(5):674-83.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1877078
http://www.ncbi.nlm.nih.gov/pubmed/17457158?tool=bestpractice.com
Uma metanálise de 11 estudos prospectivos randomizados demonstrou que o número necessário para tratar foi de 1429 para um paciente se beneficiar do uso de antibióticos profiláticos na pancreatite aguda grave.[104]Jiang K, Huang W, Yang XN, et al. Present and future of prophylactic antibiotics for severe acute pancreatitis. World J Gastroenterol. 2012 Jan 21;18(3):279-84.
https://www.wjgnet.com/1007-9327/full/v18/i3/279.htm
http://www.ncbi.nlm.nih.gov/pubmed/22294832?tool=bestpractice.com
Necrose infectada
As coleções necróticas se tornam infectadas em cerca de um terço dos pacientes.[87]van Dijk SM, Hallensleben NDL, van Santvoort HC, et al. Acute pancreatitis: recent advances through randomised trials. Gut. 2017 Nov;66(11):2024-32.
http://www.ncbi.nlm.nih.gov/pubmed/28838972?tool=bestpractice.com
Acredita-se que isso ocorra como resultado da translocação bacteriana a partir do intestino.[87]van Dijk SM, Hallensleben NDL, van Santvoort HC, et al. Acute pancreatitis: recent advances through randomised trials. Gut. 2017 Nov;66(11):2024-32.
http://www.ncbi.nlm.nih.gov/pubmed/28838972?tool=bestpractice.com
Quando comparados com pacientes com necrose estéril, os pacientes com necrose pancreática infectada apresentam uma maior taxa de mortalidade (média de 30%, variação de 14% a 69%).[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Os antibióticos devem ser usados de maneira criteriosa nos pacientes com pancreatite aguda necrosante se houver suspeita de infecção. Antibióticos com boa penetração pancreática são recomendados, como um carbapenêmico (por exemplo, imipeném/cilastatina), uma fluoroquinolona (por exemplo, ciprofloxacino) ou metronidazol.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[28]Leppäniemi A, Tolonen M, Tarasconi A, et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg. 2019 Jun 13;14:27.
https://wjes.biomedcentral.com/articles/10.1186/s13017-019-0247-0
http://www.ncbi.nlm.nih.gov/pubmed/31210778?tool=bestpractice.com
Os antibióticos fluoroquinolonas sistêmicos podem causar eventos adversos graves, incapacitantes e potencialmente duradouros ou irreversíveis. Isso inclui, mas não está limitado a: tendinopatia/ruptura de tendão; neuropatia periférica; artropatia/artralgia; aneurisma e dissecção da aorta; regurgitação da valva cardíaca; disglicemia; e efeitos no sistema nervoso central, incluindo convulsões, depressão, psicose e pensamentos e comportamento suicida.[105]Rusu A, Munteanu AC, Arbănași EM, et al. Overview of side-effects of antibacterial fluoroquinolones: new drugs versus old drugs, a step forward in the safety profile? Pharmaceutics. 2023 Mar 1;15(3).
https://www.doi.org/10.3390/pharmaceutics15030804
http://www.ncbi.nlm.nih.gov/pubmed/36986665?tool=bestpractice.com
Aplicam-se restrições de prescrição ao uso das fluoroquinolonas, e essas restrições podem variar entre os países. Em geral, o uso das fluoroquinolonas deve ser restrito para o uso nas infecções bacterianas graves e com risco à vida, somente. Algumas agências regulatórias também podem recomendar que elas sejam usadas apenas nas situações em que outros antibióticos comumente recomendados para a infecção forem inadequados (por exemplo, resistência, contraindicações, falha do tratamento e indisponibilidade).
Consulte as diretrizes locais e o formulário de medicamentos para obter mais informações sobre adequação, contraindicações e precauções.
Historicamente, todos os pacientes com necrose pancreática infectada têm sido submetidos a desbridamento cirúrgico imediato. Isso não é mais recomendado, a menos que o paciente esteja clinicamente instável.[18]Hines OJ, Pandol SJ. Management of severe acute pancreatitis. BMJ. 2019 Dec 2;367:l6227.
http://www.ncbi.nlm.nih.gov/pubmed/31791953?tool=bestpractice.com
[106]Boxhoorn L, van Dijk SM, van Grinsven J, et al. Immediate versus postponed intervention for infected necrotizing pancreatitis. N Engl J Med. 2021 Oct 7;385(15):1372-81.
http://www.ncbi.nlm.nih.gov/pubmed/34614330?tool=bestpractice.com
[107]Yang Y, Zhang Y, Wen S, et al. The optimal timing and intervention to reduce mortality for necrotizing pancreatitis: a systematic review and network meta-analysis. World J Emerg Surg. 2023 Jan 27;18(1):9.
https://www.doi.org/10.1186/s13017-023-00479-7
http://www.ncbi.nlm.nih.gov/pubmed/36707836?tool=bestpractice.com
[108]Nakai Y, Shiomi H, Hamada T, et al. Early versus delayed interventions for necrotizing pancreatitis: a systematic review and meta-analysis. DEN Open. 2023 Apr;3(1):e171.
https://www.doi.org/10.1002/deo2.171
http://www.ncbi.nlm.nih.gov/pubmed/36247314?tool=bestpractice.com
Nos pacientes clinicamente estáveis, o manejo inicial da necrose infectada para os pacientes deve ser um ciclo de antibióticos de 30 dias para permitir que a reação inflamatória se torne mais bem organizada.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
Neste momento, quando a necrose estiver totalmente isolada, pode-se decidir sobre o método de drenagem preferencial, que pode incluir intervenção endoscópica, radiológica e/ou cirúrgica minimamente invasiva.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[47]Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidence-based guidelines for the management of acute pancreatitis. Pancreatology. 2013 Jul-Aug;13(4 Suppl 2):e1-15.
https://www.sciencedirect.com/science/article/pii/S1424390313005255?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/24054878?tool=bestpractice.com
[109]Gurusamy KS, Belgaumkar AP, Haswell A, et al. Interventions for necrotising pancreatitis. Cochrane Database Syst Rev. 2016 Apr 16;(4):CD011383.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD011383.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/27083933?tool=bestpractice.com
[110]Gluck M, Ross A, Irani S, et al. Endoscopic and percutaneous drainage of symptomatic walled-off pancreatic necrosis reduces hospital stay and radiographic resources. Clin Gastroenterol Hepatol. 2010 Dec;8(12):1083-8.
https://www.cghjournal.org/article/S1542-3565(10)00896-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/20870036?tool=bestpractice.com
Se não houver resposta imediata aos antibióticos ou se a situação clínica piorar, a necrosectomia/desbridamento deve ser realizada.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Necrose pancreática delimitadaGut. 2017 Nov;66(11):2024-32; usado com permissão [Citation ends].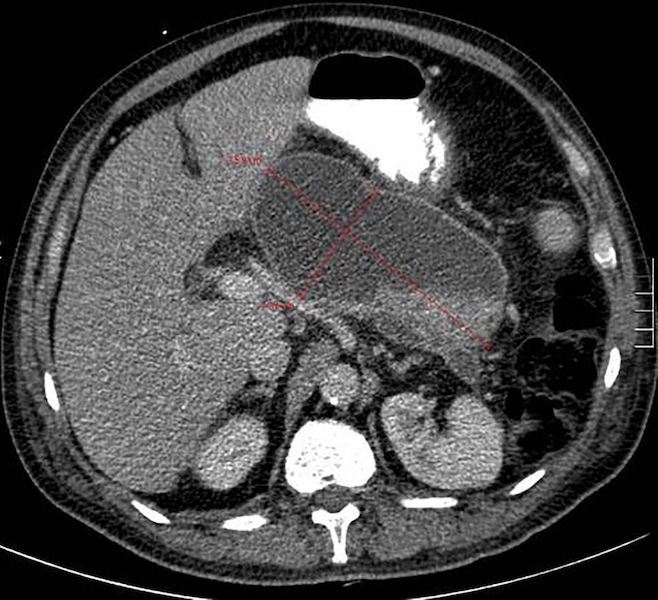 [Figure caption and citation for the preceding image starts]: Coleção necrótica infectada, não totalmente encapsulada, no dia 20 após o início da doençaGut. 2017 Nov;66(11):2024-32; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Coleção necrótica infectada, não totalmente encapsulada, no dia 20 após o início da doençaGut. 2017 Nov;66(11):2024-32; usado com permissão [Citation ends].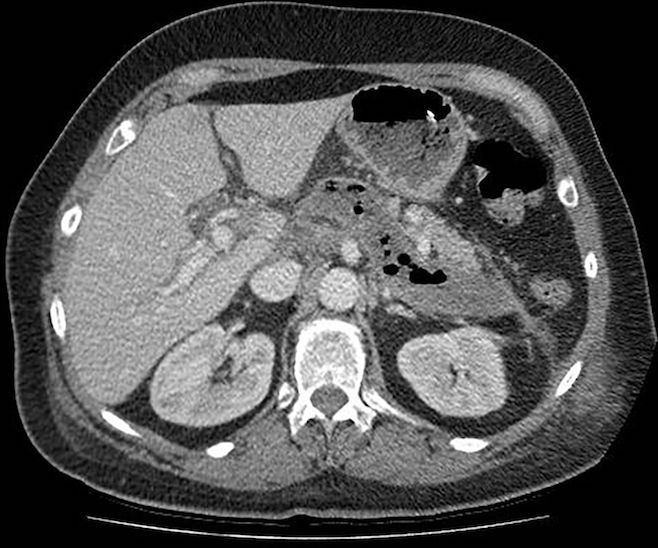
Pseudocistos
Os pseudocistos são comuns e não aparecem até pelo menos 2-4 semanas após o início de um episódio de pancreatite aguda.[18]Hines OJ, Pandol SJ. Management of severe acute pancreatitis. BMJ. 2019 Dec 2;367:l6227.
http://www.ncbi.nlm.nih.gov/pubmed/31791953?tool=bestpractice.com
No início da evolução da pancreatite aguda, grandes volumes de fluido podem deixar o compartimento intravascular e formar coleções de fluido no abdome. A maior parte desse fluido é reabsorvida nas primeiras semanas.[18]Hines OJ, Pandol SJ. Management of severe acute pancreatitis. BMJ. 2019 Dec 2;367:l6227.
http://www.ncbi.nlm.nih.gov/pubmed/31791953?tool=bestpractice.com
No entanto, em quase um terço dos pacientes, as coleções de fluidos persistirão e desenvolverão uma parede fibrosa não epitelizada, tornando-se um pseudocisto. Os "pseudocistos" diagnosticados na apresentação inicial provavelmente representam uma patologia alternativa: um paciente com pancreatite crônica, uma antiga área de necrose pancreática delimitada ou uma neoplasia pancreática cística.
A necrose pancreática, especialmente a necrose pancreática delimitada, não pode ser diferenciada de um pseudocisto pela tomografia computadorizada. Isso é importante, pois o tratamento de um pseudocisto sintomático ou infectado (abscesso) e a necrose pancreática são bastante diferentes. A diferenciação entre necrose pancreática e pseudocistos só pode ser feita pela localização do cisto em relação ao pâncreas. Enquanto os pseudocistos estão localizados fora do parênquima do pâncreas ou estruturas adjacentes, a necrose pancreática sempre envolverá o pâncreas. A ressonância nuclear magnética e a ultrassonografia endoscópica (com aspiração com agulha fina) podem determinar a presença de tecido na necrose pancreática delimitada, mas essas modalidades de imagem não são usadas de maneira rotineira.
Historicamente, pacientes com pseudocistos maiores que 6 cm ou com aumento em imagens seriadas foram submetidos à drenagem. No entanto, hoje existe um consenso de que, independentemente do tamanho, os pseudocistos podem ser tratados de forma conservadora, sem intervenção.[18]Hines OJ, Pandol SJ. Management of severe acute pancreatitis. BMJ. 2019 Dec 2;367:l6227.
http://www.ncbi.nlm.nih.gov/pubmed/31791953?tool=bestpractice.com
[111]Vitas GJ, Sarr MG. Selected management of pancreatic pseudocysts: operative versus expectant management. Surgery. 1992 Feb;111(2):123-30.
http://www.ncbi.nlm.nih.gov/pubmed/1736380?tool=bestpractice.com
Se um pseudocisto for infectado, é melhor descrito como um abscesso, que requer antibióticos e drenagem. Os pseudocistos podem se tornar dolorosos ou causar saciedade precoce e perda de peso quando seu tamanho afeta o estômago e o intestino; a drenagem desses pseudocistos é recomendada para o alívio dos sintomas, independentemente da infecção.[8]Tenner S, Vege S, Sheth S, et al. American College of Gastroenterology guidelines: management of acute pancreatitis. Am J Gastroenterol. 2024 Mar 119(3):419-37.
https://journals.lww.com/ajg/fulltext/2024/03000/american_college_of_gastroenterology_guidelines_.14.aspx
http://www.ncbi.nlm.nih.gov/pubmed/38857482?tool=bestpractice.com
[18]Hines OJ, Pandol SJ. Management of severe acute pancreatitis. BMJ. 2019 Dec 2;367:l6227.
http://www.ncbi.nlm.nih.gov/pubmed/31791953?tool=bestpractice.com
Dependendo da experiência disponível, a drenagem pode ser realizada por meio de técnicas endoscópicas, radiológicas ou cirúrgicas.
 ]
[Evidência C]
]
[Evidência C] [Figure caption and citation for the preceding image starts]: Coleção necrótica infectada, não totalmente encapsulada, no dia 20 após o início da doençaGut. 2017 Nov;66(11):2024-32; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Coleção necrótica infectada, não totalmente encapsulada, no dia 20 após o início da doençaGut. 2017 Nov;66(11):2024-32; usado com permissão [Citation ends].