História
Os médicos devem suspeitar de PPC ao tratarem de pacientes adultos ou adolescentes HIV-positivos, especialmente se eles não aderiram à terapia antirretroviral (TAR) combinada ou à profilaxia da PPC, tiveram episódio prévio de PPC e/ou tiverem uma celularidade CD4 <200 células/microlitro.[60]Katz MH, Baron RB, Grady D. Risk stratification of ambulatory patients suspected of Pneumocystis pneumonia. Arch Intern Med. 1991 Jan;151(1):105-10.
http://www.ncbi.nlm.nih.gov/pubmed/1985585?tool=bestpractice.com
Crianças HIV-positivas e lactentes com sintomas respiratórios, diagnóstico de HIV indeterminado e mães infectadas por HIV também devem ser avaliados em relação a PPC.
Outros grupos de pacientes com suspeita de PPC são aqueles com imunocomprometimento e com história de:[31]Stern A, Green H, Paul M, et al. Prophylaxis for Pneumocystis pneumonia (PCP) in non-HIV immunocompromised patients. Cochrane Database Syst Rev. 2014 Oct 1;(10):CD005590.
http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD005590.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/25269391?tool=bestpractice.com
[47]Taplitz RA, Kennedy EB, Bow EJ, et al. Antimicrobial prophylaxis for adult patients with cancer-related immunosuppression: ASCO and IDSA clinical practice guideline update. J Clin Oncol. 2018 Oct 20;36(30):3043-54.
https://ascopubs.org/doi/10.1200/JCO.18.00374?url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org&rfr_dat=cr_pub++0pubmed
http://www.ncbi.nlm.nih.gov/pubmed/30179565?tool=bestpractice.com
[48]Tomblyn M, Chiller T, Einsele H, et al. Guidelines for preventing infectious complications among hematopoietic cell transplantation recipients: a global perspective. Biol Blood Marrow Transplant. 2009 Oct;15(10):1143-238.
https://www.bbmt.org/article/S1083-8791(09)00300-0/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/19747629?tool=bestpractice.com
[49]Fishman JA, Gans H, AST Infectious Diseases Community of Practice. Pneumocystis jiroveci in solid organ transplantation: guidelines from the American Society of Transplantation Infectious Diseases Community of Practice. Clin Transplant. 2019 Sep;33(9):e13587.
http://www.ncbi.nlm.nih.gov/pubmed/31077616?tool=bestpractice.com
Neoplasia hematológica
Transplante de células hematopoéticas
Outras neoplasias malignas em que o esquema de quimioterapia esteja associado a um risco >3.5% de PPC
Transplante de órgão sólido
Uso crônico de corticosteroides com ou sem outros medicamentos imunossupressores
Certas imunodeficiências primárias (por exemplo, imunodeficiência combinada grave)
Em pacientes com apresentações atípicas de pneumonia, a avaliação dos fatores de risco para HIV e a realização de teste de HIV também podem ajudar a identificar o risco de PPC.
Na PPC de pacientes HIV-positivos, a apresentação geralmente é uma progressão insidiosa de fadiga, febre, calafrios, sudorese, tosse não produtiva e dispneia ao longo de várias semanas. Outros achados associados à PPC são história de pneumonias bacterianas recorrentes, perda de peso e candidíase oral.[43]Salzer HJF, Schäfer G, Hoenigl M, et al. Clinical, diagnostic, and treatment disparities between HIV-infected and non-HIV-infected immunocompromised patients with Pneumocystis jirovecii pneumonia. Respiration. 2018;96(1):52-65.
https://www.karger.com/Article/FullText/487713
http://www.ncbi.nlm.nih.gov/pubmed/29635251?tool=bestpractice.com
Em pacientes HIV-negativos, a apresentação costuma ser mais rápida e mais grave.[43]Salzer HJF, Schäfer G, Hoenigl M, et al. Clinical, diagnostic, and treatment disparities between HIV-infected and non-HIV-infected immunocompromised patients with Pneumocystis jirovecii pneumonia. Respiration. 2018;96(1):52-65.
https://www.karger.com/Article/FullText/487713
http://www.ncbi.nlm.nih.gov/pubmed/29635251?tool=bestpractice.com
O início dos sintomas pode ocorrer enquanto a dose habitual de agentes imunossupressores está sendo diminuída ou descontinuada.[61]Pareja JGR, Garland R, Koziel H. Use of adjunctive corticosteroids in severe adult non-HIV Pneumocystis carinii pneumonia. Chest. 1998 May;113(5):1215-24.
http://www.ncbi.nlm.nih.gov/pubmed/9596297?tool=bestpractice.com
Raramente a infecção causa manifestações extrapulmonares naqueles com HIV avançado; contudo, nos pacientes com síndrome de imunodeficiência adquirida (AIDS) avançada ou HIV-positivos que não estejam fazendo uso da profilaxia, pode haver infecção sistêmica com sintomas visuais, comprometimento cognitivo devido a envolvimento do sistema nervoso central e sintomas gastrointestinais, como diarreia.
Investigações
Se a suspeita de PPC for baseada no quadro clínico e a radiografia torácica for compatível com PPC, o primeiro passo para o diagnóstico deverá ser um escarro induzido para visualização do Pneumocystis jirovecii.[62]Singh N, Shafer RW, Swindells S (eds). HIV clinical manual. Pittsburgh, PA: ESun Technologies; 2003. O escarro expectorado espontaneamente tem baixa sensibilidade para o diagnóstico de PPC, e não deve ser usado. A sensibilidade do teste do escarro induzido é de 50% a 90%, dependendo da qualidade da amostra, da carga de patógenos, do método de coloração utilizado e da experiência da instituição.[32]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV. Pneumocystis pneumonia. Sep 2024 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/adult-and-adolescent-opportunistic-infection/pneumocystis-pneumonia
[63]Fortun J, Navas E, Marti-Belda P, et al. Pneumocystis carinii pneumonia in HIV-infected patients: diagnostic yield of induced sputum and immunofluorescent stain with monoclonal antibodies. Eur Respir J. 1992 Jun;5(6):665-9.
http://www.ncbi.nlm.nih.gov/pubmed/1628723?tool=bestpractice.com
[64]Kovacs JA, Ng VL, Masur H, et al. Diagnosis of Pneumocystis carinii pneumonia: improved detection in sputum with use of monoclonal antibodies. N Engl J Med. 1988 Mar 10;318(10):589-93.
http://www.ncbi.nlm.nih.gov/pubmed/2449613?tool=bestpractice.com
[65]Midgley J, Parsons P, Leigh TR, et al. Increased sensitivity of immunofluorescence for detection of Pneumocystis carinii. Lancet. 1989 Dec 23-30;2(8678-8679):1523.
http://www.ncbi.nlm.nih.gov/pubmed/2574793?tool=bestpractice.com
[66]Ng VL, Virani NA, Chaisson RE, et al. Rapid detection of Pneumocystis carinii using a direct fluorescent monoclonal antibody stain. J Clin Microbiol. 1990 Oct;28(10):2228-33.
http://www.ncbi.nlm.nih.gov/pubmed/1699968?tool=bestpractice.com
Se o resultado do exame de indução do escarro for negativo, o exame broncoscópico com LBA deverá ser realizado. A sensibilidade para a LBA é de 90% a 99% em pacientes HIV-positivos, portanto, ela geralmente é realizada sem biópsia transbrônquica.[32]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV. Pneumocystis pneumonia. Sep 2024 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/adult-and-adolescent-opportunistic-infection/pneumocystis-pneumonia
Em geral, se a LBA for negativa em um paciente HIV-positivo, outra etiologia deve ser considerada e o tratamento pode ser descontinuado.
Biópsias transbrônquicas poderão ser realizadas se a LBA inicial for negativa, mas a suspeita clínica de PPC for alta, ou se outros diagnósticos forem considerados prováveis. A sensibilidade das biópsias transbrônquicas é de 95% a 100%.[32]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV. Pneumocystis pneumonia. Sep 2024 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/adult-and-adolescent-opportunistic-infection/pneumocystis-pneumonia
Nos pacientes HIV-negativos, a biópsia transbrônquica é necessária mais frequentemente para confirmar um diagnóstico porque a LBA é menos sensível. A biópsia transbrônquica tem risco mais elevado de complicações, como sangramento e pneumotórax. O pneumotórax ocorreu em 9% dos pacientes HIV-positivos submetidos a biópsias transbrônquicas em uma série, e 5% precisaram da inserção de um dreno torácico.[67]Harcup C, Baier HJ, Pitchenik AE. Evaluation of patients with the acquired immunodeficiency syndrome (AIDS) by fiberoptic bronchoscopy. Endoscopy. 1985 Nov;17(6):217-20.
http://www.ncbi.nlm.nih.gov/pubmed/3877629?tool=bestpractice.com
Se a suspeita clínica de PPC permanecer alta ou se o exame prévio não revelar a etiologia da doença do paciente, uma biópsia pulmonar a céu aberto poderá ser considerada para confirmar ou descartar a PPC, bem como para determinar a presença de outra patologia. A sensibilidade das biópsias pulmonares a céu aberto é de 95% a 100%.[32]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV. Pneumocystis pneumonia. Sep 2024 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/adult-and-adolescent-opportunistic-infection/pneumocystis-pneumonia
A lactato desidrogenase (LDH) sérica elevada (>220 unidades internacionais/L) tem importância tanto no diagnóstico quanto no prognóstico, com um nível de LDH mais elevado associado ao aumento da mortalidade.[68]Zaman MK, White DA. Serum lactate dehydrogenase levels and Pneumocystis carinii pneumonia. Diagnostic and prognostic significance. Lancet. 1988 Nov 5;2(8619):1049-51.
http://www.ncbi.nlm.nih.gov/pubmed/3258483?tool=bestpractice.com
A gasometria arterial é usada para determinar a gravidade:[32]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV. Pneumocystis pneumonia. Sep 2024 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/adult-and-adolescent-opportunistic-infection/pneumocystis-pneumonia
Os pacientes com quadro clínico sugestivo de PPC, mas com radiografia torácica normal ou inalterada, devem ser submetidos a uma tomografia computadorizada de alta resolução (TCAR) do tórax ou a testes de função pulmonar com medição da capacidade de difusão do monóxido de carbono (CDCO). Se a TCAR mostrar opacidades em vidro fosco, ou se a CDCO estiver diminuída, o paciente deve ser submetido à indução do escarro, seguida por uma LBA (se a indução do escarro for negativa), uma vez que a presença de opacidades em vidro fosco ou a CDCO diminuída são sensíveis, mas não são testes específicos para a PPC.[69]Gruden JF, Huang L, Turner J, et al. High-resolution CT in the evaluation of clinically suspected Pneumocystis carinii pneumonia in AIDS patients with normal, equivocal, or nonspecific radiographic findings. AJR Am J Roentgenol. 1997 Oct;169(4):967-75.
http://www.ncbi.nlm.nih.gov/pubmed/9308446?tool=bestpractice.com
[70]Huang L, Stansell J, Osmond D, et al. Performance of an algorithm to detect Pneumocystis carinii pneumonia in symptomatic HIV-infected persons. Chest. 1999 Apr;115(4):1025-32.
http://www.ncbi.nlm.nih.gov/pubmed/10208204?tool=bestpractice.com
[71]Sankary RM, Turner J, Lipavsky A, et al. Alveolar-capillary block in patients with AIDS and Pneumocystis carinii pneumonia. Am Rev Respir Dis. 1988 Feb;137(2):443-9.
http://www.ncbi.nlm.nih.gov/pubmed/3257662?tool=bestpractice.com
Se os dois testes forem negativos, outra etiologia deve ser considerada e investigações diagnósticas apropriadas devem ser realizadas. Se todas as amostras diagnósticas para o Pneumocystis jirovecii forem negativas, será muito pouco provável que o paciente tenha PPC; ele deverá ser observado e outras etiologias deverão ser consideradas. Exames adicionais podem ser necessários, dependendo da situação clínica.
O diagnóstico de PPC não descarta a possibilidade de um segundo processo simultâneo. Apesar de ser preferível confirmar o diagnóstico da PPC por meio da microscopia, já que muitos quadros clínicos têm apresentações semelhantes, o tratamento empírico dos pacientes com quadro clínico sugestivo de PPC pode ser realizado, principalmente em locais onde há recursos limitados para realização do escarro induzido ou da LBA.
A identificação do Pneumocystis jirovecii no escarro ou no fluido da LBA geralmente tem sido realizada com colorações, como a de azul de toluidina, Giemsa, Diff-Quik e prata metenamina. Ensaios de imunofluorescência (teste de antígeno fluorescente direto) também podem ser utilizados e têm sensibilidade mais elevada.[72]Shelhamer JH, Gill VJ, Quinn TC, et al. The laboratory evaluation of opportunistic pulmonary infections. Ann Intern Med. 1996 Mar 15;124(6):585-99.
http://www.ncbi.nlm.nih.gov/pubmed/8597323?tool=bestpractice.com
As biópsias transbrônquicas junto com a LBA podem aumentar o rendimento diagnóstico.[73]Broaddus C, Dake MD, Stulbarg MS, et al. Bronchoalveolar lavage and transbronchial biopsy for the diagnosis of pulmonary infections in the acquired immunodeficiency syndrome. Ann Intern Med. 1985 Jun;102(6):747-52.
http://www.ncbi.nlm.nih.gov/pubmed/2986505?tool=bestpractice.com
Outros ensaios, como a reação em cadeia da polimerase, a reação em cadeia da polimerase em tempo real e a reação em cadeia da polimerase via transcriptase reversa, podem detectar baixos níveis do DNA do Pneumocystis jirovecii. Esses ensaios, juntamente com os níveis plasmáticos de S-adenosilmetionina, podem aumentar a sensibilidade do diagnóstico da PPC, mas geralmente não estão clinicamente disponíveis. Técnicas da reação em cadeia da polimerase têm uma taxa de falso-positivos maior que a coloração histoquímica.[74]Fillaux J, Malvy S, Alvarez M, et al. Accuracy of a routine real-time PCR assay for the diagnosis of Pneumocystis jiroveci pneumonia. J Microbiol Methods. 2008 Oct;75(2):258-61.
http://www.ncbi.nlm.nih.gov/pubmed/18606198?tool=bestpractice.com
[75]Tuncer S, Erguven S, Kocagoz S, et al. Comparison of cytochemical staining, immunofluorescence and PCR for diagnosis of Pneumocystis carinii on sputum samples. Scand J Infect Dis. 1998;30(2):125-8.
http://www.ncbi.nlm.nih.gov/pubmed/9730296?tool=bestpractice.com
[76]Larsen HH, Masur H, Kovacs JA, et al. Development and evaluation of a quantitative, touch-down, real-time PCR assay for diagnosing Pneumocystis carinii pneumonia. J Clin Microbiol. 2002 Feb;40(2):490-4.
http://www.ncbi.nlm.nih.gov/pubmed/11825961?tool=bestpractice.com
[77]Helweg-Larsen J, Jensen JS, Lundgren B. Diagnostic use of PCR for detection of Pneumocystis carinii in oral wash samples. J Clin Microbiol. 1998 Jul;36(7):2068-72.
http://www.ncbi.nlm.nih.gov/pubmed/9650964?tool=bestpractice.com
[78]Larsen HH, Huang L, Kovacs JA, et al. A prospective, blinded study of quantitative touch-down polymerase chain reaction using oral-wash samples for diagnosis of Pneumocystis pneumonia in HIV-infected patients. J Infect Dis. 2004 May 1;189(9):1679-83.
http://www.ncbi.nlm.nih.gov/pubmed/15116305?tool=bestpractice.com
[79]Skelly MJ, Holzman RS, Merali S. S-adenosylmethionine levels in the diagnosis of Pneumocystis carinii pneumonia in patients with HIV infection. Clin Infect Dis. 2008 Feb 1;46(3):467-71.
http://cid.oxfordjournals.org/content/46/3/467.long
http://www.ncbi.nlm.nih.gov/pubmed/18177224?tool=bestpractice.com
[80]Summah H, Zhu YG, Falagas ME, et al. Use of real-time polymerase chain reaction for the diagnosis of Pneumocystis pneumonia in immunocompromised patients: a meta-analysis. Chin Med J (Engl). 2013;126(10):1965-73.
http://www.ncbi.nlm.nih.gov/pubmed/23673119?tool=bestpractice.com
Também há interesse na medição sorológica (1,3)-beta-D-glicano, um elemento da parede fúngica, para o diagnóstico da PPC.[81]Watanabe T, Yasuoka A, Tanuma J, et al. Serum (1-->3) beta-D-glucan as a noninvasive adjunct marker for the diagnosis of Pneumocystis pneumonia in patients with AIDS. Clin Infect Dis. 2009 Oct 1;49(7):1128-31.
http://cid.oxfordjournals.org/content/49/7/1128.long
http://www.ncbi.nlm.nih.gov/pubmed/19725788?tool=bestpractice.com
[82]Shimizu Y, Sunaga N, Dobashi K, et al. Serum markers in interstitial pneumonia with and without Pneumocystis jirovecii colonization: a prospective study. BMC Infect Dis. 2009 Apr 22;9:47.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2676289/?tool=pubmed
http://www.ncbi.nlm.nih.gov/pubmed/19383170?tool=bestpractice.com
[83]Desmet S, Van Wijngaerden E, Maertens J, et al. Serum (1-3)-beta-D-glucan as a tool for diagnosis of Pneumocystis jirovecii pneumonia in patients with human immunodeficiency virus infection or hematological malignancy. J Clin Microbiol. 2009 Dec;47(12):3871-4.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2786638/?tool=pubmed
http://www.ncbi.nlm.nih.gov/pubmed/19846641?tool=bestpractice.com
[84]Del Bono V, Mularoni A, Furfaro E, et al. Clinical evaluation of a (1,3)-beta-D-glucan assay for presumptive diagnosis of Pneumocystis jiroveci pneumonia in immunocompromised patients. Clin Vaccine Immunol. 2009 Oct;16(10):1524-6.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2756857/?tool=pubmed
http://www.ncbi.nlm.nih.gov/pubmed/19692624?tool=bestpractice.com
[85]Nakamura H, Tateyama M, Tasato D, et al. Clinical utility of serum beta-D-glucan and KL-6 levels in Pneumocystis jirovecii pneumonia. Intern Med. 2009;48(4):195-202.
https://www.jstage.jst.go.jp/article/internalmedicine/48/4/48_4_195/_article
http://www.ncbi.nlm.nih.gov/pubmed/19218768?tool=bestpractice.com
Esses estudos mostram o (1,3)-beta-D-glicano significativamente elevado em pacientes com PPC, embora em menor grau em pacientes HIV-negativos com PPC, e os níveis não apresentaram correlação com a gravidade ou com a resposta à terapia.[86]Huang L. Clinical and translational research in pneumocystis and pneumocystis pneumonia. Parasite. 2011 Feb;18(1):3-11.
http://www.ncbi.nlm.nih.gov/pubmed/21395200?tool=bestpractice.com
Uma metanálise de 2012 dos estudos sobre o (1,3)-beta-D-glicano no diagnóstico da PPC em várias populações (infectadas por HIV ou não) mostrou que a sensibilidade e a especificidade agrupadas foram de 96% e 84%, respectivamente.[87]Onishi A, Sugiyama D, Kogata Y, et al. Diagnostic accuracy of serum 1,3-β-D-glucan for pneumocystis jiroveci pneumonia, invasive candidiasis, and invasive aspergillosis: systematic review and meta-analysis. J Clin Microbiol. 2012 Jan;50(1):7-15.
http://jcm.asm.org/content/50/1/7.long
http://www.ncbi.nlm.nih.gov/pubmed/22075593?tool=bestpractice.com
Uma metanálise mais recente de 2015 demonstrou sensibilidade (92%) e especificidade (78%) semelhantes para pacientes infectados pelo HIV; entretanto, em pacientes não infectados pelo HIV, a sensibilidade e a especificidade foram inferiores, de 85% e 73%, respectivamente.[88]Li WJ, Guo YL, Liu TJ, et al. Diagnosis of pneumocystis pneumonia using serum (1-3)-β-D-Glucan: a bivariate meta-analysis and systematic review. J Thorac Dis. 2015 Dec;7(12):2214-25.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4703639
http://www.ncbi.nlm.nih.gov/pubmed/26793343?tool=bestpractice.com
Em um dos maiores estudos de participantes infectados por HIV (n=282), em que 69% apresentavam PPC, a sensibilidade e a especificidade eram de 92% e 65%, respectivamente.[89]Sax PE, Komarow L, Finkelman MA, et al. Blood (1->3)-beta-D-glucan as a diagnostic test for HIV-related Pneumocystis jirovecii pneumonia. Clin Infect Dis. 2011 Jul 15;53(2):197-202.
http://cid.oxfordjournals.org/content/53/2/197.long
http://www.ncbi.nlm.nih.gov/pubmed/21690628?tool=bestpractice.com
Em um estudo com 159 pacientes de AIDS com pelo menos um sintoma respiratório, dos quais 139 tinham PPC, a sensibilidade e a especificidade do (1,3)-beta-D-glicano foram de 92.8% e 75.0%, respectivamente.[90]Wood BR, Komarow L, Zolopa AR, et al. Test performance of blood beta-glucan for Pneumocystis jirovecii pneumonia in patients with AIDS and respiratory symptoms. AIDS. 2013 Mar 27;27(6):967-72.
http://www.ncbi.nlm.nih.gov/pubmed/23698062?tool=bestpractice.com
Embora a sensibilidade possa ser útil para descartar a PPC em cenários em que testes mais sensíveis não estão disponíveis, a redução na especificidade deve-se à detecção do (1,3)-beta-D-glicano durante outras infecções fúngicas, uma vez que o (1,3)-beta-D-glicano não é uma proteína específica do Pneumocystis e pode ser menos confiável em pessoas não infectadas pelo HIV.[Figure caption and citation for the preceding image starts]: Radiografia torácica posteroanterior mostrando infiltrados intersticiais pulmonares leves, reticulares e bilateraisDo acervo de Matthew Gingo, UPMC [Citation ends].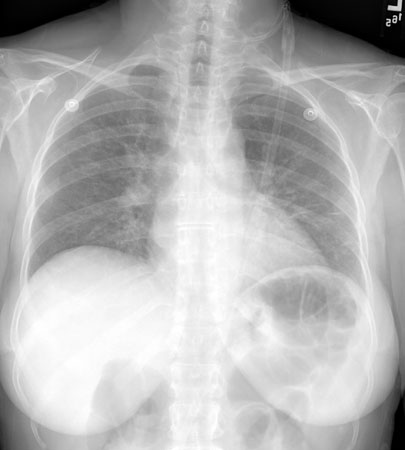 [Figure caption and citation for the preceding image starts]: Radiografia torácica posteroanterior mostrando infiltrados intersticiais pulmonares graves com pneumatocelesDo acervo de Matthew Gingo, UPMC [Citation ends].
[Figure caption and citation for the preceding image starts]: Radiografia torácica posteroanterior mostrando infiltrados intersticiais pulmonares graves com pneumatocelesDo acervo de Matthew Gingo, UPMC [Citation ends].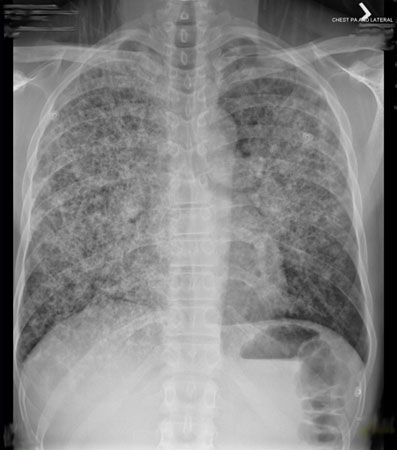 [Figure caption and citation for the preceding image starts]: Tomografia computadorizada do tórax mostrando infiltrados intersticiais pulmonares bilaterais e pneumatoceles (cistos), que são típicos da pneumonia por Pneumocystis (PPC)Do acervo de Matthew Gingo, UPMC [Citation ends].
[Figure caption and citation for the preceding image starts]: Tomografia computadorizada do tórax mostrando infiltrados intersticiais pulmonares bilaterais e pneumatoceles (cistos), que são típicos da pneumonia por Pneumocystis (PPC)Do acervo de Matthew Gingo, UPMC [Citation ends].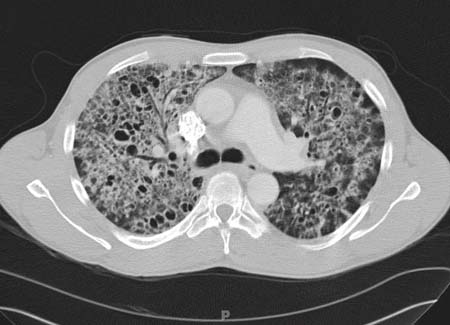 [Figure caption and citation for the preceding image starts]: Fotomicrografia da lavagem broncoalveolar (LBA) mostrando cistos de Pneumocystis corados de preto pela coloração de Grocott-Gomori com metenamina de prata (contracoloração com verde de metila)Do acervo de Matthew Gingo, UPMC [Citation ends].
[Figure caption and citation for the preceding image starts]: Fotomicrografia da lavagem broncoalveolar (LBA) mostrando cistos de Pneumocystis corados de preto pela coloração de Grocott-Gomori com metenamina de prata (contracoloração com verde de metila)Do acervo de Matthew Gingo, UPMC [Citation ends].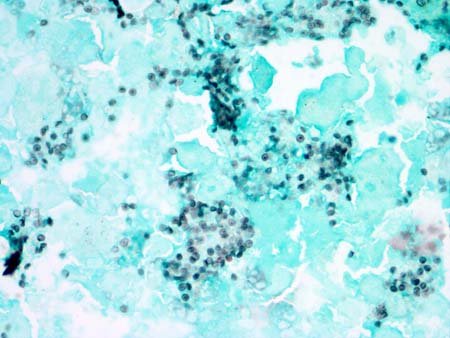
[Figure caption and citation for the preceding image starts]: Algoritmo para o diagnóstico de pneumonia por Pneumocystis; lavagem broncoalveolar (LBA)Matthew Gingo, adapted from Singh, HIV Clinical Manual, 2003 [Citation ends].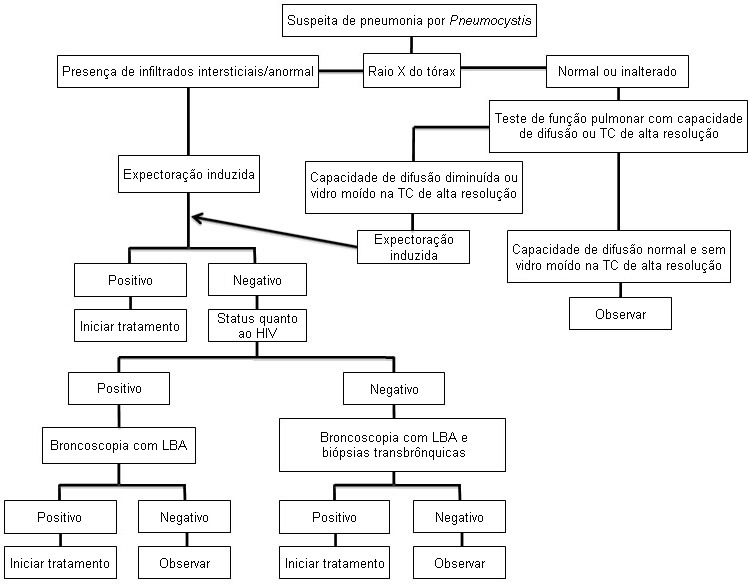
 [Figure caption and citation for the preceding image starts]: Radiografia torácica posteroanterior mostrando infiltrados intersticiais pulmonares graves com pneumatocelesDo acervo de Matthew Gingo, UPMC [Citation ends].
[Figure caption and citation for the preceding image starts]: Radiografia torácica posteroanterior mostrando infiltrados intersticiais pulmonares graves com pneumatocelesDo acervo de Matthew Gingo, UPMC [Citation ends]. [Figure caption and citation for the preceding image starts]: Tomografia computadorizada do tórax mostrando infiltrados intersticiais pulmonares bilaterais e pneumatoceles (cistos), que são típicos da pneumonia por Pneumocystis (PPC)Do acervo de Matthew Gingo, UPMC [Citation ends].
[Figure caption and citation for the preceding image starts]: Tomografia computadorizada do tórax mostrando infiltrados intersticiais pulmonares bilaterais e pneumatoceles (cistos), que são típicos da pneumonia por Pneumocystis (PPC)Do acervo de Matthew Gingo, UPMC [Citation ends]. [Figure caption and citation for the preceding image starts]: Fotomicrografia da lavagem broncoalveolar (LBA) mostrando cistos de Pneumocystis corados de preto pela coloração de Grocott-Gomori com metenamina de prata (contracoloração com verde de metila)Do acervo de Matthew Gingo, UPMC [Citation ends].
[Figure caption and citation for the preceding image starts]: Fotomicrografia da lavagem broncoalveolar (LBA) mostrando cistos de Pneumocystis corados de preto pela coloração de Grocott-Gomori com metenamina de prata (contracoloração com verde de metila)Do acervo de Matthew Gingo, UPMC [Citation ends].
