O diagnóstico pode ser evidente em alguns casos, mas é frequentemente difícil. É importante que haja um alto nível de suspeita na avaliação de um paciente com fatores de risco. A confirmação do diagnóstico exige a cultura do Mycobacterium tuberculosis. Os atrasos no diagnóstico e início da terapia estão associados a transmissão da doença e a mortalidade elevada.[12]Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention clinical practice guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis. 2017 Jan 15;64(2):e1-33.
https://academic.oup.com/cid/article/64/2/e1/2629583
http://www.ncbi.nlm.nih.gov/pubmed/27932390?tool=bestpractice.com
Em caso de alta suspeita da doença, o paciente deve ser isolado (no domicílio ou em unidade hospitalar de pressão negativa) por até 5 dias a 2 semanas de tratamento concluídas. A tuberculose (TB) ativa, confirmada ou extremamente suspeita, é uma doença que deve ser relatada para as autoridades locais de saúde.
História clínica e fatores de risco
A possibilidade de TB deve ser considerada em qualquer indivíduo com fatores de risco para exposição à TB, que apresente sintomas sugestivos (por exemplo, febre, mal-estar, dor torácica pleurítica, tosse persistente por mais de 2-3 semanas, sudorese noturna e perda de peso, hemoptise, sintomas psicológicos, baqueteamento digital, eritema nodoso) ou anormalidades na radiografia torácica. Embora a presença de infiltrados no lobo superior seja característica da doença, a apresentação atípica da radiografia torácica é comum em crianças e em pessoas imunocomprometidas, com infecção por HIV ou diabetes.[Figure caption and citation for the preceding image starts]: Tuberculose pulmonar com cavitaçãoDo acervo pessoal de David Horne e do Dr. Masahiro Narita; usado com permissão [Citation ends].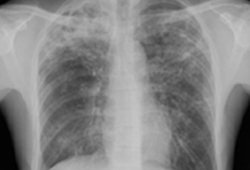
Investigações diagnósticas
As investigações para infecção ativa incluem radiografia torácica, três amostras de escarro obtidas para teste de bacilos álcool-ácido resistentes (BAAR), teste de amplificação de ácido nucleico (NAAT), hemograma completo e eletrólitos (por exemplo, sódio). Caso o paciente seja incapaz de produzir escarro espontaneamente, ele deverá ser induzido (com precauções adequadas para evitar transmissão) ou obtido por meio de broncoscopia ou aspirado gástrico.[12]Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention clinical practice guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis. 2017 Jan 15;64(2):e1-33.
https://academic.oup.com/cid/article/64/2/e1/2629583
http://www.ncbi.nlm.nih.gov/pubmed/27932390?tool=bestpractice.com
Esfregaços corados devem ser feitos a partir de amostras de escarro para identificar BAAR, que é a primeira evidência bacteriológica de infecção e fornece uma estimativa do grau de infectividade do paciente. Caso sejam observados BAARs no esfregaço, a terapia deverá ser iniciada e o paciente mantido em isolamento.
A cultura do escarro respalda o diagnóstico de TB, é mais sensível e específica que a coloração do esfregaço, facilita a identificação da espécie de micobactéria pela amplificação ou hibridização de ácido nucleico e avalia a sensibilidade ao medicamento. Os sistemas de meio de cultura líquidos permitem rápido crescimento e detecção em 1 a 3 semanas, em oposição a 4 a 8 semanas em meio sólido.[12]Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention clinical practice guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis. 2017 Jan 15;64(2):e1-33.
https://academic.oup.com/cid/article/64/2/e1/2629583
http://www.ncbi.nlm.nih.gov/pubmed/27932390?tool=bestpractice.com
O NAAT deve ser realizado em pelo menos uma amostra respiratória quando o diagnóstico de TB estiver sendo considerado. O NAAT pode acelerar o diagnóstico em casos de esfregaço negativo e pode ser útil para diferenciar as micobactérias não tuberculosas quando o escarro para BAAR for positivo no esfregaço, mas negativo no NAAT.[33]Centers for Disease Control and Prevention (CDC). Updated guidelines for the use of nucleic acid amplification tests in the diagnosis of tuberculosis. MMWR Morb Mortal Wkly Rep. 2009 Jan 16;58(1):7-10.
https://www.cdc.gov/mmwr/preview/mmwrhtml/mm5801a3.htm
http://www.ncbi.nlm.nih.gov/pubmed/19145221?tool=bestpractice.com
Genotipagem pode ser considerada útil em surtos de TB para identificar a transmissão recente de TB, principalmente quando não foi identificado contato no curso das investigações epidemiológicas. Vários NAATs rápidos estão disponíveis e alguns também são capazes de detectar genes que codificam resistência aos medicamentos para TB.[30]World Health Organization. WHO consolidated guidelines on tuberculosis: module 5: management of tuberculosis in children and adolescents. Mar 2022 [internet publication].
https://www.who.int/publications/i/item/9789240046764
[34]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: rapid diagnostics for tuberculosis detection, 3rd ed. Mar 2024 [internet publication].
https://www.who.int/publications/i/item/9789240089488
[35]Zifodya JS, Kreniske JS, Schiller I, et al. Xpert Ultra versus Xpert MTB/RIF for pulmonary tuberculosis and rifampicin resistance in adults with presumptive pulmonary tuberculosis. Cochrane Database Syst Rev. 2021 Feb 22;(2):CD009593.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD009593.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/33616229?tool=bestpractice.com
[36]Shapiro AE, Ross JM, Yao M, et al. Xpert MTB/RIF and Xpert Ultra assays for screening for pulmonary tuberculosis and rifampicin resistance in adults, irrespective of signs or symptoms. Cochrane Database Syst Rev. 2021 Mar 23;(3):CD013694.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013694.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/33755189?tool=bestpractice.com
[37]Pillay S, Steingart KR, Davies GR, et al. Xpert MTB/XDR for detection of pulmonary tuberculosis and resistance to isoniazid, fluoroquinolones, ethionamide, and amikacin. Cochrane Database Syst Rev. 2022 May 18;(5):CD014841.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD014841.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/35583175?tool=bestpractice.com
[38]Haraka F, Kakolwa M, Schumacher SG, et al. Impact of the diagnostic test Xpert MTB/RIF on patient outcomes for tuberculosis. Cochrane Database Syst Rev. 2021 May 6;(5):CD012972.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012972.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/34097769?tool=bestpractice.com
[39]Kay AW, Ness T, Verkuijl SE, et al. Xpert MTB/RIF Ultra assay for tuberculosis disease and rifampicin resistance in children. Cochrane Database Syst Rev. 2022 Sep 6;(9):CD013359.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013359.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/36065889?tool=bestpractice.com
Um NAAT positivo é adequado para o início do tratamento antituberculose. Quando o paciente tiver sido previamente tratado para TB, especialmente nos últimos 2 anos, um NAAT positivo pode representar um resultado falso-positivo.
O uso de amostras fecais é uma alternativa às amostras respiratórias no diagnóstico de TB pulmonar (o escarro é engolido e o M tuberculosis pode passar pelo trato gastrointestinal). Uma revisão sistemática avaliando o exame de fezes como esfregaço para BAAR, cultura e NAAT (reação em cadeia da polimerase) na TB pulmonar revelou uma sensibilidade combinada de um ou mais dos três exames como 79.1% (IC de 95%: 61.5 a 92.5).[40]Laursen LL, Dahl VN, Wejse C. Stool testing for pulmonary TB diagnosis in adults. Int J Tuberc Lung Dis. 2022 Jun 1;26(6):516-23.
http://www.ncbi.nlm.nih.gov/pubmed/35650697?tool=bestpractice.com
A sensibilidade da microscopia de fezes, reação em cadeia da polimerase e cultura foi de 41.1% (IC de 95%: 24.9 a 58.2), 89.7% (IC de 95%: 81.4 a 95.9) e 38.0% (IC de 95%: 26.2 a 50.6), respectivamente.[40]Laursen LL, Dahl VN, Wejse C. Stool testing for pulmonary TB diagnosis in adults. Int J Tuberc Lung Dis. 2022 Jun 1;26(6):516-23.
http://www.ncbi.nlm.nih.gov/pubmed/35650697?tool=bestpractice.com
A Organização Mundial da Saúde (OMS) recomenda que, em crianças com sinais e sintomas de TB pulmonar, o NAAT Xpert Ultra seja usado para testes de diagnóstico iniciais e detecção de resistência à rifampicina no escarro, aspirado nasofaríngeo, aspirado gástrico ou fezes, em vez de microscopia do esfregaço/cultura e testes fenotípicos de suscetibilidade a medicamentos.[30]World Health Organization. WHO consolidated guidelines on tuberculosis: module 5: management of tuberculosis in children and adolescents. Mar 2022 [internet publication].
https://www.who.int/publications/i/item/9789240046764
Embora a tomografia computadorizada (TC) do tórax não seja realizada de forma rotineira, pode ser usada para descartar outras patologias: por exemplo, câncer.
Os testes de fluxo lateral que detectam antígeno lipoarabinomanano (LAM) na urina surgiram como potenciais testes laboratoriais remotos. Uma revisão Cochrane constatou que o ensaio de lipoarabinomanano de fluxo lateral na urina (LF-LAM) tem uma sensibilidade de 42% para diagnosticar TB em indivíduos HIV-positivos com sintomas de TB, e de 35% em indivíduos HIV-positivos não avaliados para sintomas de TB.[41]Bjerrum S, Schiller I, Dendukuri N, et al. Lateral flow urine lipoarabinomannan assay for detecting active tuberculosis in people living with HIV. Cochrane Database Syst Rev. 2019 Oct 21;(10):CD011420.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD011420.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/31633805?tool=bestpractice.com
[  ]
What is the accuracy of lateral flow urine lipoarabinomannan (LF‐LAM) for detecting tuberculosis (TB) in unselected HIV‐positive adults (symptomatic or asymptomatic)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2825/fullMostre-me a resposta
[
]
What is the accuracy of lateral flow urine lipoarabinomannan (LF‐LAM) for detecting tuberculosis (TB) in unselected HIV‐positive adults (symptomatic or asymptomatic)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2825/fullMostre-me a resposta
[  ]
What is the accuracy of lateral flow urine lipoarabinomannan (LF‐LAM) for detecting tuberculosis (TB) in symptomatic HIV‐positive adults?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2824/fullMostre-me a resposta A OMS recomenda que o LF-LAM pode ser usado para auxiliar no diagnóstico de TB ativa em adultos, adolescentes e crianças HIV-positivos.[30]World Health Organization. WHO consolidated guidelines on tuberculosis: module 5: management of tuberculosis in children and adolescents. Mar 2022 [internet publication].
https://www.who.int/publications/i/item/9789240046764
[34]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: rapid diagnostics for tuberculosis detection, 3rd ed. Mar 2024 [internet publication].
https://www.who.int/publications/i/item/9789240089488
Essa abordagem é respaldada por outra revisão Cochrane, que constatou reduções na mortalidade e um aumento nos inícios de tratamento com o uso dos LF-LAM em pacientes hospitalizados e ambulatoriais.[42]Nathavitharana RR, Lederer P, Chaplin M, et al. Impact of diagnostic strategies for tuberculosis using lateral flow urine lipoarabinomannan assay in people living with HIV. Cochrane Database Syst Rev. 2021 Aug 20;(8):CD014641.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD014641/full
http://www.ncbi.nlm.nih.gov/pubmed/34416013?tool=bestpractice.com
A cultura ainda seria necessária para teste de sensibilidade a medicamentos (TSM).
]
What is the accuracy of lateral flow urine lipoarabinomannan (LF‐LAM) for detecting tuberculosis (TB) in symptomatic HIV‐positive adults?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2824/fullMostre-me a resposta A OMS recomenda que o LF-LAM pode ser usado para auxiliar no diagnóstico de TB ativa em adultos, adolescentes e crianças HIV-positivos.[30]World Health Organization. WHO consolidated guidelines on tuberculosis: module 5: management of tuberculosis in children and adolescents. Mar 2022 [internet publication].
https://www.who.int/publications/i/item/9789240046764
[34]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: rapid diagnostics for tuberculosis detection, 3rd ed. Mar 2024 [internet publication].
https://www.who.int/publications/i/item/9789240089488
Essa abordagem é respaldada por outra revisão Cochrane, que constatou reduções na mortalidade e um aumento nos inícios de tratamento com o uso dos LF-LAM em pacientes hospitalizados e ambulatoriais.[42]Nathavitharana RR, Lederer P, Chaplin M, et al. Impact of diagnostic strategies for tuberculosis using lateral flow urine lipoarabinomannan assay in people living with HIV. Cochrane Database Syst Rev. 2021 Aug 20;(8):CD014641.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD014641/full
http://www.ncbi.nlm.nih.gov/pubmed/34416013?tool=bestpractice.com
A cultura ainda seria necessária para teste de sensibilidade a medicamentos (TSM).
Recomenda-se que todos os pacientes portadores de TB devam ser testados para o HIV em até 2 meses depois do diagnóstico.
Esfregaço ou culturas negativas
Cerca de 40% a 50% dos casos apresentam esfregaço BAAR negativo, e as culturas são negativas em 15% a 20% dos casos. Nos pacientes para os quais exista uma forte suspeita clínica de TB, principalmente se o teste tuberculínico for positivo (reação de induração ≥5 mm), a terapia empírica para a TB pode ser tentada antes da confirmação laboratorial da infecção. A melhora clínica e radiográfica com o tratamento antituberculose adequado respalda o diagnóstico. Um NAAT de culturas do escarro também pode ser útil nessa situação. A broncoscopia pode ser realizada para obtenção de amostras de lavado broncoalveolar ou biópsia transbrônquica, e o aspirado gástrico pode ser utilizado nos pacientes incapazes de fornecer uma amostra de escarro adequada, como as crianças pequenas. Em pacientes nos quais haja baixa suspeita de TB ativa e os esfregaços sejam BAAR negativos, é aceitável aguardar os resultados da cultura para BAAR ou repetir a radiografia torácica antes de se iniciar o tratamento.[9]Nahid P, Dorman SE, Alipanah N, et al. Official American Thoracic Society/Centers for Disease Control and Prevention/Infectious Diseases Society of America clinical practice guidelines: treatment of drug-susceptible tuberculosis. Clin Infect Dis. 2016 Oct 1;63(7):e147-95.
https://academic.oup.com/cid/article/63/7/e147/2196792
http://www.ncbi.nlm.nih.gov/pubmed/27516382?tool=bestpractice.com
Pacientes que apresentam doença com esfregaço negativo podem estar infecciosos, embora o risco de transmissão seja menor que na doença com esfregaço positivo.[43]Behr MA, Warren SA, Salamon H, et al. Transmission of Mycobacterium tuberculosis from patients smear-negative for acid-fast bacilli. Lancet. 1999 Feb 6;353(9151):444-9.
http://www.ncbi.nlm.nih.gov/pubmed/9989714?tool=bestpractice.com
Se a suspeita de TB for alta, deve-se considerar o início da administração de medicamentos antituberculose antes da confirmação laboratorial.
Teste de suscetibilidade
Em ambientes com recursos adequados, o teste de suscetibilidade a medicamentos baseado em cultura é realizado rotineiramente em isolados de M tuberculosis. Uma limitação do teste de suscetibilidade a medicamentos baseado em cultura é que pode demorar >2 semanas para que o isolado cresça para a realização do teste. Quando há uma suspeita maior de resistência a medicamentos, um teste rápido molecular de suscetibilidade a medicamentos pode ser adequado para orientar o tratamento. O teste rápido molecular de suscetibilidade a medicamentos para rifampicina com ou sem isoniazida usando espécimes respiratórios de pessoas com esfregaço BAAR positivo ou NAAT positivo deve ser considerado em pacientes que:
Foram tratados para TB no passado, ou
Nasceram ou moraram por pelo menos 1 ano em outro país com ao menos uma incidência moderada de TB (≥20 por 100,000) ou uma alta prevalência de TB primariamente resistente a múltiplos medicamentos (≥2%), ou
São contatos de pacientes com TB resistente a múltiplos medicamentos, ou
São HIV-positivos.
É importante observar que, quando o Xpert MTB/RIF ou o Xpert Ultra (testes moleculares rápidos recomendados pela Organização Mundial da Saúde) são usados como parte do diagnóstico de TB, a resistência à rifampicina será avaliada automaticamente.[12]Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention clinical practice guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis. 2017 Jan 15;64(2):e1-33.
https://academic.oup.com/cid/article/64/2/e1/2629583
http://www.ncbi.nlm.nih.gov/pubmed/27932390?tool=bestpractice.com
[34]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: rapid diagnostics for tuberculosis detection, 3rd ed. Mar 2024 [internet publication].
https://www.who.int/publications/i/item/9789240089488
As revisões Cochrane do Xpert MTB/RIF e do Xpert Ultra revelaram que eles fornecem resultados acurados para a TB resistente à rifampicina e a TB resistente a múltiplos medicamentos.[35]Zifodya JS, Kreniske JS, Schiller I, et al. Xpert Ultra versus Xpert MTB/RIF for pulmonary tuberculosis and rifampicin resistance in adults with presumptive pulmonary tuberculosis. Cochrane Database Syst Rev. 2021 Feb 22;(2):CD009593.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD009593.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/33616229?tool=bestpractice.com
[36]Shapiro AE, Ross JM, Yao M, et al. Xpert MTB/RIF and Xpert Ultra assays for screening for pulmonary tuberculosis and rifampicin resistance in adults, irrespective of signs or symptoms. Cochrane Database Syst Rev. 2021 Mar 23;(3):CD013694.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013694.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/33755189?tool=bestpractice.com
[39]Kay AW, Ness T, Verkuijl SE, et al. Xpert MTB/RIF Ultra assay for tuberculosis disease and rifampicin resistance in children. Cochrane Database Syst Rev. 2022 Sep 6;(9):CD013359.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013359.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/36065889?tool=bestpractice.com
O Xpert MTB/XDR avalia a resistência à isoniazida, fluoroquinolonas, injetáveis (amicacina, canamicina, capreomicina) e etionamida. Uma revisão Cochrane revelou que o Xpert MTB/XDR é preciso para detectar a resistência à isoniazida e às fluoroquinolonas.[37]Pillay S, Steingart KR, Davies GR, et al. Xpert MTB/XDR for detection of pulmonary tuberculosis and resistance to isoniazid, fluoroquinolones, ethionamide, and amikacin. Cochrane Database Syst Rev. 2022 May 18;(5):CD014841.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD014841.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/35583175?tool=bestpractice.com
Ensaios de sonda de linha (ESLs) são testes em tiras capazes de detectar tuberculose e determinar perfis de resistência a medicamentos. Os ensaios de sonda em linha (ESLs) são recomendados pela OMS apenas para detectar resistência a medicamentos anti-TB.[34]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: rapid diagnostics for tuberculosis detection, 3rd ed. Mar 2024 [internet publication].
https://www.who.int/publications/i/item/9789240089488
A OMS também inclui agora o sequenciamento de nova geração (NGS) em suas recomendações para o teste da sensibilidade a medicamentos nos casos de TB pulmonar confirmada.[34]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: rapid diagnostics for tuberculosis detection, 3rd ed. Mar 2024 [internet publication].
https://www.who.int/publications/i/item/9789240089488
O NGS é uma nova classe de testes que pode ser usada para detectar a resistência a uma ampla lista de medicamentos.
Teste tuberculínico e testes de liberação de gamainterferona
Investigações para infecção latente em indivíduos expostos ao M tuberculosis, mas sem sinais de TB ativa, baseiam-se no teste tuberculínico (TT) ou em testes de liberação de gamainterferona (IGRAs). Os TT e IGRA medem a resposta das células T aos antígenos de TB. Uma vez que ocorrem resultados falso-negativos em 20% a 25% de pacientes com TB pulmonar ativa, esses testes não devem ser utilizados isoladamente para descartar um diagnóstico de TB ativa.[44]Metcalfe JZ, Everett CK, Steingart KR, et al. Interferon-γ release assays for active pulmonary tuberculosis diagnosis in adults in low- and middle-income countries: systematic review and meta-analysis. J Infect Dis. 2011 Nov 15;204 (suppl 4):S1120-9.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3192542
http://www.ncbi.nlm.nih.gov/pubmed/21996694?tool=bestpractice.com
A American Academy of Pediatrics orienta que um resultado negativo no TT ou no IGRA deve ser considerado especialmente não confiável em uma criança com menos de 3 meses.[45]Nolt D, Starke JR. Tuberculosis infection in children and adolescents: testing and treatment. Pediatrics. 2021 Dec 1;148(6):e2021054663.
https://www.doi.org/10.1542/peds.2021-054663
http://www.ncbi.nlm.nih.gov/pubmed/34851422?tool=bestpractice.com
A interpretação do TT depende de características do paciente, incluindo o estado de imunocompetência e vacinação. Para pacientes com imunidade normal e sem fatores de risco adicionais, uma induração de ≥15 mm de diâmetro significa um resultado positivo, mas um diâmetro menor é usado como limite em indivíduos com fatores de risco adicionais e em crianças.[12]Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention clinical practice guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis. 2017 Jan 15;64(2):e1-33.
https://academic.oup.com/cid/article/64/2/e1/2629583
http://www.ncbi.nlm.nih.gov/pubmed/27932390?tool=bestpractice.com
[30]World Health Organization. WHO consolidated guidelines on tuberculosis: module 5: management of tuberculosis in children and adolescents. Mar 2022 [internet publication].
https://www.who.int/publications/i/item/9789240046764
[46]Pai M, Zwerling A, Menzies D. Systematic review: T-cell-based assays for the diagnosis of latent tuberculosis infection: an update. Ann Intern Med. 2008 Aug 5;149(3):177-84.
http://www.ncbi.nlm.nih.gov/pubmed/18593687?tool=bestpractice.com
Um IGRA pode ser usado no lugar de um TT em todas as situações em que os TTs são usados para diagnosticar infecção latente, embora o TT possa ser preferencial nas crianças menores de 2 anos.[45]Nolt D, Starke JR. Tuberculosis infection in children and adolescents: testing and treatment. Pediatrics. 2021 Dec 1;148(6):e2021054663.
https://www.doi.org/10.1542/peds.2021-054663
http://www.ncbi.nlm.nih.gov/pubmed/34851422?tool=bestpractice.com
[47]Mazurek GH, Jereb J, Vernon A, et al; IGRA Expert Committee; Centers for Disease Control and Prevention (CDC). Updated guidelines for using Interferon Gamma Release Assays to detect Mycobacterium tuberculosis infection - United States, 2010. MMWR Recomm Rep. 2010 Jun 25;59(RR-5):1-25.
https://www.cdc.gov/mmwr/preview/mmwrhtml/rr5905a1.htm
http://www.ncbi.nlm.nih.gov/pubmed/20577159?tool=bestpractice.com
Um IGRA é preferível nos indivíduos com uma história de vacinação por bacilo de Calmette e Guérin (BCG) em virtude de uma especificidade superior.[46]Pai M, Zwerling A, Menzies D. Systematic review: T-cell-based assays for the diagnosis of latent tuberculosis infection: an update. Ann Intern Med. 2008 Aug 5;149(3):177-84.
http://www.ncbi.nlm.nih.gov/pubmed/18593687?tool=bestpractice.com
Além disso, o IGRA é preferível para testar indivíduos de grupos que historicamente apresentam baixos índices de retorno para a leitura dos TTs.
Exames direcionados para a infecção latente por TB são recomendados pelos Centros de Controle e Prevenção de Doenças dos EUA/American Thoracic Society como parte do controle estratégico e da redução da TB. Grupos de alto risco incluem indivíduos com HIV, usuários de drogas intravenosas, profissionais da saúde que atendem populações de alto risco e contatos de indivíduos portadores de TB pulmonar.[12]Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention clinical practice guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis. 2017 Jan 15;64(2):e1-33.
https://academic.oup.com/cid/article/64/2/e1/2629583
http://www.ncbi.nlm.nih.gov/pubmed/27932390?tool=bestpractice.com
O teste para infecção latente por TB também deve ser realizado em pacientes antes da terapia com antagonista do fator de necrose tumoral alfa.[48]Doherty SD, Van Voorhees A, Lebwohl MG, et al. National Psoriasis Foundation consensus statement on screening for latent tuberculosis infection in patients with psoriasis treated with systemic and biologic agents. J Am Acad Dermatol. 2008 Aug;59(2):209-17.
http://www.ncbi.nlm.nih.gov/pubmed/18485527?tool=bestpractice.com
Os testes cutâneos baseados em antígenos para TB (TCTB) são uma nova classe de testes que foram desenvolvidos para medir a resposta imunológica celularmente mediada a antígenos específicos do M tuberculosis. A OMS recomenda que os TCTB possam ser usados para testar a infecção por TB latente, relatando que a acurácia diagnóstica dos TCTB é semelhante à do IGRA e maior que a do TT.[49]World Health Organization. WHO consolidated guidelines on tuberculosis: module 3: diagnosis: tests for TB infection. Sep 2022 [internet publication].
https://www.who.int/publications/i/item/9789240056084

 ]
[
]
[  ]
A OMS recomenda que o LF-LAM pode ser usado para auxiliar no diagnóstico de TB ativa em adultos, adolescentes e crianças HIV-positivos.[30][34] Essa abordagem é respaldada por outra revisão Cochrane, que constatou reduções na mortalidade e um aumento nos inícios de tratamento com o uso dos LF-LAM em pacientes hospitalizados e ambulatoriais.[42] A cultura ainda seria necessária para teste de sensibilidade a medicamentos (TSM).
]
A OMS recomenda que o LF-LAM pode ser usado para auxiliar no diagnóstico de TB ativa em adultos, adolescentes e crianças HIV-positivos.[30][34] Essa abordagem é respaldada por outra revisão Cochrane, que constatou reduções na mortalidade e um aumento nos inícios de tratamento com o uso dos LF-LAM em pacientes hospitalizados e ambulatoriais.[42] A cultura ainda seria necessária para teste de sensibilidade a medicamentos (TSM).