A maioria das pessoas (até 60%) infectadas por Coxiella burnetii permanece assintomática.[2]Hartzell JD, Wood-Morris RN, Martinez LJ, et al. Q fever: epidemiology, diagnosis, and treatment. Mayo Clin Proc. 2008 May;83(5):574-9.
https://www.mayoclinicproceedings.org/article/S0025-6196(11)60733-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/18452690?tool=bestpractice.com
[38]Maurin M, Raoult D. Q fever. Clin Microbiol Rev. 1999 Oct;12(4):518-53.
https://cmr.asm.org/content/12/4/518.full
http://www.ncbi.nlm.nih.gov/pubmed/10515901?tool=bestpractice.com
Em muitos pacientes com sintomas, a infecção aguda é leve e autolimitada, apresentando remissão espontânea dentro de 2 semanas.[5]Parker NR, Barralet JH, Bell AM. Q fever. Lancet. 2006 Feb 25;367(9511):679-88.
http://www.ncbi.nlm.nih.gov/pubmed/16503466?tool=bestpractice.com
[38]Maurin M, Raoult D. Q fever. Clin Microbiol Rev. 1999 Oct;12(4):518-53.
https://cmr.asm.org/content/12/4/518.full
http://www.ncbi.nlm.nih.gov/pubmed/10515901?tool=bestpractice.com
No entanto, pacientes sintomáticos devem ser tratados com antibióticos orais por 14 dias. A endocardite e outras infecções focalizadas persistentes exigem antibioticoterapia em longo prazo. Cerca de 65% dos pacientes com endocardite não tratada podem ir a óbito em decorrência da doença.[1]Marrie TJ, Raoult D. Coxiella burnetii. In: Mandell GL, Bennett JE, Dolin R, eds. Principles and practice of infectious diseases. 6th ed. Philadelphia, PA: Churchill Livingstone; 2005.[2]Hartzell JD, Wood-Morris RN, Martinez LJ, et al. Q fever: epidemiology, diagnosis, and treatment. Mayo Clin Proc. 2008 May;83(5):574-9.
https://www.mayoclinicproceedings.org/article/S0025-6196(11)60733-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/18452690?tool=bestpractice.com
Com terapia combinada prolongada (doxiciclina associada a hidroxicloroquina) em pacientes com endocardite, a mortalidade é inferior a 5% em 5 anos.[84]Million M, Thuny F, Richet H, et al. Long-term outcome of Q fever endocarditis: a 26-year personal survey. Lancet Infect Dis. 2010 Aug;10(8):527-35.
http://www.ncbi.nlm.nih.gov/pubmed/20637694?tool=bestpractice.com
O tratamento deve ser iniciado com base na suspeita clínica apenas e não deve esperar os resultados dos exames confirmatórios.
Infecção aguda
As infecções agudas geralmente são leves e autolimitadas, durando de 2 a 14 dias. O tratamento não é recomendado em pacientes com infecção aguda sem valvopatia que estejam assintomáticos antes da consulta médica. No entanto, se o paciente for sintomático, a antibioticoterapia poderá encurtar a duração da doença. O tratamento é mais eficaz se administrado nos primeiros três dias após o início dos sintomas.[33]National Association of State Public Health Veterinarians, National Assembly of State Animal Health Officials. Prevention and control of coxiella burnetii infection among humans and animals: guidance for a coordinated public health and animal health response, 2013. 2013 [internet publication].
https://www.nasphv.org/Documents/Q_Fever_2013.pdf
A doxiciclina oral por 14 dias é o tratamento recomendado, pois é o antibiótico mais eficaz para infecções por C burnetii e demonstrou-se que ela diminui a taxa de hospitalização.[26]Anderson A, Bijlmer H, Fournier PE, et al. Diagnosis and management of Q fever - United States, 2013: recommendations from CDC and the Q fever working group. MMWR Recomm Rep. 2013 Mar 29;62(RR-03):1-23.
https://www.cdc.gov/mmwr/preview/mmwrhtml/rr6203a1.htm
http://www.ncbi.nlm.nih.gov/pubmed/23535757?tool=bestpractice.com
[33]National Association of State Public Health Veterinarians, National Assembly of State Animal Health Officials. Prevention and control of coxiella burnetii infection among humans and animals: guidance for a coordinated public health and animal health response, 2013. 2013 [internet publication].
https://www.nasphv.org/Documents/Q_Fever_2013.pdf
[53]Drancourt M, Raoult D, Xeridat B, et al. Q fever meningoencephalitis in five patients. Eur J Epidemiol. 1991 Mar;7(2):134-8.
http://www.ncbi.nlm.nih.gov/pubmed/2044709?tool=bestpractice.com
[85]Dijkstra F, Riphagen-Dalhuisen J, Wijers N, et al. Antibiotic therapy for acute Q fever in The Netherlands in 2007 and 2008 and its relation to hospitalization. Epidemiol Infect. 2011 Sep;139(9):1332-41.
http://www.ncbi.nlm.nih.gov/pubmed/21087542?tool=bestpractice.com
Se o paciente não tolerar a doxiciclina, outros antibióticos podem ser usados (por exemplo, moxifloxacino, claritromicina, rifampicina ou sulfametoxazol/trimetoprima).[2]Hartzell JD, Wood-Morris RN, Martinez LJ, et al. Q fever: epidemiology, diagnosis, and treatment. Mayo Clin Proc. 2008 May;83(5):574-9.
https://www.mayoclinicproceedings.org/article/S0025-6196(11)60733-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/18452690?tool=bestpractice.com
[86]Centers for Disease Control and Prevention. Q fever: information for healthcare providers. Jan 2019 [internet publication].
https://www.cdc.gov/qfever/healthcare-providers/index.html
Os antibióticos fluoroquinolonas sistêmicos, como o moxifloxacino, podem causar eventos adversos graves, incapacitantes e potencialmente duradouros ou irreversíveis. Isso inclui, mas não está limitado a: tendinopatia/ruptura de tendão; neuropatia periférica; artropatia/artralgia; aneurisma e dissecção da aorta; regurgitação da valva cardíaca; disglicemia; e efeitos no sistema nervoso central, incluindo convulsões, depressão, psicose e pensamentos e comportamento suicida.[87]Rusu A, Munteanu AC, Arbănași EM, et al. Overview of side-effects of antibacterial fluoroquinolones: new drugs versus old drugs, a step forward in the safety profile? Pharmaceutics. 2023 Mar 1;15(3):804.
https://www.mdpi.com/1999-4923/15/3/804
http://www.ncbi.nlm.nih.gov/pubmed/36986665?tool=bestpractice.com
Restrições de prescrição aplicam-se ao uso de fluoroquinolonas e essas restrições podem variar entre os países. Em geral, o uso de fluoroquinolonas deve ser restrito apenas em infecções bacterianas graves e de risco de vida. Algumas agências regulatórias também podem recomendar que eles sejam usados apenas em situações em que outros antibióticos comumente recomendados para a infecção sejam inadequados (por exemplo, resistência, contraindicações, falha do tratamento, indisponibilidade).
Consulte as diretrizes locais e o formulário de medicamentos para obter mais informações sobre adequação, contraindicações e precauções.
Deve-se aconselhar o paciente a repousar no leito e beber bastante líquido. Podem ser usados antitussígenos, mas não paracetamol ou anti-inflamatórios não esteroidais (AINEs) para febre e qualquer desconforto, já que o paracetamol pode piorar o envolvimento hepático e os AINEs podem piorar a infecção.
Em pacientes com infecção aguda, altos níveis de anticorpos anticardiolipina (aCL) da imunoglobulina G (IgG) (ou seja, ≥75 GPLU [unidades G antifosfolipídicas]) estiveram associados a valvopatia, vegetação (na endocardite aguda) e progressão para endocardite crônica e trombose.[55]Ordi-Ros J, Selva-O'Callaghan A, Monegal-Ferran F, et al. Prevalence, significance, and specificity of antibodies to phospholipids in Q fever. Clin Infect Dis. 1994 Feb;18(2):213-8.
http://www.ncbi.nlm.nih.gov/pubmed/8161629?tool=bestpractice.com
[57]Million M, Thuny F, Bardin N, et al. Antiphospholipid antibody syndrome with valvular vegetations in acute Q fever. Clin Infect Dis. 2016 Mar 1;62(5):537-44.
http://www.ncbi.nlm.nih.gov/pubmed/26585519?tool=bestpractice.com
[71]Million M, Walter G, Bardin N, et al. Immunoglobulin G anticardiolipin antibodies and progression to Q fever endocarditis. Clin Infect Dis. 2013 Jul;57(1):57-64.
https://academic.oup.com/cid/article/57/1/57/279982
http://www.ncbi.nlm.nih.gov/pubmed/23532474?tool=bestpractice.com
[77]Million M, Raoult D. The pathogenesis of the antiphospholipid syndrome. N Engl J Med. 2013 Jun 13;368(24):2335.
http://www.ncbi.nlm.nih.gov/pubmed/23758255?tool=bestpractice.com
O medicamento imunomodulador hidroxicloroquina pode evitar os efeitos trombogênicos dos anticorpos antifosfolipídeos.[88]Schmidt-Tanguy A, Voswinkel J, Henrion D, et al. Antithrombotic effects of hydroxychloroquine in primary antiphospholipid syndrome patients. J Thromb Haemost. 2013 Oct;11(10):1927-9.
http://www.ncbi.nlm.nih.gov/pubmed/23902281?tool=bestpractice.com
[89]Espinola RG, Pierangeli SS, Gharavi AE, et al. Hydroxychloroquine reverses platelet activation induced by human IgG antiphospholipid antibodies. Thromb Haemost. 2002 Mar;87(3):518-22.
http://www.ncbi.nlm.nih.gov/pubmed/11916085?tool=bestpractice.com
[90]Edwards MH, Pierangeli S, Liu X, et al. Hydroxychloroquine reverses thrombogenic properties of antiphospholipid antibodies in mice. Circulation. 1997 Dec 16;96(12):4380-4.
https://www.ahajournals.org/doi/full/10.1161/01.cir.96.12.4380
http://www.ncbi.nlm.nih.gov/pubmed/9416907?tool=bestpractice.com
[91]Belizna C. Hydroxychloroquine as an anti-thrombotic in antiphospholipid syndrome. Autoimmun Rev. 2015 Apr;14(4):358-62.
http://www.ncbi.nlm.nih.gov/pubmed/25534016?tool=bestpractice.com
A hidroxicloroquina também pode reduzir o risco de desenvolver anticorpos antifosfolipídeos persistentemente positivos e anticoagulante lúpico.[92]Nuri E, Taraborelli M, Andreoli L, et al. Long-term use of hydroxychloroquine reduces antiphospholipid antibodies levels in patients with primary antiphospholipid syndrome. Immunol Res. 2017 Feb;65(1):17-24.
http://www.ncbi.nlm.nih.gov/pubmed/27406736?tool=bestpractice.com
[93]Broder A, Putterman C. Hydroxychloroquine use is associated with lower odds of persistently positive antiphospholipid antibodies and/or lupus anticoagulant in systemic lupus erythematosus. J Rheumatol. 2013 Jan;40(1):30-3.
https://www.jrheum.org/content/40/1/30.long
http://www.ncbi.nlm.nih.gov/pubmed/22859353?tool=bestpractice.com
Portanto, o tratamento combinado com doxiciclina e hidroxicloroquina é recomendado em pacientes com anticorpos aCL à IgG ≥75 GPLU. Os pacientes recebem receber essa terapia combinada até redução dos níveis de anticorpo aCL da IgG para <75 GPLU. Pacientes com deficiência conhecida de glicose-6-fosfato desidrogenase (G6PD) não devem ser tratados com hidroxicloroquina.
Pacientes com infecção aguda e valvopatia significativa têm altíssimo risco de endocardite, que pode ser fatal se deixada sem tratamento. Para esses pacientes, recomenda-se um ciclo de 12 meses de profilaxia antibiótica com a combinação de doxiciclina associada a hidroxicloroquina. Um estudo descobriu que esse tratamento combinado é altamente eficaz em evitar endocardite em pacientes com risco.[45]Million M, Walter G, Thuny F, et al. Evolution from acute Q fever to endocarditis is associated with underlying valvulopathy and age and can be prevented by prolonged antibiotic treatment. Clin Infect Dis. 2013 Sep;57(6):836-44.
https://academic.oup.com/cid/article/57/6/836/330624
http://www.ncbi.nlm.nih.gov/pubmed/23794723?tool=bestpractice.com
Essa profilaxia também é recomendada para pacientes com história de enxerto vascular ou aneurisma que apresentaram uma PET/TC com PET com 18-fluordesoxiglucose (FDG) negativa durante a infecção aguda.
Pacientes com infecção aguda e imunodeficiência grave (por exemplo, pacientes transplantados, pacientes em quimioterapia ou corticoterapia, pacientes HIV-positivos e <200 células T CD4+ e pacientes com neoplasia hematológica) têm alto risco de desenvolver infecções focalizadas persistentes, como endocardite.[94]Fenollar F, Fournier PE, Carrieri MP, et al. Risks factors and prevention of Q fever endocarditis. Clin Infect Dis. 2001 Aug 1;33(3):312-6.
https://academic.oup.com/cid/article/33/3/312/277191
http://www.ncbi.nlm.nih.gov/pubmed/11438895?tool=bestpractice.com
Recomenda-se monoterapia com doxiciclina para esses pacientes. A hidroxicloroquina não é recomendada para esses pacientes. Em quem tem imunodeficiência em longo prazo, recomenda-se doxiciclina em longo prazo até que a imunossupressão seja resolvida, pois a infecção pode se reativar vários meses após a infecção primária em imunocomprometidos.
Muitos medicamentos (por exemplo, doxiciclina, fluoroquinolonas) podem não ser recomendados para gestantes. A terapia em longo prazo (≥5 semanas) com sulfametoxazol/trimetoprima protege contra complicações obstétricas, incluindo óbito intrauterino, aborto espontâneo e parto prematuro.[26]Anderson A, Bijlmer H, Fournier PE, et al. Diagnosis and management of Q fever - United States, 2013: recommendations from CDC and the Q fever working group. MMWR Recomm Rep. 2013 Mar 29;62(RR-03):1-23.
https://www.cdc.gov/mmwr/preview/mmwrhtml/rr6203a1.htm
http://www.ncbi.nlm.nih.gov/pubmed/23535757?tool=bestpractice.com
[95]Carcopino X, Raoult D, Bretelle F, et al. Managing Q fever during pregnancy: the benefits of long term cotrimoxazole therapy. Clin Infect Dis. 2007 Sep 1;45(5):548-55.
https://academic.oup.com/cid/article/45/5/548/273863
http://www.ncbi.nlm.nih.gov/pubmed/17682987?tool=bestpractice.com
A alternativa de tratamento para gestantes alérgicas a sulfametoxazol/trimetoprima é a azitromicina.[96]Cerar D, Karner P, Avsic-Zupanc T, et al. Azithromycin for acute Q fever in pregnancy. Wien Klin Wochenschr. 2009;121(13-14):469-72.
http://www.ncbi.nlm.nih.gov/pubmed/19657611?tool=bestpractice.com
Após o parto, mães com infecção aguda deverão ser avaliadas quanto ao risco de infecção focal persistente e receber o devido tratamento.
A C burnetii é encontrada no leite materno; portanto, não se recomenda amamentação para as pacientes infectadas. Para confirmar se a amamentação deve ser interrompida, uma reação em cadeia da polimerase para C burnetii pode ser executada no leite materno.
Infecção focalizada persistente
As infecções focalizadas persistentes incluem endocardite (até 70% dos casos) e infecção vascular (por exemplo, aneurisma, infecção protética vascular).[2]Hartzell JD, Wood-Morris RN, Martinez LJ, et al. Q fever: epidemiology, diagnosis, and treatment. Mayo Clin Proc. 2008 May;83(5):574-9.
https://www.mayoclinicproceedings.org/article/S0025-6196(11)60733-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/18452690?tool=bestpractice.com
O tratamento recomendado para endocardite é doxiciclina oral associada a hidroxicloroquina por 18 meses em pacientes com endocardite de valva nativa, ou por 24 meses em pessoas com endocardite de valva protética ou C burnetii relacionado a corpo estranho (por exemplo, de um dispositivo cardiovascular eletrônico implantado/marca-passo).[2]Hartzell JD, Wood-Morris RN, Martinez LJ, et al. Q fever: epidemiology, diagnosis, and treatment. Mayo Clin Proc. 2008 May;83(5):574-9.
https://www.mayoclinicproceedings.org/article/S0025-6196(11)60733-7/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/18452690?tool=bestpractice.com
[5]Parker NR, Barralet JH, Bell AM. Q fever. Lancet. 2006 Feb 25;367(9511):679-88.
http://www.ncbi.nlm.nih.gov/pubmed/16503466?tool=bestpractice.com
[97]Raoult D, Tissot-Dupont H, Foucault C, et al. Q fever 1985-1998: clinical and epidemiologic features of 1,383 infections. Medicine. 2000 Mar;79(2):109-23.
http://www.ncbi.nlm.nih.gov/pubmed/10771709?tool=bestpractice.com
[84]Million M, Thuny F, Richet H, et al. Long-term outcome of Q fever endocarditis: a 26-year personal survey. Lancet Infect Dis. 2010 Aug;10(8):527-35.
http://www.ncbi.nlm.nih.gov/pubmed/20637694?tool=bestpractice.com
[26]Anderson A, Bijlmer H, Fournier PE, et al. Diagnosis and management of Q fever - United States, 2013: recommendations from CDC and the Q fever working group. MMWR Recomm Rep. 2013 Mar 29;62(RR-03):1-23.
https://www.cdc.gov/mmwr/preview/mmwrhtml/rr6203a1.htm
http://www.ncbi.nlm.nih.gov/pubmed/23535757?tool=bestpractice.com
A cirurgia de substituição da valva deverá ser levada em consideração para todos os pacientes com endocardite infecciosa que tiverem comprometimento hemodinâmico. Os antibióticos devem ser prolongados na ausência de um bom desfecho sorológico (ou seja, diminuição de duas vezes no título de diluição da IgG de fase I e ausência de IgM de fase II em 1 ano).[84]Million M, Thuny F, Richet H, et al. Long-term outcome of Q fever endocarditis: a 26-year personal survey. Lancet Infect Dis. 2010 Aug;10(8):527-35.
http://www.ncbi.nlm.nih.gov/pubmed/20637694?tool=bestpractice.com
Neste caso, o monitoramento deve continuar e os níveis dos medicamentos deverão ser repetidamente medidos, de forma a verificar os níveis medicamentosos terapêuticos. Será necessário obter um parecer especializado se os níveis terapêuticos forem alcançados sem que seja observada melhora nos desfechos sorológicos.
A endocardite pode ser diagnosticada em pacientes com cardiopatia grave (habitualmente na unidade de cirurgia cardíaca) que tenham níveis de IgG de fase I de apenas 1:200.[73]Edouard S, Million M, Lepidi H, et al. Persistence of DNA in a cured patient and positive culture in cases with low antibody levels bring into question diagnosis of Q fever endocarditis. J Clin Microbiol. 2013 Sep;51(9):3012-7.
https://jcm.asm.org/content/51/9/3012.long
http://www.ncbi.nlm.nih.gov/pubmed/23850956?tool=bestpractice.com
[79]Grisoli D, Million M, Edouard S, et al. Latent Q fever endocarditis in patients undergoing routine valve surgery. J Heart Valve Dis. 2014 Nov;23(6):735-43.
http://www.ncbi.nlm.nih.gov/pubmed/25790621?tool=bestpractice.com
Neste contexto específico (ou seja, cirurgia cardíaca e cirurgia vascular e títulos sorológicos baixíssimos entre 1:200 e 1:400), deverá ser prescrito o tratamento da endocardite e da infecção vascular, mesmo na ausência de sintomas infecciosos ou na ausência de reação em cadeia da polimerase positiva, pois o risco de mortalidade é alto se deixado sem tratamento.
Se o paciente tiver marca-passo artificial implantado, recomenda-se um PET/TC com 18F-FDG.[98]Oteo JA, Pérez-Cortés S, Santibáñez P, et al. Q fever endocarditis associated with a cardiovascular implantable electronic device. Clin Microbiol Infect. 2012 Nov;18(11):E482-4.
https://www.clinicalmicrobiologyandinfection.com/article/S1198-743X(14)60761-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/22967271?tool=bestpractice.com
Se o exame mostrar alta captação de FDG no marca-passo, a bolsa do marca-passo deverá ser trocada após 1 mês de tratamento com combinação de doxiciclina e hidroxicloroquina ter sido concluído. Se o exame mostrar alta captação de FDG nos eletrodos intracavitários, não haverá necessidade de remover imediatamente; será realizada uma nova PET/TC com 18F-FDA após 2 meses de tratamento. Será necessária opinião especializada se a captação elevada de FDG persistir no exame.
As infecções vasculares são um desafio muito importante no tratamento da infecção por C burnetii, pois os antibióticos não evitam a ruptura vascular. O tratamento recomendado para infecções vasculares é doxiciclina associada a hidroxicloroquina por 18 meses em pacientes sem material protético vascular ou por 24 meses naqueles com material protético vascular, seguido por remoção cirúrgica do tecido vascular infectado ou do material protético vascular infectado após 3 a 4 semanas de tratamento, a menos que haja necessidade de cirurgia de urgência. A cirurgia está associada a um prognóstico melhorado.[99]Eldin C, Mailhe M, Lions C, et al. Treatment and prophylactic strategy for Coxiella burnetii infection of aneurysms and vascular grafts: a retrospective cohort study. Medicine (Baltimore). 2016 Mar;95(12):e2810.
https://journals.lww.com/md-journal/fulltext/2016/03220/Treatment_and_Prophylactic_Strategy_for_Coxiella.1.aspx
http://www.ncbi.nlm.nih.gov/pubmed/27015164?tool=bestpractice.com
Assim, faz-se necessária a ressecção cirúrgica de rotina do material vascular tecidual/protético infectado.[99]Eldin C, Mailhe M, Lions C, et al. Treatment and prophylactic strategy for Coxiella burnetii infection of aneurysms and vascular grafts: a retrospective cohort study. Medicine (Baltimore). 2016 Mar;95(12):e2810.
https://journals.lww.com/md-journal/fulltext/2016/03220/Treatment_and_Prophylactic_Strategy_for_Coxiella.1.aspx
http://www.ncbi.nlm.nih.gov/pubmed/27015164?tool=bestpractice.com
Em pacientes gravemente imunocomprometidos (como pacientes transplantados, pacientes recebendo quimioterapia ou corticoterapia, pacientes HIV-positivos e <200 células T CD4+ ou pacientes com neoplasia hematológica) com endocardite por C burnetii ou infecção vascular, recomenda-se monoterapia em longo prazo com doxiciclina.
Para todas as infecções focalizadas persistentes e infecções agudas com valvopatia, o monitoramento sorológico e medicamentoso mensal é de suma importância e está associado ao sucesso terapêutico.[100]Rolain JM, Mallet MN, Raoult D. Correlation between serum doxycycline concentrations and serologic evolution in patients with Coxiella burnetii endocarditis. J Infect Dis. 2003 Nov 1;188(9):1322-5.
https://academic.oup.com/jid/article/188/9/1322/801903
http://www.ncbi.nlm.nih.gov/pubmed/14593588?tool=bestpractice.com
[101]Rolain JM, Boulos A, Mallet MN, et al. Correlation between ratio of serum doxycycline concentration to MIC and rapid decline of antibody levels during treatment of Q fever endocarditis. Antimicrob Agents Chemother. 2005 Jul;49(7):2673-6.
https://aac.asm.org/content/49/7/2673.long
http://www.ncbi.nlm.nih.gov/pubmed/15980335?tool=bestpractice.com
[102]Lecaillet A, Mallet MN, Raoult D, et al. Therapeutic impact of the correlation of doxycycline serum concentrations and the decline of phase I antibodies in Q fever endocarditis. J Antimicrob Chemother. 2009 Apr;63(4):771-4.
https://academic.oup.com/jac/article/63/4/771/712547
http://www.ncbi.nlm.nih.gov/pubmed/19218274?tool=bestpractice.com
Os níveis de doxiciclina devem ser mantidos entre 5 e 10 mg/L e os de hidroxicloroquina entre 0.8 e 1.2 mg/L.[103]van Roeden SE, Bleeker-Rovers CP, Kampschreur LM, et al. The effect of measuring serum doxycycline concentrations on clinical outcomes during treatment of chronic Q fever. J Antimicrob Chemother. 2018 Apr 1;73(4):1068-76.
https://academic.oup.com/jac/article/73/4/1068/4792989
http://www.ncbi.nlm.nih.gov/pubmed/29325142?tool=bestpractice.com
As principais causas de fracasso no tratamento e recidiva são falta de monitoramento medicamentoso mensal, níveis insuficientes de medicamento no plasma e ausência de cirurgia em pacientes com infecções vasculares.
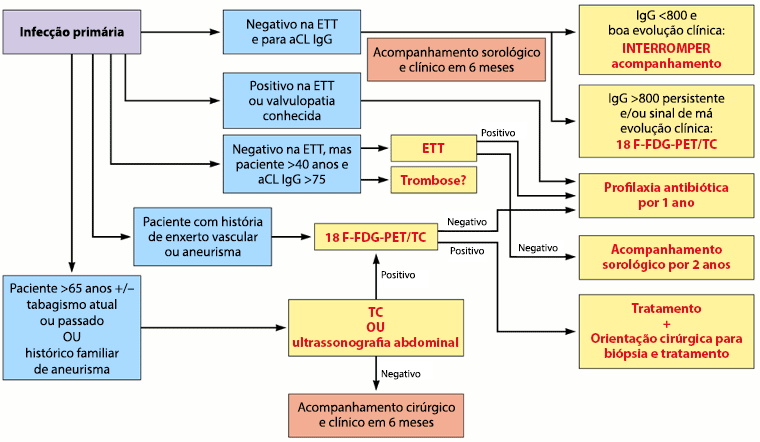
[Figure caption and citation for the preceding image starts]: Algoritmo para o diagnóstico e manejo da infecção por C burnetii. ETT: ecocardiografia transtorácica; anticorpos IgG anticardiolipina (aCL); PET/TC com 18-FDG: PET com 18-fluordesoxiglucose combinada com TCEldin C, et al. Clin Microbiol Rev 2017; usado com permissão [Citation ends].