Abordagem
A investigação diagnóstica de pacientes com suspeita de síndrome de Budd-Chiari (SBC) deve incluir não só confirmação diagnóstica de oclusão da veia hepática, mas também identificação da causa hematológica pró-coagulante subjacente. O diagnóstico de SBC é sugerido por suspeita clínica e deve ser confirmado por técnicas de exame de imagem.
Avaliação clínica
Deve-se suspeitar de SBC em pacientes com uma história pessoal ou familiar de trombofilia que apresentam a tríade clássica de dor abdominal (especialmente dor abdominal no quadrante superior direito), ascite e hepatomegalia.
Os pacientes podem também apresentar ou desenvolver esplenomegalia e hemorragia digestiva em consequência da doença mieloproliferativa subjacente, de trombose da veia porta ou como sequelas de cirrose (com hipertensão portal) que se desenvolve na forma crônica da SBC.
Um exame cardiovascular cuidadoso e a ausência de refluxo hepatojugular são necessários para excluir doenças cardíacas com apresentação semelhante, como regurgitação tricúspide, pericardite constritiva e mixoma atrial direito.
Edema de membros inferiores e veias colaterais dilatadas no tronco indicam compressão da veia cava inferior (VCI) ou trombose.[9]
A forma fulminante da SBC é incomum. Os pacientes desenvolvem rapidamente icterícia, encefalopatia hepática, insuficiência renal e coagulopatia. O fígado fica aumentado e sensível.[10] Os sintomas da forma fulminante da SBC são semelhantes àqueles observados na hepatite aguda.
Exames por imagem
Ultrassonografia com Doppler pulsado e colorido é considerada a investigação de primeira linha para pacientes com suspeita de SBC (sensibilidade e especificidade >85%).[33] A combinação de achados específicos (trombose, estenose, cordão fibroso ou recanalização insuficiente das veias hepáticas e/ou cava) e hipertrofia do lobo caudal têm o maior valor preditivo para identificar pacientes com SBC.
Tomografia computadorizada (TC) abdominal e/ou ressonância nuclear magnética (RNM) são usadas para visualizar as veias hepáticas e todo o comprimento da VCI e demonstram oclusão de veias hepáticas, da VCI ou de ambas.[1] Elas também oferecem melhor visualização de anormalidades parenquimatosas no fígado e áreas necróticas que diferenciam a forma aguda da SBC da doença crônica e podem excluir diagnósticos alternativos.[34] A ressonância nuclear magnética é mais precisa que a TC e permite o delineamento ideal da obstrução venosa para decisões terapêuticas.[35]
A venografia hepática (invasiva) é considerada a ferramenta diagnóstica definitiva. A presença de um padrão em teia de aranha na venografia hepática confirma o diagnóstico da SBC.[1] Ela é necessária para determinar a extensão da trombose e uma medição do gradiente de pressão venosa porto-cava, que geralmente é útil antes de procedimentos de anastomose porto-cava. Ela também facilita a biópsia hepática transjugular, que pode ser útil para avaliar a presença de cirrose e excluir diagnósticos hepáticos alternativos ou concomitantes. A venografia hepática é realizada quando a suspeita de SBC é alta, mesmo na ausência de achados típicos em outros exames de imagem radiológicos. Ela também deve ser realizada quando é considerado um shunt cirúrgico ou percutâneo.
Uma angiografia por ressonância magnética tridimensional com contraste demonstra estruturas vasculares, no fígado e no abdome superior, em vários planos, e também gera informações quanto ao estado parenquimatoso do fígado.[36] Ela é mais útil que outras técnicas de exame de imagem na avaliação das opções de tratamento e na avaliação dos efeitos terapêuticos no período de acompanhamento.[37] É realizada quando é impossível puncionar as veias hepáticas durante a venografia hepática e em pacientes com insuficiência renal, já que a venografia geralmente requer o uso de quantidades consideráveis de meio de contraste com iodo.
A SBC secundária é causada pela compressão externa ou invasão do lúmen venoso por abscessos, tumores ou cistos. Exames de imagem do fígado permitem o reconhecimento de lesões causadoras da SBC secundária.[38][Figure caption and citation for the preceding image starts]: Venografia hepática mostrando "teia de aranha" e trombo na veia cava inferiorLiver Transplantation Journal. 2006;12:S21-S22; reimpresso com permissão de John Wiley & Sons, Inc. [Citation ends].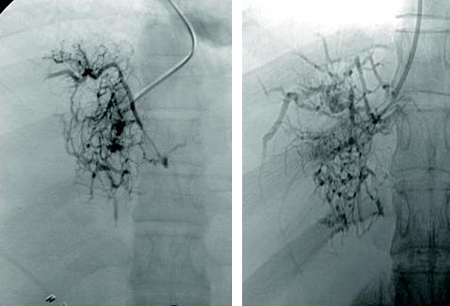
Exames para distúrbios hematológicos subjacentes
Um hemograma completo deve ser realizado para procurar evidências de uma doença mieloproliferativa (DMP) primária como policitemia vera, trombocitose essencial ou mielofibrose. É necessária uma consulta com um hematologista.[1] Cerca de 80% dos pacientes com SBC e com uma DMP possuem a mutação JAK2(V617F).[3][39] Uma metanálise demonstrou que a prevalência conjunta da mutação JAK2(V617F) é de 37% em pacientes com SBC. Depois de excluir a DMP preexistente, a prevalência conjunta diminuiu para 26%. Essa mutação mostrou-se mais específica da trombose em áreas esplâncnicas e está fortemente associada ao desenvolvimento de DMP nesses pacientes.[40]
O teste de mutação JAK2 tem facilitado o diagnóstico de um tipo oculto de DMP. O teste de mutação JAK2 é feito quando o diagnóstico de uma DMP revela-se difícil: por exemplo, se as alterações típicas no sangue periférico, como altos níveis de hemoglobina, plaquetas ou leucócitos, estiverem ausentes ou se os critérios de diagnóstico convencionais não forem atendidos. (Os padrões de referência para um diagnóstico de DMP incluem trombose da veia esplâncnica e agrupamentos de megacariócitos anormais na biópsia da medula óssea, combinados com a formação de colônias de eritrócitos endógenas e a combinação de esplenomegalia acentuada e contagem plaquetária >200 x 10⁹/L [>200 x 10³/microlitro]).[41] No entanto, em casos de suspeita de DMP que são negativos para JAK2, a biópsia da medula óssea é necessária. Os exames para mutação JAK2 e a biópsia da medula óssea substituíram exames usados anteriormente que usavam culturas de progenitores eritroides para demonstrar colônias endógenas.
O rastreamento para trombofilia geralmente é feito se for observada doença hepática em pacientes com trombofilia conhecida e, como uma etiologia combinada é encontrada em pelo menos 25% dos pacientes, a identificação de uma única causa não deve excluir a investigação de outros fatores etiológicos. Os exames incluem:[1]
Teste genético para fator V de Leiden, fator da protrombina, mutação da metilenotetraidrofolato redutase
Níveis séricos da proteína C e S, antitrombina III e homocisteína; anticoagulante lúpico, anticorpos antibeta-2-glicoproteína-1, anticorpos anticardiolipina (síndrome antifosfolipídica)
Citometria de fluxo para células sanguíneas com deficiência de CD55 e CD59 (hemoglobinúria paroxística noturna).[Figure caption and citation for the preceding image starts]: Testes para condições protrombóticas em pacientes com síndrome de Budd-ChiariDo acervo pessoal de Soha Saoud Abdel Moneim, MD, PhD e Vijay H. Shah, MD; usado com permissão [Citation ends].
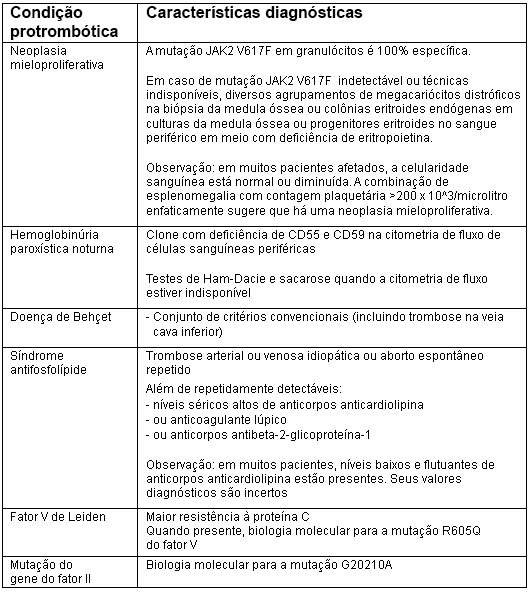 [Figure caption and citation for the preceding image starts]: Testes para condições protrombóticas em pacientes com síndrome de Budd-ChiariDo acervo pessoal de Soha Saoud Abdel Moneim, MD, PhD e Vijay H. Shah, MD; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Testes para condições protrombóticas em pacientes com síndrome de Budd-ChiariDo acervo pessoal de Soha Saoud Abdel Moneim, MD, PhD e Vijay H. Shah, MD; usado com permissão [Citation ends].
Outras investigações
Os resultados do teste da função hepática são inespecíficos, mas quase sempre elevados até certo ponto. Geralmente é observada elevação significativa nos níveis de aspartato e alanina aminotransferases séricas, até 5 vezes ou mais acima do limite superior, nas formas fulminante e aguda da SBC. Isso também pode ser observado em pacientes com hepatite aguda decorrente de etiologias diferentes. Os níveis de fosfatase alcalina e bilirrubina também podem aumentar junto com uma diminuição na albumina sérica. O comprometimento grave do tempo de protrombina ocorre na forma fulminante.[1]
Um nível alto do gradiente de albumina soro-ascite (GASA) em combinação com uma proteína ascítica total >25 g/L (>2.5 g/dL) dá suporte a um diagnóstico de SBC não cirrótica, embora a proteína ascítica possa ser baixa na SBC crônica com cirrose concomitante. No entanto, um GASA alto com ascite alta em proteínas também pode ser observado em causas cardíacas de ascite.[42]
Estudos da função renal e de coagulação devem ser realizados como linha basal e podem ser anormais na SBC fulminante.
A biópsia hepática não é necessária para confirmar o diagnóstico, pois a doença é heterogênea, causando um alto risco de erro na amostra.[43] A biópsia hepática não é recomendada como padrão em crianças, adolescentes ou adultos jovens.[44] Ela é necessária somente no pequeno subconjunto de pacientes nos quais a SBC está relacionada a envolvimento trombótico puro das pequenas veias hepáticas, onde as grandes veias hepáticas e a VCI parecem patentes no exame de imagem.[1][2] Ela também é útil para excluir outros processos como doença veno-oclusiva e cirrose de outras etiologias. Uma biópsia hepática deve ser realizada ao mesmo tempo que a investigação angiográfica para confirmar o diagnóstico (se possível) e avaliar a reserva hepática e o potencial de reversibilidade da lesão hepática antes de procedimentos de shunt. Ela pode ser especialmente útil para avaliar a presença de cirrose, que indica a necessidade de eventual transplante de fígado.
O uso deste conteúdo está sujeito ao nosso aviso legal