Abordagem
O diagnóstico de nevo melanocítico normalmente pode ser feito somente com base em história e exame físico. Existem testes diagnósticos (dermatoscopia, fotografia de corpo inteiro, imagens não invasivas com algoritmos gerados por computador e biópsia) que podem ser usados para aumentar a precisão do diagnóstico. Dermatoscopia ou microscopia de epiluminescência pode ser um adjuvante útil para o exame físico para um médico treinado ao decidir se o nevo em questão é um melanoma. Além disso, a análise espectrofotométrica intracutânea envolve a criação de algoritmos gerados por computador com dispositivos portáteis não invasivos mais recentes, que usam a dispersão da luz para ajudar os médicos a preverem a desorganização e, assim, a probabilidade de malignidade de uma lesão. A biópsia também é necessária quando há suspeita clínica de melanoma.
História
A história da lesão em questão é parte central da definição do diagnóstico de nevo melanocítico. Determinar se a lesão estava presente no nascimento ou se apareceu logo depois apontará para o diagnóstico de nevo congênito. A diferenciação entre benigno e maligno é a principal preocupação clínica ao discutir sobre nevos melanocíticos. Portanto, ao investigar se os nevos estão mudando ou foram adquiridos recentemente, as perguntas devem incluir se o nevo está mudando de cor ou se desenvolveu várias cores, se houve um crescimento relativamente rápido com mudança de tamanho, forma ou superfície ou se houve sangramento fácil, além dos "ABCDEs" do melanoma:[27][28]
A: assimetria
B: borda irregular
C: cor variável
D: diâmetro >6 mm
E: evolução.
Prurido, ardência ou dor podem ou não ser indícios adicionais que alertam o médico para a possibilidade de melanoma, mas a maioria dos pacientes com melanoma é assintomática.[24]
Exame físico
Um exame físico da pele do corpo inteiro é fundamental para o diagnóstico de nevos melanocíticos e a diferenciação entre lesões pigmentadas benignas e malignas.[24] Os pacientes normalmente não têm conhecimento de lesões cutâneas em áreas que não são visíveis.
Nevos adquiridos comuns
Têm uma grande variedade de características clínicas, mas costumam ser simétricos, uniformemente pigmentados, redondos a ovais, homogêneos e com bordas regulares.[7] Eles costumam aparecer como manchas planas de cor marrom, mas também podem ser pápulas mamiladas em forma de domo de cor rosa a marrom.[Figure caption and citation for the preceding image starts]: Um nevo adquirido comumDo acervo de Laurel Schwartz, Thomas Jefferson University [Citation ends].
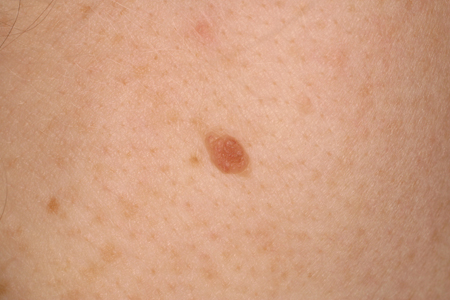 [Figure caption and citation for the preceding image starts]: Um nevo adquirido comumDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Um nevo adquirido comumDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].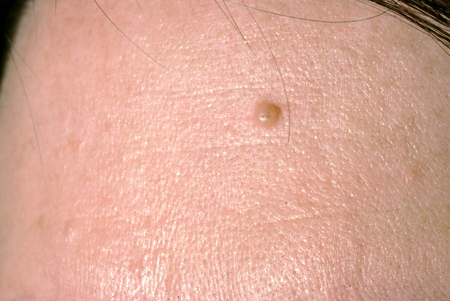
Nevos congênitos pequenos
Podem ser clinicamente indistinguíveis de nevos adquiridos comuns.[6] Os nevos congênitos pequenos a médios geralmente são manchas ou máculas redondas a ovais de cor marrom claro a escuro com uma borda bem definida, e podem ter um pelo proeminente. Os nevos congênitos grandes costumam ficar localizados na parte posterior do tronco, podem ter tamanho considerável e podem ter lesões satélites.[Figure caption and citation for the preceding image starts]: Nevo melanocítico congênito pequenoDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
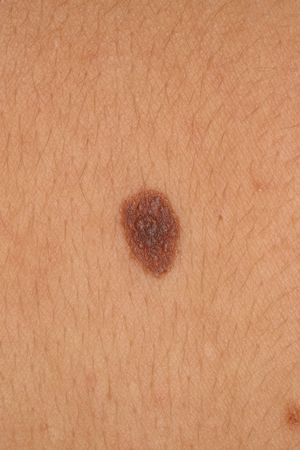 [Figure caption and citation for the preceding image starts]: Um nevo congênito médioDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Um nevo congênito médioDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].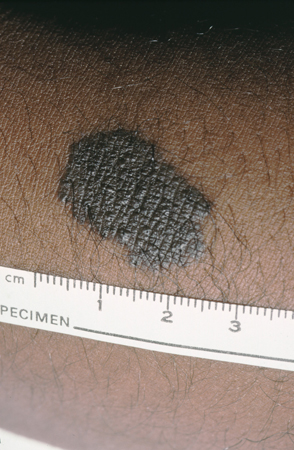 [Figure caption and citation for the preceding image starts]: Nevo melanocítico congênito giganteDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Nevo melanocítico congênito giganteDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].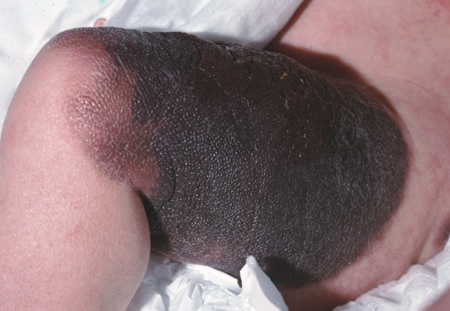
Nevo spilus
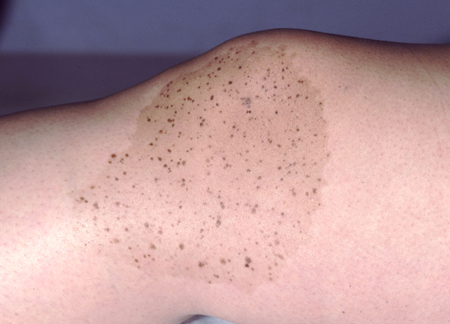
São placas de cor marrom claro cheias de manchas ou pápulas de cor marrom mais escuro. O diagnóstico frequentemente é feito apenas com base nos achados clínicos.[7][29][Figure caption and citation for the preceding image starts]: Um nevo spilusDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
Nevos azuis
São pequenas manchas e pápulas cinza-azuladas a pretas, geralmente encontradas nos membros dorsais, no sacro, na cabeça e no pescoço.[1][5][7][Figure caption and citation for the preceding image starts]: Um nevo azulDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
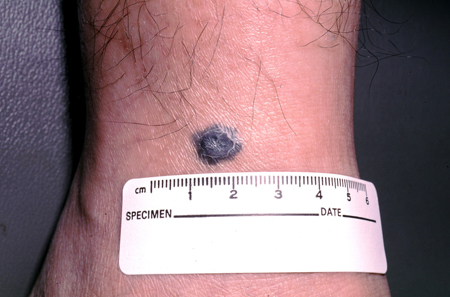 [Figure caption and citation for the preceding image starts]: Um nevo azulDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Um nevo azulDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].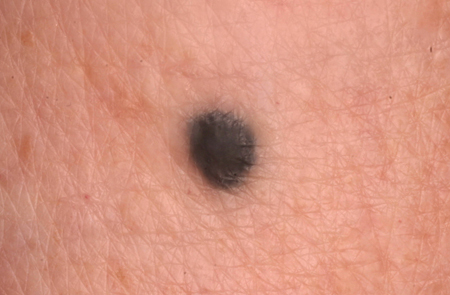
Nevos com halo
Contêm um nevo de morfologia variada com um halo de despigmentação.[7] O nevo normalmente regride depois de algum tempo, deixando uma mancha despigmentada, que pode acabar sendo novamente pigmentada com o passar do tempo. Eles costumam aparecer na parte superior das costas em adultos jovens e crianças, e estão associados a um maior número de nevos e a uma história pessoal ou familiar de vitiligo.[5][7] O diagnóstico frequentemente é feito apenas com base nos achados clínicos.[Figure caption and citation for the preceding image starts]: Um nevo com haloDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].

Nevos de Spitz
São pápulas uniformemente isoladas em forma de domo na cor rosa, marrom claro, vermelha ou marrom avermelhado.[7] Os nevos de Spitz costumam aparecer na cabeça e no pescoço e podem ser isolados ou, raramente, agrupados.[5] Uma variante com pigmentação escura, também conhecida como nevo de célula fusiforme pigmentado (de Reed), geralmente aparece no tronco e nos membros.[5] Os nevos pigmentados de Spitz são pequenos (2 a 5 mm), planos e de cor marrom escuro a preto, em vez de forma de domo e avermelhados.[Figure caption and citation for the preceding image starts]: Nevo de Spitz na orelhaDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
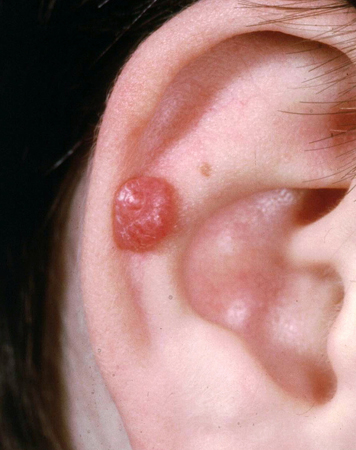 [Figure caption and citation for the preceding image starts]: Nevo de Spitz pigmentadoDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Nevo de Spitz pigmentadoDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].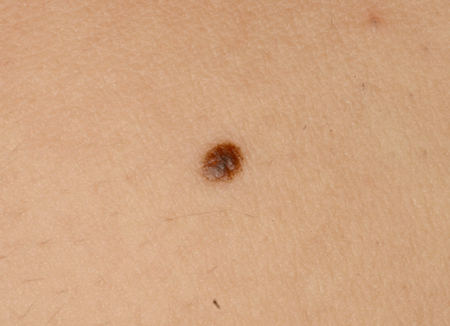
Nevos atípicos, displásicos ou de Clark
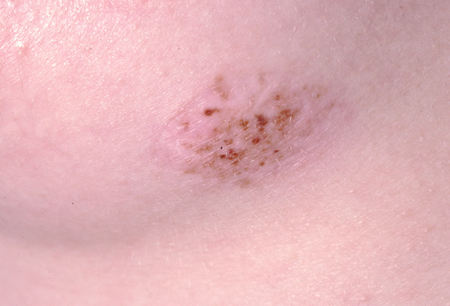
São designações que têm sido usadas para descrever um tipo de nevo que possui algumas características clínicas do melanoma, incluindo os critérios ABCDE (assimetria da lesão, borda irregular ou falta de circunscrição, cor variável, diâmetro >6 mm e evolução), mas em menor grau.[7][17][30][31][32] Normalmente, eles têm >5 mm, são planos ou levemente salientes, possuem cores variadas e bordas irregulares. As lesões variam de marrom claro a marrom escuro, mas podem ter áreas hipopigmentadas e de cor rosa.[Figure caption and citation for the preceding image starts]: Nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
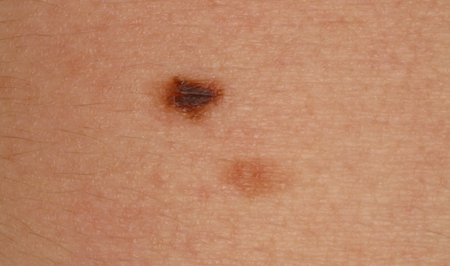 [Figure caption and citation for the preceding image starts]: Nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].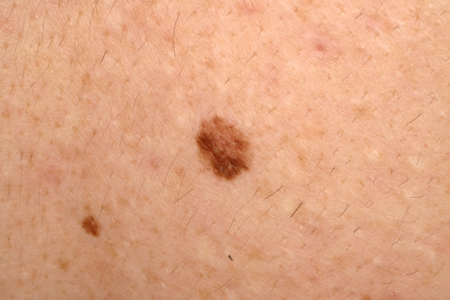
Em pacientes com muitos nevos, alguns médicos falam do sinal do "patinho feio".[33] Esse método utiliza reconhecimento de padrões para identificar lesões discrepantes em relação aos nevos típicos do paciente. Por exemplo, se um paciente tiver vários nevos que satisfazem os critérios ABCDE, usar os nevos do próprio paciente como um controle para encontrar aquele que difere dos demais pode ajudar os médicos no rastreamento de melanoma.
O nevo de Wiesner, o nevo penetrante profundo e o melanocitoma epitelioide pigmentado são neoplasias benignas melanocíticas raras com características histopatológicas e mutações distintas. Eles geralmente são nevos combinados que consistem em duas populações diferentes de melanócitos. Uma população geralmente abriga uma mutação no BRAF, enquanto a outra população, que caracteriza o nevo, abriga uma mutação específica do respectivo nevo.
Nevo de Wiesner (nevo deficiente em BAP1)
O nevo de Wiesner tem características clínicas semelhantes ao nevo adquirido comum ou ao nevo congênito pequeno. A população que caracteriza o nevo consiste em grandes melanócitos epitelioides que apresentam características citológicas de um nevo de Spitz e, portanto, são muitas vezes mal interpretados como tal. O componente epitelioide abriga a mutação na proteína 1 associada ao BRCA1 (BAP1). A grande maioria dos nevos de Wiesner é resultado de mutações somáticas esporádicas no BAP1. Aqueles que abrigam a rara mutação das linhas germinativas em BAP1 têm um risco aumentado de desenvolverem mesoteliomas, melanomas uveais e cutâneos e carcinoma de células renais.[34]
Nevo penetrante profundo
Também conhecido como nevo de células fusiformes plexiformes, o nevo penetrante profundo é um nevo intradérmico raro que geralmente se apresenta em adultos jovens como pápula marrom-escura a preta azulada que pode simular um melanoma.[35]
Melanocitoma epitelioide pigmentado
O melanocitoma epitelioide pigmentado geralmente se apresenta como uma pápula ou nódulo de pigmentação escura em crianças e adultos jovens. As designações anteriores incluem melanoma tipo animal e nevo azul epitelioide. Sabe-se que essas lesões ocorrem em pacientes com complexo de Carney. De acordo com a classificação da Organização Mundial da Saúde (OMS), elas são classificadas como lesões melanocíticas de grau intermediário, em parte devido ao envolvimento frequente dos linfonodos. Por ser uma neoplasia melanocítica rara, não existe acompanhamento em longo prazo de um grande número de casos. O pequeno número de casos com acompanhamento limitado indica uma evolução benigna.[36]
Dermatoscopia
Essa técnica pode ser realizada para aumentar a precisão do diagnóstico de um médico experiente ao decidir se a lesão em questão é um nevo melanocítico ou um melanoma (ou outra neoplasia).[37] Também chamada de microscopia de epiluminescência, pois permite visualizar lesões pigmentadas in vivo. O dermatoscópio deixa a camada cornificada translúcida, resultando na melhor visualização das estruturas subsuperficiais na epiderme viável e na derme superficial. A cor da lesão pode indicar o local do pigmento na pele: cinza-azulado indica melanina na derme, como acontece nos nevos azuis; marrom claro ou escuro indica melanina na junção dermoepidérmica e na camada córnea, como nos nevos adquiridos. A presença de uma rede pigmentar, glóbulos agrupados e pontos pode favorecer um nevo melanocítico benigno.
A dermatoscopia pode ser um adjuvante útil para o exame físico para um médico experiente quando o nevo melanocítico tem algumas características clínicas dos critérios ABCDE. Como esses critérios são subjetivos e variam somente em termos de grau entre nevos displásicos e melanoma, costuma ser um desafio diagnóstico para o médico diferenciar os dois.[17][32] Para essas lesões questionáveis, fotos dermatoscópicas permitem detectar alterações sutis ao longo de um período curto, as quais podem fornecer um indício melhor sobre a natureza da lesão. Um grande repositório de imagens dermatoscópicas foi criado para desenvolver inteligência artificial no futuro para auxiliar no tratamento de lesões melanocíticas.[38][Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo azulDo acervo de Jason Lee, Thomas Jefferson University [Citation ends]. [Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo com rede pigmentar reticularDo acervo de Laurel Schwartz, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo com rede pigmentar reticularDo acervo de Laurel Schwartz, Thomas Jefferson University [Citation ends]. [Figure caption and citation for the preceding image starts]: Dermatoscopia de um padrão pavimentoso com rede pigmentar periféricaDo acervo de Jason B. Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Dermatoscopia de um padrão pavimentoso com rede pigmentar periféricaDo acervo de Jason B. Lee, Thomas Jefferson University [Citation ends].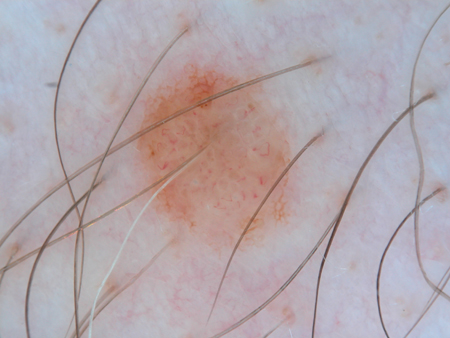 [Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].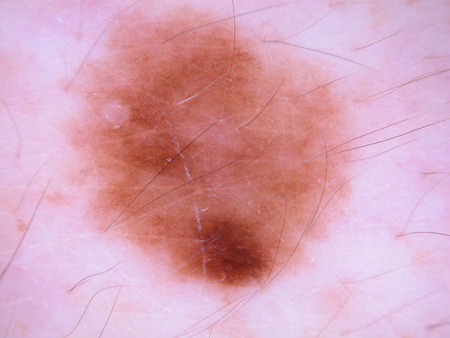 [Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].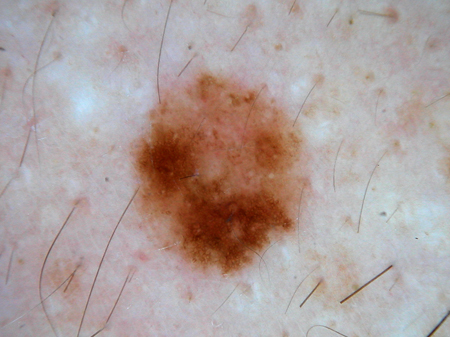 [Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
[Figure caption and citation for the preceding image starts]: Dermatoscopia de um nevo displásico ou de ClarkDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].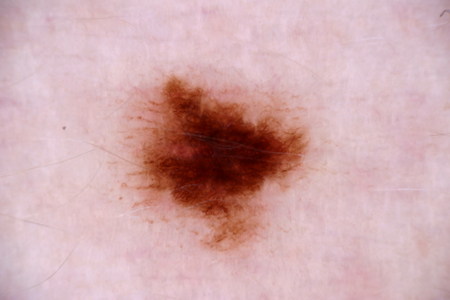
Tecnologias de imagem não invasivas
Vários dispositivos têm sido desenvolvidos para tentar ajudar médicos de atenção primária e dermatologistas na precisão diagnóstica de neoplasias melanocíticas pigmentadas benignas versus malignas. Existem diversas tecnologias de imagem não invasivas diferentes disponíveis para fins clínicos e de pesquisa. Técnicas ópticas, como tomografia de coerência óptica (TCO) e microscopia confocal, são diferentes da dermatoscopia ou microscopia de epiluminescência, que usam imagens multiespectrais para fornecer a visualização do plano horizontal.[39][40] Usando um dispositivo portátil para medir a dispersão da luz de uma neoplasia, essas técnicas de imagem multiespectrais mais recentes utilizam algoritmos gerados por computador para determinar o nível de desorganização e, assim, o risco de malignidade de uma lesão individual.
A análise espectrofotométrica intracutânea (AEI) ou AEIscopia foi desenvolvida para lesões que são neoplasias melanocíticas pigmentadas clinicamente atípicas e, portanto, suspeitas, e não para as lesões que são claramente benignas ou malignas.[41][42]
A SIAscopia tem sido recomendada para uso por médicos de atenção primária para aumentar a precisão do diagnóstico de neoplasias melanocíticas suspeitas antes do encaminhamento para atenção secundária. No entanto, um ensaio clínico randomizado e controlado no Reino Unido não encontrou evidências de que o uso de AEIscopia associado ao escore de atenção primária melhorou a adequação do encaminhamento a um especialista em comparação com a aplicação sistemática das boas práticas (história clínica, exame físico a olho nu, checklist de sete itens) isolada.[43][44]
Um dermatoscópio digital multiespectral aprovado pela Food and Drug Administration (FDA) nos EUA está disponível para uso especificamente por dermatologistas para fornecer uma imagem morfológica tridimensional das neoplasias pigmentadas clinicamente atípicas com, pelo menos, uma característica de melanoma. Em estudos de viabilidade, dependendo dos parâmetros utilizados, esse dispositivo registrou 95% de sensibilidade e 68% de especificidade na detecção de melanomas.[39][45]
Apesar da possível utilidade desses dispositivos, o padrão ouro do diagnóstico continua sendo o exame histológico da neoplasia em questão.
Fotografia de corpo inteiro
Alguns centros especializados em lesões pigmentadas utilizam a fotografia de corpo inteiro como adjuvante para auxiliar na identificação de alterações nos nevos a fim de detectar melanomas em estágios iniciais.[32] Quando executada de forma ideal, essa prática tranquiliza o paciente e o médico, e pode resultar em menos excisões de nevos benignos. As limitações dessa abordagem são o fato de que alterações em nevos não implicam necessariamente uma transformação maligna, pois cada nevo tem uma história natural ao longo da vida do paciente.
Biópsia
Os motivos da biópsia clínica para diagnóstico histopatológico devem ser considerados se houver suspeita clínica de melanoma; se houver história de alteração da lesão, respaldada pelo exame físico; e/ou se houver alta suspeita de características atípicas sugestivas de melanoma.[46]
Nevos displásicos são um tipo de nevo benigno que pode ser clinicamente difícil de diferenciar de melanoma, pois possuem algumas características dos critérios ABCDE, mas em grau menor que melanomas. É importante entender que eles são um tipo de nevo benigno e a biópsia não deve ser feita indiscriminadamente.[17][32][47][48] A maioria dos melanomas surge 'de novo', e não em associação com um nevo, de modo que a remoção profilática de nevos não é justificada.[32][47][48] A biópsia deve ser reservada para lesões sugestivas de alterações malignas; a remoção de todos os nevos displásicos não é recomendada.[1][4][5][30][31][32][47][48] Se o médico tiver dúvidas quanto à distinção entre nevo melanocítico e melanoma, deve-se considerar encaminhamento a um dermatologista. Outros motivos para biópsia ou remoção podem se basear no desejo do paciente, por exemplo, se a lesão for traumatizada ou irritada várias vezes, se sangrar ou coçar e por cosmese. Alguns médicos, principalmente cirurgiões plásticos e de reconstrução, recomendam a ressecção cirúrgica profilática de nevos melanocíticos congênitos gigantes em alguns casos para diminuir a carga melanocítica e possivelmente reduzir o risco de melanoma.[49] Isso é controverso, pois metade dos melanomas que surgem em nevos congênitos gigantes aparecem em locais extracutâneos. No entanto, a excisão cirúrgica de nevos congênitos gigantes pode ser feita por outros motivos, incluindo o benefício psicológico devido à aparência estética da lesão.[49]
A técnica de biópsia é um componente importante para definir o diagnóstico.[5][24][46] Métodos comuns para coletar amostras de nevos melanocíticos incluem biópsia por lâmina, punção e excisão. Nevos removidos de modo incompleto resultam em nevo persistente ou recorrente, que pode mostrar um padrão clínico e histológico de pseudomelanoma. Pode ser um dilema diagnóstico para o histopatologista.[50][51] Uma biópsia por excisão, na qual a lesão inteira é removida com margens pequenas, geralmente é o método preferido para remoção de nevos melanocíticos, além de ser a biópsia mais apropriada para lesões pigmentadas com suspeita clínica de melanoma.[24][32][46] Biópsias por excisão removem erros de amostragem, fornecendo ao patologista a arquitetura completa da lesão para garantir um diagnóstico preciso, e são a melhor forma de garantir a remoção completa da lesão com margens de segurança.[46]
A análise histopatológica revela uma coleção localizada e bem aninhada de melanócitos com aparência arquitetônica e citológica benigna. Dependendo da localização dos melanócitos, o nevo pode ser classificado como juncional (epidérmico), dérmico (na derme) ou composto (epidérmico e dérmico), e a maioria dos nevos adquiridos é classificada dessa maneira.
Nevos congênitos envolvem a derme inferior, são espalhados entre grupos de colágeno, seguem estruturas anexas da pele e, em lesões gigantes, podem se estender na gordura subcutânea e até envolver a fáscia e o músculo.[52]
O nevo spilus tem hiperplasia melanocítica lentiginosa de fundo, pontuada por melanócitos aninhados ou solitários em maior número.
Nevos azuis comuns têm melanócitos fusiformes com depósito de melanina na derme.
Nevos com halo mostram um infiltrado linfo-histiocitário denso tipo faixa na derme papilar, com melanócitos aninhados na epiderme.
Nevos de Spitz têm grandes ninhos de melanócitos fusiformes ou epitelioides. Histologicamente, eles podem mimetizar melanoma, embora sejam um processo benigno.
Nevos atípicos, displásicos ou de Clark têm uma arquitetura característica de melanócitos na ponta das cristas da rede alongadas que são rodeadas por um fino aro de esclerose (fibrose concêntrica e lamelar).[7][17][31][47][48] Infiltrados linfocíticos irregulares e histiócitos com melanina também costumam estar presentes na derme. Quando o componente intradérmico está presente, os melanócitos estão presentes dentro da derme papilar expandida no centro da lesão. A arquitetura epidérmica encontrada em nevos melanocíticos displásicos não é exclusiva, e pode ser encontrada em outros nevos melanocíticos, especialmente em nevos congênitos pequenos. Aqueles que acreditam que nevos displásicos são lesões precursoras de melanoma falam em displasia melanocítica e usam um sistema de classificação histológica de nível leve, moderado e grave para descrever o distúrbio arquitetônico e a atipia citológica, implicando uma progressão gradual de nevo para melanoma. A presença de atipia citológica deve ser "aleatória". Não há abordagem padrão ou diretriz sobre quais níveis necessitam de excisão adicional; isso fica a critério do médico ou dermatopatologista. Geralmente, a excisão não é realizada em nevos levemente displásicos, mas nevos com displasia moderada a grave são removidos de forma rotineira. Quando os desfechos da excisão de nevos que foram categorizados histologicamente como leve ou moderadamente displásicos foram examinados não revelou presença de melanomas, e a ocorrência de alterações clinicamente significativa foi muito rara, indicando que a excisão subsequente a nevos leve ou moderadamente displásicos diagnosticados na biópsia é com frequência desnecessária.[53][54][55][56] À luz desses achados, foi publicada uma declaração de consenso que desencoraja uma nova excisão dos nevos displásicos leves a moderados.[57] Além disso, a OMS recomenda uma classificação histológica mais simples de baixo e alto graus, abandonando a escala de classificação de leve, moderada e grave.[8] A implicação é que apenas os de alto grau devem ser excisados completamente.
Apesar do nome, a correlação clínica e histológica de atipia nos nevos displásicos é insatisfatória. Por esse motivo, e como muitos médicos acreditam que esses nevos não são lesões precursoras de melanoma, uma alternativa é classificar esses nevos como nevos de Clark. Esse epônimo é usado para enfatizar que esses nevos são benignos com um padrão histológico específico que pode ser clinicamente difícil de diferenciar do melanoma com base no cumprimento dos critérios ABCDE.
Embora o índice de concordância entre os patologistas seja excelente no diagnóstico de nevos rotineiros e melanomas invasivos espessos, essa taxa é, no melhor dos casos, de baixa a moderada para nevos de Spitz, classificação de nevos displásicos, melanoma in situ e melanomas finos, ilustrando a natureza altamente subjetiva e a limitação do diagnóstico padrão ouro.[58]
Um teste de tape stripping não invasivo para perfil genético foi desenvolvido com uma sensibilidade relatada de 95% e uma especificidade de 60%, apresentando um valor preditivo negativo de 99%.[59] Como é um teste relativamente novo que não foi validado independentemente, ele ainda não é amplamente utilizado. O teste detecta a expressão dos genes PRAME e LINC00518 associados ao melanoma, e a mutação TERT, encontrada na maioria dos melanomas.
Foram desenvolvidos testes moleculares adjuvantes para melhorar a classificação das lesões melanocíticas. Foi desenvolvido um ensaio de perfil da expressão de 23 genes que diferencia melanomas de nevos com uma sensibilidade de 93.8% e especificidade de 96.2%.[60]
Para lesões melanocíticas spitzoides histológicas ambíguas, os histopatologistas confiam cada vez mais na análise citogenética molecular para facilitar o diagnóstico, especialmente para lesões spitzoides atípicas.[61] Sabe-se que os melanomas abrigam aberrações cromossômicas diferentes dos nevos de Spitz e de outros nevos melanocíticos. Aberrações no número de cópias de ácido desoxirribonucleico (DNA) podem ser detectadas por meio da hibridização in situ fluorescente (FISH) e hibridização genômica comparativa (CGH).[62] Enquanto a CGH examina todo o genoma, a FISH detecta loci específicos de cromossomos com sondas disponíveis. As sondas FISH comercialmente disponíveis incluem alvos para 6p25 (RREB1), 6q23 (MYB), 11q13 (CCND1), CEP6 (sonda centromérica para cromossomo 6) e 9p21 (CDKN2A). Ganhos na 6p25 e 11q13 e deleções homozigóticas na 9p21 foram relatadas como de alta associação ao melanoma.[61] Relatou-se que a sensibilidade e a especificidade da FISH para o diagnóstico do melanoma atingem até 94% e 98%, respectivamente.[61] Embora esses resultados tenham sido validados para lesões claras, a validação para as lesões melanocíticas ambíguas está em andamento.
[Figure caption and citation for the preceding image starts]: Um nevo recorrente ou persistenteDo acervo de Jason Lee, Thomas Jefferson University [Citation ends].
A aplicação da coloração imuno-histoquímica PRAME (antígeno PReferencialmente expresso no MElanoma) em lesões melanocíticas ambíguas tem sido amplamente adotada por patologistas, pois a maioria dos nevos melanocíticos não se coram para esse marcador.[63]
À medida que o diagnóstico molecular continua avançando, ferramentas diagnósticas adicionais estão surgindo para auxiliar no manejo e no diagnóstico das lesões melanocíticas. A mutação no gene promotor TERT é encontrada em aproximadamente 80% dos melanomas. A presença de mutação no gene TERT é útil para diferenciar um melanoma de um nevo.[64]
Demonstração de técnicas de injeção usadas para administrar anestesia local, para teste cutâneo de alergia e teste tuberculínico cutâneo.
O uso deste conteúdo está sujeito ao nosso aviso legal
