El reconocimiento y tratamiento tempranos de la sepsis es clave para lograr mejores resultados. La Surviving Sepsis Campaign ha elaborado guías de práctica clínica sobre el tratamiento que siguen siendo los estándares de aceptación más generalizados.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
La práctica recomendada actual está basada en la evidencia de paquetes de medidas en la sepsis.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[121]Rhodes A, Phillips G, Beale R, et al. The Surviving Sepsis Campaign bundles and outcome: results from the International Multicentre Prevalence Study on Sepsis (the IMPreSS study). Intensive Care Med. 2015 Sep;41(9):1620-8.
http://www.ncbi.nlm.nih.gov/pubmed/26109396?tool=bestpractice.com
[122]Levy MM, Rhodes A, Phillips GS, et al. Surviving Sepsis Campaign: association between performance metrics and outcomes in a 7.5-year study. Intensive Care Med. 2014 Nov;40(11):1623-33.
https://link.springer.com/article/10.1007/s00134-014-3496-0
http://www.ncbi.nlm.nih.gov/pubmed/25270221?tool=bestpractice.com
[123]Seymour CW, Gesten F, Prescott HC, et al. Time to treatment and mortality during mandated emergency care for sepsis. N Engl J Med. 2017 Jun 8;376(23):2235-44.
https://www.nejm.org/doi/10.1056/NEJMoa1703058
http://www.ncbi.nlm.nih.gov/pubmed/28528569?tool=bestpractice.com
[124]Kahn JM, Davis BS, Yabes JG, et al. Association between state-mandated protocolized sepsis care and in-hospital mortality among adults with sepsis. JAMA. 2019 Jul 16;322(3):240-50.
https://jamanetwork.com/journals/jama/fullarticle/2738290
http://www.ncbi.nlm.nih.gov/pubmed/31310298?tool=bestpractice.com
Entre ellas se incluyen:
Obtener hemocultivos antes de la administración de antibióticos
Administrar antibióticos de amplio espectro que ataquen al agente o agentes patógenos
Se debe administrar 30 mL/kg de cristaloide para la hipotensión o el lactato ≥4 mmol/L (≥36 mg/dL), si no se presentan contraindicaciones
Obtener mediciones en series de lactato en sangre
Usar vasopresores para mantener una presión arterial media (PAM) ≥65 mmHg en pacientes refractarios a la fluidoterapia
En pacientes con lactato inicial ≥4 mmol/L (≥36 mg/dL) o hipotensión persistente (es decir, PAM <65 mmHg), evaluación del estado del volumen y perfusión mediante repetición de un examen específico (incluyendo las constantes vitales y los hallazgos cardiopulmonares, llenado capilar, pulso y en la piel) o dos de los métodos siguientes:
Medición de la presión venosa central
Medición de la saturación de oxígeno venoso central
Ultrasonido cardiovascular a pie de cama
Evaluación dinámica de la respuesta a los líquidos con elevación pasiva de la pierna o sobrecarga líquida.
Los seis factores para el tratamiento de la sepsis
Uno de los grupos que trabaja con las terapias básicas, la “Sepsis Six", ha demostrado mejorar los resultados de los pacientes con sepsis. Si los seis factores se aplican en el transcurso de la primera hora posterior al reconocimiento de la sepsis, la mortalidad asociada se reduce hasta un 50%.[68]Daniels R, Nutbeam I, McNamara G, et al. The sepsis six and the severe sepsis resuscitation bundle: a prospective observational cohort study. Emerg Med J. 2011 Jun;28(6):507-12.
http://www.ncbi.nlm.nih.gov/pubmed/21036796?tool=bestpractice.com
Los seis factores son los siguientes:
Administrar oxígeno para mantener saturaciones de oxígeno objetivo superior al 94% (o del 88% al 92% en personas con riesgo de insuficiencia respiratoria hipercápnica)
Tomar hemocultivos y considerar otras muestras
Administrar antibióticos intravenosos.
Iniciar la rehidratación intravenosa.
Verificar el nivel de lactato en serie
Monitorizar la diuresis a cada hora.
Los pacientes refractarios a los tratamientos iniciales, en especial aquellos con shock séptico, pueden requerir monitorización invasiva y la consideración de soporte orgánico (p. ej., catéter venoso central y vasopresores), por lo que bien se podría necesitar manejo en una unidad de cuidados intensivos (UCI) o de cuidados intermedios.
Un aspecto de la intervención básica, la administración de sobrecargas líquidas rápidas adecuadas, tiene como objetivo restablecer el desequilibrio entre el suministro y el requerimiento de oxígeno de los tejidos. Los pacientes que no responden a la administración rápida de volúmenes adecuados de fluidoterapia intravenosa presentan shock séptico. La prioridad inmediata en este grupo de pacientes es el restablecimiento de la circulación y del suministro de oxígeno.
La fluidoterapia temprana dirigida por objetivos era el estándar de oro en la atención.[64]Rivers E, Nguyen B, Havstad S, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med. 2001 Nov 8;345(19):1368-77.
https://www.nejm.org/doi/10.1056/NEJMoa010307
http://www.ncbi.nlm.nih.gov/pubmed/11794169?tool=bestpractice.com
[66]Jones AE, Focht A, Horton JM, et al. Prospective external validation of the clinical effectiveness of an emergency department-based early goal-directed therapy protocol for severe sepsis and septic shock. Chest. 2007 Aug;132(2):425-32.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2703721
http://www.ncbi.nlm.nih.gov/pubmed/17573521?tool=bestpractice.com
[67]Puskarich MA, Marchick MR, Kline JA, et al. One year mortality of patients treated with an emergency department based early goal directed therapy protocol for severe sepsis and septic shock: a before and after study. Crit Care. 2009;13(5):R167.
https://ccforum.biomedcentral.com/articles/10.1186/cc8138
http://www.ncbi.nlm.nih.gov/pubmed/19845956?tool=bestpractice.com
[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[110]Freire AX, Bridges L, Umpierrez GE, et al. Admission hyperglycemia and other risk factors as predictors of hospital mortality in a medical ICU population. Chest. 2005 Nov;128(5):3109-16.
http://www.ncbi.nlm.nih.gov/pubmed/16304250?tool=bestpractice.com
[125]Gerlach H, Keh D. Sepsis in 2003: are we still in the middle of nowhere? Curr Opin Anaesthesiol. 2004 Apr;17(2):97-106.
http://www.ncbi.nlm.nih.gov/pubmed/17021536?tool=bestpractice.com
[126]Trzeciak S, Dellinger RP. Other supportive therapies in sepsis: an evidence-based review. Crit Care Med. 2004 Nov;32(11 suppl):S571-7.
http://www.ncbi.nlm.nih.gov/pubmed/15542966?tool=bestpractice.com
Sin embargo, varios estudios prospectivos aleatorizados no han encontrado ningún beneficio discernible con esta terapia sobre el cuidado habitual.[127]Yealy DM, Kellum JA, Huang DT, et al; ProCESS Investigators. A randomized trial of protocol-based care for early septic shock. N Engl J Med. 2014 May 1;370(18):1683-93.
https://www.nejm.org/doi/10.1056/NEJMoa1401602
http://www.ncbi.nlm.nih.gov/pubmed/24635773?tool=bestpractice.com
[128]Peake SL, Delaney A, Bailey M, et al; ARISE Investigators; ANZICS Clinical Trials Group. Goal-directed resuscitation for patients with early septic shock. N Engl J Med. 2014 Oct 16;371(16):1496-506.
https://www.nejm.org/doi/full/10.1056/NEJMoa1404380
http://www.ncbi.nlm.nih.gov/pubmed/25272316?tool=bestpractice.com
[129]Mouncey PR, Osborn TM, Power GS, et al. Trial of early, goal-directed resuscitation for septic shock. N Engl J Med. 2015 Apr 2;372(14):1301-11.
https://www.nejm.org/doi/full/10.1056/NEJMoa1500896
http://www.ncbi.nlm.nih.gov/pubmed/25776532?tool=bestpractice.com
[130]Andrews B, Muchemwa L, Kelly P, et al. Simplified severe sepsis protocol: a randomized controlled trial of modified early goal-directed therapy in Zambia. Crit Care Med. 2014 Nov;42(11):2315-24.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4199893
http://www.ncbi.nlm.nih.gov/pubmed/25072757?tool=bestpractice.com
[131]Mouncey PR, Osborn TM, Power GS, et al. Protocolised Management In Sepsis (ProMISe): a multicentre randomised controlled trial of the clinical effectiveness and cost-effectiveness of early, goal-directed, protocolised resuscitation for emerging septic shock. Health Technol Assess. 2015 Nov;19(97):i-xxv;1-150.
https://www.journalslibrary.nihr.ac.uk/hta/hta19970/#/full-report
http://www.ncbi.nlm.nih.gov/pubmed/26597979?tool=bestpractice.com
Sin embargo, las premisas centrales de la terapia temprana dirigida por objetivos (p. ej., restauración del volumen circulatorio, corrección de la hipotensión y evaluación del gasto cardíaco) siguen siendo importantes para el manejo de la sepsis y se han convertido ahora en una práctica estándar en muchos servicios de urgencias.
Es esencial la monitorización de las constantes vitales y de la respuesta a la fluidoterapia. La evaluación de la oxigenación por medio de la oximetría de pulso y las mediciones seriadas del lactato pueden ser útiles, junto con la supervisión de la diuresis. Si el nivel de lactato no mejora con la terapia, se trata de un desenlace desfavorable. Se ha demostrado que la eliminación de lactato presenta una correlación positiva con la supervivencia.[88]Nguyen HB, Rivers EP, Knoblich BP, et al. Early lactate clearance is associated with improved outcome in severe sepsis and septic shock. Crit Care Med. 2004 Aug;32(8):1637-42.
http://www.ncbi.nlm.nih.gov/pubmed/15286537?tool=bestpractice.com
A todos los pacientes que reciben vasopresores se les debe insertar un catéter arterial tan pronto como sea posible con el fin de controlar con mayor precisión la presión arterial.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
En una revisión sistemática de pacientes adultos gravemente enfermos, incluidos los pacientes con sepsis, se informó de un aumento de la mortalidad entre los que recibían una oxigenoterapia liberal, en comparación con los que recibían oxigenoterapia conservadora. Se sugirió un rango de objetivo SpO₂ de 94% a 96% para todos los pacientes con enfermedades críticas.[132]Chu DK, Kim LH, Young PJ, et al. Mortality and morbidity in acutely ill adults treated with liberal versus conservative oxygen therapy (IOTA): a systematic review and meta-analysis. Lancet. 2018 Apr 28;391(10131):1693-705.
http://www.ncbi.nlm.nih.gov/pubmed/29726345?tool=bestpractice.com
Antibioticoterapia
Antes de la identificación de un agente patógeno, se deben administrar antibióticos de amplio espectro intravenosos.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[133]Kumar A, Ellis P, Arabi Y, et al. Initiation of inappropriate antimicrobial therapy results in a fivefold reduction of survival in human septic shock. Chest. 2009 Nov;136(5):1237-48.
http://www.ncbi.nlm.nih.gov/pubmed/19696123?tool=bestpractice.com
[134]Kumar A, Roberts D, Wood KE, et al. Duration of hypotension prior to initiation of effective antimicrobial therapy is the critical determinant of survival in human septic shock. Crit Care Med. 2006 Jun;34(6):1589-96.
http://www.ncbi.nlm.nih.gov/pubmed/16625125?tool=bestpractice.com
Por cada hora de retraso en el inicio del tratamiento con antibióticos para el shock séptico, hay un aumento del 7.5% al 10.0% en la mortalidad.[134]Kumar A, Roberts D, Wood KE, et al. Duration of hypotension prior to initiation of effective antimicrobial therapy is the critical determinant of survival in human septic shock. Crit Care Med. 2006 Jun;34(6):1589-96.
http://www.ncbi.nlm.nih.gov/pubmed/16625125?tool=bestpractice.com
[135]Kalil AC, Johnson DW, Lisco SJ, et al. Early goal-directed therapy for sepsis: a novel solution for discordant survival outcomes in clinical trials. Crit Care Med. 2017 Apr;45(4):607-14.
http://www.ncbi.nlm.nih.gov/pubmed/28067711?tool=bestpractice.com
El tratamiento de antibióticos debe comenzar una vez que se sospeche de la presencia de sepsis, preferiblemente después de que se hayan obtenido los cultivos.[5]National Institute for Health and Care Excellence. Sepsis: recognition, diagnosis and early management. Sep 2017 [internet publication].
https://www.nice.org.uk/guidance/ng51
[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
La administración oportuna de antibióticos adecuados es de importancia crítica para maximizar las posibilidades de supervivencia.[68]Daniels R, Nutbeam I, McNamara G, et al. The sepsis six and the severe sepsis resuscitation bundle: a prospective observational cohort study. Emerg Med J. 2011 Jun;28(6):507-12.
http://www.ncbi.nlm.nih.gov/pubmed/21036796?tool=bestpractice.com
[136]Gaieski DF, Mikkelsen ME, Band RA, et al. Impact of time to antibiotics on survival in patients with severe sepsis or septic shock in whom early goal-directed therapy was initiated in the emergency department. Crit Care Med. 2010 Apr;38(4):1045-53.
http://www.ncbi.nlm.nih.gov/pubmed/20048677?tool=bestpractice.com
[137]Johnston AN, Park J, Doi SA, et al. Effect of immediate administration of antibiotics in patients with sepsis in tertiary care: a systematic review and meta-analysis. Clin Ther. 2017 Jan;39(1):190-202;e6.
http://www.ncbi.nlm.nih.gov/pubmed/28062114?tool=bestpractice.com
[138]National Institute for Health Research. NIHR Alert: giving immediate antibiotics reduces deaths from sepsis. Apr 2017 [internet publication].
https://evidence.nihr.ac.uk/alert/giving-immediate-antibiotics-reduces-deaths-from-sepsis
[139]Kashiouris MG, Zemore Z, Kimball Z, et al. Supply chain delays in antimicrobial administration after the initial clinician order and mortality in patients with sepsis. Crit Care Med. 2019 Oct;47(10):1388-95.
http://www.ncbi.nlm.nih.gov/pubmed/31343474?tool=bestpractice.com
[140]Sherwin R, Winters ME, Vilke GM, et al. Does early and appropriate antibiotic administration improve mortality in emergency department patients with severe sepsis or septic shock? J Emerg Med. 2017 Oct;53(4):588-95.
http://www.ncbi.nlm.nih.gov/pubmed/28916120?tool=bestpractice.com
[141]Baghdadi JD, Brook RH, Uslan DZ, et al. Association of a care bundle for early sepsis management with mortality among patients with hospital-onset or community-onset sepsis. JAMA Intern Med. 2020 May 1;180(5):707-16.
http://www.ncbi.nlm.nih.gov/pubmed/32250412?tool=bestpractice.com
Los antibióticos se deben administrar de forma dirigida hacia el sitio supuesto de la infección. Aunque no exista evidencia clínica que sugiera el sitio de la infección y se sospeche sepsis, se deben administrar antibióticos de amplio espectro empíricos.
En una revisión sistemática se observó que la infusión prolongada de antibióticos betalactámicos antipseudomona durante al menos 3 horas (en lugar de un bolo o dentro de los 60 minutos) redujo la mortalidad hasta en un 30% en los pacientes con sepsis en cuidados intensivos.[142]Vardakas KZ, Voulgaris GL, Maliaros A, et al. Prolonged versus short-term intravenous infusion of antipseudomonal β-lactams for patients with sepsis: a systematic review and meta-analysis of randomised trials. Lancet Infect Dis. 2018 Jan;18(1):108-20.
http://www.ncbi.nlm.nih.gov/pubmed/29102324?tool=bestpractice.com
Sin embargo, los tiempos de infusión prolongada están fuera de indicación dado que la mayoría de las recomendaciones de administración de los fabricantes aconsejan la infusión de antibióticos betalactámicos durante 15 a 60 minutos.
Conocer los agentes patógenos prevalentes a nivel local y sus patrones de resistencia a antibióticos es importante para decidir un tratamiento empírico.[17]Angus DC, Linde-Zwirble WT, Lidicker J, et al. Epidemiology of severe sepsis in the United States: analysis of incidence, outcome, and associated costs of care. Crit Care Med. 2001 Jul;29(7):1303-10.
http://www.ncbi.nlm.nih.gov/pubmed/11445675?tool=bestpractice.com
[133]Kumar A, Ellis P, Arabi Y, et al. Initiation of inappropriate antimicrobial therapy results in a fivefold reduction of survival in human septic shock. Chest. 2009 Nov;136(5):1237-48.
http://www.ncbi.nlm.nih.gov/pubmed/19696123?tool=bestpractice.com
Las recomendaciones de antibióticos empíricos necesariamente serán individualizadas a nivel institucional, según los protocolos locales de antibióticos. Una vez que se dispone de los resultados de los cultivos y de la sensibilidad, se pueden adecuar los antibióticos según los agentes patógenos conocidos.
Los cultivos se deben repetir (p. ej., a intervalos de 6 u 8 horas) si existen picos de fiebre repetidos o persistentes, o si se identifica un nuevo sitio de infección.
Se deben reducir los antibióticos empíricos tan pronto como se haya identificado un agente patógeno y existan sensibilidades.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[143]Paul M, Dickstein Y, Raz-Pasteur A. Antibiotic de-escalation for bloodstream infections and pneumonia: systematic review and meta-analysis. Clin Microbiol Infect. 2016 Dec;22(12):960-7.
http://www.ncbi.nlm.nih.gov/pubmed/27283148?tool=bestpractice.com
Los antibióticos de fluoroquinolona deben evitarse cuando se disponga de alternativas eficaces y adecuadas y puedan administrarse con prontitud. Las fluoroquinolonas se han asociado a efectos adversos graves, incapacitantes y potencialmente irreversibles, como la tendinitis, la ruptura de tendones, la artralgia, las neuropatías y otros efectos sobre el sistema musculoesquelético o nervioso.[144]European Medicines Agency. Quinolone- and fluoroquinolone-containing medicinal products. Nov 2018 [internet publication].
https://www.ema.europa.eu/en/medicines/human/referrals/quinolone-fluoroquinolone-containing-medicinal-products
[145]US Food and Drug Administration. FDA drug safety communication: FDA updates warnings for oral and injectable fluoroquinolone antibiotics due to disabling side effects. Jul 2016 [internet publication].
https://www.fda.gov/drugs/drug-safety-and-availability/fda-drug-safety-communication-fda-updates-warnings-oral-and-injectable-fluoroquinolone-antibiotics
Además, la Administración de Medicamentos y Alimentos de EE. UU. (FDA) ha emitido advertencias sobre el aumento del riesgo de disección de la aorta, la hipoglucemia significativa y los efectos adversos para la salud mental en los pacientes que toman fluoroquinolonas.[146]US Food and Drug Administration. FDA drug safety communication. FDA warns about increased risk of ruptures or tears in the aorta blood vessel with fluoroquinolone antibiotics in certain patients. Dec 2018 [internet publication].
https://www.fda.gov/drugs/drug-safety-and-availability/fda-warns-about-increased-risk-ruptures-or-tears-aorta-blood-vessel-fluoroquinolone-antibiotics
[147]US Food and Drug Administration. FDA drug safety communication. FDA reinforces safety information about serious low blood sugar levels and mental health side effects with fluoroquinolone antibiotics; requires label changes. Jul 2018 [internet publication].
https://www.fda.gov/drugs/drug-safety-and-availability/fda-reinforces-safety-information-about-serious-low-blood-sugar-levels-and-mental-health-side
Fuente respiratoria
Las infecciones respiratorias representan, aproximadamente, entre el 30% y el 50% de los casos. Los regímenes de tratamiento deben abarcar agentes patógenos respiratorios frecuentes y microorganismos atípicos, tales como Legionella pneumophilia.
Los antibióticos se mencionan con fines orientativos únicamente. Siempre que sea posible, se deben solicitar y seguir políticas nacionales o locales que puedan tomar en cuenta el conocimiento experto de los patrones de sensibilidad.
Las guías de práctica clínica de la American Thoracic Society/Infectious Diseases Society of America (ATS/IDSA) recomiendan que el tratamiento combinado para los pacientes ingresados en el hospital incluya un betalactámico, como la cefotaxima, la ceftriaxona, la ceftarolina o la ampicilina/sulbactámico, con un macrólido, como la azitromicina.[148]Metlay JP, Waterer GW, Long AC, et al. Diagnosis and treatment of adults with community-acquired pneumonia. An official clinical practice guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med. 2019 Oct 1;200(7):e45-67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581ST
http://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Aunque las guías de práctica clínica de la ATS/IDSA recomiendan la claritromicina en estos pacientes, solo está disponible como formulación oral en los EE.UU., por lo que es poco probable que sea útil en este contexto. También puede administrarse una combinación de betalactámicos y fluoroquinolona respiratoria (p. ej., moxifloxacina, levofloxacina) a pacientes con neumonía grave adquirida en la comunidad. Hay evidencias más sólidas de la combinación de betalactámico y macrólido.
Los factores de riesgo de la presencia de Pseudomonas aeruginosa resistente a múltiples medicamentos y de Staphylococcus aureus resistente a la meticilina (SARM) influirán en la elección de los fármacos antimicrobianos y deben evaluarse. Esto incluye el ingreso hospitalario, el aislamiento previo de estos organismos (especialmente del tracto respiratorio), o el uso de antibióticos sistémicos en los 90 días anteriores.[148]Metlay JP, Waterer GW, Long AC, et al. Diagnosis and treatment of adults with community-acquired pneumonia. An official clinical practice guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med. 2019 Oct 1;200(7):e45-67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581ST
http://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
En los pacientes con riesgo de padecer SARM que presenten una neumonía grave, o que hayan tenido un aislamiento respiratorio previo de SARM, se debe añadir vancomicina o linezolid al régimen de combinación empírica de betalactámicos.[148]Metlay JP, Waterer GW, Long AC, et al. Diagnosis and treatment of adults with community-acquired pneumonia. An official clinical practice guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med. 2019 Oct 1;200(7):e45-67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581ST
http://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Los pacientes con infección por Pseudomonas que padecen neumonía grave, o que han tenido un aislamiento respiratorio previo de P aeruginosa, deben ser tratados con piperacilina/tazobactam, cefepime, ceftazidime, imipenem/cilastatina, meropenem o aztreonam, además del régimen empírico de combinación de betalactámicos. La cobertura de las Enterobacterias productoras de betalactámicos de espectro ampliado debe considerarse únicamente sobre la base de los datos microbiológicos del paciente o locales.[148]Metlay JP, Waterer GW, Long AC, et al. Diagnosis and treatment of adults with community-acquired pneumonia. An official clinical practice guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med. 2019 Oct 1;200(7):e45-67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581ST
http://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Fuente de las vías urinarias
Las infecciones urinarias representan, aproximadamente, entre el 10% y el 20% de los casos. Garantizar la permeabilidad de las vías urinarias es vital. La cobertura debe incluir coliformes gramnegativos y Pseudomonas. Los antibióticos se mencionan con fines orientativos únicamente. Siempre que sea posible, se deben solicitar y seguir políticas nacionales o locales que puedan tomar en cuenta el conocimiento experto de los patrones de sensibilidad.
Un régimen de tratamiento adecuado es el uso de una combinación de ampicilina o una cefalosporina, como cefotaxima con gentamicina. La ciprofloxacina es una alternativa adecuada en pacientes con alergia a la penicilina; se sigue recomendando para la pielonefritis aguda o la infección urinaria complicada (considerando cuestiones de seguridad).
Fuente abdominal
Las infecciones derivadas de fuentes abdominales representan, aproximadamente, entre el 20% y el 25% de los casos. Se deben cubrir los microorganismos grampositivos y gramnegativos, incluidos los anaerobios. La peritonitis o los abscesos intraperitoneales requieren un drenaje quirúrgico urgente o un drenaje percutáneo urgente (según corresponda).
Los antibióticos se mencionan con fines orientativos únicamente. Siempre que sea posible, se deben solicitar y seguir políticas nacionales o locales que puedan tomar en cuenta el conocimiento experto de los patrones de sensibilidad.
El tratamiento con ampicilina o cefotaxima con metronidazol y gentamicina es un régimen adecuado, o, alternativamente, piperacilina/tazobactam con gentamicina. Un régimen de tigeciclina y gentamicina es una opción adecuada para pacientes con alergia a la penicilina.
Los pacientes con perforación recurrente del intestino grueso presentan mayor riesgo de fungemia invasiva. A la cobertura antibacteriana se debe agregar un azol, como fluconazol, o una equinocandina, como micafungina. Las especies de Candida no albicans son cada vez más resistentes a los azoles.[46]Solomkin JS, Mazuski J. Intra-abdominal sepsis: newer interventional and antimicrobial therapies. Infect Dis Clin North Am. 2009 Sep;23(3):593-608.
http://www.ncbi.nlm.nih.gov/pubmed/19665085?tool=bestpractice.com
[47]Montravers P, Dupont H, Gauzit R, et al. Candida as a risk factor for mortality in peritonitis. Crit Care Med. 2006 Mar;34(3):646-52.
http://www.ncbi.nlm.nih.gov/pubmed/16505648?tool=bestpractice.com
[149]Pappas PG, Kauffman CA, Andes DR, et al. Clinical practice guideline for the management of candidiasis: 2016 update by the Infectious Diseases Society of America. Clin Infect Dis. 2016 Feb 15;62(4):e1-50.
https://academic.oup.com/cid/article/62/4/e1/2462830
http://www.ncbi.nlm.nih.gov/pubmed/26679628?tool=bestpractice.com
Fuente articular y del tejido blando
Este grupo heterogéneo de infecciones incluye la artritis séptica, las infecciones de heridas, la celulitis y las superinfecciones agudas derivadas de ulceraciones crónicas, y representa aproximadamente, entre el 5% y el 10% de los casos.
También se debe tener un índice de sospecha elevado de fascitis necrosante, que requiere una intervención quirúrgica inmediata (al igual que la artritis séptica). La mayoría de las infecciones son polimicrobianas, y se debe utilizar una cobertura de amplio espectro contra los microorganismos grampositivos y gramnegativos, incluidos los anaerobios.
Los antibióticos se mencionan con fines orientativos únicamente. Siempre que sea posible, se deben solicitar y seguir políticas nacionales o locales que puedan tomar en cuenta el conocimiento experto de los patrones de sensibilidad.
Un régimen adecuado es la flucloxacilina (o tigeciclina en los pacientes alérgicos a la penicilina) junto con el metronidazol. Otra posibilidad es utilizar clindamicina. Si el paciente presenta factores de riesgo para SARM, se debe agregar vancomicina (o, alternativamente, linezolid).
Si existe sospecha de fascitis necrosante, el uso de clindamicina junto con flucoxacilina o tigeciclina sería una opción razonable.
Fuente del sistema nervioso central (SNC)
Las infecciones del SNC son una causa de sepsis relativamente infrecuente aunque potencialmente devastadora que representa menos del 5% de los casos. La septicemia meningocócica puede resultar mortal de forma extremadamente rápida y, si se sobrevive, puede conducir a una mayor morbilidad que otras formas. La antibioticoterapia inmediata en casos donde exista sospecha es esencial.
Los antibióticos se mencionan con fines orientativos únicamente. Siempre que sea posible, se deben solicitar y seguir políticas nacionales o locales que puedan tomar en cuenta el conocimiento experto de los patrones de sensibilidad.
La sospecha de meningitis o septicemia meningocócica se debe tratar de inmediato con una cefalosporina de tercera generación, como ceftriaxona o cefotaxima. Para los pacientes con alergia a la penicilina, la vancomicina con cloranfenicol es una alternativa adecuada. Algunos sugieren la incorporación de rifampicina a cualquier régimen, a fin de ayudar con la penetración.
En el caso de pacientes de más de 50 años de edad y de personas con antecedentes de alcoholismo u otra enfermedad debilitante, o con mayor riesgo de infección por Listeria (p. ej., embarazadas), las cefalosporinas como medicamento único no proporcionan la cobertura adecuada. Siempre que el paciente no sea alérgico a la penicilina, se debe agregar ampicilina al régimen. En el caso de aquellos pacientes alérgicos a la penicilina, se puede utilizar eritromicina o sulfametoxazol/trimetoprima.
En aquellos pacientes con un inicio más lento de los síntomas en el SNC se debe sospechar encefalitis viral. Los virus causan sepsis con extremadamente poca frecuencia, pero el uso temprano de agentes antivirales, como el aciclovir, puede mejorar los resultados.
Los corticosteroides para la meningitis bacteriana pueden mejorar los resultados neurológicos.[150]Brouwer MC, McIntyre P, Prasad K, et al. Corticosteroids for acute bacterial meningitis. Cochrane Database Syst Rev. 2015 Sep 12;(9):CD004405.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD004405.pub5/full
http://www.ncbi.nlm.nih.gov/pubmed/26362566?tool=bestpractice.com
Sepsis de origen desconocido
Se deben tomar medidas intensivas, incluidos los estudios por imágenes, a fin de intentar evaluar la fuente de infección. Se debe administrar cobertura de amplio espectro urgente a fin de incluir todos los agentes patógenos comunes.
Los antibióticos se mencionan con fines orientativos únicamente. Siempre que sea posible, se deben solicitar y seguir políticas nacionales o locales que puedan tomar en cuenta el conocimiento experto de los patrones de sensibilidad.
Los carbapenémicos proporcionan una cobertura adecuadamente amplia, siendo la imipenem/cilastatina o el meropenem algunas de las opciones adecuadas. La piperacilina/tazobactam con gentamicina es una alternativa. Si el paciente presenta factores de riesgo para SARM, se debe agregar vancomicina.
Rehidratación
Se necesita una rehidratación temprana y vigorosa de los fluidos en la hipoperfusión inducida por la sepsis (iniciada en el plazo de 1 hora siguiente a la sospecha de sepsis) con al menos 30 mL/kg de peso corporal de cristaloide administrado dentro de las primeras 3 horas.[151]Levy MM, Evans LE, Rhodes A. The Surviving Sepsis Campaign bundle: 2018 update. Intensive Care Med. 2018 Jun;44(6):925-8.
https://link.springer.com/article/10.1007%2Fs00134-018-5085-0
http://www.ncbi.nlm.nih.gov/pubmed/29675566?tool=bestpractice.com
Se puede necesitar fluidoterapia adicional, pero debe estar guiada por una evaluación clínica detallada del estado hemodinámico del paciente.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
La administración reiterada de bolos de líquidos cristaloides (volumen típico de 500 mL) durante 5 a 30 minutos puede resultar eficaz para corregir la hipotensión como consecuencia de la hipovolemia. Como alternativa, se pueden utilizar bolos de solución coloidal (volumen típico de 250-300 mL), pero no se cuenta con evidencia que apoye el uso de coloides en lugar de otros líquidos como los cristaloides o la albúmina.[152]Choi PTL, Yip G, Quinonez LG, et al. Crystalloids vs. colloids in fluid resuscitation: a systematic review. Crit Care Med. 1999 Jan;27(1):200-10.
http://www.ncbi.nlm.nih.gov/pubmed/9934917?tool=bestpractice.com
[153]Finfer S, Bellomo R, Boyce N, et al; the SAFE Study Investigators. A comparison of albumin and saline for fluid resuscitation in the intensive care unit. N Engl J Med. 2004 May 27;350(22):2247-56.
https://www.nejm.org/doi/full/10.1056/NEJMoa040232
http://www.ncbi.nlm.nih.gov/pubmed/15163774?tool=bestpractice.com
[154]Lewis SR, Pritchard MW, Evans DJ, et al. Colloids versus crystalloids for fluid resuscitation in critically ill people. Cochrane Database Syst Rev. 2018 Aug 3;(8):CD000567.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000567.pub7/full
http://www.ncbi.nlm.nih.gov/pubmed/30073665?tool=bestpractice.com
[155]Roberts I, Blackhall K, Alderson P, et al. Human albumin solution for resuscitation and volume expansion in critically ill patients. Cochrane Database Syst Rev. 2011 Nov 9;(11):CD001208.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001208.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/22071799?tool=bestpractice.com
[156]Rochwerg B, Alhazzani W, Sindi A, et al. Fluid resuscitation in sepsis: a systematic review and network meta-analysis. Ann Intern Med. 2014 Sep 2;161(5):347-55.
http://www.ncbi.nlm.nih.gov/pubmed/25047428?tool=bestpractice.com
[  ]
How do colloids compare with crystalloids for fluid resuscitation in critically ill people?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2307/fullMostrarme la respuesta
]
How do colloids compare with crystalloids for fluid resuscitation in critically ill people?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2307/fullMostrarme la respuesta
Se deben administrar cristaloides y albúmina, según los protocolos locales. La evidencia actual sugiere que la fluidoterapia con soluciones con albúmina es segura, pero la evidencia sobre la eficacia es insuficiente para recomendar su uso por encima de los cristaloides.[156]Rochwerg B, Alhazzani W, Sindi A, et al. Fluid resuscitation in sepsis: a systematic review and network meta-analysis. Ann Intern Med. 2014 Sep 2;161(5):347-55.
http://www.ncbi.nlm.nih.gov/pubmed/25047428?tool=bestpractice.com
[157]Patel A, Laffan MA, Waheed U, et al. Randomised trials of human albumin for adults with sepsis: systematic review and meta-analysis with trial sequential analysis of all-cause mortality. BMJ. 2014 Jul 22;349:g4561. [Erratum in: BMJ. 2014;349:g4850.]
https://www.bmj.com/content/349/bmj.g4561
http://www.ncbi.nlm.nih.gov/pubmed/25099709?tool=bestpractice.com
[158]Delaney AP, Dan A, McCaffrey J, et al. The role of albumin as a resuscitation fluid for patients with sepsis: a systematic review and meta-analysis. Crit Care Med. 2011 Feb;39(2):386-91.
http://www.ncbi.nlm.nih.gov/pubmed/21248514?tool=bestpractice.com
[159]Zou Y, Ma K, Xiong JB, et al. Comparison of the effects of albumin and crystalloid on mortality among patients with septic shock: systematic review with meta-analysis and trial sequential analysis. Sao Paulo Med J. 2018 Sep-Oct;136(5):421-32.
https://www.scielo.br/scielo.php?script=sci_arttext&pid=S1516-31802018000500421&lng=en&tlng=en
http://www.ncbi.nlm.nih.gov/pubmed/30570093?tool=bestpractice.com
Se prefieren los cristaloides equilibrados a la solución salina normal en pacientes en situación crítica en cuidados intensivos.[160]Semler MW, Self WH, Wanderer JP, et al. Balanced crystalloids versus saline in critically ill adults. N Engl J Med. 2018 Mar 1;378(9):829-39.
http://www.ncbi.nlm.nih.gov/pubmed/29485925?tool=bestpractice.com
Las soluciones con almidón pueden ser perjudiciales y deben evitarse.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[161]Rochwerg B, Alhazzani W, Gibson A, et al; FISSH Group (Fluids in Sepsis and Septic Shock). Fluid type and the use of renal replacement therapy in sepsis: a systematic review and network meta-analysis. Intensive Care Med. 2015 Sep;41(9):1561-71.
http://www.ncbi.nlm.nih.gov/pubmed/25904181?tool=bestpractice.com
La evidencia demostró que el uso de soluciones que contienen almidón hidroxietílico (AHE) está asociado con un mayor riesgo de disfunción renal y resultado adverso.[162]Zarychanski R, Abou-Setta AM, Turgeon AF, et al. Association of hydroxyethyl starch administration with mortality and acute kidney injury in critically ill patients requiring volume resuscitation: a systematic review and meta-analysis. JAMA. 2013 Feb 20;309(7):678-88.
https://jamanetwork.com/journals/jama/fullarticle/1653505
http://www.ncbi.nlm.nih.gov/pubmed/23423413?tool=bestpractice.com
Se puede considerar la transfusión de plasma o eritrocitos para tratar deficiencias específicas, pero no se debe utilizar para aumentar el volumen. No se ha demostrado que la transfusión agresiva de eritrocitos mejore los resultados.[163]Holst LB, Haase N, Wetterslev J, et al; TRISS Trial Group; Scandinavian Critical Care Trials Group. Lower versus higher hemoglobin threshold for transfusion in septic shock. N Engl J Med. 2014 Oct 9;371(15):1381-91.
https://www.nejm.org/doi/full/10.1056/NEJMoa1406617
http://www.ncbi.nlm.nih.gov/pubmed/25270275?tool=bestpractice.com
Se debe monitorizar de cerca a los pacientes para detectar signos de sobrecarga de líquidos (p. ej., edema pulmonar o sistémico).[164]Hollenberg SM, Ahrens TS, Annane D, et al. Practice parameters for hemodynamic support of sepsis in adult patients; 2004 update. Crit Care Med. 2004 Sep;32(9):1928-48.
http://www.ncbi.nlm.nih.gov/pubmed/15343024?tool=bestpractice.com
Se ha demostrado que los cambios en el diámetro de la vena cava inferior (VCI) durante la respiración (que se visualizan mediante un ultrasonido a pie de cama) son un medio preciso para juzgar el grado de respuesta a los líquidos y un requisito para seguir con la fluidoterapia intravenosa. En los pacientes que respiran espontáneamente, una VCI colapsada o por colapsar indica que el gasto cardíaco mejorará con la rehidratación adicional. En el paciente ventilado mecánicamente, se espera una respuesta de los fluidos con un aumento del tamaño de la VCI >18% (o visible a simple vista) con ventilación de presión positiva.[165]Feissel M, Michard F, Faller JP, et al. The respiratory variation in inferior vena cava diameter as a guide to fluid therapy. Intensive Care Med. 2004 Sep;30(9):1834-7.
http://www.ncbi.nlm.nih.gov/pubmed/15045170?tool=bestpractice.com
[166]Barbier C, Loubières Y, Schmit C, et al. Respiratory changes in inferior vena cava diameter are helpful in predicting fluid responsiveness in ventilated septic patients. Intensive Care Med. 2004 Sep;30(9):1740-6.
http://www.ncbi.nlm.nih.gov/pubmed/15034650?tool=bestpractice.com
Una revisión sistemática demostró que la elevación pasiva de la pierna es un factor pronóstico preciso de la respuesta a los líquidos en pacientes ventilados, sin importar el modo o la técnica de ventilación, y con variables de flujo (p. ej., gasto cardíaco) con mayor precisión comparado con la presión del pulso.[167]Cherpanath TG, Hirsch A, Geerts BF, et al. Predicting fluid responsiveness by passive leg raising: a systematic review and meta-analysis of 23 clinical trials. Crit Care Med. 2016 May;44(5):981-91.
http://www.ncbi.nlm.nih.gov/pubmed/26741579?tool=bestpractice.com
Control glucémico en pacientes en estado crítico
Se ha producido un cambio de opinión y de práctica en lo que respecta al control glucémico en los pacientes gravemente enfermos, que ha pasado de un control glucémico estricto a objetivos glucémicos más convencionales. Las evidencias sugieren un aumento de los eventos adversos (p. ej., hipoglucemia grave) en los pacientes tratados con un control glucémico estricto (objetivo de glucemia 6.1 mmol/l).[168]Brunkhorst FM, Engel C, Bloos F, et al; German Competence Network Sepsis (SepNet). Intensive insulin therapy and pentastarch resuscitation in severe sepsis. N Engl J Med. 2008 Jan 10;358(2):125-39.
http://www.nejm.org/doi/full/10.1056/NEJMoa070716#t=article
http://www.ncbi.nlm.nih.gov/pubmed/18184958?tool=bestpractice.com
[169]Wiener RS, Wiener DC, Larson RJ. Benefits and risks of tight glucose control in critically ill adults: a meta-analysis. JAMA. 2008 Aug 27;300(8):933-44.
https://jamanetwork.com/journals/jama/fullarticle/182432
http://www.ncbi.nlm.nih.gov/pubmed/18728267?tool=bestpractice.com
Un ensayo aleatorizado controlado internacional demostró un aumento en el riesgo absoluto de muerte a los 90 días de 2.6 puntos porcentuales en el grupo de pacientes sometido a control glucémico intensivo en comparación con el grupo con control glucémico convencional (glucosa sanguínea deseada de 10 mmol/L [180 mg/dL]).[170]Finfer S, Chittock DR, Yu-Shuo Su S, et al; NICE-SUGAR Study Investigators. Intensive versus conventional glucose control in critically ill patients. N Engl J Med. 2009 Mar 26;360(13):1283-97.
https://www.nejm.org/doi/full/10.1056/NEJMoa0810625
http://www.ncbi.nlm.nih.gov/pubmed/19318384?tool=bestpractice.com
La American Diabetes Association recomienda un objetivo de glucosa general de entre 7.8 y 10.0 mmol/L (140-180 mg/dL) en pacientes diabéticos en estado crítico, preferentemente con el uso de un protocolo de infusión de insulina.[171]American Diabetes Association. Standards of Medical Care in Diabetes - 2020. Diabetes Care. 2020 Jan;43(Suppl 1):S1-212.
https://care.diabetesjournals.org/content/43/Supplement_1
La Surviving Sepsis Campaign recomienda el uso de protocolos de infusión de insulina validados que tengan como objetivo un nivel de glucemia <10 mmol/L (180 mg/dL).[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
Inestabilidad hemodinámica persistente
Si la hipotensión persiste, con una PAM <65 mmHg, se debe iniciar la administración de un vasopresor.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[172]Rivers PE, McIntyre L, Morro DC, et al. Early and innovative interventions for severe sepsis and septic shock: taking advantage of a window of opportunity. CMAJ. 2005 Oct 25;173(9):1054-65.
https://www.cmaj.ca/content/173/9/1054.full
http://www.ncbi.nlm.nih.gov/pubmed/16247103?tool=bestpractice.com
El fármaco de elección es la noradrenalina (norepinefrina) administrada por un catéter venoso central, ya que aumenta la PAM.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[173]Avni T, Lador A, Lev S, et al. Vasopressors for the treatment of septic shock: systematic review and meta-analysis. PLoS One. 2015 Aug 3;10(8):e0129305.
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0129305
http://www.ncbi.nlm.nih.gov/pubmed/26237037?tool=bestpractice.com
[174]Møller MH, Claudius C, Junttila E, et al. Scandinavian SSAI clinical practice guideline on choice of first-line vasopressor for patients with acute circulatory failure. Acta Anaesthesiol Scand. 2016 Nov;60(10):1347-66.
https://onlinelibrary.wiley.com/doi/10.1111/aas.12780
http://www.ncbi.nlm.nih.gov/pubmed/27576362?tool=bestpractice.com
Puede agregarse vasopresina o adrenalina a la noradrenalina para lograr la PAM deseada (≥65 mmHg), o puede agregarse vasopresina para eliminar la dependencia a la noradrenalina.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
La dopamina es una opción, pero se debe administrar solamente a pacientes seleccionados, ya que se la ha asociado con una mortalidad mayor que la noradrenalina.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[175]De Backer D, Aldecoa C, Njimi H, et al. Dopamine versus norepinephrine in the treatment of septic shock: a meta-analysis. Crit Care Med. 2012 Mar;40(3):725-30.
http://www.ncbi.nlm.nih.gov/pubmed/22036860?tool=bestpractice.com
[176]Vasu TS, Cavallazzi R, Hirani A, et al. Norepinephrine or dopamine for septic shock: Systematic review of randomized clinical trials. J Intensive Care Med. 2012 May-Jun;27(3):172-8.
http://www.ncbi.nlm.nih.gov/pubmed/21436167?tool=bestpractice.com
[  ]
How does norepinephrine compare with other vasopressors in people with hypotensive shock?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1296/fullMostrarme la respuesta
]
How does norepinephrine compare with other vasopressors in people with hypotensive shock?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1296/fullMostrarme la respuesta
En un metanálisis realizado a nivel de paciente, la fijación de objetivos de presión arterial más elevados (PAM >65 mmHg) no se asoció con una mejoría de la supervivencia a 28 días, independientemente de la presencia de hipertensión o insuficiencia cardíaca previas, en pacientes adultos con shock tratados con vasopresores.[177]Lamontagne F, Day AG, Meade MO, et al. Pooled analysis of higher versus lower blood pressure targets for vasopressor therapy septic and vasodilatory shock. Intensive Care Med. 2018 Jan;44(1):12-21.
http://www.ncbi.nlm.nih.gov/pubmed/29260272?tool=bestpractice.com
Todas las infusiones de medicamentos vasoactivos para corregir el shock se deben administrar por medio de un catéter seguro en una vena central con alto flujo, como mediante un catéter venoso central, excepto que no lo permitan los recursos y que la situación sea urgente. No se recomienda el uso de dosis bajas de dopamina para la protección renal.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
Terapias suplementarias
En pacientes con gasto cardíaco bajo a pesar de una rehidratación adecuada, se pueden agregar inotrópicos (p. ej., dobutamina). La sospecha de gasto cardíaco bajo a partir de la exploración física (tiempos de llenado capilar prolongados, diuresis baja, perfusión periférica deficiente) se puede confirmar mediante el uso de la monitorización del gasto cardíaco o el muestreo de sangre arterial pulmonar o venosa central a fin de medir las saturaciones de oxígeno. La frecuencia cardíaca se debe mantener en <100 lpm a fin de minimizar el requerimiento de oxígeno del miocardio.[172]Rivers PE, McIntyre L, Morro DC, et al. Early and innovative interventions for severe sepsis and septic shock: taking advantage of a window of opportunity. CMAJ. 2005 Oct 25;173(9):1054-65.
https://www.cmaj.ca/content/173/9/1054.full
http://www.ncbi.nlm.nih.gov/pubmed/16247103?tool=bestpractice.com
Las guías de práctica clínica vigentes recomiendan que se administren bajas dosis de corticosteroides solamente a pacientes cuya presión arterial responda de manera deficiente tanto a la rehidratación como al tratamiento con vasopresores.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[178]Annane D, Pastores SM, Rochwerg B, et al. Guidelines for the diagnosis and management of critical illness-related corticosteroid insufficiency (CIRCI) in critically ill patients (Part I): Society of Critical Care Medicine (SCCM) and European Society of Intensive Care Medicine (ESICM) 2017. Crit Care Med. 2017 Dec;45(12):2078-88.
http://www.ncbi.nlm.nih.gov/pubmed/28938253?tool=bestpractice.com
Sin embargo, la evidencia para la administración de corticosteroides a pacientes con sepsis o con shock séptico es mixta.[179]Annane D, Bellissant E, Bollaert PE, et al. Corticosteroids for treating sepsis in children and adults. Cochrane Database Syst Rev. 2019 Dec 6;(12):CD002243.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002243.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/31808551?tool=bestpractice.com
[180]Kalil AC, Sun J. Low-dose steroids for septic shock and severe sepsis: the use of Bayesian statistics to resolve clinical trial controversies. Intensive Care Med. 2011 Mar;37(3):420-9.
http://www.ncbi.nlm.nih.gov/pubmed/21243334?tool=bestpractice.com
[181]Rygård SL, Butler E, Granholm A, et al. Low-dose corticosteroids for adult patients with septic shock: a systematic review with meta-analysis and trial sequential analysis. Intensive Care Med. 2018 Jul;44(7):1003-16.
http://www.ncbi.nlm.nih.gov/pubmed/29761216?tool=bestpractice.com
[  ]
What are the effects of corticosteroids for people with sepsis?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2908/fullMostrarme la respuesta
]
What are the effects of corticosteroids for people with sepsis?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2908/fullMostrarme la respuesta
Una guía de práctica clínica, basada en un metanálisis, informó que los corticoesteroides pueden reducir la mortalidad (en aproximadamente el 2%) y aumentar el riesgo de debilidad neuromuscular, pero las evidencias no son definitivas.[182]Lamontagne F, Rochwerg B, Lytvyn L, et al. Corticosteroid therapy for sepsis: a clinical practice guideline. BMJ. 2018 Aug 10;362:k3284.
https://www.bmj.com/content/362/bmj.k3284.long
http://www.ncbi.nlm.nih.gov/pubmed/30097460?tool=bestpractice.com
[183]Rochwerg B, Oczkowski SJ, Siemieniuk RAC, et al. Corticosteroids in sepsis: an updated systematic review and meta-analysis. Crit Care Med. 2018 Sep;46(9):1411-20.
http://www.ncbi.nlm.nih.gov/pubmed/29979221?tool=bestpractice.com
Se ha visto este efecto en la sepsis, con y sin shock; sin embargo, el mayor beneficio de los corticosteroides se observó entre los pacientes con shock séptico. En las guías de práctica clínica para la práctica clínica se llegó a la conclusión de que, tanto los métodos de tratamiento con corticoides, como los que no lo son, son adecuados y se sugirió que los valores y preferencias del paciente pueden orientar la decisión.[182]Lamontagne F, Rochwerg B, Lytvyn L, et al. Corticosteroid therapy for sepsis: a clinical practice guideline. BMJ. 2018 Aug 10;362:k3284.
https://www.bmj.com/content/362/bmj.k3284.long
http://www.ncbi.nlm.nih.gov/pubmed/30097460?tool=bestpractice.com
Los pacientes que priorizan la vida por encima de la calidad de vida probablemente optarían por someterse a un tratamiento con corticoesteroides, mientras que los que valoran más el evitar el deterioro funcional y maximizar la calidad de vida que evitar la muerte, es más probable que opten por no utilizar corticoesteroides.[182]Lamontagne F, Rochwerg B, Lytvyn L, et al. Corticosteroid therapy for sepsis: a clinical practice guideline. BMJ. 2018 Aug 10;362:k3284.
https://www.bmj.com/content/362/bmj.k3284.long
http://www.ncbi.nlm.nih.gov/pubmed/30097460?tool=bestpractice.com
[183]Rochwerg B, Oczkowski SJ, Siemieniuk RAC, et al. Corticosteroids in sepsis: an updated systematic review and meta-analysis. Crit Care Med. 2018 Sep;46(9):1411-20.
http://www.ncbi.nlm.nih.gov/pubmed/29979221?tool=bestpractice.com
BMJ Rapid Recommendations: corticosteroid therapy for sepsis - a clinical practice guideline
Opens in new window
MAGICapp: recommendations, evidence summaries and consultation decision aids
Opens in new window
[Figure caption and citation for the preceding image starts]: Recomendaciones rápidas de BMJ: corticosteroides intravenosos y atención habitual frente atención habitual solamenteLamontagne F, et al. BMJ 2018;362:k3284 [Citation ends].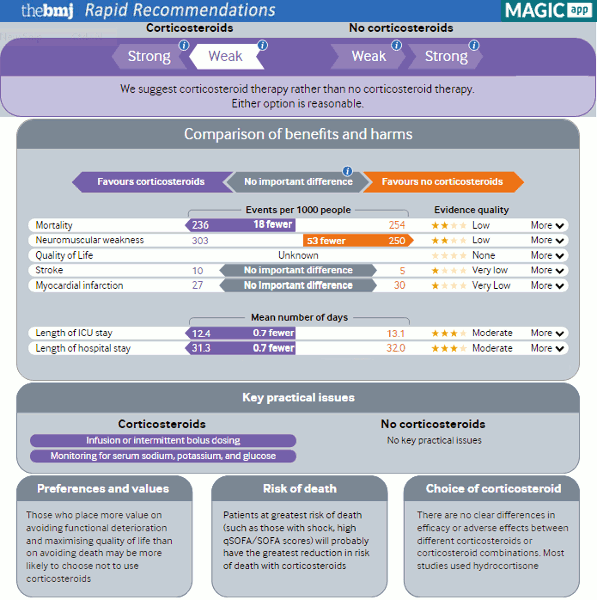
Bañar a los pacientes con lavados de clorhexidina puede reducir el riesgo de infección intrahospitalaria.[184]Climo MW, Yokoe DS, Warren DK, et al. Effect of daily chlorhexidine bathing on hospital-acquired infection. N Engl J Med. 2013 Feb 7;368(6):533-42.
https://www.nejm.org/doi/10.1056/NEJMoa1113849
http://www.ncbi.nlm.nih.gov/pubmed/23388005?tool=bestpractice.com
Se ha comprobado que la N-acetilcisteína intravenosa como terapia adyuvante en la SIRS y la sepsis es ineficaz y no se recomienda su uso.[185]Szakmany T, Hauser B, Radermacher P. N-acetylcysteine for sepsis and systemic inflammatory response in adults. Cochrane Database Syst Rev. 2012 Sep 12;(9):CD006616.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD006616.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/22972094?tool=bestpractice.com
Cuidados de soporte estándares en la UCI
Se deben considerar a todos los pacientes con sepsis para ingreso en la unidad de alta dependencia o unidad de cuidados intensivos (UCI).[164]Hollenberg SM, Ahrens TS, Annane D, et al. Practice parameters for hemodynamic support of sepsis in adult patients; 2004 update. Crit Care Med. 2004 Sep;32(9):1928-48.
http://www.ncbi.nlm.nih.gov/pubmed/15343024?tool=bestpractice.com
[186]Rivers E, Nguyen B, Havstad S, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med. 2001 Nov 8;345(19):1368-77.
https://www.nejm.org/doi/full/10.1056/NEJMoa010307#t=article
http://www.ncbi.nlm.nih.gov/pubmed/11794169?tool=bestpractice.com
Entre las medidas de cuidados intensivos generales, se incluyen la profilaxis para úlcera gastroduodenal aguda con antagonistas del receptor H2 de la histamina o inhibidores de la bomba de protones (en pacientes con riesgo de sangrado gastrointestinal), la profilaxis de la trombosis venosa profunda (con heparina y medias de compresión), la nutrición parenteral o enteral y el control glucémico.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[187]Trzeciak S, Dellinger RP. Other supportive therapies in sepsis: an evidence-based review. Crit Care Med. 2004 Nov;32(suppl 11):S571-7.
http://www.ncbi.nlm.nih.gov/pubmed/15542966?tool=bestpractice.com
[188]Nguyen HB, Rivers EP, Abrahamian FM, et al; Emergency Department Sepsis Education Program and Strategies to Improve Survival (ED-SEPSIS) Working Group. Severe sepsis and septic shock: review of the literature and emergency department management guidelines. Ann Emerg Med. 2006 Jul;48(1):28-54.
http://www.ncbi.nlm.nih.gov/pubmed/16781920?tool=bestpractice.com
[189]Wang Y, Ye Z, Ge L, et al. Efficacy and safety of gastrointestinal bleeding prophylaxis in critically ill patients: systematic review and network meta-analysis. BMJ. 2020 Jan 6;368:l6744.
https://www.bmj.com/content/368/bmj.l6744
http://www.ncbi.nlm.nih.gov/pubmed/31907166?tool=bestpractice.com
Puede ser necesaria la transfusión de concentrados de células; se recomienda una concentración de hemoglobina objetivo de 70 g/L (7 g/dL).[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
[163]Holst LB, Haase N, Wetterslev J, et al; TRISS Trial Group; Scandinavian Critical Care Trials Group. Lower versus higher hemoglobin threshold for transfusion in septic shock. N Engl J Med. 2014 Oct 9;371(15):1381-91.
https://www.nejm.org/doi/full/10.1056/NEJMoa1406617
http://www.ncbi.nlm.nih.gov/pubmed/25270275?tool=bestpractice.com
[190]Hébert PC, Wells G, Blajchman MA, et al. A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. N Engl J Med. 1999 Feb 11;340(6):409-17.
https://www.nejm.org/doi/full/10.1056/NEJM199902113400601
http://www.ncbi.nlm.nih.gov/pubmed/9971864?tool=bestpractice.com
Puede ser necesario un nivel mayor de hemoglobina en determinadas circunstancias (isquemia miocárdica, hipoxemia grave, hemorragia aguda, cardiopatía cianótica o acidosis láctica).[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
En la fase de reposición inicial, en especial con la aplicación de la terapia temprana dirigida por objetivos, puede ser adecuado mantener un hematocrito más elevado ≥30%.[64]Rivers E, Nguyen B, Havstad S, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med. 2001 Nov 8;345(19):1368-77.
https://www.nejm.org/doi/10.1056/NEJMoa010307
http://www.ncbi.nlm.nih.gov/pubmed/11794169?tool=bestpractice.com
Los pacientes que requieren asistencia respiratoria prolongada deben recibir ventilación con protección pulmonar, utilizando mínimas presiones inspiratorias máximas (<30 cmH₂O) e hipercapnia permisiva para limitar de manera específica el compromiso pulmonar.[191]Brower RG, Matthay MA, Morris A, et al; Acute Respiratory Distress Syndrome Network. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med. 2000 May 4;342(18):1301-8.
https://www.nejm.org/doi/full/10.1056/NEJM200005043421801
http://www.ncbi.nlm.nih.gov/pubmed/10793162?tool=bestpractice.com
La fracción inspiratoria de oxígeno (FiO₂) se debe ajustar a los niveles eficaces más bajos con el fin de evitar la toxicidad del oxígeno y mantener la tensión de oxígeno venoso central. En una revisión sistemática de los pacientes adultos gravemente enfermos, incluidos los pacientes con sepsis, se informó de un aumento de la mortalidad entre los que recibían un suplemento de oxígeno liberal en comparación con los que recibían oxigenoterapia conservadora. Se sugirió un rango de objetivo SpO₂ de 94% a 96% para todos los pacientes con enfermedades críticas.[132]Chu DK, Kim LH, Young PJ, et al. Mortality and morbidity in acutely ill adults treated with liberal versus conservative oxygen therapy (IOTA): a systematic review and meta-analysis. Lancet. 2018 Apr 28;391(10131):1693-705.
http://www.ncbi.nlm.nih.gov/pubmed/29726345?tool=bestpractice.com
Los pacientes se deben colocar en una posición en semidecúbito, con la cabeza elevada de 30° a 45°.[97]Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med. 2017 Mar;43(3):304-77.
https://link.springer.com/article/10.1007/s00134-017-4683-6
http://www.ncbi.nlm.nih.gov/pubmed/28101605?tool=bestpractice.com
 ]
]
 ]
]
 ]
]