Abordaje
La sepsis es un espectro de enfermedad en el que existe una respuesta sistémica y no regulada del huésped a una infección.[1] Su presentación varía desde síntomas inespecíficos o no localizados (p. ej., sensación de malestar con temperatura normal) a señales graves acompañadas de evidencia de disfunción multiorgánica y shock séptico. Varios factores determinan el riesgo de avance de la enfermedad a enfermedad fulminante, incluidos los siguientes:
Magnitud y naturaleza del foco infeccioso
Momento y calidad de las intervenciones; y
Predisposición genética y adquirida del paciente.
La importancia del reconocimiento temprano de la sospecha de sepsis
El reconocimiento temprano de la sepsis es esencial ya que el tratamiento temprano - cuando hay sospecha de sepsis pero todavía no se ha confirmado - se asocia con importantes beneficios a corto y largo plazo sobre el desenlace.[5][64][65][66][67][68] Sin embargo, la detección puede ser difícil porque la presentación clínica de la sepsis puede ser sutil y no específica. Por lo tanto, es importante establecer un umbral bajo para la sospecha de sepsis.
La clave del reconocimiento temprano es la identificación sistemática de cualquier paciente que cumpla estos dos criterios:
Presenta síntomas sugestivos de infección. Las fuentes más comunes en los pacientes que desarrollan sepsis son las infecciones de las vías respiratorias, urinarias y gastrointestinales inferiores. También contribuyen las infecciones de piel y tejidos blandos.
Corre el riesgo de deterioro a causa de una disfunción orgánica. Se han sugerido varios métodos para identificar pacientes con riesgo de deterioro. Incluyen el uso de: una escala de advertencia temprana; la escala rápida (o relacionada con sepsis) de evaluación de fallo orgánico secuencial (qSOFA); o criterios de estratificación de riesgo. Todos estos enfoques se basan en una evaluación sistemática y en el registro de constantes vitales. Es importante comprobar las guías locales para información sobre el enfoque recomendado por su institución.
Presentación inicial de infección
Inicialmente, la sepsis se puede presentar con síntomas inespecíficos, no localizados, como sensación de malestar con temperatura normal. Debe considerarse la sepsis si un paciente presenta signos o síntomas que sugieran una posible infección, sin importar la temperatura.[5] Esto fue en parte porque, aunque frecuentemente se asocia la fiebre con la sepsis, la hipotermia es un signto de inicio común y conlleva un pronóstico peor.[69] Los pacientes de edad avanzada son muy propensos a una respuesta febril mitigada y pueden sufrir normotermia.[3][4]
Las fuentes más comunes en los pacientes que desarrollan sepsis son las vías respiratorias, las vías urinarias y las infecciones gastrointestinales inferiores.[70] Los síntomas de la infección subyacente pueden o no, ser evidentes en la presentación inicial.
En el historial del paciente deben buscarse factores de riesgo de sepsis, incluidos:
Mayores de 65 años
Deterioro de la inmunidad
Diabetes
Cirugía reciente u otro procedimiento invasivo
Afectación de la integridad de la piel
Embarazo actual o reciente
Sondas intravenosas o urinarias permanentes
Consumo de drogas ilícitas por vía intravenosa.
Se sospecha un mayor índice de sepsis cuando un paciente en uno de estos grupos en riesgo presenta signos de infección y enfermedad aguda.
Diagnóstico de sepsis e identificación de pacientes que corren el riesgo de deterioro a causa de una disfunción orgánica.
La identificación temprana de sepsis se basa en la evaluación sistemática de pacientes que presentan una supuesta infección para identificar los que corren el riesgo de deterioro debido a la disfunción orgánica.
Se han propuesto varios enfoques para la evaluación rápida y pragmática del riesgo de deterioro en la práctica clínica diaria sin la necesidad de esperar los resultados de análisis clínicos. Se necesita investigación adicional para determinar el enfoque óptimo, que incluye:
Escalas de advertencia tempranas (p. ej. el National Early Warning Score [NEWS2] desarrollado en el Reino Unido)
La escala qSOFA; o
El uso de un sistema de estratificación del riesgo, según lo recomendado por los diversos grupos de guías de práctica clínica en el Reino Unido y en Estados Unidos.
Todo paciente con sospecha de infección en los que valore que hay riesgo de deterioro utilizando cualquiera de estos enfoques debe ser diagnosticado como sospecha de sepsis y priorizado para tratamiento inmediato.
Todos estos enfoques se basan en una evaluación sistemática y en el registro de constantes vitales del paciente.
Las observaciones vitales deben interpretarse siempre en relación con el valor inicial conocido o probable del paciente para ese parámetro; por ejemplo, una caída de la presión arterial sistólica (PA) de ≥40 mmHg desde el valor inicial del paciente es motivo de alarma, independientemente de la lectura de la PA sistólica en sí.[5]
Escalas de advertencia temprana
Las puntuaciones de advertencia temprana se utilizan ampliamente en la atención secundaria para clasificar a los pacientes y facilitar la detección de deterioro clínico o mejoría a lo largo del tiempo.[71] Cuando se sospecha infección, estas escalas de advertencia temprana se pueden utilizar para identificar a los pacientes con mayor riesgo de sepsis y deterioro resultante.[72][73][74][75] Al igual que con cualquier sistema de puntuación, las escalas de advertencia temprana no son sensibles al 100% ni específicas al 100%, y por ello, es crucial el juicio clínico.
Las escalas de advertencia temprana se basan en varios parámetros fisiológicos, en los cuales cuanto mayor sea la desviación de la norma, mayor será el puntaje. Cada parámetro se evalúa individualmente y luego se agrega el puntaje final. Entre los ejemplos se incluyen NEWS2, desarrollado por el Royal College of Physicians del Reino Unido, y la Modified Early Warning Score (MEWS).[76] La evidencia sugiere que las escalas de advertencia temprana presentan mejor sensibilidad y especificidad que la escala qSOFA para predecir el deterioro y la mortalidad entre pacientes que acuden al servicio de urgencias con una posible infección.[72][77]
[Figure caption and citation for the preceding image starts]: National Early Warning Score 2 (NEWS2) es una escala de advertencia temprana producida por el Royal College of Physicians en el Reino Unido. Se basa en la evaluación de seis parámetros individuales, a los que se asigna una puntuación de 0 a 3: frecuencia respiratoria, saturaciones de oxígeno, temperatura, presión arterial, frecuencia cardíaca y nivel de consciencia. Existen diferentes escalas de niveles de saturación de oxígeno basadas en el objetivo fisiológico del paciente (la escala 2 se utiliza para pacientes con riesgo de insuficiencia respiratoria hipercápnica). El resultado se agrega entonces para dar una puntuación total final; cuanto mayor sea la puntuación, mayor será el riesgo de deterioro clínicoReproducido de: Colegio Real de Médicos. National Early Warning Score (NEWS) 2: Estandarización de la evaluación de la gravedad de la enfermedad aguda en el NHS. Informe actualizado de un grupo de trabajo. Londres: RCP, 2017. [Citation ends].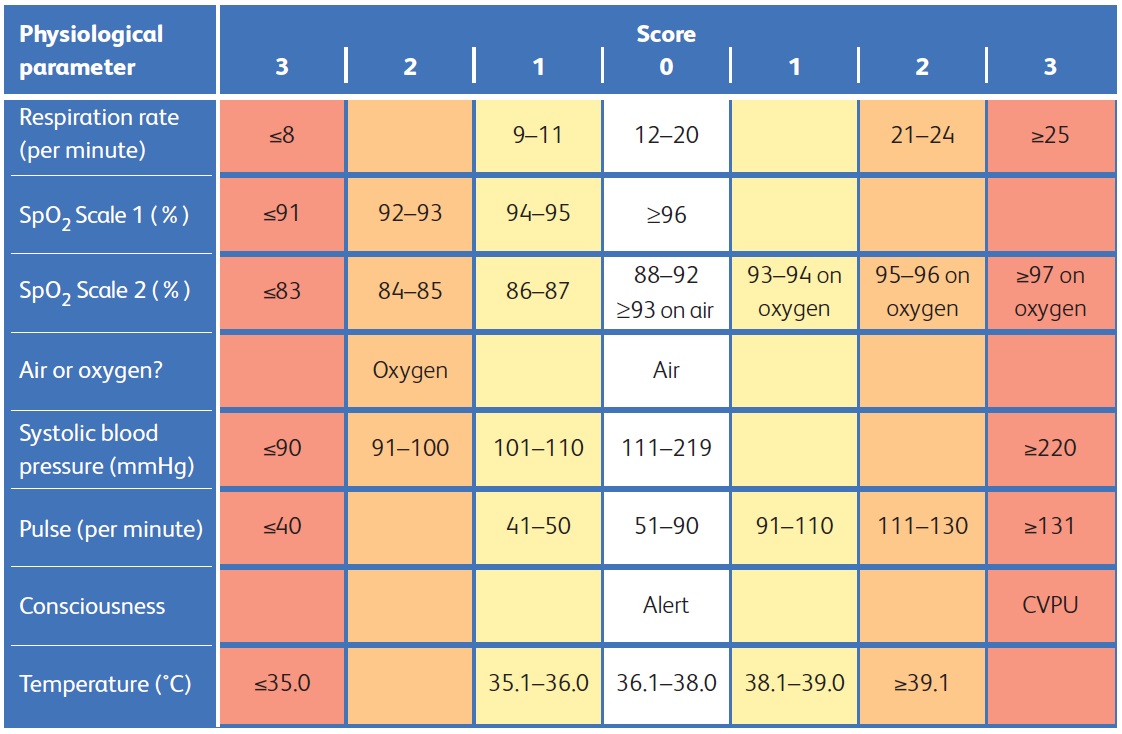
La puntuación total de NEWS2 motiva el nivel de respuesta requerido, incluida la antigüedad de la persona que toma la decisión clínica, la urgencia de la revisión, y el lugar más apropiado de la atención. Los factores desencadenantes de NEWS2 que motivan la intensificación de la atención en un paciente con infección o con sospecha de infección son los siguientes:[76][78]
Una puntuación total ≥5 probablemente representa sepsis Debe activar el inicio inmediato del protocolo de manejo adecuado de la sepsis y una revisión urgente por un médico senior, quien debe evaluar si el manejo por el equipo de atención crítica es necesario.
En pacientes con una puntuación de NEWS2 < 5, se debe ejercitar el juicio clínico, con alta sospecha de sepsis si alguno de los siguientes están presentes:
Un único parámetro NEWS2 de 3
Piel con erupción que no palidece/moteada/cenicienta/cianótica
Responde únicamente a la voz o al dolor, o no responde
No haber orinado durante las últimas 18 horas o diuresis <0.5 mL/kg/horas; o
Lactato ≥2 mmol/L (≥18 mg/dL).
Una puntuación total ≥7 tiene un riesgo significativo de mortalidad, por lo que debe incitar a la evaluación urgente por parte de un especialista en atención crítica y a la transferencia a un entorno de gran dependencia para monitoreo continuo de las constantes vitales.[76]
Un análisis de los datos de auditoría de 20 servicios de urgencias en el Reino Unido determinó que una sola puntuación de NEWS calculada a partir de observaciones iniciales del paciente fue fuertemente predictiva de resultados adversos en la sepsis; los pacientes con una puntuación de NEWS de 5-6 arrojaron el doble de mortalidad que las personas con una puntuación de 0-4 (mortalidad a 30 días de 11.3% frente al 5.5%).[75] Un estudio observacional de 30,677 adultos ingresados en el servicio de urgencias con sospecha de infección encontró que el puntaje del NEWS se desempeñó mejor que las puntuaciones del MEWS o del qSOFA en la predicción del riesgo de muerte o de la necesidad de traslado a una unidad de cuidados intensivos (UCI).[72]
Es importante tener en cuenta que NEWS2 y MEWS no han sido validadas para su uso en embarazadas. Si bien existen variantes de las escalas de advertencia temprana que se pueden utilizar en el embarazo (p. ej., la Modified Early Obstetric Warning Score [MEOWS]), estas tampoco han sido validadas para uso en pacientes con sepsis.
La escala qSOFA
La escala qSOFA es una alternativa a las escalas de advertencia temprana para detectar signos de disfunción orgánica temprana en un paciente con una presunta infección (es decir, sepsis).
La puntuación de qSOFA es una simple evaluación clínica recomendada por el Third International Consensus Group (Sepsis-3) para el uso a pie de cama para detectar el riesgo de deterioro debido a la sepsis.[1] Utilizando qSOFA, un paciente se considera en alto riesgo de un resultado adverso si hay al menos dos de los tres criterios siguientes:[1]
Alteración del estado mental (Escala de Coma de Glasgow [GCS] <15).
Presión arterial sistólica ≤100 mmHg
Frecuencia respiratoria ≥22 respiraciones/minuto.
Sin embargo, un creciente cúmulo de evidencias sugiere que la qSOFA presenta poca sensibilidad para los pacientes con sospecha de infección (en comparación con otras puntuaciones de alerta temprana de cabecera y los criterios del síndrome de respuesta inflamatoria sistémica [SIRS]) y que es un indicador tardío de deterioro.[72][77]
Sistemas de estratificación del riesgo
Algunas guías de práctica clínica se centran en el uso de la estratificación sistemática del riesgo para identificar a los pacientes con infección que corren el riesgo de deterioro debido a la sepsis. Entre ellas se encuentran las guías de práctica clínica del National Institute for Health and Care Excellence (NICE) del Reino Unido (NICE) para 2017 y la herramienta Detect, Act, Reassess, Titrate (DART) recomendada por el American College of Emergency Physicians Expert Panel on Sepsis.[5][79]
Las guías de práctica clínica del NICE recomiendan la clasificación de los pacientes en riesgo bajo, riesgo moderado a alto o riesgo alto de enfermedad grave y muerte por sepsis en función de los siguientes criterios:
Antecedentes (comportamiento alterado; estado mental alterado; capacidad funcional; inmunidad afectada; o traumatismo, cirugía o procedimientos invasivos recientes)
Respiratorios (frecuencia respiratoria; necesidades nuevas de oxígeno para mantener la saturación)
Presión arterial sistólica
Circulación e hidratación (frecuencia cardíaca; diuresis elevada)
Temperatura (hipotermia)
Piel (signos de infección; apariencia moteada o grisácea; cianosis de la piel, labios o lengua; o presencia de erupción petequial en la piel).
Los umbrales para las categorías de riesgo alto, moderado a alto y bajo varían según el grupo etario. Los criterios para adultos y niños ≥12 años se enumeran en la sección "criterios diagnósticos" de este tema.
Las recomendaciones de NICE también aconsejan diferentes vías de evaluación clínica hospitalaria y análisis clínicos, basadas en la categoría de riesgo de cada paciente (p. ej., gasometría venosa para gases arteriales, incluidas la medición de glucosa y lactato, hemocultivo, hemograma completo, proteína C-reactiva, urea y electrolitos séricos , creatinina y coagulación).[5]
Las guías de práctica clínica del NICE son respaldadas por vías desarrolladas por UK Sepsis Trust: UK Sepsis Trust: clinical resources Opens in new window
Adultos, mujeres no embarazadas y niños ≥12 años en atención secundaria
Mujeres embarazadas en atención secundaria
Adultos, mujeres no embarazadas y niños ≥12 años en atención primaria
Mujeres embarazadas en atención primaria
Puntuaciones de riesgo de sepsis que requieren análisis clínicos
Tanto los criterios SOFA para diagnosticar la sepsis, como los criterios SIRS a los que sustituyeron, requieren análisis de sangre. Esto puede conducir a retrasos en el reconocimiento de pacientes con riesgo de deterioro y disfunción orgánica debido a la sepsis.
SOFA
En 2016, la definición de sepsis ha sido actualizada por el Third International Consensus Group (Sepsis-3) basándose en su totalidad en los criterios SOFA.[1] La escala SOFA se utiliza principalmente en investigación y cuando se utiliza en la práctica clínica, generalmente se reduce a un contexto de la unidad de cuidados intensivos (UCI). La puntuación SOFA se calcula en función de la evaluación de los siguientes sistemas (con una puntuación ≥2 en un paciente con una infección que se sospecha como sepsis):[1]
[Figure caption and citation for the preceding image starts]: Criterios SOFA (Sequential (or Sepsis-related) Organ Failure Assessment)Creada por BMJ, adaptada de Vincent JL, Moreno R, Takala J, et al. La escala SOFA (Sepsis-related Organ Failure Assessment) para describir la disfunción orgánica. En nombre del Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine. Intensive Care Med 1996;22:707-10. [Citation ends].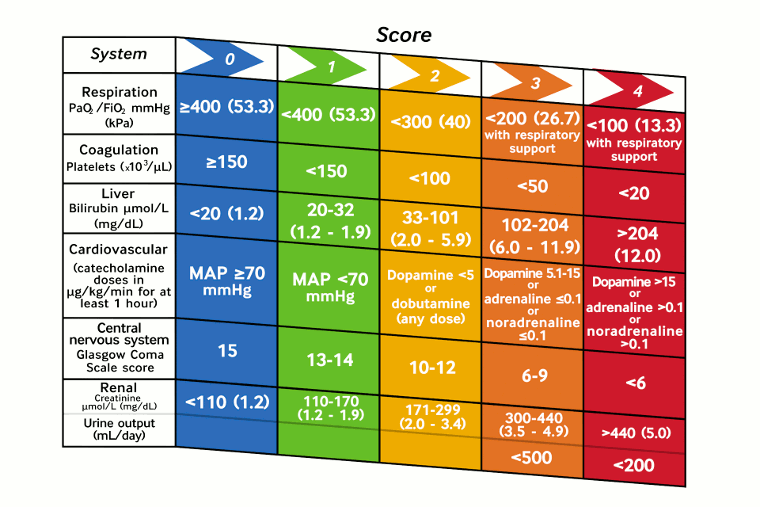
Debido a que la escala SOFA se ha validado principalmente en pacientes en la unidad de cuidados intensivos y requiere los resultados de varios análisis clínicos, el Third International Consensus Group sugiere el uso de la evaluación qSOFA a pie de cama para la identificación temprana de pacientes en riesgo de deterioro debido a sepsis.
Las definiciones 2016 Sepsis-3 también predefinieron el shock séptico como un subconjunto de la sepsis en el cual las alteraciones circulatorias, celulares y metabólicas profundas se asocian con un mayor riesgo de mortalidad que la sepsis sola (la mortalidad en el shock séptico es >40%)..[1] El choque séptico se diagnostica cuando un paciente con sepsis cumple con ambos de los siguientes criterios a pesar de una fluidoterapia adecuada:[1]
Hipotensión persistente que requiere vasopresores para mantener una presión arterial media ≥65 mmHg; y
Lactato sérico >2 mmol/L (>18 mg/dL).
Bajo las revisiones de Sepsis-3 de 2016, el término 'sepsis grave' se convirtió en obsoleto dado que la definición de sepsis ahora también incluye disfunción orgánica.[1]
criterios de síndrome de respuesta inflamatoria sistémica (SRIS)
En la práctica clínica generalizada, se siguen usando los criterios de SRIS (junto con la sospecha de infección) para el diagnóstico de sepsis, a pesar de su sustitución por las definiciones de Sepsis-3 en 2016. Los criterios de SRIS fueron reemplazados porque, aunque tienen una alta sensibilidad, su especificidad es muy baja.[72] Las guías internacionales ya no recomiendan el uso de los criterios de SRIS en la práctica clínica para diagnosticar sepsis en adultos.
SRIS se define por la presencia de dos o más de los siguientes signos clínicos y resultados de laboratorio:[2][80]
Temperatura >38.3 °C (101 °F) o <36.0 °C (96.8 °F)
Taquicardia >90 lpm.
Taquipnea >20 respiraciones/minuto o PaCO₂ <4.3 kPa (32 mmHg)
Leucocitosis (recuento de leucocitos >12×10⁹/L [>12,000/microlitro])
Leucopenia (recuento de leucocitos <4×10⁹/L [<4000/microlitro])
Recuento de leucocitos normal con >10% de formas inmaduras
Hiperglucemia (glucemia >7.7 mmol/L [>140 mg/dL]) en ausencia de diabetes mellitus
Alteración aguda del estado mental.
Evaluación inicial
La evaluación inicial incluye la identificación de la fuente más probable de infección, la identificación de factores de riesgo para la sepsis, la determinación de la necesidad de un control urgente de la fuente (p.ej., incisión y drenaje de un absceso), la identificación de alteraciones en el comportamiento, así como de la circulación o la respiración.
Como con todos los pacientes gravemente enfermos, la evaluación inicial debe seguir el formato Vías respiratorias, Respiración, Circulación, Discapacidad, Exposición (ABCDE), a fin de incluir la evaluación de la suficiencia circulatoria, respiratoria y de las vías respiratorias, y el nivel de consciencia (Escala de Coma de Glasgow [GCS] o AVPU [alerta, responde a la voz, responde al dolor, no responde]).
Se debe prestar atención a la búsqueda de otros signos de disfunción orgánica (p. ej., ictericia, púrpura fulminante, cianosis) y de signos de insuficiencia circulatoria, incluidos la oliguria, la piel moteada y el tiempo de llenado capilar prolongado. Se deben monitorizar la saturación de oxígeno, la frecuencia respiratoria, la frecuencia cardíaca, la presión arterial, la temperatura y el equilibrio hidroelectrolítico preciso (incluida la diuresis) cada hora.
Es importante buscar evidencia clínica de la fuente de infección. Esto ayudará a realizar un diagnóstico y proporcionará información vital en cuanto a los factores de riesgo del paciente con respecto a la sepsis.
Entre los factores de riesgo claramente asociados con la sepsis se encuentran: neoplasia maligna subyacente, deterioro de la inmunidad (p. ej., debido a una enfermedad o a los fármacos), cirugía reciente u otros procedimientos invasivos, integridad cutánea dañada (p. ej., heridas, infección de la piel), sondas permanentes urinarias e intravenosas, consumo de drogas ilícitas por vía intravenosa, edad >65 años o debilidad, embarazo o embarazo reciente, hemodiálisis, antecedentes de alcoholismo, inmunocompromiso y diabetes mellitus.[Figure caption and citation for the preceding image starts]: Púrpura fulminante grave normalmente asociada con septicemia neumocócicaDe la colección de Ron Daniels, MB, ChB, FRCA; usado con autorización [Citation ends].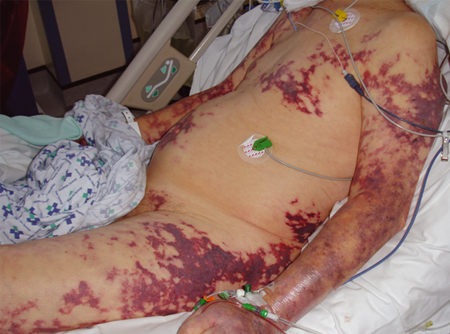 [Figure caption and citation for the preceding image starts]: Tiempo de llenado capilar. Imagen superior: tono de piel normal; imagen central: presión aplicada durante 5 segundos; imagen inferior: tiempo medido hasta la hiperemiaDe la colección de Ron Daniels, MB, ChB, FRCA; usado con autorización [Citation ends].
[Figure caption and citation for the preceding image starts]: Tiempo de llenado capilar. Imagen superior: tono de piel normal; imagen central: presión aplicada durante 5 segundos; imagen inferior: tiempo medido hasta la hiperemiaDe la colección de Ron Daniels, MB, ChB, FRCA; usado con autorización [Citation ends].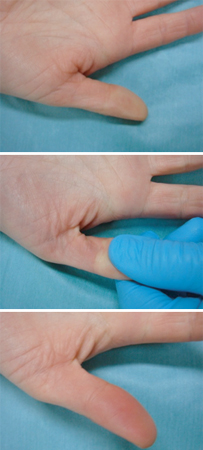
La sepsis, por lo general, se diagnostica cuando se presentan alteraciones en el nivel de consciencia, hipotensión y disfunción orgánica que se manifiestan, por ejemplo, como oliguria, hipoxemia, ictericia o erupción petequial. El retraso en el diagnóstico y la intervención se asocian con un aumento en la morbilidad, y se debe mantener un índice de sospecha elevado en todos los pacientes con signos anómalos y posibilidad de infección. Se debe sospechar de una sepsis en pacientes con un estado mental alterado inexplicable, taquipnea con un tórax despejado y una oxigenación normal, o si el instinto del clínico indica algo inusual en una infección aparentemente rutinaria.[79]
Pruebas diagnósticas
Las pruebas diagnósticas iniciales cubren cuatro objetivos:
Identificar los microorganismos causales.
Evaluar la disfunción orgánica.
Identificar la fuente de infección.
Ayudar a pronosticar y seleccionar un nivel de atención adecuado.
Se debe dar prioridad a aquellas pruebas diagnósticas que ayuden a responder preguntas clínicas importantes, como la fuente de la infección y la gravedad de la enfermedad. Los cultivos de sangre y de otros líquidos demorarán entre 48 y 72 horas en arrojar sensibilidades a los microorganismos causales (si se los identifica), pero son mucho menos sensibles si se los posterga hasta después de la administración antimicrobiana.
Pruebas diagnósticas para identificar microorganismos causales:
Los hemocultivos se deben obtener de inmediato, preferentemente antes del inicio de la administración de antibióticos, siempre que la toma de muestras no retrase dicha administración. Idealmente, se debe tomar al menos un conjunto por vía percutánea y un conjunto proveniente de cualquier dispositivo de acceso vascular que haya estado in situ durante más de 24 horas.[81][82] Otros cultivos (p. ej., esputo, líquido cefalorraquídeo [LCR], líquido pleural, líquido sinovial, heces y orina) se deben recoger según lo indicado clínicamente.
Si no se presentan signos localizadores, se requieren la exploración systemática y el cultivo de todos los sitios de infección potenciales, incluidos las heridas, los catéteres, los implantes protésicos, las zonas de las epidurales y el líquido peritoneal o pleural, según lo indiquen la presentación clínica y los antecedentes del paciente.
Si existe sospecha de meningitis (p. ej., cefalea, fotofobia, rigidez en el cuello, vómitos), se debe realizar una punción lumbar para el cultivo y la microscopia del líquido cefalorraquídeo (LCR). Si antes de la punción lumbar existe sospecha clínica de aumento de la presión intracraneal, se debe realizar una exploración por tomografía computarizada (TC) para descartar este diagnóstico.
Si existe sospecha de una acumulación cerrada, como un absceso o empiema, se recomienda su drenaje y cultivo en la fase inicial del curso de la enfermedad (dentro de las 6 horas a partir de su identificación).[83]
En los pacientes intubados en quienes se sospecha neumonía, se deben realizar aspirados traqueales, lavado broncoalveolar u obtener muestras tomadas con cepillo protegido.
Evaluación de la disfunción orgánica:
Evaluación inicial de las pruebas de función hepática (en particular la bilirrubina), un hemograma completo (con diferencial), coagulación (ratio internacional normalizado, tiempo de tromboplastina parcial activada), creatinina sérica y urea en sangre.
La glucosa y los electrolitos séricos generalmente se encuentran alterados y se deben medir al inicio y a intervalos regulares hasta que el paciente mejore.
El lactato sérico elevado destaca hipoperfusión tisular y se evalúa de manera más confiable utilizando una muestra de gasometría arterial (GSA).[84] Sin embargo, en la práctica, en general se utiliza una muestra de gasometría venosa, ya que es más fácil y rápida de obtener comparado con la GSA. La mayoría de los pacientes no se someten a la toma de muestras para GSA a menos que haya un compromiso respiratorio.
Los marcadores de inflamación, incluidas la proteína C-reactiva y la procalcitonina, son de utilidad para determinar el avance clínico y la respuesta al tratamiento. Pueden ser de utilidad las medidas en serie de procalcitonina como guía para la necesidad de continuar o interrumpir la toma de antibióticos empíricos.[85][86]
Pruebas diagnósticas para identificar la fuente de infección:
La fuente de infección puede ser evidente de inmediato, por ejemplo, con signos y síntomas clásicos de neumonía (esputo purulento, disnea, taquipnea, cianosis) o peritonismo (dolor abdominal, rigidez, distensión, sensibilidad a la palpación, ausencia de borborigmos). Sin embargo, en muchos pacientes, se debe buscar activamente el origen.
Los estudios diagnósticos pueden identificar una fuente de infección que requiera la extirpación de un cuerpo extraño o un drenaje, con el fin de maximizar la probabilidad de una respuesta satisfactoria a la terapia. Se pueden realizar las radiografías de tórax y los ultrasonidos a pie de cama. Las exploraciones físicas, como las exploraciones por TC, requieren el traslado de pacientes potencialmente inestables, por lo que se deben evaluar los beneficios en comparación con los riesgos.
Se puede realizar un electrocardiograma (ECG) con el fin de descartar otros diagnósticos diferenciales, incluidos el infarto de miocardio, la pericarditis y la miocarditis. La sepsis también predispone a la disfunción miocárdica (particularmente en el shock séptico) y a las arritmias (p. ej., la fibrilación auricular).[5][87]
En pacientes que presentan riesgo de endocarditis bacteriana o con síntomas compatibles, resulta útil la realización de un ecocardiograma transtorácico o transesofágico. Esto también resulta útil para la diferenciación entre shock séptico, cardíaco e hipovolémico, así como para diagnósticos alternativos, como anomalías valvulares, émbolo pulmonar, isquemia miocárdica (con disfunción global o segmentaria), hipovolemia e hipertensión pulmonar. Si se encuentra disponible, también puede ser adecuado un ecocardiograma en pacientes con sepsis de origen desconocido.
Ciertas pruebas diagnósticas tienen un valor pronóstico y pueden ayudar a determinar la necesidad de medicina intensiva:
La medición de lactato es una evaluación útil de la perfusión una vez que se ha establecido un diagnóstico de sepsis. Los niveles elevados de lactato se asocian con niveles elevados de metabolismo anaerobio. Niveles persistentemente elevados de lactato se pueden equiparar con el grado de hipoperfusión o disfunción orgánica. Un lactato elevado conlleva un valor pronóstico adverso si se eleva a >2 mmol/L (>18 mg/dL) y se asocia con peores resultados a niveles >4 mmol/L (>36 mg/dL).[5] La eliminación del lactato (la tasa a la que el lactato se elimina durante un periodo de 6 horas) ha demostrado ser igual de útil que las pruebas más invasivas, como la saturación de oxígeno venoso central, para determinar la respuesta del paciente al tratamiento.[88][89]
Algunos estudios con pacientes con traumatismos han evaluado los niveles de lactato, en comparación con las puntuaciones del sistema APACHE (Acute Physiology and Chronic Health Evaluation) y las tasas de aclaramiento del lactato, y han hallado que los niveles de lactato son inferiores para informar del pronóstico. Sin embargo, el cálculo de una puntuación del sistema APACHE tarda 24 horas.[90]
Una medida alternativa son los niveles de procalcitonina sérica. En los pacientes con infecciones respiratorias agudas (incluidos los que padecen sepsis), se ha demostrado que la terapia de antibióticos guiada por procalcitonina reduce la duración del curso de los antibióticos, disminuye las complicaciones relacionadas con los mismos y reduce la tasa de mortalidad a 30 días.[91] Sin embargo, las evidencias para un valor pronóstico de la procalcitonina no están claras, y su uso en la identificación de la sepsis se excluye de muchas guías de práctica clínica.[92][93][94] Los cambios en los niveles de procalcitonina pueden ocurrir después que los cambios en los niveles de lactato, aunque los cambios en ambos marcadores combinados son altamente predictivos de un desenlace entre las 24 y 48 horas.[95] Por lo tanto, puede tener mayor utilidad para permitir el cese temprano del tratamiento antimicrobiano.[96][97]
Algunos expertos recomiendan el uso del índice de shock (frecuencia cardíaca dividida por presión arterial sistólica) como factor pronóstico de la necesidad de medicina intensiva; un grupo halló que un índice >0.9 resulta predictivo.[98]
Se ha demostrado que la ecocardiografía de impedancia no invasiva pronostica desenlace desfavorable si se identifica un índice cardíaco de <2 o una reducción de la excursión sistólica del plano anular mitral.[99][100]
Los pacientes que padecen shock séptico y que no han respondido a la rehidratación inicial requerirán una monitorización y un tratamiento invasivos en unidades de cuidados intermedios.
Pruebas emergentes
Se están desarrollando ensayos diagnósticos moleculares que pueden analizar los patógenos frecuentes. Esos ensayos permiten una identificación de microorganismos y una prueba de susceptibilidad antimicrobiana más rápidas que los sistemas estándar de hemocultivo.[107][108][109]
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad