Abordagem
O diagnóstico precoce está associado a um melhor prognóstico em longo prazo; o atraso no diagnóstico pode resultar em progressão e na necessidade de tratamento mais intensivo.[2] Qualquer massa intratesticular deve ser considerada um câncer de testículo, até que se prove o contrário. A idade do paciente, história familiar de câncer de testículo, diagnóstico prévio de câncer de testículo e, mais importante, história de criptorquidia devem alertar o médico para um possível diagnóstico. Além disso, o reconhecimento das possibilidades de diagnóstico diferencial com base em elementos de microscopia óptica de rotina e outras observações direcionadas ou estudos sorológicos podem ajudar a definir um diagnóstico preciso.[41]
Avaliação clínica
O paciente típico tem entre 20 e 34 anos de idade.[13] Ele pode relatar um desconforto testicular inespecífico e a sensação de uma massa nos testículos. O início dos sintomas geralmente dura mais de 2 semanas, mas os pacientes podem apresentar edema doloroso de início súbito (devido a hemorragia ou infecção associada) em 10% dos casos.[42]
O exame físico dos testículos é fundamental para detectar essa condição o quanto antes. O exame físico genital é uma avaliação clínica simples e relativamente rápida, e deve ser realizado quando o paciente apresentar sintomas genitais.[43] O exame deve primeiro ser realizado com o paciente em pé para avaliar a assimetria de um testículo mais baixo que o outro. O local da massa pode ser apalpado rolando com cuidado o testículo entre o polegar e os dedos. A massa deve estar firmemente presa no testículo (intratesticular) no lado ou no polo inferior do testículo. Deve ser dada atenção especial à forma e consistência da massa. A massa geralmente é lisa, firme e não flutuante. No entanto, às vezes, ela se manifesta como uma distorção desigual do contorno do testículo ou como um aumento homogêneo. A palpação do cordão espermático para verificar a espessura e a motilidade, e a presença de inchaço inguinal devem ser observados. Em caso de dúvida, uma ultrassonografia do testículo é obrigatória. Um urologista deve avaliar todas as massas testiculares.
Um exame sistêmico completo deve ser realizado, pois cerca de 5% a 10% dos pacientes têm manifestações extratesticulares no momento da apresentação com ou sem tumor primário aparente nos testículos.[44]
Investigações
A ultrassonografia do testículo é a modalidade de imagem inicial preferida e tem alta sensibilidade para neoplasia testicular.[2][45][46][Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica da massa testicular como lesão hipoecoicaBMJ Case Reports 2011; doi:10.1136/bcr.12.2010.3565 [Citation ends]. Entretanto, uma ultrassonografia negativa não descarta a presença de câncer e deve ser repetida em 6 a 8 semanas em pacientes com achados indeterminados na ultrassonografia ou no exame físico e marcadores tumorais séricos normais.[2] A ultrassonografia deve ser realizada com avaliação por Doppler colorido para confirmar a presença de massa testicular antes da orquiectomia.[47] O uso de Doppler colorido pode ajudar a distinguir tumores de outros edemas escrotais (por exemplo, varicocele).[48] O testículo contralateral também deve ser avaliado quanto à presença de tumores síncronos e microcalcificações, bem como para medir o volume testicular.[47] A biópsia do testículo contralateral pode ser indicada se uma massa suspeita for identificada, o testículo estiver atrofiado ou houver história de criptorquidia. Não é recomendado apenas para microcalcificações testiculares.[46][49][50] Aglomerados de microcalcificações podem estar associados ao aumento do risco de câncer de testículo na presença de outros fatores de risco, embora o significado clínico disso permaneça controverso.[51]
Entretanto, uma ultrassonografia negativa não descarta a presença de câncer e deve ser repetida em 6 a 8 semanas em pacientes com achados indeterminados na ultrassonografia ou no exame físico e marcadores tumorais séricos normais.[2] A ultrassonografia deve ser realizada com avaliação por Doppler colorido para confirmar a presença de massa testicular antes da orquiectomia.[47] O uso de Doppler colorido pode ajudar a distinguir tumores de outros edemas escrotais (por exemplo, varicocele).[48] O testículo contralateral também deve ser avaliado quanto à presença de tumores síncronos e microcalcificações, bem como para medir o volume testicular.[47] A biópsia do testículo contralateral pode ser indicada se uma massa suspeita for identificada, o testículo estiver atrofiado ou houver história de criptorquidia. Não é recomendado apenas para microcalcificações testiculares.[46][49][50] Aglomerados de microcalcificações podem estar associados ao aumento do risco de câncer de testículo na presença de outros fatores de risco, embora o significado clínico disso permaneça controverso.[51]
A tomografia computadorizada (TC) da pelve e do abdome com contraste é usada para avaliar o estádio de disseminação do câncer.[2][49][52] A ressonância nuclear magnética (RNM) pode ser útil como modalidade alternativa, se a TC for inconclusiva ou se o meio de contraste for contraindicado devido à alergia do paciente ou à insuficiência renal.[2] A imagem do tórax é obrigatória para avaliar a presença de metástases pulmonares.[2][52] A radiografia torácica é recomendada como exame de imagem do tórax de primeira linha apenas para seminoma em estádio clínico I. A TC de tórax é recomendada como primeira linha para outros tipos de tumor, ou aqueles com marcadores tumorais séricos crescentes pós-orquiectomia, ou com evidência de metástases nos exames de imagem abdominais/pélvicos, radiografia torácica ou exame físico.[2] A tomografia por emissão de pósitrons (PET)-CT não demonstrou ser superior à TC isoladamente e não é recomendada para o estadiamento.[2]
Os marcadores tumorais séricos devem ser obtidos antes e depois da orquiectomia, com estadiamento baseado nos valores mais baixos pós-orquiectomia.[2][49] A combinação de gonadotrofina coriônica humana beta (beta-hCG), alfafetoproteína (AFP) e lactato desidrogenase (LDH) elevadas é diagnóstica da doença. A AFP pode ser elevada por carcinoma embrionário, teratoma, tumores do saco vitelino ou tumores mistos. Os coriocarcinomas e seminomas puros não estão associados a níveis elevados de AFP. Se a histologia mostrar seminoma puro, mas a AFP sérica estiver elevada sem outra causa identificável, o tumor deverá ser reclassificado e tratado como não seminomatoso. Os seminomas podem apresentar elevações modestas de beta-hCG devido à presença de sinciciotrofoblastos no tumor. A LDH está elevada em 40% a 60% de todos os pacientes com seminoma ou tumores de células germinativas não seminomatosos.[53] Em 10% dos não seminomas persistentes ou recorrentes, a LDH é o único marcador elevado.[54] No entanto, ela tem uma alta taxa de falsos-positivos e deve ser usada principalmente para avaliar a carga do tumor. Aproximadamente 80% dos tumores não seminomatosos apresentam marcadores séricos elevados. A AFP e a beta-hCG estão aumentadas em 44% dos casos, a AFP isoladamente está elevada em 26% dos casos e a beta-hCG isoladamente está elevada em 9% dos casos.[53]
A fosfatase alcalina placentária está elevada em até 40% dos casos com doença avançada.[53] No entanto, a fosfatase alcalina placentária não é utilizada na prática clínica de rotina e deve ser limitada a cenários experimentais ou de ensaios clínicos. O microRNA-371a-3p (M371) sérico emergiu como um potencial biomarcador para tumores de células germinativas seminomatosos e não seminomatosos, com sensibilidade e especificidade melhoradas em comparação com marcadores tumorais convencionais.[55] Estudos prospectivos adicionais são necessários para orientar a implementação do M371 na prática clínica de rotina.[56]
Geralmente, o diagnóstico de câncer do testículo é estabelecido por meio da remoção e exame do testículo envolvido (orquiectomia) após obtenção dos marcadores tumorais séricos.
[Figure caption and citation for the preceding image starts]: Seminoma metastático. Imagem à esquerda: coloração H&E em baixa potência. Imagem à direita, coloração de fosfatase alcalina placentária (PLAP) em alta potência. A imagem de H&E mostra ninhos de células malignas com citoplasma claro; as células tumorais são fortemente positivas para PLAP, confirmando o diagnósticoLaw C et al. BMJ Case Rep. 2020 Apr 22;13(4):e233368. doi: 10.1136/bcr-2019-233368; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Não seminomaDo acervo do Dr. Francisco G. La Rosa; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Não seminomaDo acervo do Dr. Francisco G. La Rosa; usado com permissão [Citation ends].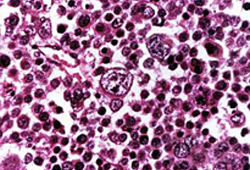 A orquiectomia é fundamental em todos os estádios da doença.[2] A orquiectomia inguinal radical deve ser realizada precocemente na avaliação de uma massa testicular suspeita. Na doença em estádio inicial, uma orquiectomia geralmente é curativa.
A orquiectomia é fundamental em todos os estádios da doença.[2] A orquiectomia inguinal radical deve ser realizada precocemente na avaliação de uma massa testicular suspeita. Na doença em estádio inicial, uma orquiectomia geralmente é curativa.
O uso deste conteúdo está sujeito ao nosso aviso legal