Этиология
Аутоиммунные субэпидермальные пузырные заболевания кожи включают группу буллезных пемфигоидных заболеваний (буллезный пемфигоид, пемфигоид беременных, пемфигоидный плоский лишай, IgA зависимый линейный дерматоз, рубцующийся пемфигоид и анти-p200, анти-p105 и анти-p450 пемфигоид, приобретённый буллезный эпидермолиз и герпетиформный дерматит. За исключением герпетиформного дерматита, все эти нарушения характеризуются циркулирующими и фиксированными в тканях аутоантителами против различных компонентов дермально-эпидермального соединительного комплекса,[15] который является супрамолекулярной структурой, опосредующей адгезию базальных кератиноцитов к лежащей в основе дерме. Связывание антител с различными белками в этом комплексе приводит к дермально-эпидермальному отслаиванию и образованию напряженного пузыря.
Дермально-эпидермальный соединительный комплекс состоит из полудесмосом базальных кератиноцитов, якорных филаментов базальной мембраны и якорных фибрилл папиллярной дермы. Структурные белки в этом комплексе, описанные как аутоантигены при различных аутоиммунных буллезных дерматозах, включают буллезный пемфигоидный антиген 180 (буллезный пемфигоид, пемфигоид беременных, пемфигоид слизистых оболочек, линеарный IgA-зависимый буллезный дерматоз), БП230 (буллезный пемфигоид), интегрин альфа 6 бета 4 (пемфигоид слизистых оболочек), ламинин 5 и 6 (пемфигоид слизистых оболочек) и коллаген типа VII (приобретённый буллезный эпидермолиз).[16] Описано более 300 определенных мутаций 10 различных генов, соответствующих структурным компонентам базальной мембраны, которые приводят к хрупкости кожи и дермально-эпидермальному отслаиванию, связанному с характерными внекожными проявлениями.[15]
Патофизиология
Аутоантитела направлены против двух гемидесмосомных белков, обозначенных БП180 и БП230. В то время как БП230 локализуется внутриклеточно и ассоциируется с гемидесмосомной бляшкой, БП180 является трансмембранным гликопротеином с внеклеточным доменом, состоящим примерно из 1000 аминокислот. Не коллагеновый 16A-домен, который охватывает 76 аминокислот и локализуется непосредственно в прилегающей к трансмембранной области, идентифицируется как иммунодоминантная область эктодомена БП180.[17]
В большинстве сывороток буллезного пемфигоида циркулирующие антитела к BP180NC16A обнаруживаются при уровнях сыворотки, коррелирующих с активностью заболевания.[18] Для формирования поражения необходимы аутоантитела буллезного пемфигоида (с помощью активации комплемента), инфильтрация воспалительных клеток и высвобождение протеаз и различных воспалительных медиаторов, включая цитокины.[19][20] Дальнейшие исследования с применением аналогичного подхода показали, что за это повреждение ткани ответственны анти-BP180NC16A-антитела и нейтрофилы, чужеродные для человека.[21] Применяя подход пассивной передачи IgG, существует in vivo доказательство того, что антитела кроликов, направленные против мышиного гомолога BP180NC16A, являются патогенными для мышей.[22] Данные in vitro и in vivo показывают, что антитела, специфичные для домена BP180NC16A, являются патогенными. Очевидно, что связывание анти-БП180-антитела с антигенными мишенями является критической первой стадией формирования субэпидермального пузыря при буллезном пемфигоиде. Неясно, как подкласс IgG, который является патогенным, непосредственно связан с тяжестью заболевания. Новые данные указывают на аутоантитела против BP180-N IgG1 как на преобладающий подкласс IgG, связанный с острым началом буллезного пемфигоида. Поскольку антитела IgG1 способны фиксировать комплемент, выявляется связь между аутоантителами против БП180 и комплементом в их патогенной роли в возникновении буллезного пемфигоида.[1][23]
Буллезный пемфигоид часто провоцирует эозинофилию крови и тканей, что указывает на то, что хемоаттрактанты могут модулировать инфильтрацию эозинофилов. Эотаксин и интерлейкин (ИЛ)-5 тесно связаны с эозинофилией ткани при буллезном пемфигоиде. Эти данные свидетельствуют о том, что эотаксин и ИЛ-5 являются важными для миграции эозинофилов при поражениях буллезным пемфигоидом и что методы лечения, направленные на ингибирование выработки эотаксина и ИЛ-5, могут снизить воспаление и образование пузырей.[24]
Классификация
Клиническая классификация
Описано несколько клинических вариантов буллезного пемфигоида:[2][3]
Классический (буллезный): наиболее распространенный, напряженные буллы возникают в любом месте, поражение полости рта и глаз редкое, менее значительное, заживление происходит без рубцов или милий[Figure caption and citation for the preceding image starts]: Напряженные, наполненные жидкостью пузыри на нормальной и эритематозной кожеИз коллекции д-ра Весны Петрон-Росик (Dr Vesna Petronic-Rosic) [Citation ends].
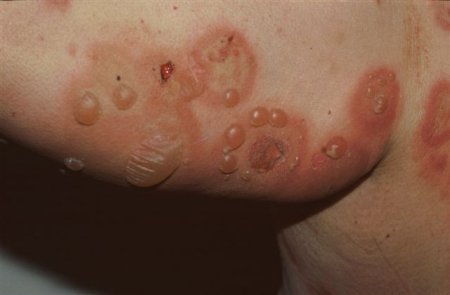 [Figure caption and citation for the preceding image starts]: Напряженные, наполненные жидкостью пузыри на нормальной и эритематозной коже туловища и конечностейИз коллекции д-ра Весны Петрон-Росик (Dr Vesna Petronic-Rosic) [Citation ends].
[Figure caption and citation for the preceding image starts]: Напряженные, наполненные жидкостью пузыри на нормальной и эритематозной коже туловища и конечностейИз коллекции д-ра Весны Петрон-Росик (Dr Vesna Petronic-Rosic) [Citation ends].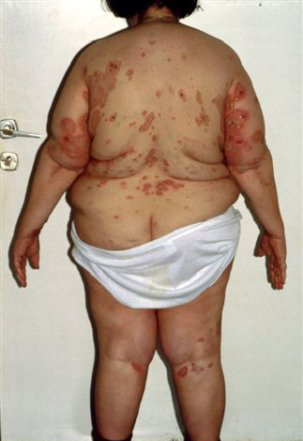
Везикулезный: необычный; группы маленьких, напряженных пузырей на красной или зудящей коже[Figure caption and citation for the preceding image starts]: Везикулезный вариант: напряженные блистерыИз коллекции д-ра Весны Петрон-Росик (Dr Vesna Petronic-Rosic) [Citation ends].

Узловой: редкий; пузыри на нормальной или узловатой коже
Претибиальный: буллы ограничены одной областью тела, такой как голени
Дисгидрозиформный: пузыри локализованы на ладонях и подошвах стоп
Вегетирующий: очень редкий; вегетирующие бляшки в подмышечной впадине, на шее и/или в паховой складке
Генерализованный: редкий, может выглядеть как псориаз или атопический дерматит, могут развиваться везикулы или буллы
Уртикарный: первично проявляется уртикарными областями, которые становятся буллезными поражениями, некоторые никогда не переходят в буллы
Детский: связан с вакцинацией; буллы на ладонях, подошвах стоп, лице
Эритродермический: эритродермия наблюдается сначала по всему телу, затем сыпь в виде изолированных булл.
Использование этого контента попадает под действие нашего заявления об отказе от ответственности