A leucoplasia oral, como definida pela Organização Mundial da Saúde (OMS), é uma lesão predominantemente branca da mucosa oral que não pode ser caracterizada como nenhuma outra lesão definida.[1]Kramer IR, Lucas RB, Pindborg JJ, et al. Definition of leukoplakia and related lesions: an aid to studies on oral precancer. Oral Surg Oral Med Oral Pathol. 1978 Oct;46(4):518-39.
http://www.ncbi.nlm.nih.gov/pubmed/280847?tool=bestpractice.com
[2]Axell T, Holmstrup P, Kramer IRH, et al. International seminar on oral leukoplakia and associated lesions related to tobacco habits. Community Dent Oral Epidemiol. 1984 June;12(3):145-54.[3]Axell T, Pindborg JJ, Smith CJ, et al. Oral white lesions with special reference to precancerous and tobacco-related lesions: conclusions of an international symposium held in Uppsala, Sweden, May 18-21 1994. International Collaborative Group on Oral White Lesions. J Oral Pathol Med. 1996 Feb;25(2):49-54.
http://www.ncbi.nlm.nih.gov/pubmed/8667255?tool=bestpractice.com
Portanto, o diagnóstico é de exclusão de todos os outros possíveis diagnósticos de lesões brancas conhecidas. Diagnósticos alternativos para muitas lesões podem ser sugeridos após uma anamnese e um exame clínico completos, com confirmação por biópsia, se houver dúvidas clínicas.[59]Sankaranarayanan R, Fernandez Garrote L, Lence Anta J, et al. Visual inspection in oral cancer screening in Cuba: a case-control study. Oral Oncol. 2002 Feb;38(2):131-6.
http://www.ncbi.nlm.nih.gov/pubmed/11854059?tool=bestpractice.com
[60]Shugars DC, Patton LL. Detecting, diagnosing, and preventing oral cancer. Nurse Pract 1997 Jun;22(6):105;109-10;113-5.
http://www.ncbi.nlm.nih.gov/pubmed/9211456?tool=bestpractice.com
Uma investigação completa e um diagnóstico preciso são essenciais, pois, embora muitas leucoplasias possam ser benignas, algumas têm potencial significativo de transformação maligna em carcinoma de células escamosas oral.[61]Waldron CA, Shafer WG. Leukoplakia revisited. A clinicopathologic study 3256 oral leukoplakias. Cancer. 1975 Oct;36(4):1386-92.
http://www.ncbi.nlm.nih.gov/pubmed/1175136?tool=bestpractice.com
[62]Wright JM. Oral precancerous lesions and conditions. Semin Dermatol. 1994 Jun;13(2):125-31.
http://www.ncbi.nlm.nih.gov/pubmed/8060824?tool=bestpractice.com
[63]Jaber MA, Porter SR, Gilthorpe MS, et al. Risk factors for oral epithelial dysplasia - the role of smoking and alcohol. Oral Oncol. 1999 Mar;35(2):151-6.
http://www.ncbi.nlm.nih.gov/pubmed/10435149?tool=bestpractice.com
[31]Petti S, Scully C. Association between different alcoholic beverages and leukoplakia among non- to moderate-drinking adults: a matched case-control study. Eur J Cancer. 2006 Mar;42(4):521-7.
http://www.ncbi.nlm.nih.gov/pubmed/16427777?tool=bestpractice.com
Sendo assim, o médico deve estar ciente da importância da leucoplasia e de sua diversidade de comportamentos, pois o diagnóstico precoce de lesões potencialmente malignas pode também reduzir a morbidade e a mortalidade.[64]Sankaranarayanan R. Screening for cervical and oral cancers in India is feasible and effective. Natl Med J India. 2005 Nov-Dec;18(6):281-4.
http://www.ncbi.nlm.nih.gov/pubmed/16483024?tool=bestpractice.com
O exame histológico é recomendado para avaliar a presença e o grau de qualquer displasia epitelial, que tem sido o método convencional utilizado para prever o potencial maligno.[65]Mashberg A, Samit A. Early diagnosis of asymptomatic oral and oropharyngeal squamous cancers. CA Cancer J Clin. 1995 Nov-Dec;45(6):328-51.
http://onlinelibrary.wiley.com/doi/10.3322/canjclin.45.6.328/epdf
http://www.ncbi.nlm.nih.gov/pubmed/7583906?tool=bestpractice.com
Em algumas partes do mundo, os dentistas podem não ser treinados para realizar uma biópsia; portanto, recomenda-se encaminhamento para um especialista para a realização desse procedimento.
Leucoplasias com potencial maligno
As lesões da mucosa oral potencialmente malignas (pré-cânceres orais) incluem, principalmente, algumas leucoplasias e eritroplasia (também conhecida como eritroleucoplasia). A eritroplasia, embora muito menos comum que as leucoplasias, tem maior potencial maligno. A eritroplasia apresenta-se como uma placa vermelha aveludada e, pelo menos, 85% dos casos mostram franca malignidade ou displasia epitelial grave.[66]Quah SR, Cockerham WC, eds. International encyclopedia of public health. 2nd ed. Oxford: Elsevier; 2017. A leucoplasia, especialmente quando apresenta lesões vermelhas misturadas (leucoplasia salpicada), é potencialmente maligna. Ao utilizar um sistema microscópico binário de classificação, em que as lesões são classificadas em displasia de baixo risco ou displasia de alto risco, esta última foi um indicativo significativo na avaliação da transformação maligna.[67]Liu W, Wang YF, Zhou HW, et al. Malignant transformation of oral leukoplakia: a retrospective cohort study of 218 Chinese patients. BMC Cancer. 2010 Dec 16;10:685.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3009685/?tool=pubmed
http://www.ncbi.nlm.nih.gov/pubmed/21159209?tool=bestpractice.com
Lesões, tais como a leucoplasia verrucosa proliferativa, a leucoplasia sublingual (ceratose sublingual) e a leucoplasia por Candida, têm também maior potencial maligno; a leucoplasia verrucosa proliferativa tem risco mais significativo de transformação maligna quando comparada com os outros tipos de leucoplasia. Um grande estudo de coorte de casos realizado com adultos nos EUA com 65 anos ou mais de idade constatou que pacientes com câncer oral e leucoplasia prévia apresentavam um risco menor de morte relacionada a este câncer que aqueles que desenvolveram carcinoma escamoso oral sem nenhuma leucoplasia precursora. O estudo concluiu que a identificação e a análise da leucoplasia pode levar à detecção antecipada de câncer e melhorar os níveis de sobrevida.[68]Yanik EL, Katki HA, Silverberg MJ, et al. Leukoplakia, oral cavity cancer risk, and cancer survival in the US elderly. Cancer Prev Res (Phila). 2015 Sept;8(9):857-63.
http://www.ncbi.nlm.nih.gov/pubmed/4560597?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: EritroplasiaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].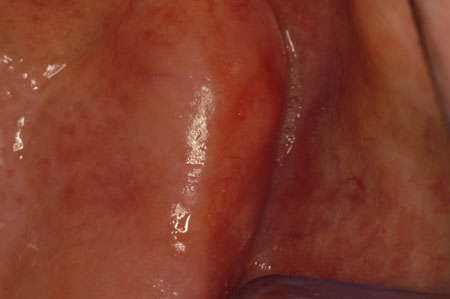 [Figure caption and citation for the preceding image starts]: Leucoplasia salpicadaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia salpicadaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].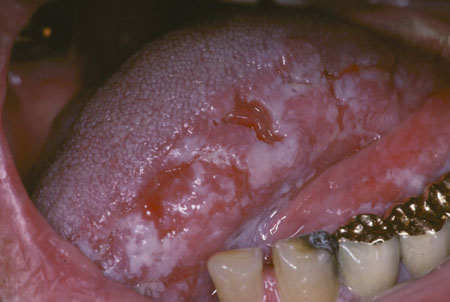 [Figure caption and citation for the preceding image starts]: Leucoplasia verrucosa proliferativaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia verrucosa proliferativaCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Leucoplasia sublingualCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia sublingualCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Leucoplasia por CandidaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia por CandidaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].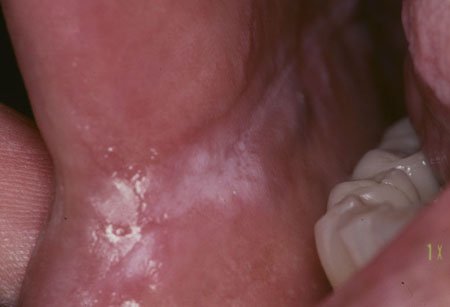
Exame físico clínico
Um exame físico completo da cavidade oral e dos linfonodos regionais é essencial. Muitas lesões orais potencialmente malignas (incluindo a leucoplasia) e cânceres podem ser detectados visualmente, mas são fáceis de serem ignorados, especialmente se o exame físico não for exaustivo.[59]Sankaranarayanan R, Fernandez Garrote L, Lence Anta J, et al. Visual inspection in oral cancer screening in Cuba: a case-control study. Oral Oncol. 2002 Feb;38(2):131-6.
http://www.ncbi.nlm.nih.gov/pubmed/11854059?tool=bestpractice.com
[60]Shugars DC, Patton LL. Detecting, diagnosing, and preventing oral cancer. Nurse Pract 1997 Jun;22(6):105;109-10;113-5.
http://www.ncbi.nlm.nih.gov/pubmed/9211456?tool=bestpractice.com
[69]Massano J, Regateiro FS, Januario G, et al. Oral squamous cell carcinoma: review of prognostic and predictive factors. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006 Jul;102(1):67-76.
http://www.ncbi.nlm.nih.gov/pubmed/16831675?tool=bestpractice.com
A possibilidade de disseminação das alterações na mucosa ("mudança de campo") ou de uma segunda neoplasia exige um exame de toda a mucosa oral.[70]Slaughter DP, Southwick HW, Smejkal W. Field cancerization in oral stratified squamous epithelium; clinical implications of multicentric origin. Cancer. 1953 Sept;6(5):963-8.
http://www.ncbi.nlm.nih.gov/pubmed/13094644?tool=bestpractice.com
Alterações moleculares indicativas de potencial maligno podem não produzir lesões clinicamente evidentes e podem se estender muito além da lesão clinicamente identificável, o que explica, em parte, o aumento do risco de segundos tumores primários em pacientes com pré-câncer e câncer oral.[71]Braakhuis BJ, Brakenhoff RH, Leemans CR. Head and neck cancer: molecular carcinogenesis. Ann Oncol. 2005;16(suppl 2):ii249-50.
http://annonc.oxfordjournals.org/cgi/reprint/16/suppl_2/ii249
http://www.ncbi.nlm.nih.gov/pubmed/15958466?tool=bestpractice.com
[72]Braakhuis BJ, Leemans CR, Brakenhoff RH. Expanding fields of genetically altered cells in head and neck squamous carcinogenesis. Semin Cancer Biol. 2005 Apr;15(2):113-20.
http://www.ncbi.nlm.nih.gov/pubmed/15652456?tool=bestpractice.com
[73]Tabor MP, Brakenhoff RH, Ruijter-Schippers HJ, et al. Genetically altered fields as origin of locally recurrent head and neck cancer: a retrospective study. Clin Cancer Res. 2004 Jun 1;10(11):3607-13.
http://clincancerres.aacrjournals.org/content/10/11/3607.full
http://www.ncbi.nlm.nih.gov/pubmed/15173066?tool=bestpractice.com
[74]Braakhuis BJ, Tabor MP, Kummer JA, et al. A genetic explanation of Slaughter's concept of field cancerization: evidence and clinical implications. Cancer Res. 2003 Apr 16;63(8):1727-30.
http://cancerres.aacrjournals.org/cgi/content/full/63/8/1727
http://www.ncbi.nlm.nih.gov/pubmed/12702551?tool=bestpractice.com
[75]Lippman SM, Hong WK. Second malignant tumors in head and neck squamous cell carcinoma: the overshadowing threat for patients with early-stage disease. Int J Radiat Oncol Biol Phys. 1989 Sept;17(3):691-4.
http://www.ncbi.nlm.nih.gov/pubmed/2674081?tool=bestpractice.com
Algumas condições comuns que podem causar confusão no diagnóstico incluem os grânulos de Fordyce e a língua geográfica. Coleções de resíduos (matéria alba) ou fungos (candidíase) também podem ser brancas, mas, em geral, estas podem ser facilmente removidas com uma gaze. Outras lesões também aparentam ser brancas, pois geralmente são compostas por queratina espessa. A leucoplasia pilosa oral, uma lesão de etiologia viral, é observada principalmente em pessoas imunossuprimidas (por exemplo, infecção pelo vírus da imunodeficiência humana [HIV]) e não tem potencial maligno conhecido.
As lesões brancas são geralmente indolores, mas podem ser focais, multifocais, estriadas ou difusas, e essas características podem guiar o diagnóstico. Por exemplo:
As lesões focais são muitas vezes causadas por mordidas na bochecha, na linha oclusal
As lesões multifocais são comuns na candidíase (candidíase pseudomembranosa) e no líquen plano; lesões estriadas são típicas do líquen plano
Áreas brancas difusas são observadas na mucosa oral (no leucoedema) e no palato (na estomatite nicotínica).
Outras causas das lesões orais brancas devem ser consideradas. Após a exclusão dessas causas, pode-se fazer um diagnóstico de leucoplasia.[Figure caption and citation for the preceding image starts]: Leucoplasia homogêneaCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Leucoplasia pilosa oralCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia pilosa oralCortesia do Dr. James Sciubba; usado com permissão [Citation ends].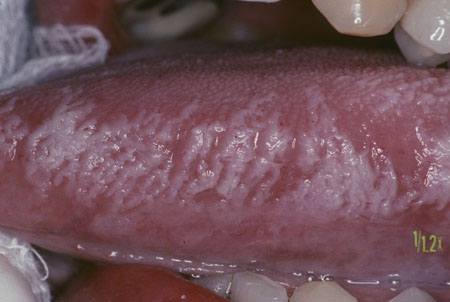 [Figure caption and citation for the preceding image starts]: Mastigação de lábios/bochechasCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Mastigação de lábios/bochechasCortesia do Dr. James Sciubba; usado com permissão [Citation ends].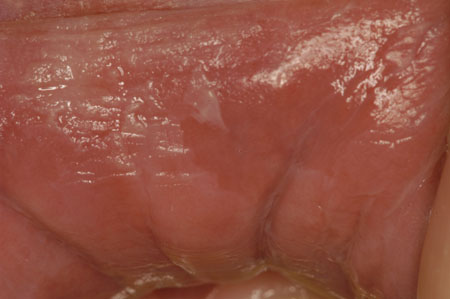
Causas das lesões orais brancas
[Figure caption and citation for the preceding image starts]: Causas das lesões orais brancasCriado pela equipe do BMJ Knowledge Centre [Citation ends].
Testes para excluir outros diagnósticos
Embora, em muitos casos, as causas possam ser diagnosticadas após história e exame físico criteriosos, outras podem ser confirmados apenas após uma biópsia representativa da lesão. Investigações laboratoriais adicionais podem auxiliar na exclusão de diagnósticos alternativos. Elas podem incluir sorologia para Treponema pallidum e teste para autoanticorpos quando se considera a possibilidade de lúpus eritematoso da mucosa.
Teste de primeira linha
A dificuldade está na determinação do potencial maligno da leucoplasia, o que requer uma avaliação das formas clínicas específicas e a estimativa da probabilidade de transformação. No entanto, o diagnóstico clínico isolado é insuficiente na determinação e na exclusão das doenças maligna e pré-maligna; até mesmo profissionais experientes e altamente treinados não conseguem identificar todos os pré-cânceres e carcinomas de células escamosas orais (CCEO) em estágios iniciais apenas pela inspeção visual.[76]Silverman S Jr. Early diagnosis of oral cancer. Cancer. 1988 Oct 15;62(suppl 8):1796-9.
http://www.ncbi.nlm.nih.gov/pubmed/3167796?tool=bestpractice.com
Além disso, as características clássicas reconhecidas do CCEO, como ulceração, induração, elevação, sangramento e linfadenopatia cervical são características da doença em estágio avançado, e não precoce.[77]Mashberg A, Feldman LJ. Clinical criteria for identifying early oral and oropharyngeal carcinoma: erythroplasia revisited. Am J Surg. 1988 Oct;156(4):273-5.
http://www.ncbi.nlm.nih.gov/pubmed/3177749?tool=bestpractice.com
Infelizmente, dados clínicos sugerem que frequentemente há um atraso substancial na obtenção do espécime de biópsia, até mesmo quando as lesões orais apresentam características evidentes de câncer.[78]Scully C, Malamos D, Levers BG, et al. Sources and patterns of referrals of oral cancer: role of general practitioners. Br Med J (Clin Res Ed). 1986 Sept 6;293(6547):599-601.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1341389
http://www.ncbi.nlm.nih.gov/pubmed/3092946?tool=bestpractice.com
[79]Dimitroulis G, Reade P, Wiesenfeld D. Referral patterns of patients with oral squamous cell carcinoma, Australia. Eur J Cancer B Oral Oncol. 1992 Jul;28B(1):23-7.
http://www.ncbi.nlm.nih.gov/pubmed/1422466?tool=bestpractice.com
Biópsia
Uma biópsia incisional é invariavelmente indicada para a maior parte das leucoplasias e deve ser suficientemente grande e representativa. Uma biópsia excisional deve ser evitada, pois é improvável que as excisões tenham uma margem adequada de tecido se a lesão for comprovadamente maligna e pode limitar as evidências clínicas do local e natureza da lesão para o cirurgião.
Resultados falso-negativos são ocasionalmente possíveis na biópsia incisional e, mesmo quando a displasia tiver sido excluída em uma leucoplasia por biópsia incisional, estudos têm mostrado que as lesões, se excisionadas completamente, podem comprovar a presença de CCEO em até 10% dos pacientes.[80]Chiesa F, Sala L, Costa L, et al. Excision of oral leukoplakias by CO2 laser on an outpatient basis: a useful procedure for prevention and early detection of oral carcinomas. Tumori. 1986 Jun 30;72(3):307-12.
http://www.ncbi.nlm.nih.gov/pubmed/3739009?tool=bestpractice.com
[81]Holmstrup P, Vedtofte P, Reibel J, et al. Oral premalignant lesions: is a biopsy reliable? J Oral Pathol Med. 2007 May;36(5):262-6.
http://www.ncbi.nlm.nih.gov/pubmed/17448135?tool=bestpractice.com
Isso é explicado, em parte, por dados que mostram que mudanças malignas iniciais podem estar dispersas através e além de uma lesão clínica potencialmente maligna.[72]Braakhuis BJ, Leemans CR, Brakenhoff RH. Expanding fields of genetically altered cells in head and neck squamous carcinogenesis. Semin Cancer Biol. 2005 Apr;15(2):113-20.
http://www.ncbi.nlm.nih.gov/pubmed/15652456?tool=bestpractice.com
[82]Califano J, Westra WH, Meininger G, et al. Genetic progression and clonal relationship of recurrent premalignant head and neck lesions. Clin Cancer Res. 2000 Feb;6(2):347-52.
http://clincancerres.aacrjournals.org/cgi/content/full/6/2/347
http://www.ncbi.nlm.nih.gov/pubmed/10690509?tool=bestpractice.com
Como é mais provável que as áreas vermelhas mostrem qualquer displasia em relação às áreas brancas, a biópsia deve incluir as áreas vermelhas.
Patologia
A análise histopatológica por um patologista experiente é um aspecto crucial do manejo, uma vez que a variabilidade inter e intraobservador entre patologistas é significativa.[83]Abbey LM, Kaugars GE, Gunsolley JC, et al. Intraexaminer and interexaminer reliability in the diagnosis of oral epithelial dysplasia. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1995 Aug;80(2):188-91.
http://www.ncbi.nlm.nih.gov/pubmed/7552884?tool=bestpractice.com
[84]Karabulut A, Reibel J, Therkildsen MH, et al. Observer variability in the histologic assessment of oral premalignant lesions. J Oral Pathol Med. 1995 May;24(5):198-200.
http://www.ncbi.nlm.nih.gov/pubmed/7616457?tool=bestpractice.com
[85]Fischer DJ, Epstein JB, Morton TH, et al. Interobserver reliability in the histopathologic diagnosis of oral premalignant and malignant lesions. J Oral Pathol Med. 2004 Feb;33(2):65-70.
http://www.ncbi.nlm.nih.gov/pubmed/14720191?tool=bestpractice.com
[86]Fischer DJ, Epstein JB, Morton TH Jr, et al. Reliability of histologic diagnosis of clinically normal intraoral tissue adjacent to clinically suspicious lesions in former upper aerodigestive tract cancer patients. Oral Oncol. 2005 May;41(5):489-96.
http://www.ncbi.nlm.nih.gov/pubmed/15878753?tool=bestpractice.com
[87]Woolgar JA. Histopathological prognosticators in oral and oropharyngeal squamous cell carcinoma. Oral Oncol. 2006 Mar;42(3):229-39.
http://www.ncbi.nlm.nih.gov/pubmed/16150633?tool=bestpractice.com
Se, após uma biópsia inicial, ainda restarem dúvidas clínicas sobre a obtenção de uma amostra representativa (por exemplo, se o laudo patológico negar malignidade, mas, clinicamente, ainda houver suspeitas), a repetição da biópsia será indicada.
Em análises histológicas de rotina, as leucoplasias demonstram uma ampla gama de características histológicas, que vão de alterações benignas a displásicas de vários graus. As características histológicas benignas incluem orto/paraceratose sem sinais de queratina em áreas profundas da superfície (disceratose, uma característica da displasia). Além disso, é comum observar espessamento ou aumento no volume global da camada de células espinhosas ou espinocelular (acantose). Notavelmente, na maior parte das leucoplasias (mais de 60%), apenas a hiperceratose com ou sem acantose será observada nas análises microscópicas.[88]Lathanasupkul P, Poomsawat S, Punyasingh J. A clinicopathologic study of oral leukoplakia and erythroplakia in a Thai population. Quintessence Int. 2007 Sept;38(8):e448-55.
http://www.ncbi.nlm.nih.gov/pubmed/17823667?tool=bestpractice.com
Geralmente, há ausência de atipia celular definitiva nas camadas basais e mais superficiais do epitélio. No entanto, um estudo realizado em uma população tailandesa constatou que 10.6% das leucoplasias tinham natureza displásica, enquanto 4.9% foram diagnosticadas como carcinoma de células escamosas.[88]Lathanasupkul P, Poomsawat S, Punyasingh J. A clinicopathologic study of oral leukoplakia and erythroplakia in a Thai population. Quintessence Int. 2007 Sept;38(8):e448-55.
http://www.ncbi.nlm.nih.gov/pubmed/17823667?tool=bestpractice.com
Quando presente, a avaliação da displasia epitelial deve ser graduada (por exemplo, leve, moderada ou grave).[89]Odell E, Kujan O, Warnakulasuriya S, et al. Oral epithelial dysplasia: recognition, grading and clinical significance. Oral Dis. 2021 Nov;27(8):1947-76.
http://www.ncbi.nlm.nih.gov/pubmed/34418233?tool=bestpractice.com
A neoplasia intraepitelial, um conceito criado para a mucosa do colo uterino e estendido para outras mucosas, foi adaptada à mucosa oral (neoplasia intraepitelial oral) e utilizada por alguns como termo diagnóstico.[90]Kuffer R, Lombardi T. Premalignant lesions of the oral mucosa: a discussion about the place of oral intraepithelial neoplasia (OIN). Oral Oncol. 2002 Feb;38(2):125-30.
http://www.ncbi.nlm.nih.gov/pubmed/11854058?tool=bestpractice.com
[89]Odell E, Kujan O, Warnakulasuriya S, et al. Oral epithelial dysplasia: recognition, grading and clinical significance. Oral Dis. 2021 Nov;27(8):1947-76.
http://www.ncbi.nlm.nih.gov/pubmed/34418233?tool=bestpractice.com
As alterações epiteliais microscópicas estruturadas sob alterações arquitetônicas ou características celulares atípicas e associadas a pré-malignidade ou displasia epitelial incluem a presença de:[5]Warnakulasuriya S, Kujan O, Aguirre-Urizar JM, et al. Oral potentially malignant disorders: a consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis. 2021 Nov;27(8):1862-80.
http://www.ncbi.nlm.nih.gov/pubmed/33128420?tool=bestpractice.com
Foi também proposto um sistema de graduação binária que classifica as displasias como de baixo e alto riscos.[89]Odell E, Kujan O, Warnakulasuriya S, et al. Oral epithelial dysplasia: recognition, grading and clinical significance. Oral Dis. 2021 Nov;27(8):1947-76.
http://www.ncbi.nlm.nih.gov/pubmed/34418233?tool=bestpractice.com
Técnicas adjuvantes de diagnóstico
Há um número de auxiliares adjuvantes de diagnóstico para a avaliação clínica da patologia da mucosa oral. Contudo, há falta de evidências de eficácia.[91]Rethman M, Carpenter W, Cohen EE, et al. Evidence-based clinical recommendations regarding screening for oral squamous cell carcinomas. J Am Dent Assoc. 2010 May;14(5):509-20.
http://www.ncbi.nlm.nih.gov/pubmed/20436098?tool=bestpractice.com
[92]Fedele S. Diagnostic aids in the screening of oral cancer. Head Neck Oncol. 2009 Jan 30;1:5.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2654034/?tool=pubmed
http://www.ncbi.nlm.nih.gov/pubmed/19284694?tool=bestpractice.com
Com base em uma diretriz de práticas clínicas baseada em evidências emitida pela American Dental Association (ADA), elas incluem:[93]Lingen MW, Abt E, Agrawal N, et al. Evidence-based clinical practice guideline for the evaluation of potentially malignant disorders in the oral cavity: a report of the American Dental Association. J Am Dent Assoc. 2017 Oct;148(10):712-27;e10.
https://jada.ada.org/article/S0002-8177(17)30701-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/28958308?tool=bestpractice.com
Veja abaixo uma descrição de cada uma dessas ferramentas de rastreamento.
Biópsia por escova
Uma biópsia oral por escova pode ser utilizada para descartar displasias entre lesões orais comuns, de aparência inofensiva, não suficientemente sugestivas a ponto de justificar uma biópsia com bisturi. Esse teste usa uma pequena escova de nylon para coletar amostras celulares de uma área suspeita que, depois, são enviadas para análise computadorizada. A coleta da amostra é simples, causa pouco ou nenhum sangramento ou dor e não requer anestesia; no entanto, é necessária uma amostragem precisa da anormalidade. Um laudo destacando a presença de quaisquer células anormais e um relato escrito pelo patologista são enviados de volta ao médico com uma recomendação para biópsia incisional convencional se forem detectadas anormalidades significativas.
Esse teste revelou uma sensibilidade maior que 92% a 96% e uma especificidade maior que 90% a 94% na detecção de displasia epitelial e carcinoma de células escamosas oral (CCEO), com um valor preditivo positivo de 38% a 44%.[94]Sciubba JJ. Improving detection of precancerous and cancerous oral lesions: computer-assisted analysis of the oral brush biopsy. U.S. Collaborative OralCDx Study Group. J Am Dent Assoc. 1999 Oct;130(10):1445-57.
http://www.ncbi.nlm.nih.gov/pubmed/10570588?tool=bestpractice.com
[95]Scheifele C, Schmidt-Westhausen A, Dietrich T, et al. The sensitivity and specificity of the OralCDx technique: evaluation of 103 cases. Oral Oncol. 2004 Sept;40(8):824-8.
http://www.ncbi.nlm.nih.gov/pubmed/15288838?tool=bestpractice.com
[96]Svirsky JA, Burns JC, Carpenter WM, et al. Comparison of computer-assisted brush biopsy results with follow up scalpel biopsy and histology. Gen Dent. 2002 Nov-Dec;50(6):500-3.
http://www.ncbi.nlm.nih.gov/pubmed/12572180?tool=bestpractice.com
[97]Kosicki DM, Riva C, Pajarola GF, et al. Oral CDx brush biopsy - a tool for early diagnosis of oral squamous cell carcinoma [in German]. Schweiz Monatsschr Zahnmed. 2007;117(3):222-7.
http://www.ncbi.nlm.nih.gov/pubmed/17425240?tool=bestpractice.com
[98]Poate TW, Buchanan JA, Hodgson TA, et al. An audit of the efficacy of the oral brush biopsy technique in a specialist Oral Medicine unit. Oral Oncol. 2004 Sept;40(8):829-34.
http://www.ncbi.nlm.nih.gov/pubmed/15288839?tool=bestpractice.com
A biópsia por escova tem sido utilizada para detectar CCEO não detectado pela biópsia com bisturi.[99]Remmerbach TW, Weidenbach H, Hemprich A, et al. Earliest detection of oral cancer using non-invasive brush biopsy including DNA-image-cytometry: report on four cases. Anal Cell Pathol. 2003;25(4):159-66.
http://www.ncbi.nlm.nih.gov/pubmed/14501082?tool=bestpractice.com
Contudo, há relatos de casos de CCEO em pacientes em que a biópsia por escova foi negativa.[100]Potter TJ, Summerlin DJ, Campbell JH. Oral malignancies associated with negative transepithelial brush biopsy. J Oral Maxillofac Surg. 2003 Jun;61(6):674-7.
http://www.ncbi.nlm.nih.gov/pubmed/12796875?tool=bestpractice.com
Os desfechos da biópsia por escova podem ser melhorados com o uso de técnicas de contagem moleculares (por exemplo, mutações no p53, citometria de DNA e agNOR [contagens de proteínas da região organizadora nucleolar]).[101]Scheifele C, Schlechte H, Bethke G, et al. Detection of TP53-mutations in brush biopsies from oral leukoplakias [in German]. Mund Kiefer Gesichtschir. 2002 Nov;6(6):410-4.
http://www.ncbi.nlm.nih.gov/pubmed/12447653?tool=bestpractice.com
[102]Remmerbach TW, Mathes SN, Weidenbach H, et al. Noninvasive brush biopsy as an innovative tool for early detection of oral carcinomas [in German]. Mund Kiefer Gesichtschir. 2004 Jul;8(4):229-36.
http://www.ncbi.nlm.nih.gov/pubmed/15293118?tool=bestpractice.com
[103]Maraki D, Becker J, Boecking A. Cytologic and DNA-cytometric very early diagnosis of oral cancer. J Oral Pathol Med. 2004 Aug;33(7):398-404.
http://www.ncbi.nlm.nih.gov/pubmed/15250831?tool=bestpractice.com
[104]Remmerbach TW, Weidenbach H, Muller C, et al. Diagnostic value of nucleolar organizer regions (AgNORs) in brush biopsies of suspicious lesions of the oral cavity. Anal Cell Pathol. 2003;25(3):139-46.
http://www.ncbi.nlm.nih.gov/pubmed/12775918?tool=bestpractice.com
Coloração vital com azul de toluidina
O azul de toluidina (AT) é um corante metacromático econômico, de fácil acesso e com alta afinidade por DNA e RNA. Ele cora rapidamente os tecidos anormais, mas não a mucosa normal. Vários estudos têm demonstrado a capacidade do AT de detectar lesões pré-malignas orais, inclusive leucoplasia oral e câncer oral, com alta sensibilidade. No entanto, a coloração é também absorvida por outras condições ulcerativas. Portanto, a especificidade da técnica é baixa.[105]Jayasinghe RD, Hettiarachchi PVKS, Amugoda D, et al. Validity of toluidine blue test as a diagnostic tool for high risk oral potentially malignant disorders - a multicentre study in Sri Lanka. J Oral Biol Craniofac Res. 2020 Oct-Dec;10(4):547-51.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7475265
http://www.ncbi.nlm.nih.gov/pubmed/32923360?tool=bestpractice.com
Sistemas ópticos
O interesse no uso potencial de sistemas de espectroscopia óptica para fornecer diagnóstico tecidual em tempo real e de forma não invasiva tem aumentado.[106]Swinson B, Jerjes W, El-Maaytah M, et al. Optical techniques in diagnosis of head and neck malignancy. Oral Oncol. 2006 Mar;42(3):221-8.
http://www.ncbi.nlm.nih.gov/pubmed/16140566?tool=bestpractice.com
[107]Suhr MA, Hopper C, Jones L, et al. Optical biopsy systems for the diagnosis and monitoring of superficial cancer and precancer. Int J Oral Maxillofac Surg. 2000 Dec;29(6):453-7.
http://www.ncbi.nlm.nih.gov/pubmed/11202330?tool=bestpractice.com
[108]Sharwani A, Jerjes W, Salih V, et al. Assessment of oral premalignancy using elastic scattering spectroscopy. Oral Oncol. 2006 Apr;42(4):343-9.
http://www.ncbi.nlm.nih.gov/pubmed/16321565?tool=bestpractice.com
Os sistemas de imagem à base de autofluorescência consistem em dispositivos manuais simples e portáteis baseados na visualização direta da fluorescência tecidual. O tecido anormal geralmente se mostra como uma área irregular e escura que se destaca do padrão de fluorescência verde normal do tecido saudável circundante.[109]Awan KH, Morgan PR, Warnakulasuriya S. Utility of chemiluminescence (ViziLite™) in the detection of oral potentially malignant disorders and benign keratoses. J Oral Pathol Med. 2011 Aug;40(7):541-4.
http://www.ncbi.nlm.nih.gov/pubmed/21615500?tool=bestpractice.com
[110]Awan KH, Morgan PR, Warnakulasuriya S. Evaluation of an autofluorescence based imaging system (VELscope™) in the detection of oral potentially malignant disorders and benign keratoses. Oral Oncol. 2011 Apr;47(4):274-7.
http://www.ncbi.nlm.nih.gov/pubmed/21396880?tool=bestpractice.com
Outra técnica envolve um enxágue bucal com ácido acético, após o qual a mucosa é examinada com uma fonte de luz azul-esbranquiçada. A fonte de luz é gerada por reação química, daí o termo quimioluminescência. A base do teste é que a leucoplasia oral tem uma refletância tecidual diferencial, e a placa pode parecer "mais branca", com maior visibilidade e maior nitidez da lesão durante o exame. Entretanto, a especificidade do teste é baixa.[109]Awan KH, Morgan PR, Warnakulasuriya S. Utility of chemiluminescence (ViziLite™) in the detection of oral potentially malignant disorders and benign keratoses. J Oral Pathol Med. 2011 Aug;40(7):541-4.
http://www.ncbi.nlm.nih.gov/pubmed/21615500?tool=bestpractice.com
Tais adjuntos ópticos podem auxiliar na identificação de lesões na mucosa e na seleção de locais para biópsia.[111]Mendonca P, Sunny SP, Mohan U, et al. Non-invasive imaging of oral potentially malignant and malignant lesions: a systematic review and meta-analysis. Oral Oncol. 2022 Jul;130:105877.
http://www.ncbi.nlm.nih.gov/pubmed/35617750?tool=bestpractice.com
Eles também podem auxiliar na identificação de anormalidades celulares e moleculares não visíveis a olho nu durante o exame físico de rotina, e podem fornecer informações adicionais sobre o tecido adjacente à lesão da mucosa.[112]Westra WH, Sidransky D. Fluorescence visualization in oral neoplasia: shedding light on an old problem. Clin Cancer Res. 2006 Nov 15;12(22):6594-7.
http://clincancerres.aacrjournals.org/cgi/content/full/12/22/6594
http://www.ncbi.nlm.nih.gov/pubmed/17121876?tool=bestpractice.com
[113]Rosin MP, Cheng X, Poh C, et al. Use of allelic loss to predict malignant risk for low-grade oral epithelial dysplasia. Clin Cancer Res. 2000 Feb;6(2):357-62.
http://clincancerres.aacrjournals.org/cgi/content/full/6/2/357
http://www.ncbi.nlm.nih.gov/pubmed/10690511?tool=bestpractice.com
Os dados são conflitantes com relação aos benefícios clínicos; estudos mostraram taxas de detecção (para lesões displásicas) similares àquelas do diagnóstico clínico convencional e seleção do local da biópsia.[114]Oh ES, Laskin DM. Efficacy of the ViziLite system in the identification of oral lesions. J Oral Maxillofac Surg. 2007 Mar;65(3):424-6.
http://www.ncbi.nlm.nih.gov/pubmed/17307587?tool=bestpractice.com
[115]Epstein JB, Gorsky M, Lonky S, et al. The efficacy of oral lumenoscopy (ViziLite) in visualizing oral mucosal lesions. Spec Care Dentist. 2006 Jul-Aug;26(4):171-4.
http://www.ncbi.nlm.nih.gov/pubmed/16927741?tool=bestpractice.com
[116]Lane PM, Gilhuly T, Whitehead P, et al. Simple device for the direct visualization of oral-cavity tissue fluorescence. J Biomed Opt. 2006 Mar-Apr;11(2):024006.
http://www.ncbi.nlm.nih.gov/pubmed/16674196?tool=bestpractice.com
[117]Poh CF, Ng SP, Williams PM, et al. Direct fluorescence visualization of clinically occult high-risk oral premalignant disease using a simple hand-held device. Head Neck. 2007 Jan;29(1):71-6.
http://www.ncbi.nlm.nih.gov/pubmed/16983693?tool=bestpractice.com
[118]Poh CF, Zhang L, Anderson DW, et al. Fluorescence visualization detection of field alterations in tumor margins of oral cancer patients. Clin Cancer Res. 2006 Nov 15;12(22):6716-22.
http://clincancerres.aacrjournals.org/cgi/content/full/12/22/6716
http://www.ncbi.nlm.nih.gov/pubmed/17121891?tool=bestpractice.com
No entanto, as lesões orais visualizadas com esses adjuvantes ópticos requerem uma biópsia formal para determinar as alterações patológicas subjacentes.
O diagnóstico fotodinâmico (DFD) com ácido 5-aminolevulínico (DFD-ALA) permite a visualização de lesões de leucoplasia como fluorescência vermelha e tem demonstrado sucesso na detecção de doenças bucais.[119]Tatehara S, Sato T, Takebe Y, et al. Photodynamic diagnosis using 5-aminolevulinic acid with a novel compact system and chromaticity analysis for the detection of oral Ccancer and high-risk potentially malignant oral disorders. Diagnostics (Basel). 2022 Jun 23;12(7):1532.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9321203
http://www.ncbi.nlm.nih.gov/pubmed/35885438?tool=bestpractice.com
Em comparação com outros sistemas ópticos, é descrita uma melhora na sensibilidade e na especificidade para detectar graus mais altos de displasia. No entanto, são necessárias mais pesquisas antes de recomendá-lo para a prática de rotina.
Marcadores moleculares e cromossômicos
A habilidade de predizer a transformação maligna subsequente ao estabelecimento de uma análise clínica e histológica de condições pré-malignas está relacionada à identificação de um conjunto de marcadores moleculares que são fácil e economicamente aplicáveis. Essas técnicas são úteis nas visitas de rotina de acompanhamento necessárias após a investigação do diagnóstico.
Estudos produziram vários marcadores moleculares que têm valor potencial no auxílio à predição do futuro comportamento dessas lesões.[21]Zhang L, Rosin MP. Loss of heterozygosity: a potential tool in management of oral premalignant lesions? J Oral Pathol Med. 2001 Oct;30(9):513-20.
http://www.ncbi.nlm.nih.gov/pubmed/11555152?tool=bestpractice.com
[17]Monteiro L, Mello FW, Warnakulasuriya S. Tissue biomarkers for predicting the risk of oral cancer in patients diagnosed with oral leukoplakia: a systematic review. Oral Dis. 2021 Nov;27(8):1977-92.
http://www.ncbi.nlm.nih.gov/pubmed/33290585?tool=bestpractice.com
Por exemplo, na avaliação da leucoplasia que envolve áreas chamadas de alto risco, houve níveis mais altos de alterações genéticas associadas a um risco elevado de progressão para carcinoma por meio de perdas elevadas da heterozigosidade nas regiões dos cromossomos 3p e/ou 9p.[120]Zhang L, Cheung KJ Jr, Lam WL, et al. Increased genetic damage in oral leukoplakia from high risk sites: potential impact on staging and clinical management. Cancer. 2001 Jun 1;91(11):2148-55.
http://www.ncbi.nlm.nih.gov/pubmed/11391596?tool=bestpractice.com
A podoplanina, uma glicoproteína transmembrana, poderia ser um biomarcador valioso no futuro para avaliação de risco de transformação maligna em pacientes com leucoplasia oral.[121]de Vicente JC, Rodrigo JP, Rodriguez-Santamarta T, et al. Podoplanin expression in oral leukoplakia: tumorigenic role. Oral Oncol. 2013 Jun;49(6):598-603.
http://www.ncbi.nlm.nih.gov/pubmed/23473850?tool=bestpractice.com
Além disso, o desenvolvimento de tecnologia de análise genética e outras ferramentas moleculares é uma esperança com relação à previsibilidade de lesões leucoplásicas progredirem para um fenótipo neoplásico.[122]Patel V, Leethanakul C, Gutkind JS. New approaches to the understanding of the molecular basis of oral cancer. Crit Rev Oral Biol Med. 2001;12(1):55-63.
http://www.ncbi.nlm.nih.gov/pubmed/11349962?tool=bestpractice.com
A ploidia do DNA permanece uma opção atraente na avaliação da leucoplasia oral quando foi demonstrado aneuploidia associada a risco elevado de progressão para carcinoma escamoso.[23]Odell EW. Aneuploidy and loss of heterozygosity as risk markers for malignant transformation in oral mucosa. Oral Dis. 2021 Nov;27(8):1993-2007.
https://onlinelibrary.wiley.com/doi/10.1111/odi.13797
http://www.ncbi.nlm.nih.gov/pubmed/33577101?tool=bestpractice.com
Além disso, frações da fase S de lesões leucoplásicas com displasia demonstraram taxas de aneuploidia superiores a duas vezes as de leucoplasias sem displasia.[123]Khanna R, Agarwal A, Khanna S, et al. S-phase fraction and DNA ploidy in oral leukoplakia. ANZ J Surg. 2010m Jul-Aug;80(7-8):548-51.
http://www.ncbi.nlm.nih.gov/pubmed/20795971?tool=bestpractice.com
Somada ao progresso no entendimento das alterações carcinogênicas moleculares na leucoplasia oral está a adição da análise microarray utilizando os resultados da reação em cadeia da polimerase via transcriptase reversa, com biomarcadores candidatos identificados nos casos que resultam em formação de câncer.[124]Liu W, Zheng W, Xie J, et al. Identification of genes related to carcinogenesis of oral leukoplakia by oligo cancer microarray analysis. Oncol Rep. 2011 Jul;26(1):265-74.
http://www.ncbi.nlm.nih.gov/pubmed/21523324?tool=bestpractice.com
Biomarcadores salivares
Novos testes não invasivos que utilizam a saliva como fluido corporal para a detecção de biomarcadores estão em desenvolvimento. Há relatos de análises do proteoma salivar humano por espectrometria de massa, respaldadas por ferramentas de bioinformática. As proteínas mais estudadas, ou seja, S100A7, S100P, CD44 e COL5A1, têm mostrado aumento das suas expressões na leucoplasia em comparação com controles saudáveis.[125]Sivadasan P, Gupta MK, Sathe G, et al. Salivary proteins from dysplastic leukoplakia and oral squamous cell carcinoma and their potential for early detection. J Proteomics. 2020 Feb 10;212:103574.
http://www.ncbi.nlm.nih.gov/pubmed/31706945?tool=bestpractice.com
Dessas proteínas, a CD44 em enxaguatórios bucais demonstrou ter potencial como marcador candidato para a detecção precoce de câncer bucal em pacientes com lesões de leucoplasia.[126]Franzmann EJ, Donovan MJ. Effective early detection of oral cancer using a simple and inexpensive point of care device in oral rinses. Expert Rev Mol Diagn. 2018 Oct;18(10):837-44.
http://www.ncbi.nlm.nih.gov/pubmed/30221559?tool=bestpractice.com
Várias citocinas pró-angiogênicas e pró-inflamatórias, como IL-1, IL-6, IL-8 e fator de necrose tumoral-alfa, mostram-se também elevadas em amostras de saliva de pacientes com leucoplasia oral. Níveis elevados dessas citocinas podem indicar transformação carcinogênica de pré-câncer em câncer oral.[127]Goldoni R, Scolaro A, Boccalari E, et al. Malignancies and biosensors: a focus on oral cancer detection through salivary biomarkers. Biosensors (Basel). 2021 Oct 15;11(10):396.
https://www.mdpi.com/2079-6374/11/10/396
http://www.ncbi.nlm.nih.gov/pubmed/34677352?tool=bestpractice.com
O painel de especialistas da ADA não recomenda coloração vital, autofluorescência, refletância tecidual ou adjuntos salivares como ferramentas de triagem para uso na atenção primária.[93]Lingen MW, Abt E, Agrawal N, et al. Evidence-based clinical practice guideline for the evaluation of potentially malignant disorders in the oral cavity: a report of the American Dental Association. J Am Dent Assoc. 2017 Oct;148(10):712-27;e10.
https://jada.ada.org/article/S0002-8177(17)30701-8/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/28958308?tool=bestpractice.com
 [Figure caption and citation for the preceding image starts]: Leucoplasia salpicadaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia salpicadaCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Leucoplasia verrucosa proliferativaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia verrucosa proliferativaCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Leucoplasia sublingualCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia sublingualCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Leucoplasia por CandidaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia por CandidaCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
 [Figure caption and citation for the preceding image starts]: Leucoplasia pilosa oralCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Leucoplasia pilosa oralCortesia do Dr. James Sciubba; usado com permissão [Citation ends]. [Figure caption and citation for the preceding image starts]: Mastigação de lábios/bochechasCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Mastigação de lábios/bochechasCortesia do Dr. James Sciubba; usado com permissão [Citation ends].
