Abordagem
A avaliação inicial de pacientes com suspeita de síncope geralmente ocorre em um pronto-socorro ou clínica de urgência e emergência. Depois de se determinar tanto quanto possível que o paciente sofreu uma síncope verdadeira, a avaliação inicial deve, em seguida, concentrar-se nos seguintes pontos-chave:
Uma descrição detalhada dos eventos sintomáticos
Averiguar a ocorrência de alguma cardiopatia estrutural clinicamente importante (com ECG e, muitas vezes, uma ecocardiografia)
Características clínicas da história que sugiram um diagnóstico.
Em mãos experientes, a causa da síncope pode ser estabelecida por uma história médica abrangente e um exame físico, somente, em cerca de 60% dos pacientes.[23][24] Entretanto, até um terço dos pacientes com síncope têm uma causa indeterminada após a avaliação inicial.[25] As investigações adicionais são individualizadas, de modo que a investigação seja feita de maneira custo-efetiva e apropriada.[1] Por fim, o objetivo é descartar doenças mais graves e estabelecer de modo eficiente a(s) causa(s) de síncope com confiança suficiente.[19]
Anamnese e exame físico
A história médica é a ferramenta mais valiosa na avaliação inicial da síncope. Em alguns casos, a história é diagnóstica por si só, e não são necessários testes adicionais. O exemplo mais comum é quando a história é indicativa de um desmaio vasovagal clássico ou de um desmaio situacional neuromediado ou reflexo. No entanto, em outros casos, a história pode não ser confiável e os pacientes (especialmente idosos) ou as testemunhas podem não conseguir se lembrar dos detalhes. Os pacientes frequentemente apresentam comorbidades múltiplas e, como consequência, eles podem ter várias causas igualmente prováveis de desmaio. Se a história for sugestiva, mas inconclusiva, as etapas subsequentes na avaliação podem ser focadas, eficientes e custo-efetivas.
Dedique tempo a obter todos os detalhes do evento ao máximo possível. Procure padrões capazes de ajudar a estreitar o diagnóstico: documente as circunstâncias precedentes, os sintomas premonitórios e o desfecho subsequente, e faça anotações detalhadas das comorbidades (por exemplo, neuropatia diabética, disfunção autonômica). Um questionário pré-preparado para o paciente pode ajudar a economizar tempo enquanto se obtêm os detalhes necessários.
Embora o foco deste tópico seja a SNMR, sempre considere a possibilidade de outras causas de síncope (por exemplo, ortostática, cardiovascular). O American College of Cardiology (ACC)/American Heart Association (AHA)/Heart Rhythm Society (HRS) recomendam que o exame físico deve incluir a pressão arterial (PA) ortostática e alterações na frequência cardíaca nas posições deitada e sentada, imediatamente após se assumir a posição ortostática e após 3 minutos de postura ereta.[1] Realize um exame neurológico básico; deficits sensoriais, motores, de fala ou de visão sugerem um problema neurológico subjacente que requer investigações adicionais ou encaminhamentos.[1]
O fluxograma diagnóstico ilustrado (modificado depois do fluxograma criado pelas diretrizes da Força-tarefa de Diretrizes da European Society of Cardiology Syncope) pode ser útil.[2]
[Figure caption and citation for the preceding image starts]: Avaliação inicial e estratégia adicional de manejo de síncope baseadas nas Diretrizes da força-tarefa da European Society of Cardiology. ECG ambulatorial, eletrocardiograma ambulatorial; MSC, massagem do seio carotídeo; EF, eletrofisiológico; monitor de eventos eletrocardiográficos implantável, loop event recorder implantável; unidade de tratamento de síncopesDo acervo pessoal do Dr. David Benditt; usado com permissão [Citation ends].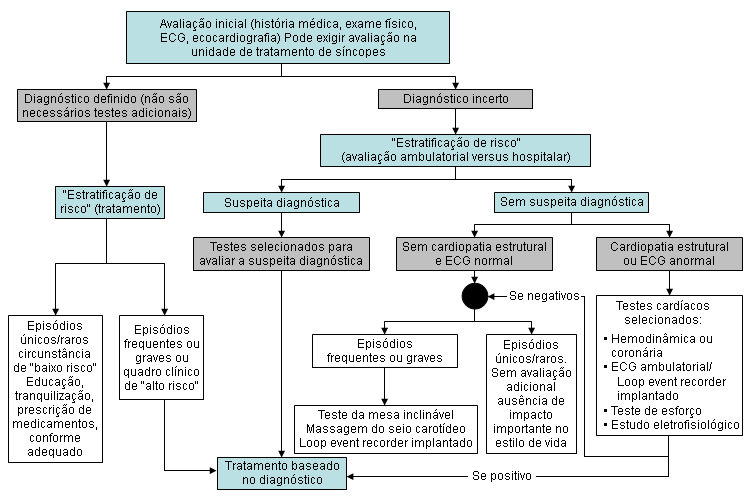
Descarte uma doença cardíaca estrutural
A doença cardíaca estrutural subjacente está entre os fatores mais importantes a serem identificados em um paciente com suspeita de síncope. Obtenha um ECG de 12 derivações em todos os pacientes para descartar bloqueio atrioventricular (AV), bradicardia, assistolia, intervalo QT longo ou um bloqueio de ramo. Uma ecocardiografia também pode ser útil. A presença de cardiopatia é um preditor independente de uma causa cardíaca para a síncope (isto é, uma causa arrítmica primária ou uma causa baseada em uma anormalidade cardíaca estrutural que acarrete uma perturbação hemodinâmica transitória), com sensibilidade de 95% e especificidade de 45%; por outro lado, a ausência de cardiopatia exclui uma causa cardíaca de síncope em 97% dos pacientes.[23]
Os pacientes com anormalidades estruturais do coração (como disfunção ventricular esquerda) ou anormalidades no ECG (como intervalos QT ou QRS prolongados devem ser encaminhados para avaliação adicional imediata.
A síncope juntamente com esforços físicos gera preocupações especiais. Em particular, se o desmaio ocorrer "a pleno voo", considere a possibilidade de lesões cardíacas estruturais e/ou dinâmicas que produzam um débito cardíaco relativamente fixo em um quadro de dilatação vascular (por exemplo, estenose aórtica ou da valva mitral grave, cardiomiopatia hipertrófica). Entretanto, a síncope durante ou logo após um exercício (mesmo esforço físico moderado, como subir escadas) também pode ocorrer em pacientes com disfunção autonômica grave (por exemplo, insuficiência autonômica pura), nos quais o controle vascular é incapaz de manter uma pressão de perfusão cerebral adequada. Em raras ocasiões, a síncope que acompanha escorço físico pode ocorrer como consequência de um desmaio neuromediado ou reflexo (isto é, variante pós-esforço físico de desmaio vasovagal); no entanto, nesses casos, o desmaio ocorre tipicamente logo após a conclusão e não durante o exercício.
Estratificação de risco
Avalia a necessidade de avaliações hospitalares e tratamentos adicionais, estabelece a urgência e estima o prognóstico.[2][26]
As diretrizes do ACC/AHA/HRS recomendam a avaliação quanto ao risco em curto prazo relacionado à síncope (necessária para tomada de decisão imediata no contexto agudo), bem como quanto a eventos adversos em longo prazo (mais provavelmente associada a doenças clínicas subjacentes, muitas das quais são cardíacas).[1] O uso de escores de estratificação de risco pode ser razoável.[1] No entanto, o principal determinante para avaliação e tratamento hospitalar adicionais é a presença de uma doença clínica grave, potencialmente relevante para a causa da síncope.[1]
As condições clínicas graves que podem exigir avaliação e tratamento hospitalar adicionais incluem:
Doenças cardíacas arrítmicas
Doenças cardíacas ou vasculares não arrítmicas
Doenças não cardíacas (por exemplo, hemorragia digestiva ou anemia grave).
Os pacientes com bradiarritmias graves, taquicardia ventricular, dissecção aguda da aorta, hemorragia abrupta ou embolia pulmonar comprovadas devem ser hospitalizados. Similarmente, é prudente hospitalizar os pacientes com disfunção ventricular esquerda moderada a grave (por exemplo, fração de ejeção ≤35%), valvopatia que cause preocupação clínica ou cardiomiopatia hipertrófica.
Um estudo constatou uma alta prevalência de embolia pulmonar entre pacientes hospitalizados por um primeiro episódio de síncope (aproximadamente 1 a cada 6 pacientes); pode ser importante considerar isso nos pacientes sem uma explicação alternativa, mas são necessárias pesquisas adicionais.[27]
Na ausência de uma doença clínica grave, é razoável tratar a síncope mediada por reflexos presuntiva em ambiente ambulatorial.[1]
As regras e os critérios que podem ajudar a estratificar o risco dos pacientes que comparecem ao pronto-socorro incluem: a regra de São Francisco para a síncope (San Francisco Syncope Rule [SFSR]), o escore de risco de síncope canadense (Canadian Risk Syncope Score [CSRS]), o escore do OESIL (Osservatorio Epidemiologico sulla Sincope nel Lazio), o escore EGSYS (Evaluation of Guidelines in Syncope Study) e o estudo ROSE (Risk Stratification of Syncope in the Emergency Department).[28][29][30][31][32] Os dois critérios mais comumente usados são a SFSR e o estudo ROSE.
O SFSR foi implementado e validado em muitos pronto-socorros e pode ser lembrado por meio do processo mnemônico "CHESS":[28] [ San Francisco Syncope Rule TreeCalc Opens in new window ]
Insuficiência cardíaca congestiva (ICC)
Hematócrito <30% (Haematocrit)
Eletrocardiograma anormal (Electrocardiogram)
Dispneia
PA sistólica <90 mm Hg.
O estudo ROSE mais recente inclui o peptídeo natriurético do tipo B (PNB) como parte dos critérios de decisão e podem ser lembrados por meio do processo mnemônico "BRACES":[29] [ Escore ROSE: estratificação de risco de síncope no pronto-socorro Opens in new window ]
Nível do PNB ≥300 picogramas/mL (Brain natriuretic peptide)
Bradicardia ≤50 no pronto-socorro ou pré-hospital
Exame Retal positivo para sangue oculto nas fezes (Rectal exam)
Anemia (hemoglobina [Hb] ≤90 g/L) (Anaemia)
Dor torácica associada à síncope (Chest pain)
Eletrocardiograma mostrando ondas Q (mas não na derivação III)
Saturação ≤94% em ar ambiente.
Outras investigações iniciais
Considere exames de sangue direcionados para descartar outras causas de síncope, incluindo:
Cortisol (para avaliar insuficiência adrenal)
Ureia e creatinina (para avaliar desidratação)
Hemoglobina (para descartar anemia)
Glicose sanguínea (para descartar hipoglicemia)
Beta-hCG (gonadotrofina coriônica humana; para descartar gravidez)
Enzimas cardíacas (para descartar infarto do miocárdio)
Dímero D (para descartar embolia pulmonar) e/ou angiotomografia pulmonar.
As diretrizes não recomendam uma testagem ampla; solicite apenas as investigações relevantes para a situação clínica.[26][33]
Os pacientes com síncope recorrente, ou os que tiverem sofrido trauma decorrente de síncope, necessitam de avaliação adicional com um monitor de ECG ambulatorial (isto é, um monitor Holter), loop event recorder ou monitor de eventos ou, possivelmente, um teste da mesa inclinável. As causas não cardiovasculares podem ser examinadas por meio dos exames de sangue adequados (por exemplo, glicose, cortisol), eletroencefalograma (EEG), ressonância nuclear magnética (RNM) cranioencefálica ou testagem autonômica.
Síncope vasovagal
O estabelecimento do diagnóstico de desmaio vasovagal depende fortemente da obtenção de uma história médica detalhada, incluindo relatos de testemunhas.
As características clássicas que sugerem síncope vasovagal incluem:
Fatores desencadeantes:
Visões desagradáveis
Dor decorrente de lesão física
Fadiga
Palpitações ou bradicardia (consistentes com, mas não diagnósticas de, síncope vasovagal)
Estresse emocional (principalmente em ambientes quentes e lotados)
Posição ortostática por tempo prolongado
Desidratação
Exercício vigoroso (caso a síncope ocorra após o exercício)
Sintomas de alerta (prodrômicos):
Sentir calor ou frio
Sudorese
Taquicardia (consistente com, mas não diagnóstica de, síncope vasovagal)
Dispneia
Perda de audição ou visão
Náuseas
Alteração no padrão respiratório
Sinais físicos relatados por testemunhas:
Palidez acentuada (branco como um fantasma, com aparência de morto)
Pele sudorética
Confusão.
Normalmente, a recuperação é rápida após um desmaio vasovagal se o paciente permanecer na posição de decúbito, mas um período de fadiga subsequente é comum.
Entretanto, os aspectos clássicos do desmaio vasovagal geralmente estão ausentes, apenas presentes de forma incompleta ou não são lembrados (principalmente em idosos). Os pacientes também podem apresentar sintomas (por exemplo, movimentos musculares erráticos enquanto inconscientes, incontinência urinária ou, raramente, intestinal) que podem resultar em confusão com transtorno convulsivo e precisar de uma consulta neurológica. Uma história familiar de morte súbita deve desencadear preocupações sobre outros diagnósticos (por exemplo, cardiopatia estrutural, síndrome do QT longo, síndrome de Brugada).
Realize exames adicionais quando a história não for clara por si só. O teste da mesa inclinável é o exame confirmatório mais comum para a síncope vasovagal.[34][35][36][37][38]
Outras SNMRs
Essas síndromes incluem síncope do seio carotídeo, desmaio situacional e neuralgia glossofaríngea e do trigêmeo.
Na síndrome do seio carotídeo (SSC), existe uma história de manipulação acidental do pescoço que resulta em pressão externa sobre os barorreceptores do seio carotídeo. Há três tipos de SSC: SSC bradicárdica, SSC predominantemente vasodepressora (o sinal predominante é uma hipotensão relativa) ou mista (bradicardia e hipotensão). A massagem diagnóstica deliberada do seio carotídeo (MSC) aplicada por um médico adequadamente experiente pode reproduzir os sintomas e confirmar o diagnóstico em paciente com SSC.[22][39] Nesses casos, o ECG mostrará bradicardia por SSC.
A síncope situacional pode ser desencadeada por hemorragia aguda, tosse, espirro, estimulação gastrointestinal (deglutição, defecação, dor visceral), micção, pós-exercício ou outras situações, incluindo execução de um instrumento de sopro, levantamento de peso ou consumo de uma refeição (pós-prandial). O diagnóstico de síncope situacional se baseia na história; ele não é facilmente avaliado em laboratório. A síncope por tosse pode ser uma exceção, mas os critérios diagnósticos para a resposta hemodinâmica à tosse induzida ainda precisam ser determinados.
A neuralgia glossofaríngea é uma síndrome dolorosa incomum associada a sincopes. Os sinais característicos dessa síndrome são sensações episódicas de dor faríngea, geralmente do lado esquerdo, que frequentemente acarretam síncope. A patogênese que relaciona a dor e a síncope não está clara; porém, acredita-se que ela seja causada por conexões entre os nervos glossofaríngeo e vago.[40]
A neuralgia do trigêmeo é uma síndrome de dor facial um tanto mais comum que se manifesta com dor em uma das divisões do nervo trigêmeo. Entretanto, a síncope resultante de neuralgia do trigêmeo é incomum e a patogênese é obscura. A neuralgia do trigêmeo já foi associada a síncopes, convulsões e até mesmo parada cardíaca.[41]
Exames laboratoriais: avaliação autonômica básica
1. Teste da mesa inclinável
O teste da mesa inclinável é uma ferramenta diagnóstica bem estudada e amplamente disponível capaz de revelar a suscetibilidade à síncope vasovagal.[4][22][34][35][36][37][38] É indicado quando houver suspeita de síncope vasovagal, mas a história médica for duvidosa. Se a história for clássica, o teste da mesa inclinável não será necessário. Os protocolos de teste mais comuns são: teste da mesa inclinável com nitroglicerina; com isoprenalina; ou sem medicamentos. Os medicamentos podem ser usados para aumentar a suscetibilidade ao teste.[42]
Uma discussão detalhada acerca dos protocolos do teste da mesa inclinável pode ser encontrada no Relatório de consenso de especialistas do ACC e em documentos de diretrizes da European Society of Cardiology e do ACC/AHA/HRS.[1][2][34] Em resumo, a primeira etapa é a inclinação passiva com a cabeça para cima a 60° a 70°, durante a qual o paciente é apoiado por uma placa de sustentação para os pés com o corpo cuidadosamente preso por fitas, por 20-45 minutos (os protocolos variam). Se necessário, o teste de inclinação é repetido com um teste de desafio medicamentoso. Até recentemente, o medicamento provocador mais frequentemente usado era a isoprenalina, geralmente administrada em doses crescentes. Entretanto, a nitroglicerina intravenosa ou sublingual tem sido preferida, em parte por acelerar o procedimento sem afetar de maneira adversa o seu uso diagnóstico.[43] O chamado protocolo italiano, em que uma inclinação passiva de 20 minutos é seguida, se necessário, pela administração por via sublingual de nitroglicerina, tornou-se o protocolo mais popular.
Um importante atributo clínico do teste da mesa inclinável é que ele proporciona a oportunidade de precipitar um ataque vasovagal típico na presença do médico. Isso aumenta a confiança do paciente no diagnóstico. Um teste positivo também pode ajudar os pacientes a aprenderem a reconhecer os sintomas e prevenir um desmaio iminente.
O teste da mesa inclinável sem provocação farmacológica apresenta sensibilidade de 37% e especificidade de 99%; com provocação farmacológica (administração de nitroglicerina), a sensibilidade é de 66% e a especificidade é de 89%.[43] Contudo, o teste da mesa inclinável é imperfeito e há controvérsias em relação ao seu uso ideal. A taxa de falso-positivos é, aproximadamente, de 10%.[2] A reprodutibilidade aguda, em termos de haver indução de síncope, é de 80% a 90%. A reprodutibilidade em prazo mais longo (isto é, >1 ano) é de cerca de 60%.[44] A experiência do médico pode ser uma limitação importante.
Outra importante desvantagem do teste da mesa inclinável é que ele nem sempre resulta no mesmo quadro hemodinâmico, quando repetido no mesmo paciente, e, assim, não é adequado para direcionar a estratégia de tratamento. Um quadro cardioinibidor (isto é, bradicardia) pode predominar em uma ocasião, ao passo que respostas vasodepressoras (vasodilatação sendo principalmente responsável pela hipotensão) podem ocorrer outras vezes.[7][45][46] No estudo Study of Syncope of Unknown Etiology (ISSUE), mesmo quando o teste da mesa inclinável indicou um componente vasodilatador proeminente, o registro subsequente dos desmaios espontâneos por um loop event recorder implantável muitas vezes revelou eventos bradicárdicos.[7] São necessários estudos adicionais desse fenômeno com dispositivos que possam monitorar a pressão arterial (PA) sistêmica ou um substituto da PA, bem como a frequência cardíaca.
Um teste da mesa inclinável positivo (especialmente se reproduz os sintomas espontâneos do paciente) pode ser considerado diagnóstico para os pacientes sem cardiopatia estrutural grave, e não são necessários testes adicionais. No entanto, para os pacientes com cardiopatia estrutural significativa, arritmias cardíacas e fatores iatrogênicos (por exemplo, efeitos medicamentosos) devem ser excluídos antes de se confiar em um resultado positivo do teste da mesa inclinável.[43]
2. Massagem do seio carotídeo (MSC)
A pressão no local em que a artéria carótida comum se bifurca produz uma diminuição reflexa na frequência cardíaca e na PA. Essa observação é a base da técnica da MSC.
A MSC é usada para diagnosticar a SSC em pacientes com história de síncope. No entanto a MSC pode ser positiva em alguns indivíduos sem história de síncope (até 40% dos idosos); isso é conhecido como hipersensibilidade do seio carotídeo.[2] A necessidade de reprodução dos sintomas aumenta a especificidade da MSC: em um estudo realizado com 1855 pacientes com síncope inexplicável, 24% demonstraram hipersensibilidade do seio carotídeo, mas apenas cerca de um terço (8.8%) tinham SSC quando os sintomas foram necessários para realizar o diagnóstico.[47]
Há o consenso de que a SSC pode ser diagnosticada quando a MSC reproduz sintomas como resultado da indução de ≥1 dos seguintes eventos: >3 segundos de assistolia, bloqueio atrioventricular (AV) paroxístico, diminuição marcante da pressão arterial sistêmica (geralmente, uma queda na PA sistólica ≥50 mmHg) ou uma combinação deles.[1][2][48] A MSC deve ser realizada em posição supina e ortostática, com pressão aplicada por 5 segundos em cada posição.[1] A European Society of Cardiology recomenda aplicar pressão por 10 segundos, para dar tempo para que os sintomas se desenvolvam.[48]
Os resultados mais convincentes da MSC são obtidos quando a mesma é realizada com o paciente em posição ereta, pois o impacto da gravidade exacerba os efeitos hemodinâmicos da bradicardia ou vasodilatação induzida. O diagnóstico pode ser incorreto em aproximadamente um terço dos casos se for realizada apenas a MSC supina. A pressão arterial e o ECG devem ser registrados durante todo o procedimento. Para a medição da pressão arterial, pode ser adequado o uso de um dispositivo não invasivo de medição da PA, mas, frequentemente, é difícil obter registros satisfatórios. Um esfigmomanômetro convencional não é apropriado.
A MSC não deve ser realizada em pacientes que tiverem apresentado ataque isquêmico transitório ou acidente vascular cerebral (AVC) nos últimos 3 meses ou em pacientes com sopros carotídeos (a menos que os exames da carótida com Doppler excluam convincentemente uma estenose significativa da artéria carótida).[2]
Raramente, a MSC pode ocasionar fibrilação atrial autolimitada de pouca importância clínica. Finalmente, achados registrados no período subsequente a um infarto agudo do miocárdio podem não ser representativos e não devem ser usados para o diagnóstico de SSC.
3. Teste de adenosina trifosfato (ATP)
O valor da administração de ATP em bolus continua a ser controverso.[2] O teste de ATP pode ser útil para identificar uma forma de síncope associada a um bloqueio AV paroxístico neuromediado em certos idosos nos quais outras causas tenham sido descartadas, e pode orientar a decisão para iniciar um marca-passo permanente ao revelar doença nodal AV oculta em indivíduos suscetíveis.[1] O valor diagnóstico e preditivo do teste ainda precisa ser confirmado por estudos prospectivos. Na ausência de dados suficientes, o teste pode ser considerado ao final da investigação diagnóstica.
O protocolo mais rigorosamente testado envolve a injeção em bolus de 20 mg de ATP em uma veia braquial em um paciente em posição supina submetido a monitoramento contínuo por ECG.[49] A PA é monitorada de forma não invasiva. O desfecho do teste (positivo ou negativo) depende da duração da pausa cardíaca induzida por ATP. Uma pausa >10 segundos, mesmo se interrompida por batimentos de escape, é definida como anormal. Alguns relatos sugerem que uma pausa >6 segundos é suficiente para declarar o teste anormal.[50] Para os pacientes com respostas anormais, a reprodutibilidade é de aproximadamente 80% em curto e longo prazos.
Em virtude da possibilidade de reações broncoespásticas, o teste de ATP é contraindicado em pacientes comprovadamente com asma.
4. Monitor de evento eletrocardiográfico implantável
Um loop event recorder implantável pode ser usado para excluir bradiarritmia ou taquiarritmia caso os eventos sejam relativamente infrequentes (<1 ou 2 por mês) e haja suspeita de arritmia.[26]
5. Estudo eletrofisiológico
O estudo eletrofisiológico é indicado com pouca frequência.[1] Ele pode ser usado caso haja presença de cardiopatia estrutural com suspeita de taquiarritmia e em pacientes que possam estar apresentando bloqueio de condução de alto grau intermitente. Ele também é indicado se houver suspeita de taquicardia supraventricular paroxística como causa dos sintomas, principalmente se o paciente descrever palpitações antes da síncope.
Outros testes do sistema autonômico
1. Manobra de Valsalva
A manobra de Valsalva é usada para avaliar a integridade do arco reflexo barorreceptor arterial, e pode indicar a presença de insuficiência autonômica, que pode causar síncope por meio da hipotensão ortostática.[2] Contudo, por si só, a manobra de Valsalva não sugere diretamente um mecanismo para síncope. A resposta de Valsalva é testada tipicamente sob monitoramento contínuo do ECG e da PA em associação com o monitoramento do paciente quanto à ocorrência de sintomas clínicos.
2. Teste ortostático ativo
Como seu nome implica, o teste ortostático ativo avalia uma resposta do paciente ao movimento ativo da postura supina à ereta. Ele pode ser considerado para descartar a hipotensão ortostática.[51]
Espera-se que o movimento muscular ativo impulsione mais sangue na direção da circulação central para fornecer o aumento do débito cardíaco exigido pela postura ereta. Entretanto, o uso ativo dos músculos das pernas também pode agravar a dilatação vascular periférica e, como resultado, induzir uma hipotensão mais intensa. O equilíbrio entre esses efeitos determina o efeito final sobre a PA sistêmica.
Um teste ortostático ativo de 3 minutos é útil na avaliação da hipotensão ortostática inicial (primeiros 30 segundos de postura ereta).[2] A hipotensão inicial ocorre na posição ortostática ativa, mas não na inclinação. Para detectar a diminuição da pressão, é essencial seu monitoramento (geralmente não invasivo) a cada batimento. Um período ≥3 minutos em posição ortostática ativa também pode demonstrar a diminuição mais tardia da PA, indicativa de hipotensão ortostática clássica (hipotensão ortostática tardia).[1][48]
3. Teste pressor ao frio
O teste pressor ao frio é realizado com a imersão da mão em um recipiente com água gelada, geralmente por 1 minuto. Quaisquer alterações na pressão arterial e na frequência cardíaca são registradas. Como na manobra de Valsalva, esse teste fornece dados relevantes sobre a integridade do reflexo autonômico. Ele não tem sido usado para identificar um diagnóstico específico.
4. Teste da tosse
A tosse induzida pode ajudar a avaliar a suscetibilidade à síncope por tosse (tussígena), mas poucos dados estão disponíveis.[52] Como na MSC, esse teste pode ser mais bem realizado com o paciente em postura ereta. Os critérios diagnósticos para a resposta hemodinâmica à tosse induzida ainda precisam ser determinados.
O uso deste conteúdo está sujeito ao nosso aviso legal