Etiologia
Fisiopatologia
Visão geral de fatores que afetam a maturação, a migração e a desmarginação dos neutrófilos.
A circulação periférica de neutrófilos, que está incluída na contagem leucocitária total, consiste principalmente em neutrófilos maduros em trânsito, oriundos da medula óssea para os tecidos periféricos. Esse trânsito é curto e depende da sinalização por meio do receptor da quimiocina CXCR4 na superfície dos neutrófilos.[1] Apenas 5% do número total de neutrófilos está presente na circulação em qualquer momento específico, pois o período de vida dos neutrófilos inclui 9 dias na medula óssea e 1 a 4 dias nos tecidos periféricos, com apenas 3 a 6 horas na circulação.
A produção de células na medula óssea dentro da linhagem mieloide é estimulada pela interleucina 3 e pelo fator estimulador de colônias de granulócitos e macrófagos (GM-CSF). O fator estimulador de colônias de granulócitos (G-CSF) é responsável por catalisar a diferenciação das células mieloides iniciais em neutrófilos maduros.
Vários sinais induzem a migração dos neutrófilos da medula óssea para a circulação periférica, incluindo corticosteroides, endotoxinas, fator mobilizador de leucócitos derivado do complemento, C5a quimioatraente, fator de necrose tumoral alfa e androgênios. Quando acionada, a liberação de neutrófilos do armazenamento na medula óssea triplica os neutrófilos circulantes em 4 horas.
Além dos neutrófilos contidos dentro da medula óssea, na circulação e nos tecidos periféricos, uma população moderada se adere ao endotélio vascular e entra na circulação por meio da desmarginação. A liberação de catecolaminas, incluindo a adrenalina, resulta na desmarginação quase imediata e subsequente duplicação da contagem de neutrófilos periféricos.[4]
Assim, a neutrofilia pode ser resultado de:
Aumento da produção de células mieloides maduras
Aumento da desmarginação (processo em que os neutrófilos entram na circulação periférica oriundos de áreas de reservatórios intravasculares de células polimorfonucleares marginadas), ou
Saída reduzida (migração para fora) de neutrófilos da circulação periférica para os tecidos.
Um valor laboratorial espúrio deve ser descartado antes de investigações adicionais.
A hematopoiese na medula óssea, assim como em locais extramedulares (fígado, timo e baço), é influenciada por condições sistêmicas que podem inibir (por exemplo, quimioterapia) ou estimular a produção de células (por exemplo, infecção). Uma contagem de neutrófilos elevada decorrente de produção aumentada pode ser classificada como neutrofilia primária ou secundária. A neutrofilia primária é resultado de um processo patológico que afeta a medula óssea; a neutrofilia secundária ocorre quando a medula óssea responde de maneira adequada a um estímulo sistêmico para o aumento da produção de neutrófilos.
Neutrofilia espúria
Antes de iniciar uma investigação intensa sobre a causa de uma neutrofilia relatada, primeiramente é importante confirmar a validade do valor laboratorial. A neutrofilia pode ser uma aberração laboratorial secundária à aglomeração de plaquetas ou à crioglobulinemia. A avaliação do esfregaço de sangue periférico permite que um dos diagnósticos seja rapidamente excluído.
Aglomeração de plaquetas
Se a amostra de sangue periférico contiver aglomerados de plaquetas, os contadores automáticos de células poderão confundir os aglomerados de plaquetas com leucócitos, mais frequentemente linfócitos. O efeito global é um pequeno aumento na contagem leucocitária, normalmente relatado com uma trombocitopenia associada.
No cenário de anticoagulação adequada das amostras, a neutrofilia e a trombocitopenia espúrias poderão ocorrer se o paciente apresentar aglutininas dependentes do ácido etilenodiaminotetracético (EDTA). Esse fenômeno, conhecido como pseudoleucocitose, ocorre em 0.1% dos pacientes e requer nova avaliação da contagem de plaquetas e de leucócitos totais em um tubo de coleta de sangue sem EDTA.
Crioglobulinemia
Se a amostra de sangue periférico for resfriada abaixo da temperatura ambiente e contiver proteínas plasmáticas insolúveis no frio, um aumento dependente da temperatura nas contagens leucocitária e plaquetária será observado em uma temperatura ≤30 °C. Partículas de crioglobulinas precipitadas retornarão à solução se a amostra for aquecida até a temperatura corporal. A hemoglobina celular média também poderá estar elevada, o que pode ser corrigido com o aquecimento.
Produção aumentada: neutrofilia primária
Na neutrofilia primária, a produção apresenta uma regulação positiva (up-regulation) como resultado direto de um processo neoplásico primário na medula óssea ou doença hereditária.
Os fatores que dão suporte à etiologia neoplásica para neutrofilia incluem contagem leucocitária sustentada >50×10⁹/L, desvio à esquerda da linhagem neutrofílica, basofilia ou eosinofilia, displasia e eritrócitos anormais, como dacriócitos (eritrócitos em formato de lágrima).[5]
Neoplasia mieloproliferativa (NMP)
É um espectro de doenças hematológicas, incluindo a leucemia mieloide crônica (LMC), a leucemia neutrofílica crônica (LNC), a mielofibrose primária (fase proliferativa), a trombocitemia essencial, a policitemia vera e a NMP não classificável, que podem evoluir para leucemia aguda. Entre um subconjunto de pacientes, incluindo os que apresentam trombocitemia essencial, o grau de elevação na contagem leucocitária total pode prever o risco da doença. Evidências de células imaturas na circulação periférica podem dar suporte ao diagnóstico de NMP.
A LNC está associada a uma neutrofilia madura persistente, com presença rara de precursores neutrofílicos no sangue periférico. A leucemia neutrofílica crônica está associada a mutações ativadoras do gene CSF3R, mais comumente T618I.[6] Se o diagnóstico de leucemia neutrofílica crônica for considerado, deve-se descartar o mieloma de plasmócitos (mieloma múltiplo).
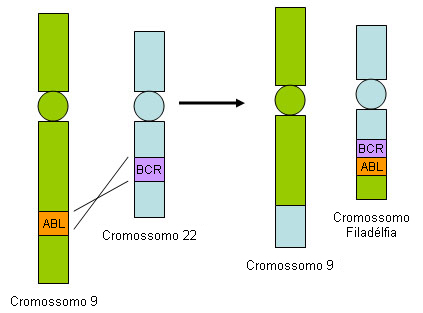
O diagnóstico de LMC é corroborado por evidências do cromossomo Filadélfia, com a translocação t(9;22)(q34.1;q11.2), que resulta na fusão gênica BCR-ABL1. Os pacientes exibem leucocitose de 12 a 1000×10⁹/L em decorrência de neutrofilia acompanhada de granulócitos com desvio à esquerda (um aumento de granulócitos imaturos na circulação periférica), tipicamente com porcentagens elevadas de neutrófilos segmentados e mielócitos (células mieloides imaturas derivadas de promielócitos que dão origem a metamielócitos e que não são observadas normalmente na circulação), basofilia, eosinofilia e, frequentemente, trombocitemia. O diagnóstico também é corroborado por um baixo escore de fosfatase alcalina leucocitária.[Figure caption and citation for the preceding image starts]: Translocação BCR-ABL1Do acervo de Dr. Han Myint; usado com permissão [Citation ends].
Neoplasia mielodisplásica/mieloproliferativa
É um espectro de síndromes sobrepostas de dispoese e proliferação celular aumentada, incluindo a leucemia mielomonocítica crônica, a LMC atípica e as neoplasias mielodisplásicas/mieloproliferativas não classificáveis. Evidências de células imaturas na circulação periférica juntamente com displasia podem dar suporte ao diagnóstico de neoplasias mielodisplásicas/mieloproliferativas.
Leucemia mieloide aguda (LMA)
Subtipos específicos de LMA podem se manifestar com neutrofilia. A presença de blastos no sangue periférico justifica uma investigação para descartar leucemia aguda. Mais de 20% de blastos no sangue ou na medula óssea é diagnóstico de LMA. A LMA é sugerida por uma contagem leucocitária total elevada com evidências de células mieloides imaturas na circulação e por anemia e trombocitopenia associadas.
Neutrofilia hereditária[7]
É uma síndrome autossômica dominante rara com um fenótipo que não causa aumento de infecções ou uma predisposição leucêmica. Está associada à disfunção plaquetária que causa diátese hemorrágica.
Os achados diagnósticos incluem contagem leucocitária total >20×10⁹/L, fosfatase alcalina leucocitária elevada, função neutrofílica normal e expressão positiva de CD18/CD11b na superfície dos neutrófilos.
Anomalia de Pelger-Huët
É um distúrbio hereditário dominante que afeta a diferenciação dos neutrófilos decorrente de mutações no gene do receptor da lamina B. Embora os núcleos dos neutrófilos pareçam ter 2 lobos com uma única fita conectora, nenhum deficit funcional ocorre secundariamente à anormalidade morfológica.
Fora do distúrbio hereditário, as células pelgeroides (pseudo-Pelger-Huët) também são observadas na síndrome mielodisplásica e, de forma menos comum, na infecção ativa, na leucemia aguda e crônica ou com o uso de medicamentos como micofenolato de mofetila, colchicinas e sulfonamidas. Esses medicamentos provocam características pelgeroides nos núcleos dos neutrófilos, os quais retêm sua granulação citoplasmática. Por outro lado, na síndrome mielodisplásica, a hipolobulação dos neutrófilos com características pelgeroides é tipicamente acompanhada por hipogranulação do citoplasma.
Trombocitopenia amegacariocítica
Essa condição manifesta-se durante a primeira infância e está associada a uma plaquetopenia hereditária. A evolução da doença é heterogênea, e um subconjunto pode evoluir para LMA.
Trissomia do cromossomo 21 (síndrome de Down)
Lactentes e crianças com síndrome de Down podem apresentar reações leucemoides temporárias de significância indeterminada no cenário de estresse ou inflamação. A mielopoiese anormal transitória no nascimento pode se assemelhar à LMA.
Deficiência de adesão leucocitária
Além de leucocitose e neutrofilia persistentes, infecções recorrentes são observadas quando a função neutrofílica está deficiente. Como os neutrófilos nessa condição não têm CD18, nenhum leucócito e integrinas beta-2 permanecem. Em pacientes com deficiência de adesão leucocitária do tipo I, os neutrófilos são defeituosos em quimiotaxia, aderência e fagocitose, e existe um defeito dependente do estímulo na ativação dos neutrófilos.
Síndrome autoinflamatória familiar por frio
Essa condição se manifesta com uma leucocitose >25×10⁹/L dentro de 12 horas de exposição ao frio.
Neutrofilia crônica idiopática
Essa condição é diagnosticada se não houver evidências de patologia após uma avaliação diagnóstica completa para a neutrofilia, incluindo aspiração da medula óssea e biópsia.
Exames de imagem abdominais devem ser considerados, já que a asplenia congênita foi identificada em um subconjunto de pacientes com neutrofilia idiopática crônica.
Produção aumentada: neutrofilia secundária
Na neutrofilia secundária, a contagem de neutrófilos elevada é decorrente da produção aumentada na medula óssea em resposta a um estímulo sistêmico, como infecção, inflamação ou reação a medicamentos. Algumas condições sistêmicas causam hematopoiese aumentada como resposta endógena.
Infecção
Infecções ativas, não limitadas às de origem bacteriana, geralmente resultam em uma contagem leucocitária total elevada com um desvio à esquerda (um aumento nos granulócitos imaturos na circulação periférica) em pacientes de todas as idades, incluindo bebês prematuros.[8] No cenário de sepse grave, mais comum em idosos e neonatos, a contagem leucocitária total e a contagem de neutrófilos podem diminuir em vez de aumentar.
Doenças infecciosas específicas estão associadas a contagens leucocitárias totais mais elevadas, como aquelas causadas por espécies de Clostridium. Uma reação leucemoide é uma leucocitose >50×10⁹/L, caracterizada por uma neutrofilia com precursores mieloides aumentados secundária a uma condição não maligna (por exemplo, neutrofilia secundária).
Em resposta a processos infecciosos, a adrenalina é liberada e induz a desmarginação de neutrófilos (processo em que os neutrófilos entram na circulação periférica oriundos de áreas de reservatórios ["pools"] intravasculares de células polimorfonucleares marginadas), o que intensifica ainda mais a elevação de neutrófilos.
Inflamação
As condições inflamatórias crônicas e agudas graves que resultam em neutrofilia incluem a doença de Kawasaki, a artrite reumatoide de início juvenil ou adulto, a doença de Crohn, a colite ulcerativa, infecções granulomatosas crônicas e a bronquiectasia. A presença de neutrofilia tipicamente prevê um prognóstico desfavorável, e, entre os pacientes com a doença de Crohn, o risco de recorrência após a cirurgia é predito pela neutrofilia pré-operatória.[9]
A imunização também pode causar neutrofilia secundária.
Anemia
Qualquer processo que resulte em anemia, incluindo hemólise e sangramento, pode causar aumento da hematopoiese para compensar a baixa hemoglobina, causando a elevação secundária das contagens de leucócitos totais, neutrófilos e plaquetas.
As anemias hemolíticas microangiopáticas incluem coagulação intravascular disseminada, púrpura trombocitopênica trombótica (PTT) e síndrome hemolítico-urêmica (SHU). O diagnóstico é sugerido por alterações microangiopáticas nos eritrócitos (eritrócitos fragmentados, reticulocitose) e por plaquetas de tamanho aumentado. Metade dos pacientes com PTT ou SHU apresenta evidências de uma neutrofilia ou leucocitose com uma contagem leucocitária total >20×10⁹/L. Alguns relatos sugerem que a neutrofilia está associada a um desfecho desfavorável na PTT e na SHU.[10]
Neoplasia de tumor sólido
A leucocitose induzida por tumor é um fenômeno comum de etiologia indeterminada. A neutrofilia pode estar presente com ou sem infiltração de tumor sólido na medula óssea. Um subconjunto de tumores sólidos, especialmente adenocarcinoma colônico, demonstrou liberar fatores de crescimento, os quais induzem a secreção ou mimetizam os fatores estimuladores de colônias de granulócitos (G-CSF) e os fatores estimuladores de colônias de granulócitos e macrófagos (GM-CSF).[11]
Uma proporção de neutrófilos/linfócitos ≥4 é um fator prognóstico adverso em pacientes com mesotelioma, câncer de pâncreas, carcinoma de células renais e câncer colorretal.[12]
Infiltração da medula óssea
Processos infiltrantes na medula óssea, como tumor, fibrose ou doença granulomatosa, podem aumentar a contagem de neutrófilos, geralmente com alterações morfológicas concomitantes nas células circulantes do sangue, incluindo um esfregaço de sangue leucoeritroblástico (com granulócitos com desvio à esquerda e eritrócitos nucleados) com eritrócitos em forma de gota de lágrima (dacriócitos).
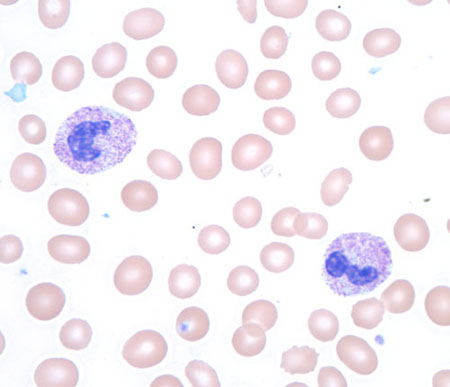
Para determinar a etiologia, é indicada uma biópsia da medula óssea.[Figure caption and citation for the preceding image starts]: Grânulos tóxicos em um paciente recebendo tratamento com fator estimulador de colônias de granulócitosDo acervo de T. George, MD [Citation ends].
 [Figure caption and citation for the preceding image starts]: Esfregaço de sangue periférico leucoeritroblástico com dacriócitosDo acervo de T. George, MD [Citation ends].
[Figure caption and citation for the preceding image starts]: Esfregaço de sangue periférico leucoeritroblástico com dacriócitosDo acervo de T. George, MD [Citation ends].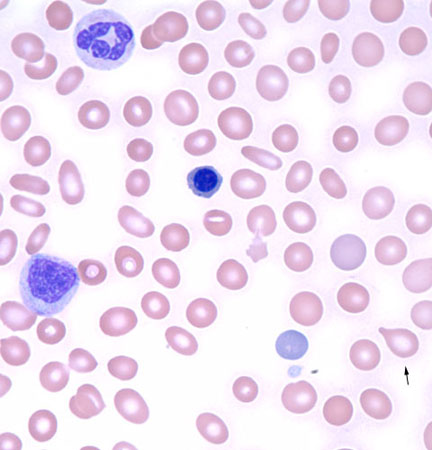
Estimulação crônica da medula óssea
As afecções clínicas crônicas que induzem a estimulação da medula óssea como compensação para a anemia ou para a trombocitopenia resultam em leucocitose secundária. Essas afecções incluem anemias hemolíticas, como a anemia falciforme, na qual a leucocitose é comumente encontrada em apresentações com crises vaso-oclusivas ou infecção.
A recuperação da função da medula óssea pode induzir uma leucocitose transitória com alterações leucoeritroblásticas após uma terapia citotóxica como a quimioterapia. Após a finalização da quimioterapia, uma neutrofilia pode estar presente até que a granulopoiese se ajuste à supressão do tratamento citotóxico.
Hipertermia
Alterações morfológicas nos neutrófilos circulantes e elevação da contagem total de neutrófilos ocorrem agudamente nos golpes de calor.
Os segmentos dos neutrófilos parecem menores que o normal com uma aparência botrioide (com numerosas protuberâncias arredondadas que se assemelham a cachos de uva).
Asplenia
É comum a neutrofilia após a ressecção do baço. Embora um grau moderado de neutrofilia seja transitório, a maioria dos pacientes continuará a apresentar uma neutrofilia leve de modo crônico.
As condições que resultam em asplenia funcional, incluindo doença falciforme, asplenia congênita, doença veno-oclusiva e autoinfarto, também induzem uma neutrofilia leve crônica. Evidências de leucocitose na doença falciforme em idade jovem, fora do cenário de infecção, são prognósticas de gravidade aumentada da doença.
Síndrome de Sweet
Essa condição é caracterizada por uma dermatose neutrofílica febril aguda.[13]
A taxa normal de hematopoiese pode ser alterada como um efeito desejado ou um efeito adverso de alguns medicamentos, incluindo:
Tabaco: a causa mais comum de neutrofilia leve. A contagem absoluta de neutrófilos duplica entre os fumantes de pelo menos 2 maços por dia, e um aumento de 25% na contagem leucocitária total é observado em todos os fumantes. O fenômeno ocorre em decorrência das alterações inflamatórias induzidas pelo tabagismo, que levam até 5 anos após o abandono do hábito de fumar para se normalizar e para que as contagens de leucócitos totais e de neutrófilos diminuam.[14]
GM-CSF: em uma dose de 250 microgramas/m^2, a produção de neutrófilos na medula óssea não é afetada, mas a migração de neutrófilos do sangue periférico para locais específicos nos tecidos diminui enquanto a liberação de neutrófilos da medula óssea aumenta.[15] A duração da neutrofilia entre voluntários saudáveis é de 14 dias.
G-CSF: uma dosagem diária de G-CSF pode resultar em um aumento de 12 vezes na contagem leucocitária total. A terapia com G-CSF parece melhorar a função neutrofílica, com aumento da expressão da integrina, da atividade da elastase celular neutrofílica e dos níveis de antígeno de elastase plasmática.
Lítio: intensifica a granulopoiese ao aumentar a produção de GM-CSF e G-CSF. Antes do desenvolvimento de fatores estimuladores recombinantes, o lítio era usado para esta finalidade, embora a resposta fosse variável.[16]
Ácido all-trans-retinoico (ATRA) ou trióxido de arsênio: 50% dos pacientes com leucemia promielocítica aguda (LMA-M3, da classificação franco-americana-britânica) desenvolvem uma leucocitose transitória provocada pela terapia com ácido all-trans-retinoico ou trióxido de arsênio. Ambas as terapias podem resultar na síndrome da diferenciação, que ocorre em 25% dos pacientes. A síndrome da diferenciação se manifesta com febre, ganho de peso, edema periférico e pulmonar, derrames pleural e pericárdico, hipotensão e disfunção renal.
Obesidade
Um subgrupo de pacientes obesos apresenta leucocitose persistente. Provavelmente, isso ocorre devido à produção de citocinas inflamatórias, inclusive interleucina 6, fator de necrose tumoral alfa, interleucina 1 e interleucina 8, pelo tecido adiposo.[17]
Além disso, os adipócitos produzem leptina, que pode agir como fator estimulador de colônias de granulócitos.[18]
Desmarginação aumentada
A desmarginação é o processo em que os neutrófilos entram na circulação periférica oriundos de áreas de reservatórios ("pools") intravasculares de células polimorfonucleares marginadas. Similar às condições subjacentes à produção elevada de neutrófilos da medula óssea, a desmarginação pode ocorrer em resposta ao estresse e a certos medicamentos.
Desmarginação induzida por estresse
O estresse fisiológico e o psicológico podem causar neutrofilia leve. Condições associadas à ansiedade e ao estresse (transtorno de ansiedade, transtorno do estresse pós-traumático, transtorno de pânico e depressão) foram demonstradas resultar em desmarginação de neutrófilos.[19]
Entre os pacientes que apresentam suspeita de infarto do miocárdio, aqueles com contagem leucocitária >9×10⁹/L tinham probabilidade 4.5 vezes maior de confirmação de infarto do miocárdio que os pacientes com contagem leucocitária total <6×10⁹/L.[20] A leucocitose é um preditor independente de mortalidade entre pacientes com infarto agudo do miocárdio.[21][22]
O débito cardíaco aumentado no exercício físico produz significativas forças mecânicas e relacionadas ao fluxo que desalojam os neutrófilos sequestrados na vasculatura pulmonar, causando desmarginação. Portanto, uma neutrofilia tardia geralmente ocorre em decorrência do aumento na liberação de neutrófilos da medula óssea.
Outras causas de neutrofilia transitória induzida por estresse são convulsões musculares (por exemplo, convulsões tônico-clônicas), êmese, ovulação, condições obstétricas (pré-eclâmpsia e parto espontâneo ou cesáreo), intoxicação por monóxido de carbono, uma tempestade tireoidiana e trauma (queimadura térmica, choque elétrico, cirurgia e picadas de cobras).
Desmarginação induzida por medicamentos
Adrenalina: beta-agonistas induzem elevações agudas na contagem de neutrófilos como resultado da liberação de neutrófilos dos reservatórios marginados.[4]
Corticosteroides: as contagens totais de leucócitos e neutrófilos aumentam moderadamente após o uso de corticosteroides em uma dose diária equivalente ou superior a 40 mg de prednisona.[23] A desmarginação provocada por corticosteroides resulta da redução da capacidade de adesão dos neutrófilos e de um aumento na liberação de neutrófilos da medula óssea.
Antidepressivos: o mecanismo não é claro.
Saída reduzida
O tráfego normal de células mieloides maduras depende da saída natural dos neutrófilos (migração para fora) do espaço intravascular circulante para os tecidos periféricos. Esse processo pode ser inibido por medicamentos como os corticosteroides.
O uso deste conteúdo está sujeito ao nosso aviso legal