Detalhes
Em todo o mundo, foram diagnosticados cerca de 660,000 novos casos de câncer cervical em 2022, com aproximadamente 350,000 mortes. WHO: cervical cancer Opens in new window O câncer cervical é o quarto câncer mais comum diagnosticado em mulheres e ocupa o segundo lugar nos países com limitação de recursos.
O câncer cervical é causado principalmente por uma infecção persistente do colo uterino pelo papilomavírus humano (HPV). O HPV é uma infecção sexualmente transmissível e é comum em indivíduos sexualmente ativos. A maioria das infecções apresenta resolução espontânea, mas a infecção persistente do colo uterino, se não for tratada, pode causar o desenvolvimento de células anormais pré-cancerosas. O rastreamento cervical pode detectar lesões pré-cancerosas e cancerosas em mulheres assintomáticas.[1][2][3][4][5]
O rastreamento do câncer cervical foi considerado uma das estratégias clínicas preventivas mais bem-sucedidas. Ele foi associado a uma redução de 70% na mortalidade por câncer cervical em países desenvolvidos desde a introdução do teste de Papanicolau em 1941.[6][7]
Cancer Research UK: Cervical cancer mortality statistics
Opens in new window[Figure caption and citation for the preceding image starts]: Visão colposcópica de um carcinoma cervicalCentros de Controle e Prevenção de Doenças (CDC) [Citation ends].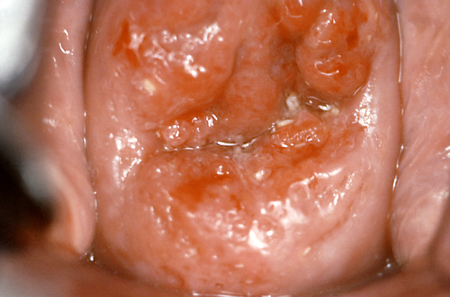
A infecção pelo HPV das células epiteliais cervicais está associada a alterações morfológicas características, e a presença do HPV pode, portanto, ser indicada por observação histopatológica. Os testes de HPV, isolados ou com citologia, são um método mais recente de rastreamento do câncer cervical.
O câncer cervical é raro em mulheres com menos de 21 anos. O rastreamento de rotina é recomendado para as pessoas com colo uterino entre 21 e 65 anos. O rastreamento pode ser clinicamente indicado nas mulheres com mais de 65 anos que não tiverem sido submetidas a um rastreamento prévio adequado, ou que tiverem alto risco de câncer cervical. As mulheres submetidas a histerectomia total (ou seja, remoção do colo uterino) não precisam mais de rastreamento para câncer cervical, desde que não tenham história pregressa de câncer ou displasia cervicais. As mulheres de qualquer idade que tiverem uma expectativa de vida limitada também podem descontinuar o rastreamento para o câncer cervical.[1][3][4][5]
ACOG: cervical cancer screening FAQs Opens in new window
National Cancer Institute: cervical cancer screening Opens in new window
Consulte Câncer cervical
As células das amostras do rastreamento cervical da junção da ectocérvice com a endocérvice (a zona de transformação ou junção escamocolunar, onde se originam 90% das neoplasias cervicais) permitem identificar lesões pré-malignas e malignas.[8]
Dados epidemiológicos, não randomizados, apoiam o impacto do rastreamento cervical. A introdução sequencial do rastreamento no Canadá, combinada com estudos controlados na região, e a introdução do rastreamento na Finlândia, Suécia e Islândia na década de 1960 foram associadas a uma queda na incidência de câncer cervical.[9][10][11] Mais da metade dos casos de câncer cervical diagnosticados nos EUA ocorrem em mulheres que não participam de rastreamentos.[12]
A citologia convencional, com o uso de células fixas em uma lâmina com amostras colhidas com espátula, apresenta sensibilidade de 30% a 87% para displasia.[13] Uma metanálise sugeriu uma sensibilidade de 58% quando usada em rastreamentos da populacionais.[14][15]
Desde meados da década de 1990, novas técnicas utilizaram um meio de transporte líquido (citologia em meio líquido) à base de etanol para preservar as células. Diversos produtos comerciais estão disponíveis. A amostra líquida tem a vantagem de possibilitar outras avaliações diagnósticas de doenças sexualmente transmissíveis, como gonorreia, clamídia e vírus do papiloma humano (HPV), para classificar o risco. Além disso, a proporção de espécimes insatisfatórios foi reduzida de 4.1% para 2.6%.[16] A citologia padrão com lâmina e a citologia em meio líquido têm precisão diagnóstica semelhante, tendo-se relatado que a citologia em meio líquido apresenta uma sensibilidade que varia de 61% a 66% com uma especificidade de 80% a 91%.[17][18]
[Figure caption and citation for the preceding image starts]: Histologia de neoplasia intraepitelial cervicalDo acervo do Dr Richard Penson, Massachusetts General Hospital, Boston; utilizadas com permissão [Citation ends].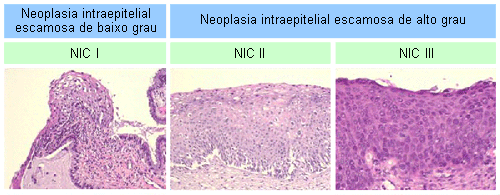
A US Preventive Services Task Force recomenda o rastreamento de mulheres com risco médio usando citologia (testes citológicos sem testes para papilomavírus humano [HPV]) a partir dos 21 anos de idade e, em seguida, uma vez a cada 3 anos, se os resultados forem normais.[1][5] As mulheres com risco médio não devem ser rastreadas para câncer cervical com citologia mais frequentemente do que uma vez a cada 3 anos.[4][5] Risco médio é definido como aquelas sem história de lesão pré-cancerosa (neoplasia intraepitelial cervical [NIC] de grau 2 ou lesão mais grave) ou câncer cervical, aquelas que não estão imunocomprometidas (incluindo infectadas por HIV) e aquelas sem exposição intra-uterina ao dietilestilbestrol
Os exames de citologia insatisfatórios devem ser repetidos em 2 a 4 meses.[2][19] Deve ser realizada uma avaliação de acompanhamento apropriada para as mulheres com citologia anormal, independentemente do status dos testes para HPV.[2][5][19] O rastreamento das mulheres com risco médio deve ser interrompido a partir dos 65 anos de idade, caso tenham tido três resultados negativos consecutivos de citologia ou dois resultados negativos consecutivos de citologia associada a testes de HPV ao longo de 10 anos, sendo o teste mais recente realizado dentro de 5 anos.[1][3][4][5]
A classificação dos resultados do exame, com base no sistema Bethesda para relatar citologia cervical, foi introduzida pela primeira vez em 1988 e revisada em 2001 para definir as amostras satisfatórias e para padronizar os relatórios.[20] Dentre as amostras inadequadas para avaliação, estão os exames com falta de informações de identificação da paciente, lâminas quebradas, componente escamoso inadequado (definido como <5000 células escamosas em meio líquido ou <8000 a 12,000 células em meio convencional) ou elementos desconhecidos em mais de 75% das células escamosas (tipicamente devido a lubrificante, inflamação ou sangue).
A terminologia do sistema Bethesda para relatórios citológicos classifica as anormalidades epiteliais da seguinte forma.[20]
Anormalidades em células escamosas
Células escamosas atípicas (ASC)
Células escamosas atípicas de significado indeterminado (ASC-US)
Células escamosas atípicas; não se pode descartar a lesão intraepitelial escamosa de alto grau (ASC-H)
Lesão intraepitelial escamosa de baixo grau (LSIL); abrange aquelas anteriormente classificadas como atipia coilocítica (alterações causadas pelo vírus do papiloma humano [HPV]) ou neoplasia intraepitelial cervical (NIC) 1
Lesão intraepitelial escamosa de alto grau (HSIL); abrange aquelas anteriormente denominadas de NIC 2 ou NIC 3
Carcinoma de células escamosas.
Anormalidades em células glandulares
Células glandulares atípicas (CGA)
Células glandulares atípicas; favorecem neoplasia
Adenocarcinoma in situ (ACIS) endocervical
Adenocarcinoma.
O sistema Bethesda classifica a LSIL e a HSIL como lesões cervicais escamosas precursoras.
Embora a terminologia "lesão intraepitelial escamosa" tenha sido usada originalmente como diagnóstico citológico, ela também pode ser usada para classificação histológica. Geralmente são usados os graus de 1 a 3 da NIC para classificar os diagnósticos histológicos. Mais de dois terços dos esfregaços que mostram atipia celular não atendem aos critérios diagnósticos para displasia e são classificados como ASC-US ou como ASC-H. Estudos demonstraram que até 90% das LSIL regredirão espontaneamente.[21][22] No entanto, algumas estimativas sugerem que a LSIL pode ter um risco de abrigar uma lesão de grau mais elevado (NIC 2 ou 3) de até 33%. A HSIL acarreta um risco de >70%.[23][24]
A infecção por HPV foi relacionada a mais de 90% dos casos de displasia cervical de alto grau e a quase 100% dos casos de câncer cervical.[25][26] A falha na eliminação do HPV é provavelmente um fator primário no desenvolvimento subsequente de displasia. Os subtipos de HPV oncogênicos ou de alto risco são o 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 e 68.[27] Pesquisas mostraram que o HPV-16 e o HPV-18 estão mais associados a lesões com grau significativamente elevado (pelo menos NIC 2) que os outros subtipos de alto risco.[28]
Nos EUA, a Food and Drug Administration (FDA) aprovou testes baseados em DNA para tipos de HPV de alto risco (hrHPV) como uma opção para o rastreamento primário do câncer cervical em mulheres com 25 anos ou mais. Devido à elevada prevalência da infecção por HPV em mulheres com idade inferior a 30 anos e ao fato de muitas infecções serem passageiras, o teste para HPV não é rotineiramente recomendado em mulheres com risco médio e idade inferior a 30 anos.[4] O teste para HPV é mais útil nas faixas etárias avançadas, pois essas mulheres têm maior probabilidade de terem uma infecção já estabelecida. A US Preventive Services Task Force recomenda o rastreamento das mulheres com risco médio usando-se o teste de hrHPV isoladamente ou em combinação com a citologia (co-teste) a cada 5 anos a partir dos 30 anos de idade.[1][5]
O manejo (retorno ao rastreamento de rotina, vigilância mais ou menos frequente, colposcopia ou tratamento) é determinado por limites de risco claramente definidos para lesões NIC 3+ derivados dos resultados do teste de HPV, isolado ou em combinação com a citologia, e da história pregressa da paciente.[2][19]
Testagem para hrHPV primária
Os EUA estão em um período de transição dos testes citológicos para os testes para hrHPV primários. A American Cancer Society (ACS) atualizou suas orientações para recomendar que as mulheres com idade entre 25 e 65 anos sejam rastreadas com testes para hrHPV isolados a cada 5 anos como alternativa ao rastreamento baseado em citologia; entretanto, se o teste para hrHPV não estiver disponível, a ACS recomenda que as pessoas com idade entre 25 e 65 anos sejam rastreadas com co-testagem (teste de hrHPV em combinação com citologia) a cada 5 anos ou com citologia isoladamente a cada 3 anos.[3]
Na Inglaterra, o Programa de Rastreamento Cervical do National Health Service (NHS) oferece a todas as mulheres entre 25 e 64 anos um teste gratuito de rastreamento cervical a cada 3 anos a 5 anos, dependendo da idade. National Health Service: cervical screening programme Opens in new window
[Figure caption and citation for the preceding image starts]: Intervalos de rastreamentoCriado pelo BMJ Evidence Centre com base em informações do Programa de Rastreamento Cervical do National Health Service [Citation ends].
As amostras são testadas para HPV. Se o teste para HPV for negativo, a paciente retorna ao rastreamento regular a cada 3 a 5 anos, dependendo da idade. Se o HPV for encontrado, a citologia em meio líquido é usada para detectar alterações celulares anormais. Se o resultado da citologia for negativo, a paciente será submetida a um novo rastreamento em 12 meses. Se o resultado da citologia for anormal, a paciente será encaminhada para uma colposcopia. Cervical screening: colposcopy and programme management Opens in new window
O teste de HPV, com ou sem triagem intermediária usando inspeção visual do colo uterino com ácido acético, pode ter um papel nos cenários com poucos recursos.[29] Se o teste de HPV não estiver disponível, recomenda-se a inspeção visual do colo uterino após a aplicação de ácido acético diluído, seguida de tratamento com crioterapia.[29] Um estudo realizado na Índia relatou uma redução dos casos de câncer cervical avançado em mulheres com mais de 30 anos, comparadas com aquelas que passaram por rastreamento com citologia.[30]
A autoamostragem para HPV tem o potencial de melhorar o acesso, e a adesão, ao rastreamento do câncer cervical. A Organização Mundial da Saúde a recomenda como uma abordagem adicional para pessoas com idades entre 30 e 60 anos, mas essa abordagem ainda está em investigação nos EUA.[31]
Co-testagem (teste para hrHPV e citologia)
No co-teste, a citologia e o teste para hrHPV são realizados em conjunto a partir da mesma amostra de células retiradas do colo uterino.
Testagem reflexa
As amostras de citologia que relatam resultados de ASC-US ou LSIL devem ser testadas quanto à presença dos tipos de HPV associados a NIC (teste reflexo de HPV ou triagem de HPV). Vários estudos, incluindo o ASCUS-LSIL Triage Study (ALTS), demonstraram que a realização do teste de HPV, depois que os resultados do teste de ASC-US foram obtidos, pode melhorar a detecção de lesões de grau mais elevado.[23][28][32][33] Em um acompanhamento de 10 anos, um estudo relatou ter encontrado NIC 3 em 21% e câncer cervical em 18% das mulheres que inicialmente apresentavam citologia negativa, mas eram positivas para HPV-16 ou HPV-18. As lesões de alto grau (NIC 3 e câncer cervical) foram identificadas em apenas 1.5% de todas as outras mulheres com citologia negativa e positivas para hrHPV em um acompanhamento de 10 anos.[28] Os testes de hrHPV primários positivos devem passar por uma revisão citológica adicional na mesma amostra (teste de citologia reflexa), para classificar as anormalidades epiteliais e informar o tratamento.[2][19]
A combinação da vacinação contra o HPV e rastreamento cervical proporciona a maior proteção contra o desenvolvimento de cânceres causados pelo HPV, incluindo o câncer cervical. Após a introdução do programa de vacinação nos EUA, houve uma redução na prevalência do HPV e na incidência de lesões cervicais pré-cancerosas.[34][35][36][37] Uma redução nas lesões NIC 2+ positivas para HPV-16 e HPV-18 também foi observada em mulheres não vacinadas, o que sugere proteção de rebanho nessas mulheres.[38]
Existem três vacinas contra o HPV licenciadas para prevenir a infecção pelo HPV: bivalente (HPV-16 e HPV-18); quadrivalente (HPV-6, HPV-11, HPV-16 e HPV-18); e nonavalente (HPV-6, HPV-11, HPV-16, HPV-18, HPV-31, HPV-33, HPV-45, HPV-52 e HPV-58). Nos EUA, apenas a vacina nonavalente está disponível e aprovada para uso em mulheres e homens com idades entre 9 e 45 anos.[39] A vacina quadrivalente está disponível em alguns outros países. Uma dose única da vacina contra o HPV é efetiva na prevenção da infecção cervical por HPV-16 e HPV-18, os dois tipos de HPV que causam 70% dos cânceres cervicais.[40][41][42] Diferentes tipos de vacina contra o HPV têm eficácias comparáveis e os dados de imunogenicidade sugerem níveis elevados de títulos de anticorpos persistentes 10 anos após a imunização.[43][44][45]
O Advisory Committee on Immunization Practices (ACIP) dos Centros de Controle e Prevenção de Doenças dos EUA recomenda a vacinação contra o HPV para todas as crianças e adultos de 9 a 26 anos.[46][47][48] A idade recomendada para a vacinação é de 11 a 12 anos; no entanto, a série de vacinas pode começar aos 9 anos de idade. A recomendação do ACIP para a vacinação contra o HPV é para uma série de duas ou três doses, dependendo da idade ou da condição à vacinação inicial.[46][47][48] Recomenda-se a tomada de decisões clínicas compartilhadas sobre a vacinação contra o HPV em indivíduos entre 27-45 anos que não tenham sido vacinados de maneira adequada quando mais jovens.[47][48]
No Reino Unido, a vacinação contra o HPV é recomendada em todos os adolescentes de 12 e 13 anos. As meninas são elegíveis para receber a vacina até completarem 25 anos, e os meninos nascidos em ou após 1º de setembro de 2006 são elegíveis para receberem a vacina até completarem 25 anos.[49] Recomenda-se que os homens que fazem sexo com homens até os 45 anos de idade, incluindo os que frequentem clínicas especializadas em saúde sexual e/ou clínicas de HIV, sejam vacinados.[49]
As vacinas são consideradas muito seguras, com efeitos colaterais típicos que incluem dor, prurido, irritação, eritema e febre baixa.[50]
As mulheres que receberam a vacina contra HPV devem ser rastreadas de acordo com as recomendações de rastreamento cervical para a população geral.[5]
A colposcopia fornece uma visão ampliada do colo uterino e do tecido vaginal, a qual permite distinguir o tecido de aparência normal do tecido de aparência anormal. Além disso, ela permite a realização de biópsias direcionadas para exame anatomopatológico. A sensibilidade relatada da colposcopia pode ser de apenas 58%, embora possa aumentar com a análise de duas ou mais biópsias direcionadas. O diagnóstico citológico e o diagnóstico histológico estão diretamente correlacionados em 50% das pacientes. Em um estudo de pacientes com LSIL, 45% das pacientes tinham NIC 1 na biópsia, 16% tinham NIC 2 ou 3 e 33% tinham histologia normal.[51] Os achados foram semelhantes para a lesão intraepitelial escamosa de alto grau (HSIL). Todas as lesões visíveis devem ser biopsiadas, com exames colposcópicos repetidos para acompanhar a citologia anormal persistente. O tratamento é determinado pelos achados na colposcopia e na biópsia.[2]
[  ]
]
O uso deste conteúdo está sujeito ao nosso aviso legal